Toxoplasma gondii igg положительный при беременности что это
Что это значит, если в анализе обнаружены антитела к токсоплазме IGG
Токсоплазма относится к ряду опасных микроорганизмов, которые попадая в человеческий организм, может нанести ему существенный вред. Если вы по каким-либо причинам обследовались на наличие токсоплазмы в теле, и в результате на распечатке анализов обнаружены антитела к токсоплазме IGG: что это значит? Давайте разбираться. Человеку без медицинского образования и без определенных познаний в этой сфере тяжело разобраться, что к чему в этих терминах и цифрах. Попробуем расшифровать значения таких результатов на общедоступном языке.
Статистика и короткая характеристика заболевания
Статистика неумолима, согласно последним исследованиям в этой сфере каждый третий житель земного шара является носителем токсоплазмоза. И превалирующее большинство людей об этом даже не догадывается.
Источником заражения чаще всего являются наши домашние любимицы кошки, но могут быть и другие животные и даже немытые овощи и фрукты, так как микроорганизм может пребывать и в почве. Если употребить в пищу мясо зараженного животного, то также вполне возможно заболеть токсоплазмозом.
Когда данный вредитель попадает внутрь человека, то естественно иммунная система начинает бурно реагировать на него. И если в расшифровке анализов токсоплазмоз igg положительный, то это обозначает, что паразит попал в организм, и иммунная система уже активизировалась и работает на полный ход.
igg к токсоплазме обозначает то, что иммунитет уже выработал антитела (ат) к данному микроорганизму, простыми словами защитные силы организма справились с инородным вредителем.
Ат к токсоплазме остаются в организме на всю жизнь и повторное заражение этими вредителями уже не возможно, ат сразу же справятся с ними.
Ат к токсоплазме igg это надежная защита от повторного инфицирования.
Такие ат другим словом называются иммуноглобулин. Его повышение в крови может означать как уже неактивную фазу болезни, так и острую. Все зависит от сроков заражения и сдачи анализа. Если после инфицирования токсоплазмозом прошло уже много времени, нет никакой выраженной симптоматики заболевания, то значит, повышенный иммуноглобулин является свидетельством того, что болезнь уже подавлена. Если же человек плохо себя чувствует, и заражение только произошло – значит, в наличии острая форма и иммунная система борется с болезнью.
Такие антитела могут обнаруживаться с помощью ифа (иммуноферментного способа обследования). Такой способ может эффективно обнаружить не только наличие в организме токсоплазмоза, но и фазу его развития. Существует два вида иммуноглобулина:
Наличие антител IgM, и отсутствие антител IgG свидетельствует о начальной острой форме заболевания. А присутствие IgG и отсутствие IgM обозначает уже неактивную форму болезни, когда иммунитет уже полностью переборол вредителя.
Если же в крови отсутствуют обе формы антител, значит, вредоносный микроорганизм не попадал к человеку, и заражения не было.
В таком случае стоит особое внимание удалить мерам профилактики заболевания: тщательно мыть руки, овощи и фрукты, не контактировать с животными.
Особенно актуальна профилактика для беременных женщин. Если до беременности женщина уже переболела данным заболеваниям и в крови есть антитела IgG, то это не несет особую опасность ни для плода, ни для будущей мамы. Но если заражение происходит непосредственно во время беременности – это очень опасно для будущего ребенка. Такая ситуация чревата многими осложнениями для плода, вплоть до выкидыша.
Чтобы оградить себя от таких непоправимых последствий токсоплазмоза, необходимо перед планируемой беременностью пройти обследование на данное заболевание. При наличии острой формы, лучше не планировать беременность, до тех пор, пока иммунитет не переборол микроорганизм. Если же у женщины вообще отсутствуют антитела и организм еще не сталкивался с такой проблемой, то необходимо строго соблюдать все меры профилактики.
©Пенза-Взгляд, 2015–2016. Портал актуальных новостей «Пенза-Взгляд».
Новости Пензы. События, факты, мнения.
Использование материалов разрешено только с предварительного согласия правообладателей. Все права на фото-видео, графический и изобразительный контент принадлежат их авторам. Допустимо цитирование не более 30% от исходного текста. Полностью дублировать материалы запрещено (в том числе с использованием RSS). При цитировании материалов гиперссылка на penzavzglyad.ru обязательна.
Редакция не несет ответственности за содержание блогов и комментариев, а также не предоставляет справочной информации. Позиция «Пенза-Взгляд» не всегда совпадает с мнением авторов статей, опубликованных на интернет-портале.
Все замечания, пожелания и предложения присылайте на penzavzglyad@yandex.ru. Прогноз погоды предоставлен сервисом Яндекс.Погода.
Настоящий ресурс может содержать материалы 18+.
TORCH-инфекции и беременность
Особенность TORCH-инфекций состоит в том, что при заражении ими женщины во время беременности они могут оказывать пагубное действие на все системы и органы плода, особенно на его центральную нервную систему, повышая риск выкидыша, мертворождения и врожденных уродств ребенка. На перинатальные инфекции приходится примерно 2-3% всех врожденных аномалий плода. Большинство инфекций опасно при первичном заражении во время беременности. Рецидивы герпеса могут быть опасны во время родов и в послеродовом периоде. Часто заражение беременной женщины инфекциями TORCH-комплекса является прямым показанием к прерыванию беременности.
Остановимся более подробно на каждой инфекции, входящей в комплекс.
Токсоплазмоз
Токсоплазмозом заражено почти 30% людей в мире. У взрослых токсоплазмоз чаще протекает бессимптомно, иногда может быть головная боль, ангина, астения, в редких случаях лимфаденит. В исключительных случаях токсоплазма может вызывать миокардит, гепатит, пневмонию, менингоэнцефалит, поражения глаз. После перенесенного заболевания вырабатывается устойчивый иммунитет к токсоплазме.
Токсоплазмоз представляет собой серьезнейшую опасность при первичном заражении женщины во время беременности. Если женщина перенесла заболевание до беременности (не менее чем за полгода), ее будущему ребенку токсоплазмоз не угрожает, если же заражение женщины произошло во время беременности, то многое зависит от того, на каком сроке беременности токсоплазмы попали в организм беременной женщины. Наиболее опасным считается заражение токсоплазмозом в первом триместре. В этих случаях врожденный токсоплазмоз часто приводит к гибели плода или развитию тяжелейших поражений глаз, печени, селезенки, а также нервной системы ребенка.
При заражении матери на более поздних сроках беременности риск передачи инфекции плоду очень высок, но риск тяжелых поражений плода снижается.
Диагноз токсоплазмоза ставится на основании клинических данных и данных лабораторного обследования (определение антител к Toxoplasma gondii в крови).
Антитела класса IgM к Toxoplasma gondii в крови появляются спустя 2-4 недели после заражения и исчезают через 3-9 месяцев. Далее появляются антитела класса IgG, и их титр постепенно повышается, а спустя 2-5 месяцев после заражения достигает пика.
Краснуха
Если женщина, планирующая беременность, не переболела ранее краснухой, ей необходимо провести профилактическую прививку. Профилактическая прививка приводит к развитию иммунитета у 95 % реципиентов.
Диагноз краснухи ставится на основании клинических данных и данных лабораторного обследования (определение антител к вирусу краснухи в крови).
Цитомегаловирусная инфекция
При внутриутробном заражении цитомегаловирусная инфекция может привести к внутриутробной гибели плода или рождению ребенка с врожденной цитомегаловирусной инфекцией. Врожденная цитомегаловирусная инфекция может проявиться сразу после рождения ребенка такими пороками развития, как недоразвитый головной мозг, водянка головного мозга, гепатит, желтуха, увеличение печени и селезенки, пневмония, пороки сердца, врожденные уродства. Родившийся ребенок может страдать задержкой психического развития, глухотой, эпилепсией, церебральным параличом, мышечной слабостью. Иногда врожденная цитомегаловирусная инфекция проявляется только на 2-5-м году жизни ребенка слепотой, глухотой, речевым торможением, отставанием в умственном развитии, психомоторными нарушениями. Все это приводит к тому, что первичная цитомегаловирусная инфекция у беременной на ранних сроках беременности является показанием к искусственному прерыванию беременности.
Если же женщина была заражена цитомегаловирусной инфекцией ранее, а во время беременности произошло ее обострение, то таких страшных последствий не возникает: женщине назначается лечение антивирусными препаратами и иммуномодуляторами.
Диагноз цитомегаловирусной инфекции ставиться на основании клинических данных и данных лабораторного обследования (определение антител к ЦМВ в крови).
После заражения ЦМВ через несколько недель повышается титр антител класса IgM. Уровень IgM к ЦМВ обычно увеличивается в течение нескольких недель и уменьшается медленно через 4-6 месяцев. Иногда антитела класса IgM к ЦМВ могут циркулировать в крови в течение многих лет. Антитела класса IgG появляются в крови через 1-2 недели после появления IgM-антител.
Герпес
При первичном заражении герпесом во время беременности, особенно на его начальной стадии, когда закладываются все органы и системы будущего ребенка, герпетическая инфекция может быть смертельно опасной для плода. В этом случае втрое повышается риск неразвивающейся беременности и выкидышей, возможно развитие уродств у плода. Если заражение герпесом происходит во второй половине беременности, то увеличивается вероятность появления врожденных аномалий плода, таких как микроцефалия, патология сетчатки, пороки сердца, врожденная вирусная пневмония. Могут произойти преждевременные роды. Ребенок может заразиться герпесом не только внутриутробно, но и во время родов, проходя родовыми путями инфицированной матери. Это происходит, если во время беременности у женщины обостряется генитальный герпес, а высыпания локализуются на шейке матки или в половых путях.
Первичная инфекция встречается у серонегативных пациентов, которые никогда не заражались. Вторичная инфекция представляет собой активацию скрытой инфекции или реинфекцию у серопозитивных пациентов.
У большинства людей, зараженных ВПГ, инфекция протекает бессимптомно, поэтому необходима серологическая диагностика.
Антитела класса IgM к вирусу простого герпеса обнаруживаются спустя одну неделю после инфекции, обычно это показатель недавней или текущей инфекции.
Антитела класса IgG появляется спустя 2-3 недели после инфицирования, и их титр снижается через несколько месяцев. У пациентов с рецидивом заболевания чаще титр антител класса IgG не повышается.
Серологическая диагностика TORCH-инфекций
В лабораториях ассоциации «Ситилаб» диагностика TORCH-инфекций выполняется на анализаторах закрытого типа LIAISON итальянского производителя DiaSorin. Метод прямой хемилюминесценции на магнитных микрочастицах конъюгированных с антигеном, позволяет количественно измерять уровень исследуемых антител (АТ) в сыворотке крови. Автоматический анализатор LIAISON обладает широкими возможностями для исследования антител к TORCH-инфекциям, все исследования уровней специфических IgM и IgG производятся количественно, а для некоторых инфекций (токсоплазмоз, цитомегаловирусная инфекция) возможно определение авидности антител класса IgG, что имеет важное прогностическое значение для определения давности заболевания у беременных.
Кровь на наличие антител к TORCH-инфекциям правильнее всего сдавать еще до наступления беременности, при ее планировании. Напомним, что наиболее опасным для плода является первичное заражение инфекциями TORCH-комплекса во время беременности, особенно на ранних ее сроках. При планировании беременности желательно обследоваться и будущему отцу ребенка на антитела к ЦМВ и ВПГ.
Если до наступления беременности исследование на TORCH-инфекции проведено не было, это совершенно необходимо сделать как можно на более ранних сроках беременности. Причем исследование на TORCH-инфекции нужно проводить вне зависимости от самочувствия беременной женщины, так как большинство инфекций TORCH-комплекса протекают бессимптомно, и до появления серьезных осложнений со стороны плода, беременная женщина может даже не догадываться об их существовании.
Положительный результат на антитела IgM характерен для острой инфекции или для прошлой инфекции с длительно сохраняющимся уровнем IgM.
Отрицательный или сомнительный результат исследования не всегда исключает острый токсоплазмоз. Если клинически подозревается токсоплазмоз, несмотря на отрицательный результат исследования, исследование необходимо повторить не ранее, чем через 1-2 недели.
Положительный результат указывает на недавнюю или прошлую инфекцию, однако, если одновременно у пациента определяются и антитела класса IgM, следует думать о недавней инфекции.
При получении сомнительного результата исследование необходимо повторить через 1-2 недели.
Отрицательный результат исследования означает, что заражения токсоплазмой не было, но не исключает острую инфекцию. Если заражение токсоплазмой подозревается, несмотря на отрицательный результат, необходимо провести второе исследование не ранее чем через 1-2 недели.
Одним из решений для дифференциальной диагностики первичной инфекции и реактивации является определение авидности антител IgG к Toxoplasma gondii.
Положительный результат исследования показателен для острой инфекции.
При получении сомнительного результата исследование необходимо повторить через 1-2 недели.
Положительный результат указывает на перенесенную инфекцию, однако уровни антител класса IgG, располагающиеся между 10 и 15 IU/ml должны интерпретироваться с осторожностью. Поэтому необходимо повторное исследование через 2-3 недели, чтобы установить падает ли уровень антител или повышается. У женщин переболевших краснухой реинфекции обычно не бывает, чаще она бывает у вакцинированных. Кроме того, реинфекция чаще бывает у людей с титром антител меньше 15 IU/ml. Титр антител к вирусу краснухи IgGменьше 15 IU/ml, является показанием для ревакцинации.
Исследования на антитела к вирусу краснухи IgM и IgG необходимо провести перед планируемой беременностью. Если анализ покажет, что женщина переболела краснухой до беременности, то опасности для плода нет. Обязательно проводится исследование на антитела к вирусу краснухи и в том случае, если у не болевшей краснухой беременной женщины был контакт с больным краснухой.
Положительный результат может быть при первичной инфекции, реинфекции и давней инфекции с длительно сохраняющимся повышенным IgM.
Сомнительный результат может быть при низких уровнях антител. При положительном результате антител класса IgG в данной пробе дополнительную информацию о давности заболевания можно получить, исследовав авидность антител IgG к цитомегаловирусу.
Положительный результат указывает на недавнюю или прошлую инфекцию. Если результаты определения антител IgG и IgM положительные, можно говорить о недавнем инфицировании или о реинфекции.
При получении сомнительного результата исследование необходимо повторить через 1-2 недели.
Отрицательный результат указывает на то, что заражения ЦМВ не было, но не исключает острую инфекцию. Исследование необходимо повторить через 1-2 недели.
Низкий индекс авидности означает возможность первичной инфекции менее чем за 3 месяца до исследования. Низкий индекс авидности однако не исключает прошлую инфекцию, поскольку у некоторого количества зараженных низкая авидность IgG-антител может определяться в течение многих месяцев после заражения.
Умеренный индекс авидности не исключает возможность недавней инфекции, но может указывать и на прошлую инфекцию с незаконченным формированием зрелых антител классаIgG.
Высокий индекс авидности исключает первичную инфекцию, которая была меньше чем за 3 месяца до исследования.
Положительный результат исследования характерен для недавней инфекции.
При сомнительном результате необходимо повторное исследование через 1-2 недели.
Отрицательный результат, однако, не всегда исключает острую инфекцию ВПГ, потому что инфекция может быть на ранней стадии, и антитела класса IgM ещё не наработались.
Положительный результат исследования указывает на наличие инфекции.
При получении сомнительного результата необходимо повторное исследование не ранее, чем через 1-2 недели.
Положительный результат исследования свидетельствует о наличии инфекции.
При сомнительном результате необходимо повторное исследование не ранее, чем через 1-2 недели.
Отрицательный результат указывает на то, что пациент не был заражен, но не всегда исключает острую инфекцию ВПГ 2-го типа. В течение первых 2-3 недель после заражения результат определения антител IgG может быть отрицательным. Если клинически подозревается заражение, несмотря на отрицательный результат, необходимо повторное исследование не ранее чем через 1-2 недели.
Определение антител IgG к ВПГ 2-го типа можно использовать для уточнения, заражен ли пациент изолированно вирусом ВПГ 1-го типа или ВПГ 1-го и 2-го типа.
Серологическая диагностика инфекции, вызванной ВПГ 1 типа и ВПГ 2 типа
Антитела к токсоплазме lgG, Toxoplasma IgG колич.
Описание
Антитела к токсоплазме lgG, Toxoplasma IgG количественный — позволяет определить наличие антител класса IgG к токсоплазме. Когда происходит контакт человека с Toxoplasma gondii, его иммунная система реагирует, вырабатывая антитела против паразита.
В крови может быть обнаружено два вида антител к токсолплазме: IgM и IgG.
Антитела IgG вырабатываются организмом через несколько недель после первичного инфицирования, чтобы обеспечить долгосрочную защиту, и сохраняются в организме годами. Уровень IgG нарастает во время активности инфекции, а затем стабилизируется, как только заболевание проходит и паразит становится неактивным. Однажды столкнувшись с т. гондии, человек на протяжении всей жизни будет иметь некоторые измеряемые количества антител IgG в крови.
Данный тест может быть использован, наряду с анализом на IgM, чтобы помочь подтвердить наличие острого или прошедшего инфицирования токсоплазмой.
Обнаружение у ранее серонегативных (то есть не имевших антител к Toxoplasma gondii) женщин при беременности IgG антител, указывает на свежую инфекцию, которая может приводить к врождённому токсоплазмозу.
Токсоплазмоз — это паразитарное заболевание, которое вызывается внутриклеточным паразитом Toxoplasma gondii (токсоплазмой гондии). Токсоплазмоз характеризуется поражением нервной системы, глаз, скелетной мускулатуры и мышцы сердца, а также увеличением лимфоузлов, печени и селезенки. Склонно к хроническому течению. Основные переносчики Toxoplasma gondii — домашние или дикие коты, которые заражаются при поедании инфицированных птиц, грызунов или контаминированного сырого мяса. Токсоплазмозом заболевают лица любого возраста, однако наиболее часто — дети.
Инфицирование возможно: при употреблении в пищу не обработанных термически мясопродуктов, дегустации сырого фарша (псевдо- или истинные цисты); при употреблении плохо промытых овощей и несоблюдении санитарно-гигиенических норм при контактах с домашними животными (ооцисты); от матери к плоду, в случае инфицирования женщины во время данной беременности (тахизоиты, паразитирующие в макрофагах крови), при последующих беременностях плод не инфицируется.
Передача возбудителя от человека к человеку исключена (кроме вертикальной передачи во время беременности), поскольку токсоплазма ни в одной из форм не выделяется из организма человека.
Клиническая картина при токсоплазмозе
Клинические проявления токсоплазмоза: увеличение лимфатических узлов; мышечная боль, длящаяся в течение месяца или более; поражение глаз и нервной системы; лимфаденопатия, макулопапулезная сыпь; увеличение печени, селезенки. Могут развиться признаки энцефалита, менингоэнцефалита и миокардита.
У лиц, обладающих стойким иммунитетом, токсоплазмоз часто протекает бессимптомно. Первичное или повторное заражение токсоплазмой гондии приводит к выраженным симптомам заболевания у людей с ослабленной иммунной системой, например у больных ВИЧ/СПИДом, проходящих курсы химиотерапии, пациентов после трансплантации органов или принимающих иммунодепрессанты. Могут поражаться глаза и нервная система, что вызывает головные боли, судороги, спутанность сознания, лихорадку, энцефалит, потерю координации и затуманенность зрения.
Беременность при токсоплазмозе
Самую большую опасность токсоплазмоз представляет для беременных женщин. Если инфицирование происходит в начале беременности, оно может вызывать выкидыши, мёртворождения или приводить к серьёзным осложнениям у новорождённых. Это связано с тем, что инфицированные дети имеют крайне тяжелые осложнения: задержку умственного развития, судороги, слепоту, увеличение печени или селезёнки, гидроцефалию (водянка головного мозга), микроцефалию (уменьшенные размеры головного мозга).
Если пренатальная инфекция протекает в тяжелой форме, то возможны изменения во многих органах с последующей внутриматочной смертью плода. Многие инфицированные дети, особенно те, кто заразился ближе к появлению на свет, рождаются здоровыми, но спустя несколько лет у них развиваются тяжёлые инфекции глаз, потеря слуха и задержка умственного развития. Конгенитальный токсоплазмоз, который передается плоду через плаценту встречается достаточно часто. Но нарушения, им порождаемые, во многом зависят от срока диагностики инфекции и даты начала лечения.
К осложняющим факторам относятся неонатальная гипоксия (недостаток кислорода) и гипогликемия (снижение уровня глюкозы в крови), глубокие повреждения, рост внутричерепного давления. Когда заражается беременная женщина, вероятность того, что инфекция передастся будущему ребёнку, составляет 30–40 %.
У новорожденных, матери которых перенесли токсоплазмоз, в крови может быть повышенное содержание антител класса IgG к Toxoplasma gondii, которое нормализуется к 10 месяцу жизни. При врожденной инфекции (первичное заражение матери во время беременности) высокий титр антител класса IgG в крови не падает, оставаясь высоким в течение длительного времени. В раннем детском возрасте у 80–90% из них могут развиться редко возникающие осложнения: гидроцефалия, хориоретинит и интракраниальные кальцификаты.
Интерпретация результатов
Единицы измерения: УЕ*
Положительный результат будет сопровождаться дополнительным комментарием с указанием коэффициента позитивности пробы (КП*).
Токсоплазмоз при беременности: симптомы, анализы, профилактика
Перевод подготовлен специалистом лаборатории ЦИР, врачом КДЛ, Бабкеевой Э.Р.
Кратко о Toxoplasma gondii: как происходит заражение
Как только происходит заражение, Toxoplasma gondii прячется в нервной и мышечной ткани, и элиминировать его становится невозможно. Исследования в Европе и Северной Америке предполагают, что большее количество иммунокомпетентных людей позволит ограничить распространение паразита и ассоциированное с ним поражение тканей, обеспечив сохранение паразита в спящей форме. Воспаление сетчатки и сосудистой оболочки (ретинохороидит) – наиболее частая перманентная манифестация токсоплазмозной инфекции. В Европе и Северной Америке такие поражения постепенно развиваются у 1% зараженных лиц.
За последние 15 лет были собраны свидетельства того, что в Латинской Америке клинические признаки инфекции куда более тяжелые, чем в других странах, вероятно, ввиду преобладания более вирулентных паразитических штаммов. Сравнение групп зараженных новорожденных в Европе и Бразилии показало, что поражения глаз у детей в Бразилии были более обширными и ведущими к нарушению зрения.
Когда женщина впервые заражается токсоплазмой во время беременности, инфекция может передаться плоду, приводя к врожденному токсоплазмозу и соответствующим поражениям нервной системы и глаз. Размножение Toxoplasma gondii и разрушения тканей в мозге плода могут появиться даже после начала иммунного ответа у матери, включая продукцию антител IgG.
Источник инфекции: токсоплазмоз у кошек и другие причины
Токсоплазма – облигатный внутриклеточный паразит, существующий в трех формах: ооциста, содержащейся только в кошачьих испражнениях (отсюда известно, что токсоплазмоз у кошек – опасное для человека заболевание), тахизоит (быстроделящаяся форма, наблюдающаяся в острой фазе инфекции) и брадизоит (медленно делящаяся форма, наблюдаемая в тканевых кистах). Во время первичной инфекции кошка может выделять из своего пищеварительного тракта миллионы ооцист ежедневно в течении 1-3 недель. Эти ооцисты становятся способны к инфицированию через 1-5 дней, и могут сохранять эту способность более одного года, особенно в теплом окружении. Кошки, как правило, после первичной инфекции приобретают иммунитет, таким образом, повторное инфицирование ооцистами маловероятно.
Считается, что в развитых странах с умеренным климатом основным источником заражения беременных женщин является непроваренное мясо, содержащее брадизоиты. Так же, одним из основных источников инфекции является контакт с ооцистами, находящимися в почве или воде, а также употребление в пищу загрязненных овощей и фруктов. Сельскохозяйственные животные (птицы, свиньи, овцы, козы) заражаются теми же путями, а от зараженных животных получают мясо, содержащее тканевые цисты.
Таким образом, токсоплазмоз у кошек – отнюдь не единственная причина, по которой опасный паразит может поселиться в человеческом теле.
Токсоплазмоз при беременности: инфицирование матери
Мать заражается токсоплазмозом оральным путем. Следствием токсоплазмоза при беременности становится инфицирование плода, которое происходит путем трансмиссии паразита через плаценту в результате первичного инфицирования матери. Вероятнее всего трансмиссия происходит во время паразитемии в первые дни после инфекции и до развития иммунного ответа. Риск заражения плода резко возрастает с увеличением гестационного срока.
Для своего существования и размножения тахизоиты проникают в клетки, особенно в мозговой и мышечной ткани, где формируют тканевые цисты, которые могут находиться в спящем состоянии годами. В иммунокомпетентных лабораторных моделях тканевые цисты формируются в течении недели с момента инфицирования. Неизвестно, какое время этот процесс занимает у относительно иммунологически незрелого плода. Переход от острофазной формы тахизоита, отвечающей за поражение клеток к спящей форме брадизоита в тканевых цистах, недостижимой для антибиотикотерапии, играет важную роль в «терапевтическом окне».
От 1 до 8 случав на 1000 беременностей, наиболее высокий уровень зарегистрирован во Франции.
Острая инфекция у матери, как правило, протекает бессимптомно. Если симптомы все-таки возникают, они неспецифичны – слабость, лихорадка, головные боли, недомогание и миалгия. Лимфоаденопатия является более специфичным признаком болезни. Вот почему токсоплазмоз при беременности диагностируется с трудом.
Анализ на токсоплазмоз: скрининг и диагностика
Беременные женщины с симптомами заболевания, подобными мононуклеозу, но с негативным гетерофильным тестом, должны пройти анализ на токсоплазмоз. Инфекция во время беременности наиболее точно диагностируется, когда как минимум два образца крови, исследованные с разницей минимум две недели, показывают сероконверсию от отрицательных показателей IgG и IgM к токсоплазме к положительным.
В части стран Европы практикуется проведение повторных тестов раз в месяц или раз в три месяца. Чем чаще проводится анализ на токсоплазмоз, тем выше шанс раннего обнаружения инфекции, когда лечение наиболее эффективно. Однако стоимость частых исследований и возможность получения ложноположительных результатов увеличиваются при увеличении частоты проведения исследования. В результате чего, женщине могут быть назначены ненужные ей инвазивные исследования и лечение. Потенциальный вред должен быть взвешен вместе с потенциальной пользой от лечения.
В США врачи-клиницисты, как правило, сталкиваются с необходимостью интерпретировать положительный тест авидности, полученный из единичного образца. Ни один из этих тестов достоверно не подтверждает недавнее инфицирование. Хотя выработка IgM длится от 10 до 13 месяцев, в зависимости от использованной методики, невозможно исключить индивидуальные особенности пациентов, и ¼ инфицированных женщин имеют положительный IgM-ответ в течение нескольких лет. Для женщин, чей первый тест на сроке 13 недель был положительным, возможность инфицирования после зачатия составляет 1-3%. Хотя высокая авидность IgG является признаком латентной инфекции, низкая авидность не является диагностическим признаком острой инфекции. Антитела IgG низкой авидности в некоторых случаях могут выявляться в течении нескольких лет.
Полезность определения титра антител igG никогда не была полностью оценена, и предположительно, имеет низкую воспроизводимость. Однако сочетание положительного результата на антитела IgM и отрицательного результата на антитела IgG, когда оба анализа на токсоплазмоз становятся положительными через две недели, таким образом исключая неспецифику, является признаком того, что инфицирование произошло примерно за две недели до получения первого положительного результата IgM.
Анализы на токсоплазмоз:
Токсоплазма гондии: инфекция у плода
Иммунокомпетентные женщины, зараженные до беременности, не заражают плод, хотя отмечены редкие исключения. Женщины с иммунодефицитом могут страдать паразитемией в течение беременности, несмотря на то, что заражение произошло до беременности. У таких женщин имеется риск внутриутробного заражения плода.
Врожденная токсоплазма гондии является довольно редким явлением; его случаи были зафиксированы у шести женщин в течении последних 30 лет. Один документально зафиксированный случай демонстрирует, что предшествовавший иммунитет к токоплазме не защитил от реинфекции атипичным штаммом.
Микроцефалия и ЗВРП как правило, не характерны для врожденного токсоплазмоза. Редким осложнением также является выкидыш. В европейских когортных исследованиях 1208 инфицированных женщин риск выкидыша в первом триместре, выявленный у 448 женщин, был не выше подобного риска у контрольной группы. Связь между преждевременными родами и инфекцией токсоплазма гондии так же может быть скорее обусловлена вмешательством в родовой процесс, а не самой инфекцией.
Инфекция токсоплазмоз: диагностика
Основной целью пренатальной диагностики инфицирования плода является подбор терапии со сменой спирамицина на пириетамин-сульфонамидный препарат. Поскольку пренатальная диагностика требует амниоцентеза, который является инвазивным тестом с маленькой, но подтвержденной вероятностью выкидыша, клиницисты должны убедиться в достаточной информированности женщины, чтобы позволить им взвесить все «за и против» инвазивной диагностики. Хотя рандомизированных исследований, сравнивающих типы лечения, не проводилось, сравнительные когортные исследования не предоставили свидетельство, что пириметамин более эффективен для лечения инфекции токсоплазмоз.
Для некоторых женщин пренатальная диагностика – существенное подспорье для решения вопроса о прерывании беременности. Исключение инфекции плода путем пренатальной диагностики также может предотвратить ненужное постнатальную терапию у детей без клинических симптомов токсоплазмоза и с низким риском развития инфекции.
ПЦР амниотической жидкости на наличие ДНК токсоплазмы – лучший метод диагностики инфекции плода, но его точность зависит от лаборатории и применяемой им методом, а чувствительность ниже на ранних сроках гестации (меньше 18 недель). Real-time ПЦР по-видимому, более чувствительный метод, чем ПЦР по конечной точке, но коммерчески недоступный. Чувствительность реал-тайм ПЦР была продемонстрирована французскими исследованиями по обнаружению токсоплазмы методом реал-тайм ПЦР, с полученными значениями чувствительности и специфичности 92,2% и 100% соответственно. Чувствительность не зависела от срока гестации. Четверо из 51 зараженных младенцев имели негативный результат ПЦР амниотической жидкости; сероконверсия матери в данных случаях произошла на сроках 13, 20, 28 и 32 недели.
Эти четыре ложно-отрицательных результата были получены на сроке 5-9 недель после сероконверсии матери, таким образом, время проведения амниоцентеза скорее всего не оказало влияния. Более того, как минимум одно исследование сообщало, что отсутствует связь между положительным результатом анализа и временем, прошедшим после сероконверсии, таким образом ставя под вопрос прежние рекомендации о проведении амниоцентеза после четырех недель с момента сероконверсии.
Некоторые клиницисты рекомендуют УЗИ для выявления нарушений развития плода у женщин с отрицательным результатом ПЦР амниотической жидкости. Однако, эта стратегия подвергает большое количество незараженных плодов излишнему количеству УЗ-исследований.
После родов, плацентарные признаки инфекции токсоплазмоз включают – гранулемы, цисты, децидуит, склероз и тромбоз хориоических сосудов.
РАЦИОНАЛЬНОСТЬ ПРЕНАТАЛЬНОЙ ТЕРАПИИ
Токсоплазмоз: лечение
На токсоплазмоз лечение во время беременности действует достаточно эффективно. Подход к нему во многом был основан на исследования Десмонта и Кувьера, которые 40 лет назад заявили, что лечение спирамицином снижало риск развития внутриутробного токсоплазмоза у плода. Однако в их работе был недочет – они не брали во внимание, что женщины, подвергавшиеся лечению, сероконвертировались на ранних сроках беременности, и таким образом, были в группе низкого риска инфицирования плода, а не пролечившиеся женщины скорее всего сероконвертировались на поздних сроках, и риск заражения плода был у них выше. В итоге эти данные были опровергнуты серией когортных исследований.
Факт того, что лечение снижает риск трансмиссии инфекции от матери к плоду, остается спорным, так как рандомизированное контролируемое испытание не проводилось. Самое явное подтверждение исходит из мета-анализа на уровне единичного пациента 20 европейских когортных исследований (1438 женщин), для которых проводился универсальный скрининг токсоплазмоза. Исследовались эффекты времени проведения терапии и вида терапии на передачу возбудителя от матери к плоду и клинической манифестации заболевания у детей до года. Виды пренатальной терапии включали в себя применение спирамицина, пириметамина-сульфониламида, а также применение спирамицина с последующим назначением пириметамин-сульфониламидов.
Было обнаружено небольшое свидетельство того, что на токсоплазмоз лечение, начатое в течении трех недель после сероконверсии, действует как снижающее риск передачи возбудителя плоду по сравнению с терапией, начатой в течение 8 недель после сероконверсии, но не удалось определить, было ли это реальным терапевтическим эффектом или неточностью, связанной с поздним обнаружением инфекции и включением пациентки в когорту. Только одна из пяти женщин была пролечена в течении трех недель с момента сероконверсии. Таким образом, даже если терапия эффективна, трудно определить и вовремя назначит лечение женщине сразу после сероконверсии.
В дополнение, не было обнаружено статистически значимого свидетельства снижения риска внутричерепных аномалий, обнаруженных после рождения, или ретинохороидита, выявленного во время младенчества. Два других когортных исследования также не выявили свидетельства, что терапия снижает риск развития ретинохороидита у детей дошкольного возраста. Однако есть точное свидетельство того, что терапия снижает риск постнатальной гибели младенца с врожденным токсоплазмозом. В европейском исследовании, в которое было включено 293 инфицированных плода, 8 процентов имели серьезные неврологические нарушения. Авторы предположили, что пренатальная терапия снижает риск серьезных неврологических последствий или гибели плода на 3/4. Они также предположили, что для предотвращения одного случая развития неврологической патологии после инфицирования матери на 10 неделе беременности, необходимо пролечить три плода с подтвержденной инфекцией. Чтобы предупредить один случай неврологической патологии или гибели плода при инфицировании на 30 неделе, необходимо провести терапию 18 плодов.
Есть свидетельство, полученное при когортных исследованиях, что терапия комбинацией пириметамина-сульфониламида не обладает большей эффективностью по сравнению с терапией спирамицином. Тем более, комбинация пириметамина-сульфониламида – довольно широко распространенный вариант, основанный на том, что уровень спирамицина в крови плода как правило, в два раза меньше уровня спирамицина в крови матери, что может быть недостаточно для лечения инфекции. Однако, эта информация остается спорной, учитывая трудность в измерении уровня спирамицина и разнице в концентрации препарата в крови у разных пациенток.
Недостаток свидетельств, что пириметамина-сульфониламида не обладает большей эффективностью по сравнению с другими препаратами, очень важен, так как он подрывает рациональность пренатальной диагностики. Клиницисты и пациентки должны понимать, что неизвестно, благотворна ли смена препарата при терапии в случае, если плод инфицирован.
Побочные эффекты наиболее часты при терапии пириметамин-сульфониламидом, чем от спирамицина, использующегося при токсоплазмозе для лечения. В европейских когортных исследованиях было выявлено, что побочные эффекты в 3,4% (11 из 322 пациенток) случаев требовали прекращения терапии пириметамин-сульфониламидом. Для сравнения, при терапии спирамицином этот показатель составил 1,7 %. Проспективное исследование, включавшее 48 детей с внутриутробным токсоплазмозом, выявленным при пренатальном скрининговом исследовании, показало, что 7 пациентов испытывали негативные последствия, приведшие к отмене лечения. У 6 из 7 пациентов с побочными эффектами наблюдалась нейтропения.
В итоге, есть свидетельства того, что пренатальная терапия снижает риск неврологических нарушений при врожденном токсоплазмозе, но нет свидетельств того, что происходит снижение риска глазных патологий, нарушения зрения или передачи инфекции от матери плоду. Для определения того, сопоставима ли польза терапии с потенциальными побочными эффектами и ценой, необходимы рандомизированные исследования. Однако, если токсоплазмоз выявлен у пациентки с симптомами заболевания или высоким риском заражения инфекцией, назначение терапии справедливо, но ее тип и продолжительность все еще не обозначены четко.
РЕЖИМЫ ТЕРАПИИ
Несмотря на недостаток свидетельств об эффективности, пренатальная терапия обычно назначается беременным женщинам с диагностированным токсоплазмозом у человека. Перед принятием решения о назначении терапии женщине стоит объяснить вопросы, связанные с эффективностью лечения, риском побочных эффектов и возможностью того, что ребенок может быть здоров.
Как правило, пациентки, заразившиеся во время беременности, немедленно получают терапию спирамицином (1 г перорально каждые восемь часов вне приема пищи), который является макролидным антибиотиком, сходным с эритромицином. Он накапливается в плаценте, и считается, что это в теории помогает предотвратить передачу возбудителя плоду.
Пириметамин является антагонистом фолиевой кислоты, который может вызывать подавление костного мозга, и как следствие – анемию, лейкопению и тромбоцитопения. В больших дозах является тератогеном. Сульфадиазин также является антагонистом фолиевой кислоты, при лечении токсоплазмоза работает в синергии с пириметамином и также может вызывать супрессию костного мозга и обратимую острую почечную недостаточность. Ввиду потенциальной токсичности этих препаратов, их использование во время беременности должно быть обосновано только при документированной инфекции плода, хотя клинических свидетельств, что эти лекарства более эффективны, чем спирамицин.
В животных моделях и у людей с приобретенным синдромом иммунодефицита для лечения токсоплазмоза успешно использовался азитромицин. Этот препарат также успешно использовался для лечения хламидиоза во время беременности. Необходимы клинические испытания, является ли азитромицин или кларитромицин эффективной альтернативой спирамицину для профилактики инфицирования плода токсоплазмозом. Пириметамин (100 мг разово перорально, затем 25-50 мг в день) в сочетании с азитромицином (500 мог в день) имели эквивалентный эффект в рандомизированных исследованиях по сравнению с сульфониламидами у пациентов с ретинохороидитом, вызванным T. Gondii (токсоплазмоз у человека). Женщины с непереносимостью пириметамина могут получать терапию триметоприм-сульфаметоксазолом или клиндамицином. Однако безопасность применения данных препаратов у беременных пациенток еще неизвестна.
Токсоплазмоз: заражение, профилактика
Профилактика первичного инфицирования основывается на избегании контакта с источником. Несмотря на то, что осведомленность и доступность информации об источниках инфекции, без сомнения, крайне важна, систематические проверки не нашли доказательство, что осведомленность населения влияет на поведение женщин во время беременности. Свидетельства исследований в Европе выделяют следующие возможности для заражения токсоплазмозом:
Мытье рук – одна наиболее важная мера профилактики для уменьшения риска трансмиссии микроорганизмов из одной локализации в другую у одного и того же пациента. Таким образом, мытье рук необходимо после таких занятий, как приготовление пищи и работа по саду. Для токсоплазмоза заражение по причине грязных рук встречается достаточно часто.
Планирование беременности после инфекции у матери
Данные о том, на чем необходимо базировать отсрочку беременности после перенесенной острой инфекции токсоплазмоз, крайне ограничены. Хотя рекомендуется отсрочка в шесть месяцев, паразитемия при токсоплазмозе очень скоротечна, и, вероятнее всего, уход паразита в стадию цист у женщины с адекватной иммунной реакцией произойдет быстро. Таким образом, иммунокомпетентные женщины, которые забеременели в срок от трех месяцев после перенесенной острой инфекции, навряд ли передадут инфекцию плоду. При изучении паразитемии после острой инфекции из 54 пациентов ни у одного не наблюдалось положительного результата ПЦР крови в срок 21-25 недель после начала лимфоаденопатии, и данные систематического обзора врожденного токсоплазмоза предполагают, что врожденная инфекция имеет место быть в течении трех недель после инфекции матери.
Реактивация латентного токсоплазмоза во время беременности может проявляться у ВИЧ-инфицированных женщин, особенно у пациенток с серьезно ослабленным иммунитетом. В объединенных европейских исследованиях, крупное проспективное исследование детей, рожденных от ВИЧ-инфицированных пациенток, 451 ребенок, участвовавший в исследовании, был рожден от матерей с наличием антител IgG к токсоплазме, и ни у кого из этих детей не было клинического свидетельства врожденного токсоплазмоза. В подгруппе из 71 ребенка врожденная инфекция была исключена серологическими исследованиями. Эти выводы позволяют предположить очень низкий риск трансмиссии паразита от матери к плоду со статистическим верхним пределом приблизительно 4%. Однако, большинство женщин, участвовавших в исследовании, не проявляли клинических симптомов, и риск трансмиссии у ВИЧ-инфицированных женщин со слабым иммунитетом может выше.
РЕЗЮМЕ И РЕКОМЕНДАЦИИ
Основные принципы при токсоплазмозе у беременных:
Для штаммов токсоплазмоза, циркулирующих вне Южной Америки
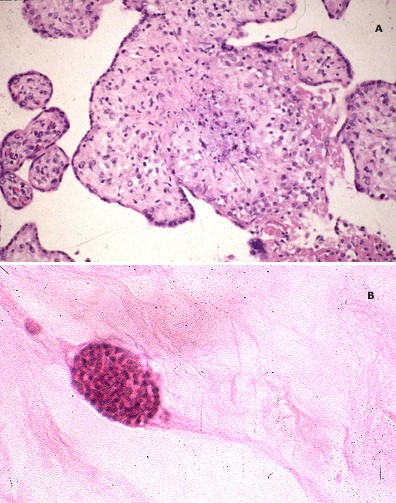
Toxoplasmosis of the placenta
(A) Granulomatous villitis (B) Trophozoites.
Courtesy of Drucilla J Roberts, MD.
Источник: UpToDate, Toxoplasmosis and pregnancy. Ruth Gilbert, MD, Eskild Petersen, MD, DMSc, DTM&H. 2013