Кишечный эпителий без атипии что это
Что такое полип толстой кишки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кравченко А. Б., эндоскописта со стажем в 10 лет.
Определение болезни. Причины заболевания
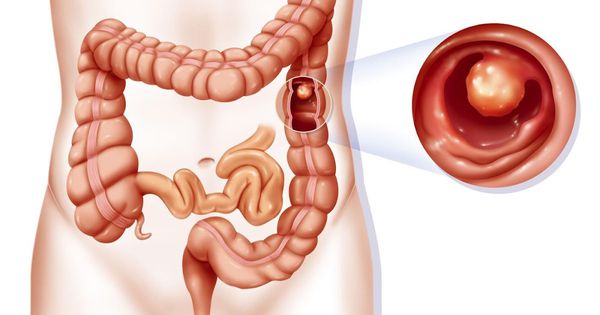
Полип толстой кишки (Colon polyp) — это патологическое разрастание железистой ткани на слизистой оболочке толстой кишки в виде объёмного образования.
Вместо термина «полип» врачи стали чаще использовать сочетание «эпителиальное образование», которое указывает на его клеточное строение (гистологическую принадлежность).
При полипах толстой кишки нет таких симптомов, которые бы точно указывали на это заболевание. Может появиться боль в животе неопределённого характера и патологические примеси в кале в виде крови и слизи.
Полипы толстой кишки являются доброкачественными образованиями, но со временем они могут перерождаться в злокачественные. Для профилактики колоректального рака их нужно своевременно выявлять и удалять.
Распространённость
Заболеваемость увеличивается с возрастом, обычно полипы толстой кишки развиваются после 40 лет, но могут возникать и раньше, если есть генетическая предрасположенность. Например, при семейном аденоматозном полипозе толстой кишки (FAP) полипы можно обнаружить уже в подростковом возрасте, в случае наследственного неполипозного колоректального рака (HNPCC) полипы развиваются в 20 – 40 лет.
Факторы риска развития полипов кишечника
Симптомы полипа толстой кишки
Клиническая картина при полипах толстой кишки зависит от таких факторов, как размеры, количество, локализация и гистологическое строение. Одиночные и мелкие, в том числе и множественные полипы, могут ничем не проявляться и быть случайной находкой при колоноскопии. Из-за крупных полипов сужается просвет кишки, что затрудняет нормальное продвижение каловых масс. В этом случае у больных появляются жалобы: боли в животе неопределённого характера, чаще периодические, неустойчивый стул с преобладанием поноса, вздутие живота, общее недомогание, потеря веса.
Патогенез полипа толстой кишки
Согласно одной из принятых теорий развития опухолей, эпителий желудочно-кишечного тракта, как и любая другая часть организма, в процессе жизнедеятельности подвергается воздействию вредных факторов окружающей среды. Из-за этого возникает хроническое воспаление.
Хронический воспалительный процесс в слизистой оболочке кишечника повреждает ДНК клеток, в результате чего в клетках накапливаются генетические мутации. При этом мутации обычно возникают в участках ДНК, ответственных за выживаемость и рост клетки.
Классификация и стадии развития полипа толстой кишки
Классификация полипов толстой кишки по количеству:
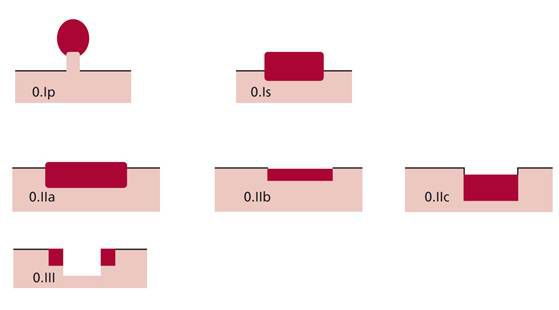
Парижская классификация делит все эпителиальные образования желудочно-кишечного тракта по форме:
Парижская классификация в описании эпителиальных образований толстой кишки позволяет оценивать риск озлокачествления и планировать оптимальный метод удаления:
По микроскопическому типу строения ткани, составляющей полип:
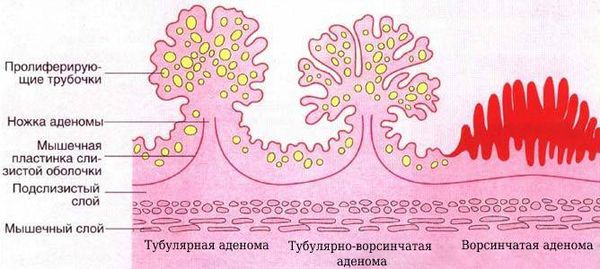
1. Аденомы. Выделяют три гистологических вида:
2. Зубчатые образования. Их так называют из-за характерной «пилообразной» структуры желёз. У зубчатых образований небольшие размеры, они протекают бессимптомно. Выявляются при скрининговой колоноскопии или во время обследования по поводу других заболеваний. Выделяют три основные категории:
3. Ювенильные (гамартоматические) образования. Это врождённые новообразования, которые представляют собой разрастание железистого эпителия и подлежащей соединительной ткани. Встречаются у детей и подростков. Клинически проявляются неустойчивым стулом со склонностью к диарее и периодически возникающими неприятными ощущениями в животе. С течением времени клиническая картина прогрессирует, присоединяется общая слабость и плохой аппетит. Часто течение болезни осложняется толстокишечным кровотечением различной интенсивности. Ювенильные образования обычно не становятся злокачественными.
Осложнения полипа толстой кишки
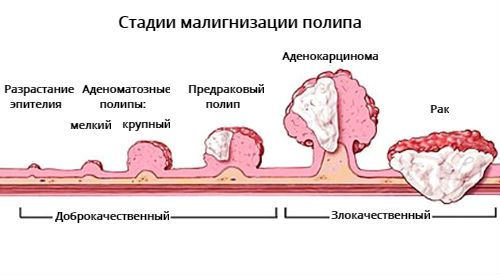
Количество клеток с предраковыми изменениями зависит от размера аденомы: чем больше размер полипа, тем выше вероятность развития в нём злокачественного процесса. Также имеет значение нарушение местного клеточного иммунитета, накопление мутаций в клетках и др. [10] Генетические мутации и показатели местного иммунитета тканей не проявляются клинически, их можно исследовать только в лабораториях.
Когда полип перерождается в рак, пациент может не заметить никаких изменений, но иногда симптомы нарастают:
Предраковый полип отличается от аденокарциномы в полипе и инвазивного рака. В процессе развития аденомы в ней могут появиться клетки с первой, второй и третьей степенью дисплазии, так образуется предраковый полип. При прогрессии дисплазии образуется аденокарцинома, её клетки начинают прорастать через ножку аденомы или стенку кишки т. е. развивается стадия инвазивного рака.
К другим осложнениям можно отнести полную или частичную кишечную непроходимость с появлением запора, вздутия живота, рвоты и других симптомов.
Диагностика полипа толстой кишки
Основными методами диагностики полипа толстой кишки являются анализ кала на скрытую кровь и колоноскопия.
Определение скрытой крови в кале. Исследование выполняется в рамках скрининга колоректального рака и диспансеризации населения в целом. Это наиболее безопасный и простой лабораторный метод диагностики полипов толстой кишки, который основан на определении гемоглобина в кале. Даже минимальные концентрации гемоглобина могут указывать на скрытое, клинически не проявляющееся кровотечение из желудочно-кишечного тракта.
Так как тест может давать ложноположительные и ложноотрицательные результаты, его может оказаться недостаточно для установки диагноза. Чтобы подтвердить или опровергнуть диагноз, нужно провести колоноскопию.
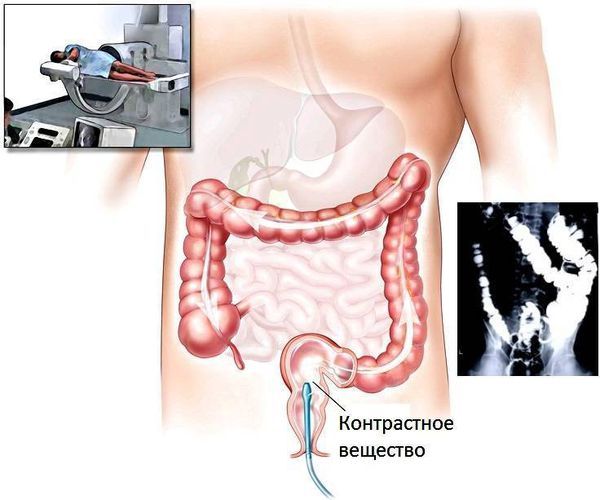
Колоноскопия. Это наиболее информативный метод диагностики полипов толстой кишки. Её рекомендуется делать всем в 45 лет, а если есть факторы риска (полипоз, колоректальный рак у родственников) — раньше. Это инструментальный метод, при котором врач в реальном времени осматривает слизистую оболочку толстой кишки c помощью гибкого эндоскопа. Во время колоноскопии можно детально рассмотреть патологическое образование, взять материал для гистологического исследования или полностью удалить новообразование.
Исследование выполняется после тщательной очистки кишки от содержимого. За 3 – 5 дней до исследования необходимо соблюдать диету с низким содержанием клетчатки. Это значит, что нужно исключить продукты растительного происхождения: фрукты, ягоды, овощи, зелень, злаковые, отруби. Также нужно применять слабительные препараты. Желательно использовать препараты большого или малого объёма (4 или 2 литра раствора) на основе полиэтиленгликоля. Схема приёма может быть двухэтапной или одноэтапной:
В 95 % случаев одной из этих схем достаточно, чтобы очистить слизистую кишки. Стоит лишь учитывать, что двухэтапная схема переносится пациентами легче, так как за один раз нужно принять меньший объём препарата.
Сигмоскопия — исследование, при котором врач осматривает не всю кишку, как при колоноскопии, а только её начальные отделы: прямую и сигмовидную кишку. Имеет такую же точность, как и колоноскопия. Этот метод применяется редко из-за широкого распространения колоноскопии.
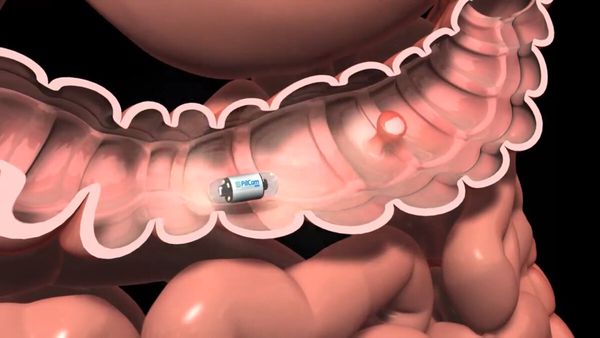
Если нет возможности провести колоноскопию, то могут применяться другие методы диагностики:
Лечение полипа толстой кишки
Лечение полипов толстой кишки только хирургическое. Методов лекарственной терапии не разработано.
Чтобы предотвратить развитие колоректального рака, все полипы толстой кишки необходимо удалять. Исключение составляют мелкие гиперпластические полипы в прямой кишке и дистальном отделе сигмовидной кишки (рядом с прямой кишкой).
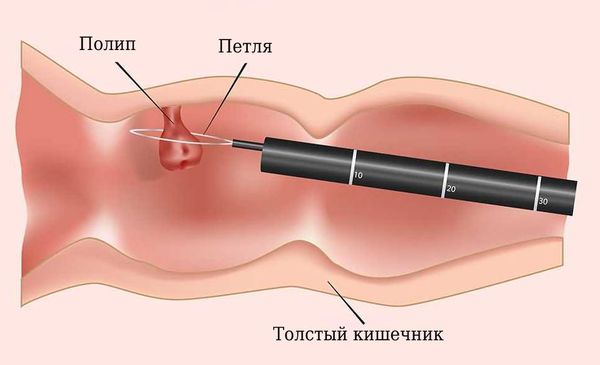
Метод удаления полипов зависит от технического оснащения клиники, подготовки медицинского персонала и особенностей клинического течения заболевания. Эндоскопическая полипэктомия — наиболее рациональный и безопасный метод удаления эпителиальных новообразований толстой кишки. Когда возможности гибкой эндоскопии были не так обширны, полипы удаляли хирургически: вскрывали брюшную полость и кишку, удаляли полип, после чего ушивали разрезы.
Методика удаления полипов зависит от внешнего вида, размеров и гистологического строения:
Все удалённые полипы, независимо от размеров, необходимо извлечь для гистологического исследования.
Рецидивы полипов после удаления могут возникнуть, если размер удалённого полипа более 40 мм, если в процесс вовлечён илеоцекальный клапан, разделяющий тонкую и толстую кишку, или ранее были неудачные попытки резекции.
Осложнения полипэктомии
Прогноз. Профилактика
Прогноз при полипах толстой кишки будет благоприятным, если их вовремя диагностировать и удалить. Без лечения полип может вызвать колоректальный рак.
Полипы толстой кишки растут медленно: обычно рак развивается примерно через 10 лет после образования небольшого полипа толстой кишки. Но если у пациента есть предрасположенность к наследственному неполипозному колоректальному раку, то озлокачествление происходит быстрее.
Полипэктомия не устраняет факторы риска образования новых полипов кишки, но снижает риски возникновения колоректального рака.
Профилактика развития полипов толстой кишки
Первичная профилактика. Чтобы предотвратить развитие полипов толстой кишки, рекомендуется вести здоровый образ жизни:
Также важно проходить скрининг на выявление злокачественных новообразований толстого кишечника:
Пациенты с генетической предрасположенностью к наследственному неполипозному колоректальному раку должны проходить обследование на полипы толстой кишки каждые 1–2 года.
Вторичная профилактика проводится, чтобы как можно раньше диагностировать рецидив и выявить вновь образовавшиеся полипы. Персональные рекомендации могут давать врачи-эндоскописты, онкологи или гастроэнтерологи, но только лечащий врач знает всё о течении заболевания и сопутствующих патологиях конкретного больного, поэтому именно он определяет стратегию наблюдения пациента и время выполнения последующей колоноскопии.
Цитологическая диагностика заболеваний шейки матки
Цитологическое исследование мазков из шейки матки позволяет оценить состояние слизистой оболочки, наличие или отсутствие признаков патологических процессов (реактивных, предопухолевых, опухолей). При выявлении другими лабораторными методами инфекционного агента (вирус папилломы человека, бактериальные и паразитарные инфекции), цитологический метод позволяет оценить реакцию организма на инфекционный агент, наличие или отсутствие признаков повреждения, пролиферации, метаплазии или трансформации эпителия. Возможно также при исследовании мазка определить причину изменений эпителия (наличие воспаления с ориентировочным или уверенным определением патогенной микробиоты (микрофлоры), патологических процессов, связанных с гормональным, лекарственным, механическим, лучевым воздействием на организм женщины и шейку матки, состояний, чреватых опасностью возникновения дисплазии и рака шейки матки, а при их развитии установить правильный диагноз. В связи с этим цитологическое исследование применяют как при скрининге (мазки с визуально нормальной шейки матки), так и при наличии видимых при гинекологическом осмотре изменений слизистой оболочки.
Получение материала
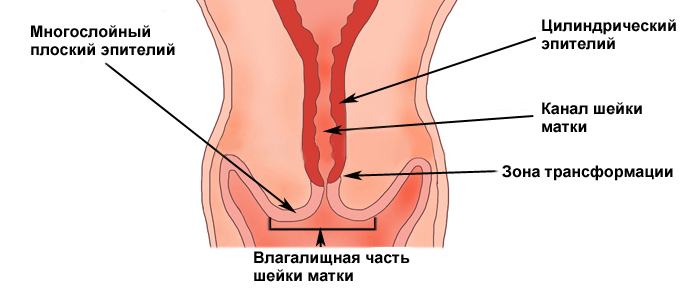
Рак шейки матки чаще всего развивается в зоне трансформации, ему предшествуют фоновые процессы и внутриэпителиальные поражения (дисплазия эпителия), которые могут располагаться на небольших участках, поэтому важно, чтобы материал был получен со всей поверхности шейки матки, особенно из зоны стыка плоского и цилиндрического эпителия. Число измененных клеток в мазке бывает различным, и если их мало, то увеличивается вероятность, что патологические изменения могут быть пропущены при просмотре препарата. Для эффективного цитологического исследования необходимо учитывать:
Материал из шейки матки должен брать врач-гинеколог или (при скрининге, профилактическом осмотре) хорошо обученная медицинская сестра (акушерка).
Важно, чтобы в мазок попадал материал из зоны трансформации, так как около 90% опухолей исходит из зоны стыка плоского и цилиндрического эпителия и зоны трансформации и только 10% из цилиндрического эпителия цервикального канала.
С диагностической целью материал получают раздельно из эктоцервикса (влагалищной порции шейки матки) и эндоцервикса (цервикального канала) с помощью шпателя и специальной щетки (типа Cytobrush). При проведении профилактического осмотра используют Cervex-Brush, различные модификации шпателя Эйра и другие приспособления для получения материала одновременно из влагалищной части шейки матки, зоны стыка (трансформации) и цервикального канала.
Перед получением материала шейку матки обнажают в “зеркалах”, дополнительных манипуляций не проводят (шейку не смазывают, слизь не удаляют; если слизи много – ее аккуратно снимают ватным тампоном, не надавливая на шейку матки.). Щетку (шпатель Эйра) вводят в наружный зев шейки матки, осторожно направляя центральную часть приспособления по оси цервикального канала. Далее ее наконечник поворачивают на 360° (по часовой стрелке), достигая тем самым получения достаточного числа клеток из эктоцервикса и из зоны трансформации. Введение инструмента выполняют очень бережно, стараясь не повредить шейку матки. Затем щетку (шпатель) выводят из канала.
Приготовление препаратов
Перенос образца на предметное стекло (традиционный мазок) должен происходить быстро, без подсушивания и потери прилипших к инструменту слизи и клеток. Обязательно перенести на стекло материал с обеих сторон шпателя или щетки.
Если предполагается приготовление тонкослойного препарата с помощью метода жидкостной цитологии, головку щетки отсоединяют от ручки и помещают в контейнер со стабилизирующим раствором.
Фиксация мазков выполняется в зависимости от предполагаемого метода окрашивания.
Окрашивание по Папаниколау и гематоксилин-эозином наиболее информативны в оценке изменений эпителия шейки матки; любая модификация метода Романовского несколько уступает этим методам, однако при наличии опыта позволяет правильно оценить и характер патологических процессов в эпителии и микрофлору.
Клеточный состав мазков представлен слущенными клетками, находящимися на поверхности эпителиального пласта. При адекватном получении материала с поверхности слизистой оболочки шейки матки и из цервикального канала в мазок попадают клетки влагалищной порции шейки матки (многослойный плоский неороговевающий эпителий), зоны стыка или трансформации (цилиндрический и, при наличии плоскоклеточной метаплазии, метаплазированный эпителий) и клетки цервикального канала (цилиндрический эпителий). Условно клетки многослойного плоского неороговевающего эпителия принято делить на четыре типа: поверхностные, промежуточные, парабазальные, базальные. Чем лучше выражена способность эпителия к созреванию, тем более зрелые клетки попадают в мазок. При атрофических изменениях на поверхности эпителиального пласта расположены менее зрелые клетки.
Интерпретация результатов цитологического исследования
Наиболее распространенная в настоящее время – классификация Bethesda (The Bethesda System), разработанная в США в 1988 г, в которую вносили несколько изменений. Классификация создана для более эффективной передачи информации из лаборатории врачам клинических специальностей и обеспечения стандартизации лечения диагностированных нарушений, а также последующего наблюдения за больными.
В классификации Bethesda выделяют плоскоклеточные интраэпителиальные поражения низкой и высокой степени (squamous intraepithelial lesions of low grade and high grade – LSIL и HSIL) и инвазивный рак. Плоскоклеточные интраэпителиальные поражения низкой степени включают изменения, связанные с папилломавирусной инфекцией и слабой дисплазией (CIN I), высокой степени – умеренную дисплазию (CIN II), тяжелую дисплазию (CIN III) и внутриэпителиальный рак (cr in situ). В этой классификации имеются также указания на специфические инфекционные агенты, вызывающие заболевания, передавае мые половым путем.
Для обозначения клеточных изменений, которые трудно дифференцировать между реактивными состояниями и дисплазией предложен термин ASCUS – atypical squamous cells of undetermined significance (клетки плоского эпителия с атипией неясного значения). Для клинициста этот термин мало информативен, однако он нацеливает врача на то, что данная пациентка нуждается в обследовании и/или в динамическом наблюдении. В классификацию Bethesda в настоящее время введен также термин NILM – no intraepithelial lesion or malignancy, объединяющий норму, доброкачественные изменения, реактивные изменения.
Так как данные классификации используются в практике врача-цитолога, ниже приведены параллели между классификацией Bethesda и классификацией, распространенной в России (Табл. 22). Цитологическое стандартизованное заключениепо материалу из шейки матки (форма № 446/у), утверждено приказом Минздрава России от 24.04.2003 № 174.
Причины получения неполноценного материала различны, поэтому цитолог перечисляет типы клеток, обнаруженные в мазках и по возможности указывает причину, по которой материал признан неполноценным.
Опасная дисплазия железистого эпителия шейки матки лечится только методом ФДТ
Дисплазия железистого эпителия шейки матки
Д.м.н., профессор Сеченовского университета, онколог, хирург, онкогинеколог, гинеколог-иммунолог, эксперт по лечению дисплазии, предраковых и опухолевых заболеваний шейки матки.
Если говорить совсем коротко, то железистая дисплазия – это предраковое заболевание шейки матки. Из-за особенности своего расположения оно практически не поддается лечению классическими хирургическими методами. Фотодинамическая терапия в этом случае – пожалуй, единственный эффективный способ лечения, который защищает от рецидивов и раковой трансформации.
А теперь обо всем по порядку.
Чтобы лучше понять, что такое железистая дисплазия шейки матки, мы немного погрузимся в теорию и изучим строение шейки матки.
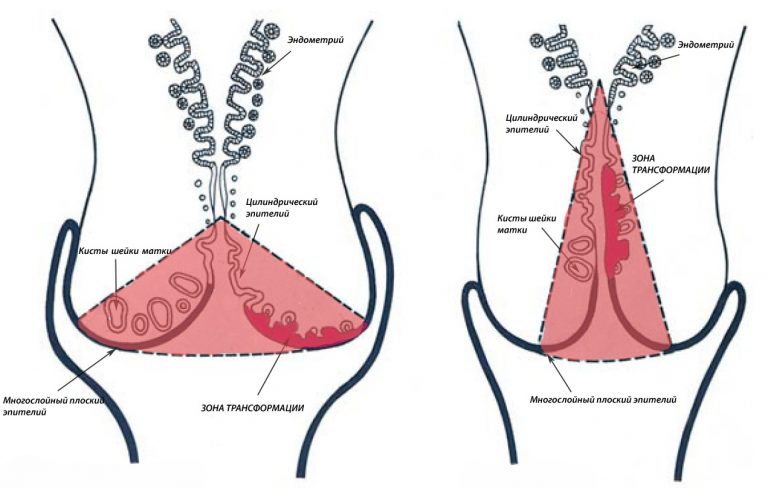
Строение шейки матки: эктоцервикс, эндоцервикс. зона трансформации.
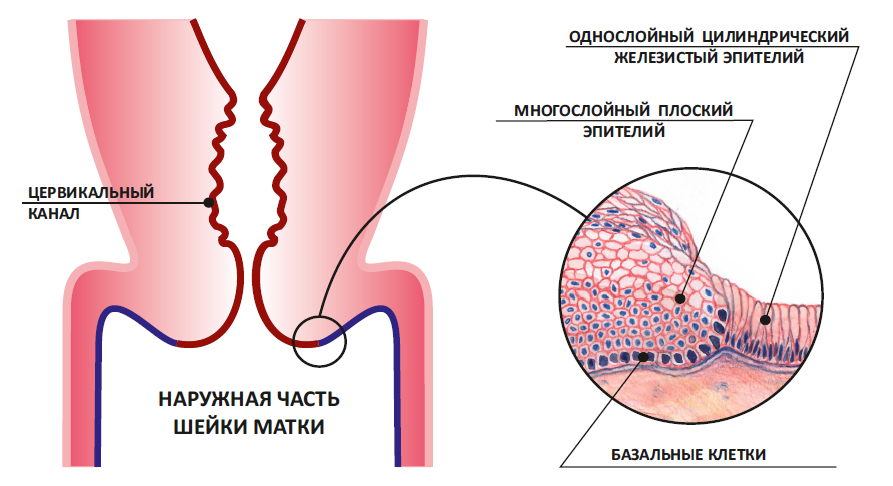
Участок шейки матки, который погружен во влагалище (синий прямоугольник) называется эктоцервиксом. Он покрыт многослойным плоским эпителием.
Участок шейки матки от наружного зева по направлению к матке называется цервикальным каналом шейки матки (оранжевый прямоугольник). Он покрыт эндоцервиксом, или железистым (цилиндрическим) эпителием.
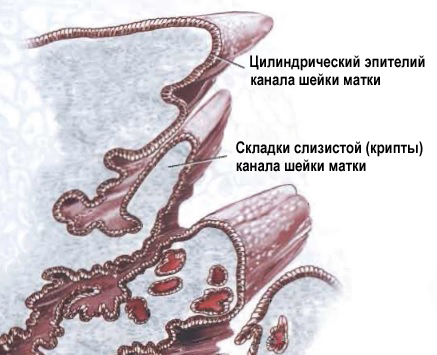
Цервикальный канал не ровный, а складчатый. На медицинском языке эти складки называются криптами. Железы цилиндрического эпителия секретирует слизь, которая составляет основной объём нормальных выделений.
Так выглядят крипты шейки матки. Всю поверхность крипты выстилает цилиндрический эпителий.
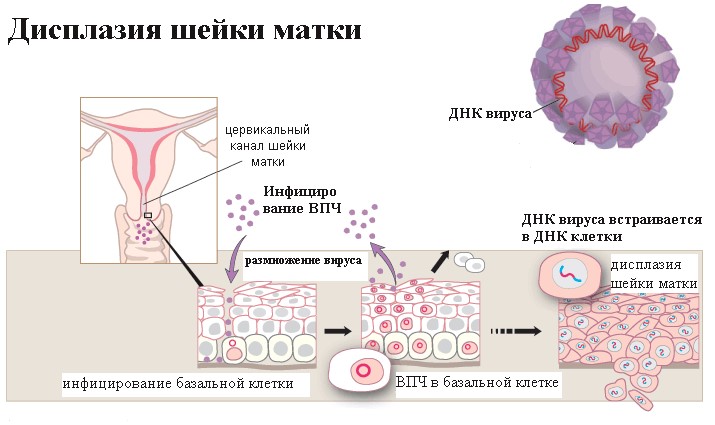
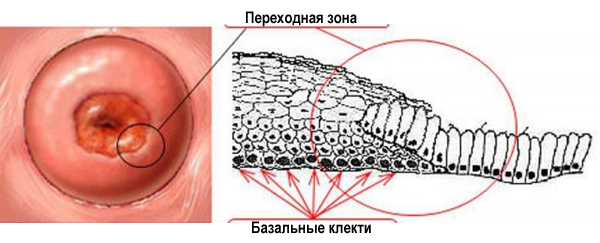
Зона, в которой многослойный плоский эпителий переходит в железистый эпителий называется переходной зоной, или зоной трансформации. Обычно дисплазия начинает свое развитие в зоне трансформации – в ней идет непрерывное клеточное деление, и вирусу папилломы легче всего проникнуть сквозь слабую защиту незрелых клеток в необходимые для его выживания базальные клетки.
Переходная зона или зона трансформации.
Дисплазия представляет собой скопление измененных вирусом клеток. Такие клетки называются атипическими, а само заболевание чаще всего относится к предраковым.
Что такое «дисплазия метаплазированного эпителия»?
Мы уже выяснили: зона, в которой сходится плоский и цилиндрический эпителий, называется зоной трансформации. Втрое ее название – переходная зона.
Но это только на схеме она представляет собой ровную линию. На самом деле, в этой зоне один эпителий заходит на другой, как морские волны на песчаный берег. Молодой плоский эпителий перекрывает молодой цилиндрический. Такой незрелый плоский эпителий и называется метаплазированным.
Незрелый метаплазированный эпителий.
Само словосочетание «метаплазированный эпителий» вызывает много вопросов. Не скрывается ли за этой формулировкой рак? – Нет, не скрывается.
Хуже, если в вашей цитологии ничего про метаплазированный эпителий не написано. Это значит, что он отсутствует в мазке, и анализ взят неправильно (помните, я писал о том, что правильная цитология начинается в кабинете врача, а не в лаборатории?).
А теперь давайте обратим внимание на то, что написано в заключении. Если в заключении написано «на фоне метаплазии очаги дисплазии», перед нами дисплазия переходного эпителия. Так как в зоне трансформации идет непрерывный процесс интенсивного деления клеток, незрелые клетки менее защищены от заражения, и вирусу папилломы (причина дисплазии) как раз в области метаплазированного эпителия легче проникнуть в глубокий базальный слой и встроиться в ДНК клетки.
Именно поэтому шейку матку так тщательно осматривают и берут с нее анализ на цитологию – дисплазия обычно начинается в переходной зоне.
А теперь поговорим о том, что означает диагноз «интраэпителиальная дисплазия железистого эпителия шейки матки».
Что такое дисплазия цервикального канала и чем она опасна
«Интраэпителиальная дисплазия железистого эпителия шейки матки» – это так называемый «цитологический» или «гистологический» диагноз. Такое заключение пишет специалист в лаборатории после изучения вашего цитологического мазка или биопсии.
Он видит в микроскоп, что в клетках железистого эпителия происходит предраковая трансформация клеток.
Формулируя таким образом свое заключение, врач-морфолог подчеркивает, что процесс происходит не в зоне трансформации, а В ЦЕРВИКАЛЬНОМ КАНАЛЕ ШЕЙКИ МАТКИ.
Поэтому заболевание еще называют «цервикальная дисплазия», или «дисплазия канала».
Такой диагноз говорит о том, что при лечении его классическими методами вероятность рецидива заболевания приближается к 80%.
Классический метод лечения дисплазии называется конизацией шейки матки. Это операция, в ходе которой хирург удаляет кусочек эктоцервикса и эндоцервикса в форме конуса. Задача хирурга – удалить участок вместе с дисплазией.
Низкая (слева) и высокая (справа) конизация шейки матки.
Но такой способ лечения для диагноза «дисплазии цилиндрического эпителия» изначально порочен.
Дело в том, что при работе с цервикальным каналом хирург действует фактически вслепую. Он не видит зоны поражения, не может оценить ее размера, глубины и по факту удаляет ткани «на ощупь». Практика показывает, что после такого лечения частота рецидива дисплазии приближается к 80%.
Фактически, когда врач-морфолог в заключении описывает наличие проблемы в области железистого эпителия, он таким образом подчеркивает сложный характер расположения дисплазии и бесперспективность хирургической тактики лечения.
Этим недостатки хирургического метода не ограничиваются.
Во-первых, радикальность и как следствие, эффективность конизации – всегда сомнительна. Объясню почему. Крипты эндоцервикса достигают глубины 5 мм. У всех разная физиология, и хирург никак не может проверить, убрал ли он достаточно цилиндрического эпителия.
У нерожавших женщин глубокое удаление тканей чревато развитием осложнений, которые могут препятствовать зачатию, вынашиванию и родам (на эту тему читайте мою статью «Беременность после конизации шейки матки»). Хирурги знают об этом, и стараются проводить операцию максимально щадящим образом.
Определение границ изменённого дисплазией эпителия носит всегда субъективный характер. А при проведении конизации глубина конуса определяется хирургом «на глазок», здесь доказательная медицина не подсказывает хирургу как действовать. Глубина обычно определяется длиной электрода – «паруса», а не тяжестью диспластического процесса.
Недостаточно радикальная конизация, как следствие, вызывает закономерный рецидив.
Во-вторых, любое лечебное воздействие само по себе является для вируса провоцирующим фактором.
После лечения вирус начинает вести себя более агрессивно и приводит к быстрому рецидиву, который развивается по негативному сценарию: дисплазия 2 степени переходит в 3, а дисплазия 3 степени и рака ин ситу могут трансформироваться в инвазивный рак шейки матки.
В-третьих, хирургия делает вирус резистентным (устойчивым) К ЛЮБОМУ лечению, даже к фотодинамической терапии. Увы, и я, и коллеги часто наблюдаем это в своей практике.
При таком развитии событий рано или поздно возникнет необходимость в удалении матки. Именно поэтому при диагнозе «дисплазия эндоцервикса» я настоятельно не рекомендую делать конизацию, так как она не устраняет причину болезни.
Как избежать рецидива?
Избежать рецидива можно единственным способом – устранить измененные клетки вместе с причиной заболевания – вирусом папилломы человека.
К сожалению, механическое удаление в процессе конизации атипических клеток не приводит к выздоровлению. ВПЧ остается в цервикальном канале. В теории, вместе с очагами дисплазии удаляются и все зараженные ВПЧ клетки. Но на практике так не происходит.
Единственный метод, который позволяет убрать из цервикального канала ВПЧ и атипичные клетки, – это правильно и в полном объеме выполненная фотодинамическая терапия с соблюдением протокола проведения.
Цервикальная дисплазия шейки матки хорошо лечится методом фотодинамической терапии
Я не буду рассказывать о самой: фотодинамической терапии – об этом очень хорошо рассказывает это видео:
Фундаментальные исследования доказали, что лазерный свет глубоко проникает в ткани и запускает фотохимические реакции на глубине минимум 7 мм. Крипты (складки) цервикального канала имеют максимальную глубину 5 мм, поэтому даже самые глубоко залегающие атипические клетки попадают под лечебное воздействие.
При соблюдении протокола проведения ФДТ в ходе фотохимических реакций образуются активные токсичные формы кислорода, которые увеличивают реальную глубину лечебного воздействия до 1,5 см! Соответственно, фотодинамическое воздействие в полной мере оказывает необходимый лечебный эффект, и даже с запасом.
Положительный терапевтический результат процедуры достигается только при неукоснительном соблюдении протокола ФДТ, который включает в себя обязательное облучение и зоны эктоцервикса, и цервикального канала специальным цилиндрическим диффузором.
Этот диффузор вводится в полость цервикального канала на всю его глубину, и по периметру облучает все поле железистого эпителия.
Только такой подход позволяет полностью уничтожить патологические клетки и содержащийся в них вирус папилломы человека (ВПЧ) на всех участках шейки матки и говорить о качественно выполненном лечении.
При такой адекватно проведённой ФДТ ВПЧ уничтожаются в 93% случаев.
Хочу отметить, что до сих пор даже очень уважаемые мои коллеги допускают ошибки в обучении специалистов-гинекологов и не показывают им необходимость облучения цервикального канала при лечении дисплазии шейки матки.
В этом случае ФДТ не оказывает нужного лечебного воздействия. Воздействие осуществляется только в области эктоцервикса, а вся полость цервикального канала шейки матки остается не задействованной в лечении. Такой «урезанный» протокол ФДТ зачастую приводит к тем же печальным последствиям, что и конизация.
Я горжусь, что могу менять медицинскую практику вокруг себя в лучшую сторону. Так, методическое пособие для врачей ГНЦ лазерной медицины МЗ РФ «Фотодинамическая терапия фоновых и предраковых заболеваний шейки матки» от 2004 года не включало в себя важный этап обработки цервикального канала.
После моего выступления на конференции StatusPraesens «Перинатальная медицина: от прегравидарной подготовки к здоровому материнству и детству», 18–20 февраля 2016 года, отель «Санкт-Петербург», методические рекомендации подверглись пересмотру и теперь включают в себя обработку цервикального при лечении дисплазии канала шейки матки как обязательный этап.
Многие теперь стали использовать диффузор для облучения цервикального канала. Однако даже после этой революции многие используют его, не понимая, какая интенсивность света выходит из этого диффузора. А это важный параметр, от которого зависит эффективность проведённой фотодинамической терапии.
Многие также используют диффузоры многократно, хотя уже после одного облучения мощность инструмента падает, и необходимое лечебное воздействие не достигается. Но никто об этом не задумывается!
Прием ведет Афанасьев Максим Станиславович, акушер-гинеколог, онкогинеколог, онколог, иммунолог, доктор медицинских наук, профессор и член ученого совета Первого МГМУ им. И.М. Сеченова МЗ РФ, эксперт по лечению дисплазии шейки матки.
После лечения я поддерживаю обратную связь со всеми пациентками и решаю все возникающие вопросы. Гепатит и положительный ВИЧ статус не является противопоказаниями для лечения методом ФДТ.