Что такое инициация в биологии
Трансляция (биология)
Трансляция (от лат. translatio — перевод) — процесс синтеза белка из аминокислот на матрице информационной (матричной) РНК (иРНК, мРНК), осуществляемый рибосомой.
Содержание
Механизм
Синтез белка является основой жизнедеятельности клетки. Для осуществления этого процесса в клетках всех без исключения организмов имеются специальные органеллы — рибосомы. Рибосомы представляют собой рибонуклеопротеидные комплексы, построенные из 2 субъединиц: большой и малой. Функция рибосом заключается в узнавании трёхбуквенных (трехнуклеотидных) кодонов мРНК, сопоставлении им соответствующих антикодонов тРНК, несущих аминокислоты, и присоединении этих аминокислот к растущей белковой цепи. Двигаясь вдоль молекулы мРНК, рибосома синтезирует белок в соответствии с информацией, заложенной в молекуле мРНК. [1]
Для узнавания аминокислот в клетке имеются специальные «адаптеры», молекулы транспортной РНК (тРНК). Эти молекулы, имеющие форму клеверного листа, имеют участок (антикодон), комплементарный кодону мРНК, а также другой участок, к которому присоединяется аминокислота, соответствующая этому кодону. Присоединение аминокислот к тРНК осуществляется в энерго-зависимой реакции ферментами аминоацил-тРНК-синтетазами, а получившаяся молекула называется аминоацил-тРНК. Таким образом, специфичность трансляции определяется взаимодействием между кодоном мРНК и антикодоном тРНК, а также специфичностью аминоацил-тРНК-синтетаз, присоединяющих аминокислоты строго к соответствующим им тРНК (например, кодону GGU будет соответствовать тРНК, содержащая антикодон CCA, а к этой тРНК будет присоединяться только аминокислота глицин).
Механизмы трансляции прокариот и эукариот существенно отличаются, поэтому многие вещества, подавляющие прокариотическую трансляцию, в значительно меньшей степени действуют на трансляцию высших организмов, что позволяет использовать их в медицинской практике как антибактериальные средства безопасные для организма млекопитающих.
Процесс трансляции разделяют на
Рамка считывания
Поскольку каждый кодон содержит три нуклеотида, один и тот же генетический текст можно прочитать тремя разными способами (начиная с первого, второго и третьего нуклеотидов), то есть в трех разных рамках считывания. За некоторыми интересными исключениями, значимой является информация, закодированная только в одной рамке считывания. По этой причине крайне важным для синтеза белка рибосомой является её правильное позиционирование на стартовом AUG-кодоне — инициация трансляции.
Инициация
Синтез белка в большинстве случаев начинается с AUG-кодона, кодирующего метионин. Этот кодон обычно называют стартовым или инициаторным. Инициация трансляции предусматривает узнавание рибосомой этого кодона и привлечение инициаторной аминоацил-тРНК. Для инициации трансляции необходимо также наличие определённых нуклеотидных последовательностей в районе стартового кодона (последовательность Шайна — Дальгарно у прокариот и последовательность Козак у эукариот). Немаловажная роль в защите 5′-конца мРНК принадлежит 5′-кэпу. Существование последовательности, отличающей стартовый AUG от внутренних совершенно необходимо, так как в противном случае инициация синтеза белка происходила бы хаотично на всех AUG-кодонах.
Процесс инициации обеспечивается специальными белками — факторами инициации (англ. initiation factors, IF ; инициаторные факторы эукариот обозначают eIF, от англ. eukaryotes ).
Механизмы инициации трансляции у про- и эукариот существенно отличаются: прокариотические рибосомы потенциально способны находить стартовый AUG и инициировать синтез на любых участках мРНК, в то время как эукариотические рибосомы обычно присоединяются к мРНК в области кэпа и сканируют её в поисках стартового кодона.
У прокариот
Малая рибосомная субъединица (30S) прокариот, если она не вовлечена в данный момент в трансляцию, существует в комплексе с инициаторными факторами IF1, IF3, и, в некоторых случаях, IF2. Рассмотрим основные функции этих белков:
Комплекс 30S субчастицы с инициаторными факторами способен узнавать специальные последовательности мРНК, так называемые участки связывания рибосомы (англ. RBS, ribosome-binding site ). Эти участки содержат, во-первых, инициаторный AUG, и, во-вторых, специальную последовательность Шайна — Дальгарно с которой комплементарно связывается рибосомная 16S РНК. Последовательность Шайна — Дальгарно служит для того, чтобы отличать инициаторный AUG от внутренних кодонов, кодирующих метионин. После того, как 30S-субъединица связалась с мРНК к ней привлекается инициаторная аминоацил-тРНК и IF2, если они ещё не были включены в комплекс. Затем присоединяется 50S-субчастица, происходит гидролиз ГТФ и диссоциация инициаторных факторов. Собранная рибосома начинает синтезировать полипептидную цепь.
У эукариот
У эукариот существуют два механизма нахождения рибосомой стартового AUG: кэп-зависимый (сканирующий) и кэп-независимый (внутренняя инициация).
Также у эукариот возможна реинициация трансляции, когда после окончания трансляции рибосома с белковыми факторами не диссоциирует от мРНК, а перескакивает с 3′ на 5′ конец мРНК и начинает инициацию ещё раз. Такое возможно благодаря замкнутой кольцевой форме мРНК в цитоплазме.
Кэп-зависимый механизм
В отличие от прокариот, инициация трансляции у которых обеспечивается лишь тремя белковыми факторами, трансляция подавляющего большинства мРНК эукариот, содержащих 5′-кэп [m7G(5′)ppp(5′)N] и 3′ поли(А)-хвост, требует участия, по крайней мере, 13 общих эукариотических факторов инициации (eIF), представленных 31 полипептидом. Инициация трансляции включает события между диссоциацией рибосомы во время терминации в предыдущем цикле трансляции и сборкой рибосомы, готовой к элонгации, на старт-кодоне мРНК. Во время инициации аппарат трансляции решает следующие задачи:
Диссоциация и антиассоциация субъединиц рибосом
Cелекция инициаторной метионил-тРНК (Met-tRNAiMet)
Этот этап включает в себя следующие процессы:
В ходе процесса (а), метионил-тРНК-синтетаза взаимодействует как с акцепторным концом тРНК, так и с антикодоном.
Процесс (б) у растений и дрожжей осуществляется с помощью посттранскрипционной модификации tRNAiMet, которая делает её отличной от элонгаторной метионин-специфичной тРНК с помощью присоединения 2′-О-фосфорибозила к рибозе нуклеотида А64. У позвоночных процесс (б) осуществляется путём дискриминации между специфическими особенностями нуклеотидных последовательностей tRNAiMet и элонгаторной метиониновой тРНК.
Элонгация
В процессе наращивания полипептидной цепи принимают участие два белковых фактора элонгации. Первый (EF1a у эукариот, EF-Tu — у прокариот) переносит аминоацилированную (заряженную аминокислотой) тРНК в А (аминоацил)-сайт рибосомы. Рибосома катализирует образование пептидной связи, происходит перенос растущей цепи пептида с Р-сайтовой тРНК на находящуюся в А-сайте, пептид удлиняется на один аминокислотный остаток. Затем второй белок (EF2 у эукариот, EF-G — у прокариот) катализирует так называемую транслокацию. Транслокация — перемещение рибосомы по мРНК на один триплет, в результате которого пептидил-тРНК оказывается вновь в Р-сайте, а «пустая» тРНК из P-сайта переходит в Е-сайт (от слова exit). Цикл элонгации завершается, когда новая тРНК с нужным антикодоном приходит в A-сайт. [источник не указан 1309 дней]
Терминация
Компартментализация у эукариот
В отличие от прокариот, у которых биосинтез белка происходит непосредственно во время транскрипции соответствующих мРНК, для эукариот характерна строгая компартментализация всех процессов, происходящих во время биосинтеза белка, в том числе и компартментализация трансляции.
Трансляция мРНК секреторных и мембранных белков (обычно они составляют 3—15 % от всех синтезируемых клеткой белков) происходит на рибосомах, связанных с гранулярной эндоплазматической сеткой. [14] По классическим представлениям, ещё 35—45 % рибосом связаны с цитоскелетом, а оставшиеся 20—40 % рибосом находятся в несвязанном состоянии в цитозоле. [15] Однако высказываются предположения, что свободные рибосомы являются артефактом, и в клетке они связаны с так называемой микротрабекулярной решеткой, образованной особым типом филаментов. [16] Впрочем, по другим данным, само существование микротрабекулярной решетки ставится под сомнение, [17] так что вопрос о существовании активных несвязанных рибосом остаётся открытым.
В настоящее время высказывается гипотеза, что трансляция у эукариот происходит не во всей цитоплазме клетки, а в отдельных областях цитоплазмы, условно называемых «трансляционными компартментами». [18] Предположительно, в состав трансляционного компартмента входят следующие структуры:
Компартментализация трансляции обеспечивает высокую скорость биосинтеза белка и широкие возможности регуляции этого процесса. [18]
Трансляция
Под трансляцией в биологии понимают синтез из аминокислот полипептидов, который протекает в цитоплазме на рибосомах при участии 1) мРНК в качестве матрицы, 2) тРНК в качестве переносчика аминокислот, а также 3) ряда белковых факторов, выполняющих каталитическую функцию на разных этапах процесса. Трансляция протекает в клетках всех живых организмов, это фундаментальный процесс живой природы.
С информационной точки зрения трансляцию можно определить как механизм перевода последовательности триплетов мРНК в последовательность аминокислот белка.
Функция рибосом состоит в удерживании в нужном положении мРНК, тРНК и белковых факторов до тех пор, пока не произойдет определенная химическая реакция. Чаще всего это образование пептидной связи между соседними аминокислотами.
Трансляция и биосинтез белка обычно означают одно и то же. Однако, когда говорят о биосинтезе белка, то нередко в него включают посттрансляционные модификации полипептидов (приобретение ими вторичной, третичной и четверичной структур), а также иногда могут включать процесс транскрипции. С этой точки зрения трансляция рассматривается как важный этап в биосинтезе белков.
Процесс трансляции у эукариот и прокариот имеет ряд отличий, в основном связанный с разнообразием и активностью белковых факторов.
На одной цепочке мРНК может находится несколько рибосом, образуя полисому. При этом сразу происходит синтез нескольких идентичных полипептидов (но каждый находится на своей стадии синтеза).
Синтез одного белка обычно длится несколько секунд.
Аминокислоты, из которых синтезируется полипептид, обязательно проходят стадию активации. Сам же процесс трансляции включает три стадии: инициацию, элонгацию и терминацию.
Процесс трансляции обладает свойством специфичности. Во-первых, определенным кодонам мРНК соответствуют свои тРНК. Во вторых, аминокислоты присоединяются только к «своим» тРНК.
Активация аминокислот
Активация аминокислот необходима, так как только в таком состоянии они способны соединяться с тРНК и позже образовывать между собой пептидные связи.
В цитоплазме клеток всегда находятся свободные (не соединенные с другими веществами) аминокислоты. Специфичные ферменты в присутствии АТФ преобразуют аминокислоту в аминоациладенилат, который уже способен соединяться с тРНК.
Существует класс ферментов – аминоацил-тРНК-синтетазы, – которые активируют аминокислоты, используя при этом энергию АТФ. Каждая аминокислота активируется своим ферментом, после чего присоединяется только к своей тРНК. Образуется комплекс аминокислоты с тРНК – аминоацил-тРНК (аа-тРНК).
Инициация трансляции
Инициация трансляции включает следующие последовательно протекающие при участии факторов инициации этапы:
Присоединение 5′-конца мРНК к малой субъединице рибосомы. При этом стартовый кодон (AUG) размещается в недостроенном (из-за отсутствия большой субъединицы) P-сайте рибосомы.
Комплекс аа-тРНК с соответствующим антикодоном присоединяется к стартовому кодону мРНК. У эукариот кодон AUG кодирует аминокислоту метионин, у прокариот — формил-метионин. Позже эти стартовые аминокислоты вырезаются из готового полипептида.
Происходит объединение субъединиц рибосом, в результате чего достраиваются их P- и A-сайты.
Таким образом, на этапе инициации происходит распознавание рибосомой стартового кодона и подготовка к началу синтеза.
Образующаяся связь между рибосомой и мРНК обратима, мРНК после синтеза полипептида может быть отсоединена от рибосомы. В последствии мРНК используется еще раз или разрушается специальными ферментами.
Стартовый кодон AUG отличается от других таких же кодонов в середине мРНК тем, что перед ним находится кэп и определенные нуклеотидные последовательности. Именно благодаря им AUG распознается как стартовый. (Это касается в основном эукариот.)
Элонгация трансляции
На этом этапе происходит непосредственный синтез полипептидной цепочки. Процесс элонгации состоит из множества циклов. Один цикл элонгации — это присоединение одной аминокислоты к растущей полипептидной цепочке.
Уже на этапе инициации P-сайт рибосомы оказывается занятым первой тРНК, несущей аминокислоту метионин. В первом цикле элонгации в A-сайт рибосомы заходит второй комплекс aa-тРНК. Это будет та тРНК, чей антикодон комплементарен следующему (за стартовым AUG) кодону.
A(аминоацил)- и P(пептидил)-сайты располагают комплексы аа-тРНК так, что между аминокислотами протекает химическая реакция, и образуется пептидная связь.
После этого первая (находящаяся в P-сайте) тРНК освобождается от своей аминокислоты. В результате последняя оказывается связанной только со второй аминокислотой пептидной связью. Вторая аминокислота связана со второй тРНК, находящейся в A-сайте.
Рибосома перемещается по нити мРНК на один триплет. При этом первая т-РНК оказывается в E-сайте (exit) рибосомы, после чего покидает ее. Вторая т-РНК, связанная с двумя аминокислотами, переходит в P-сайт. A-сайт освобождается для поступления третьего комплекса аа-тРНК.
Следующие циклы элонгации протекают аналогично первому. Когда A-сайт освобождается, в него может зайти аа-тРНК, чей антикодон комплементарен кодону мРНК, находящемся в этот момент в A-сайте.
Терминация трансляции
Терминация — это завершения синтеза полипептидной цепочки и ее отделение. Терминация наступает, когда рибосома встречает один из терминирующих кодонов (UAA, UAG, UGA), для которых не существует своих тРНК. Эти участки мРНК распознаются специальными белками — факторами терминации.
Трансляция (биология)
Трансляцией называют осуществляемый рибосомой синтез белка из аминокислот на матрице информационной (или матричной) РНК (иРНК или мРНК). Трансляция является финальной стадией реализации генетической информации.
Содержание
Механизм трансляции
Общая схема трансляции.
Инициация. 1. Узнавание стартового кодона (AUG), сопровождается присоединением тРНК аминоацилированной метионином (М) и сборкой рибосомы из большой и малой субъединиц.
Элонгация. 2. Узнавание текущего кодона соответствующей ему аминоацил-тРНК (комплементарное взаимодействие кодона мРНК и антикодона тРНК увеличено). 3. Присоединение аминокислоты, принесённой тРНК, к концу растущей полипептидной цепи. 4. Продвижение рибосомы вдоль матрицы, сопровождающееся высвобождением молекулы тРНК. 5. Аминоацилирование высвободившейся молекулы тРНК соответствующей ей аминоацил-тРНК-синтетазой. 6. Присоединение следующей молекулы аминоацил-тРНК, аналогично стадии (2). 7. Движение рибосомы по молекуле мРНК до стоп-кодона (в данном случае UAG).
Терминация. Узнавание рибосомой стоп-кодона сопровождается (8) отсоединением новосинтезированного белка и в некоторых случаях (9) диссоциацией рибосомы.
Синтез белка является основой жизнедеятельности клетки. Для осуществления этого процесса в клетках всех без исключения организмов имеются специальные органеллы — рибосомы. Рибосомы представляют собой рибонуклеопротеидные комплексы, построенные из 2 субъединиц: большой и малой. Функция рибосом заключается в узнавании трёхбуквенных ( трехнуклеотидных ) кодонов мРНК, сопоставлении им соответствующих аминокислот и присоединении этих аминокислот к растущей белковой цепи. Двигаясь вдоль молекулы мРНК рибосома распознает кодон за кодоном и синтезирует белок в соответствии с информацией, заложенной в молекуле мРНК.
Для узнавания аминокислот в клетке имеются специальные «адаптеры», молекулы транспортной РНК (тРНК). Эти молекулы, имеющие форму клеверного листа, имеют участок (антикодон), комплементарный кодону мРНК, а также другой участок, к которому присоединяется аминокислота, соответствующая этому кодону. Присоединение аминокислот к тРНК осуществляется в энегро-зависимой реакции ферментами аминоацил-тРНК-синтетазами, а получившаяся молекула называется аминоацил-тРНК. Таким образом, специфичность трансляции определяется взаимодействием между кодоном мРНК и антикодоном тРНК, а также специфичностью аминоацил-тРНК-синтетаз, присоединяющих аминокислоты строго к соответствующим им тРНК (например, кодону GGU будет соответствовать тРНК, содержащая антикодон ACC, а к этой тРНК будет присоединяться только аминокислота глицин).
Механизмы трансляции прокариот и эукариот существенно отличаются, поэтому многие вещества, подавляющие прокариотическую трансляцию в значительно меньшей степени действуют на трансляцию высших организмов, что позволяет использовать их в медицинской практике как антибактериальные средства безопасные для организма млекопитающих.
Процесс трансляции разделяют на
Рамка считывания
Инициация трансляции
Процесс инициации обеспечивается специальными белками — факторами инициации (англ. initiation factors, сокращённо IF; эукариотические инициаторные факторы обозначают eIF, от англ. eukaryotes).
Механизмы инициации трансляции у про- и эукариот существенно отличаются: прокариотические рибосомы потенциально способны находить стартовый AUG и инициировать синтез на на любых участках мРНК.
У эукариот существуют два механизма нахождения рибосомой стартового AUG. Наиболее распространён, так называемый сканирующий механизм, при котором рибосома, двигаясь вдоль молекулы мРНК от её 5′-конца «сканирует» один кодон за другим, пока не наткнётся на инициаторный AUG. Для привлечения рибосомы к 5′-концу мРНК требуется специальная структура, кэп — 7-метилгуанин, прикреплённый к 5′-концевому нуклеотиду мРНК.
Второй механизм эукариотической инициации трансляции не требует наличия кэп-структуры и позволяет инициировать трансляцию с внутреннего участка мРНК, называется IRES-зависимым механизмом. IRES (от англ. Internal Ribosomal Entry Site, участок внутренней посадки рибосомы) — участок мРНК, обладающий выраженной вторичной стуктурой, позволяющей ему направлять рибосомы на стартовый AUG. По IRES-зависимому механизму инициируется синтез лишь на небольшой части клеточных мРНК, а также на РНК некоторых вирусов.
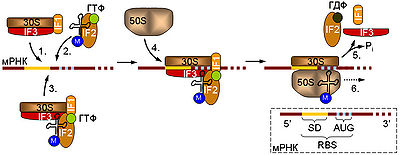
Схема инициации трансляции у прокариот.
Начальная стадия предусматривает связывание малой рибосомной субъединицы (30S) с мРНК. Это может происходить двумя способами: либо сначала к мРНК присоединяется комплекс, содержащий рибосомную субчастицу (1), а затем к нему привлекается тРНК в комплексе с IF2 и ГТФ (2), либо 30S субъединица изначально связывается с тРНК, а уже потом садится на мРНК (3). К образовавшемуся комплексу приходит большая (50S) рибосомная субъединица (4), инициаторные факторы отсоединяются от 30S субчастицы, что сопровождается гидролизом ГТФ белком IF2 (5), и собранная рибосома начинает элонгировать цепь (6). В правом нижнем углу дана схема инициаторного участка прокариотической мРНК. Отмечены 5′ и 3′ концы молекулы. RBS — сайт связывания рибосомы, SD — последовательность Шайн-Дальгарно, AUG — инициаторный кодон.
Механизм инициации трансляции у прокариот
Малая рибосомная субъединица (30S) прокариот, если она не вовлечена в данный момент в трансляцию, существует в комплексе с инициаторными факторами IF1, IF3, и, в некоторых случаях, IF2. Рассмотрим основные функции этих белков:
Комплекс 30S субчастицы с инициаторными факторами способен узнавать специальные последовательности мРНК, так называемые участки связывания рибосомы (англ. RBS — ribosomt-binding site). Эти участки содержат, во-первых, инициаторный AUG, и, во-вторых, специальную последовательность Шайн-Дальгарно с которой комплементарно связывается рибосомная 16S РНК. Последовательность Шайн-Дальгарно служит для того, чтобы отличать инициаторный AUG от внутренних кодонов, кодирующих метионин. После того, как 30S-субъединица связалась с мРНК к ней привлекается инициаторная аминоацил-тРНК и IF2, если они еще не были включены в комплекс. Затем присоединяется 50S-субчастица, происходит гидролиз ГТФ и диссоциация инициаторных факторов. Собранная рибосома начинает синтезировать полипептидную цепь.
Кэп-зависимый механизм инициации трансляции у эукариот
При помощи этого механизма транслируется подавляющее число эукариотических мРНК. Белки, принимающие участие в процессах инициации трансляции у эукариот называют eIF’s (англ. eukaryotic Initiation Factors, эукариотические факторы инициации). Помимо инициаторных факторов eIF1, eIF2 и eIF3, связывающихся с малой рибосомной субъединицей (40S), и по своим функциям приблизительно аналогичным соответствующим белкам прокариот, у эукариот появляется еще две группы факторов инициации: семейство факторов, связывающих мРНК — eIF4, и семейство факторов, связывающихся с большой (60S) субъединицей рибосомы, eIF5. Перечислим эти основные инициаторные факторы:
Элонгация
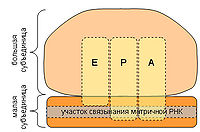
Схема РНК-связывающих участков рибосомы. Буквами обозначены участки связывания тРНК. А — аминоацил-тРНК-связывающий участок, Р — пептидил-тРНК-связывающий участок, Е — участок отсоединения тРНК от рибосомы ( англ. exit ).
В процессе наращивания полипептидной цепи принимают участие два белковых фактора элонгации. Первый (EF1a у эукариот, EF-Tu — у прокариот) переносит заряженную тРНК в А (аминоацил)-сайт рибосомы. После формирования пептидной связи, что катализируется рРНК, и переноса связанной с тРНК пептида в из Р-сайта в А-сайт второй белок (EF2 у эукариот, EF-G — у прокариот) катализирует перемещение рибосомы на один триплет. Таким образом петидил-тРНК оказывается вновь в Р-сайте, а «пустая» тРНК в Р-сайте — в Е-сайте. Цикл элонгации завершается, когда новая тРНК с антикодоном, подходящим к кодону в А-сайте доставлена EF1a (или EF-Tu).
Терминация
Примечания
Литература
Репликация ДНК: инициация
Время от времени ДНК размножается путём самоудвоения. Этот процесс называется репликацией ДНК. Репликация делится на 3 этапа: инициация (начало), элонгация (продолжение), терминация (окончание).
Репликация ДНК — это построение двух новых (дочерних) молекул ДНК на основе одной старой (родительской) молекулы с помощью матричного синтеза по принципу комплементарности. Новые молекулы состоят из одной старой и одной новосинтезированной нитей ДНК и почти ничем не отличаются от старой родительской молекулы, т.е. являются её точными копиями («репликами»).
С чего начинается процесс репликации ДНК?
Репликация начинается с инициации.
Теперь надо определить, с какого именно места начать дублирование ДНК, т.е. репликацию. Ошибаются те, кто думает, что инициация начинается от начала молекулы ДНК, но ошибаются также и те, кто думает, что она начинается с конца. На самом деле инициация начинается с множества точек, раскиданных по всей длине молекулы ДНК. Таких «запальных точек» может быть 5-50 на одну молекулу ДНК.
ДНК-реплицирующий комплекс включает в себя около 20 компонентов. Отметим главные из них.
Геликаза (хеликаза) расплетает ДНК на две отдельные цепи. Образуется репликативная вилка. По-видимому, при этом данный участок расплетённой ДНК отделяется от хромосомных белков. На разъединение комплементарной связи в каждой паре нуклеотидов тратится энергия 2-х молекул АТФ.
Молекула ДНК жестко закреплена в некоторых учакстках на ядерном матриксе и поэтому не может свободно вращаться при расплетании. Это блокирует продвижение геликазы по цепи.
Топоизомераза надрывает одну из двух нитей ДНК, и она раскручивается вокруг целой нити. Так снимается структурное напряжение при раскручивании спирали. Затем разорванные концы сращиваются обратно тем же ферментом. У бактерий другой вид топоизомеразы (гираза) разрывает сразу обе цепи ДНК, а после раскручивания спирали соединяет их вновь. Надо сказать, что в этом случае бактерии действуют более эффективно, чем человек вместе со всеми остальными эукариотами!