Что такое инициаторы полимеризации
Радикальная полимеризация
Радикальная полимеризация — это процесс образования полимера по свободнорадикальному механизму с последовательным присоединением молекул мономера к растущему макрорадикалу.
Радикальная полимеризация возможна для большинства виниловых, винилиденовых, диеновых мономеров, а также для некоторых напряженных циклических соединений.
Некоторые ненасыщенные мономеры не способны полимеризоваться по радикальному механизму вследствие стерических затруднений (напр., 1,2-дизамещенные виниловые мономеры) или в случае вырожденной передачи цепи, например пропилен, аллильные мономеры.
Как цепной процесс радикальная полимеризация включает в себя следующие стадии:
На стадии инициирования образуются первичные радикалы мономера в результате непосредственного энергетического воздействия (тепло, УФ либо ионизирующее излучение; или чаще при взаимодействии мономера с радикалами, возникающими при гомолитическом распаде специально вводимых веществ-инициаторов радикальных (напр., пероксидов, гидропероксидов, азосоединений).
Для увеличения скорости инициирования при низких температурах к пероксидам добавляют восстановители, например, соли переходных металлов или амины (так называемые окислительно-восстановительные инициаторы).
Для инициирования радикальной полимеризации обычно применяют вещества, которые легко распадаются на свободные радикалы.
Такие вещества называют инициаторами и вводят в реакцию в малых количествах (менее 1% от массы мономера).
Инициаторами радикальной полимеризации являются, например, органические пероксиды R-О-О-R.
При получении полиэтилена под высоким давлением для иницииpования используют кислород, который, являясь окислителем, ведет к образованию органических пероксидов ROOR и гидропероксидов ROOH.
Иницииpование может происходить также под действием различных видов излучения (ультрафиолетовое, радиационное) или повышенной температуры.
Механизм радикальной полимеризации
I стадия: инициирование (превращение части молекул мономеров в свободные радикалы).
Эта стадия включает 2 реакции:
1. Распад инициатора.
Инициаторы типа R-O-O-R при небольшом нагревании разлагаются с симметричным (гомолитическим) разрывом неполярной связи O-O и образованием свободных радикалов R-О• или R•.
Радикалы RO• или R•, образовавшиеся при распаде инициатора, присоединяются к молекулам мономера и превращают их в радикалы:

III стадия: обрыв цепи (взаимодействие радикальных частиц с образованием неактивных макромолекул).
Например:

Так, значительное увеличение вязкости реакционной среды ограничивает в первую очередь диффузионную подвижность макрорадикалов и, следовательно, снижает скорость обрыва, приводя к увеличению скорости радикальной полимеризации и молекулярной массы образующегося полимера (гель-эффект).
При образовании нерастворимого полимера подобные явления проявляются уже в начале процесса вследствие иммобилизации («застревания») растущих цепей в матрице полимера.
В радикальной полимеризации широко используют полифункциональные инициаторы, мономеры, агенты передачи цепи, повторное участие которых в ходе полимеризации изменяет структуру полимера или кинетические характеристики.
Так, полиинициаторы способны придавать радикальной полимеризации кинетические закономерности поликонденсации, из полифункциональных мономеров образуются сшитые полимеры, а введение полифункциональных агентов передачи цепи приводит к получению звездообразных полимеров.
Радикальная полимеризация может быть осуществлена в массе, эмульсии, суспензии, растворе и др. средах.
Что такое инициаторы полимеризации
Поливинилхлорид (ПВХ) – термопластичный полимер, получаемый из винилхлорида. Это наиболее распространённый и универсальный полимер, который входит в мировые лидеры по потреблению среди полимерных материалов. Поливинилхлорид (ПВХ) является наиболее востребованным крупнотоннажным полимером. Производится в основном суспензионным методом. В настоящее время отечественные производители суспензионного ПВХ не в полной мере удовлетворяют потребности рынка и закупают его за рубежом [1]. В этой связи повышение производительности существующих установок получения суспензионного ПВХ является важной и актуальной задачей [2].
Для инициирования реакции полимеризации применяют специальные вещества, при распаде которых образуются радикалы, зарождающие цепь. В процессе полимеризации ПВХ растет концентрация полимера, возрастает вязкость системы, вследствие чего уменьшается подвижность макрорадикалов в системе, что приводит к уменьшению скорости обрыва растущей цепи. В результате этого происходит самопроизвольное увеличение скорости реакции («гель-эффект»), а также усиливается тепловыделение. Данный эффект оказывает отрицательное влияние на процесс, так как он приводит к расширению молекулярно-массового распределения.
Для того чтобы избежать таких негативных явлений, необходимо поддерживать постоянную температуру процесса, обеспечить оптимальный теплосъем, сохранять постоянной скорость полимеризации до конца процесса. Это возможно достичь при использовании системы инициаторов, которые обеспечивают генерирование свободных радикалов и поддерживают их на необходимом уровне в течение всего процесса.
В производстве суспензионного ПВХ в качестве инициаторов используют различные мономерорастворимые пероксидные соединения: пероксиды алифатических кетонов, диацилпероксиды, персульфаты щелочных металлов, пероксиэфиры и другие.
Многообразие применяемых инициаторов вызвано тем, что применение каждого из них позволяет получать полимер с различной молекулярной массой с сохранением оптимальных условий работы реакторов.
Наиболее широкое распространение в качестве эффективных инициаторов суспензионной полимеризации винилхлорида нашли пероксидикарбонаты, такие как дибутил-, диизопропил-, дицетилперокси-дикарбонаты. Их применение позволяет сократить время процесса, улучшить теплосъем. Однако применение индивидуальных пероксидикарбонатов не всегда обеспечивает оптимальные условия полимеризации; последнее обусловлено, прежде всего, характером неравномерного тепловыделения в процессе полимеризации [3]. Также наблюдается неоднородность частиц ПВХ по структуре, что проявляется в виде дефектов структуры («рыбий глаз», стекловидные точки).
В последнее время в качестве инициаторов широкое применение получили смеси двух и более различных по строению и активности пероксидов, например лаурилпероксид и пероксидикарбонат. Смесь нескольких инициаторов позволяет сократить длительность процесса за счет выравнивания скорости полимеризации, однако данный подход не позволяет получить полимер с однородной структурой.
При синтезе поливинилхлорида также важна природа инициатора и его концентрация, способ ввода в реагирующую систему. Например, применение ступенчатого температурного режима, заключающегося в поддержании повышенной температуры процесса, которая выше на 8–12 °C начальной температуры полимеризации, в течение 60 минут после начала падения давления в автоклаве позволяет сократить длительность полимеризационного цикла на 13,3–20 % и повысить выход полимера с 80 до 90 % по сравнению с использованием индивидуального инициатора ПДЭГ при постоянном температурном режиме полимеризации [4].
Правильно подобранный инициатор позволяет получить оптимальные значения времени полимеризации и выхода продукта, а также таких качественных показателей полимера, как константы Фикентчера, массы поглощения пластификатора (МПП), времени поглощения пластификатора (ВПП), термостабильности и т.д.
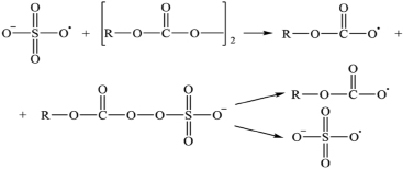
Рис. 1. Механизм образования интермедиата
В существующих производствах используются индивидуальные инициаторы. Для интенсификации процесса полимеризации винилхлорида нами предлагается использование двойной системы инициаторов: ди-2-этилгексилпероксидикарбонат-персульфат калия.
Необходимость применения персульфата калия обусловлена взаимодействием персульфат-иона с инициатором ди-2-этилгексилпероксидикарбонатом, в результате чего происходит образование нового промежуточного соединения – интермедиата. Энергия активации распада нового соединения меньше, чем у исходного инициатора, в результате чего повышается инициирующая способность и, как следствие, ускоряется процесс полимеризации винилхлорида. Механизм данного взаимодействия представлен ниже (рис. 1).
Промежуточным продуктом данной реакции является сульфоперекись, которая в соответствии с литературными данными [5] по своей активности превосходит перкарбонаты. В результате данного взаимодействия молекула ПДЭГа распадается на два свободных радикала, которые, в свою очередь, инициируют процесс полимеризации винилхлорида. Также в работе [5] было показано, что концентрация основного инициатора 0,06 % от ВХ обеспечивает наилучшее сочетание скорости процесса и качества полимера.
Материалы и методы исследования
В реактор объемом 0,005 м3, снабженный мешалкой, в соответствии с рецептурой поливинилхлорида марки ПВХ-С-7059М загружают 2170 г холодной обессоленной воды; 1670 г винилхлорида; 0,13 г Агидола-1 (присадка антиокислительная); 3,34 г эмульгатора «метоцел»; 0,12 гидрокарбоната натрия; а также 1,002 г ПДЭГ (0,06 % от ВХ); 0,17 г персульфата калия (0,01 % от ВХ). Бикарбонат натрия используется для создания в реакторе щелочной среды, что способствует снижению коркообразования. Агидол является антиокислительной присадкой, применяется для регулирования скорости реакции, способствует повышению термостабильности ПВХ. После завершения загрузки реактора исходными компонентами начинается разогрев реакционной массы для инициирования реакции полимеризации. При включенной мешалке исходную смесь нагревают до 54 °C. По прошествии времени, необходимого для осуществления полимеризации винилхлорида, давление в реакторе падает до величины порядка 0,14 МПа и полимеризация прекращается. Оценивают длительность процесса полимеризации и эффективность применяемой системы инициаторов, определяя в процентах сокращение времени синтеза по сравнению с контрольным опытом без использования соинициатора. Далее полученную смесь охлаждают, сдувают непрореагировавший винилхлорид. После выгрузки реактора его содержимое промывают водой, сушат и определяют выход продукта.
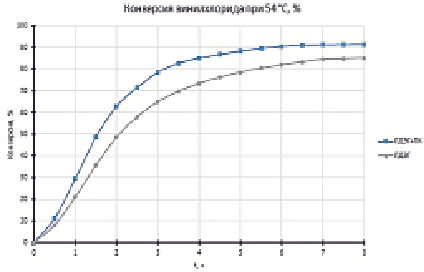
Рис. 2. Конверсионная зависимость суспензионной полимеризации винилхлорида в присутствии инициирующих систем: ПДЭГ + ПК и ПДЭГ
Результаты исследования и их обсуждение
Проведенные лабораторные испытания показывают, что в результате использования двухкомпонентной инициирующей системы время процесса сокращается с 7,0 до 6,5 часов, а выход поливинилхлорида повысился в свою очередь с 85,0 до 91,0 %. Конверсионная зависимость винилхлорида в зависимости от времени проведения процесса представлена на рис. 2.
Скорость реакции полимеризации, отражающая интенсивность превращения винилхлорида за единицу времени, была получена в результате обработки ниже представленных кинетических зависимостей. На рис. 3 видно, что использование комплексной инициирующей системы ПДЭГ + ПК позволяет повысить скорость процесса полимеризации, поддерживать ее значение в течение более длительного промежутка времени, чем при использовании индивидуального инициатора ПДЭГ.
Также было изучено влияние концентрации персульфата калия на продолжительность и выход суспензионной полимеризации винилхлорида. Результаты представлены в таблице.
Полученные в ходе лабораторных опытов образцы поливинилхлорида идентичны по своим физико-химическим качествам и удовлетворяют техническим требованиям, предъявляемым к товарному поливинилхлориду марки ПВХ-С-7059М.
На основе проведённых исследований можно сделать вывод об эффективности применения в качестве инициатора ди-2-этилгексилпероксидикарбоната при сочетании с соинициатором персульфатом калия. Данное изменение рецептуры позволит добиться сокращения процесса полимеризации на 0,5 часа, а также повысить выход поливинилхлорида.
Влияние концентрации водорастворимого соинициатора на продолжительность суспензионной полимеризации винилхлорида (Т = 54 °C, ПДЭГ – 0,06 % от ВХ)
Что такое инициаторы полимеризации
Лекция 11 РАДИКАЛЬНАЯ ПОЛИМЕРИЗАЦИЯ

Инициированная полимеризация непредельного соединения включает в себя следующие стадии:
1
r · + CH2=CHX 
R1 · + M
Rn · + M
Rn · + Rm · 
При выводе кинетических соотношений обычно делаются следующие 4 допущения:
1. Рассматривается случай, когда полимеризация протекает с длинными цепями, т.е.скорость полимеризации v >> vi;
для высокомолекулярных радикалов, так как реакционная способность радикала определяется его молекулярной структурой вблизи свободной валентности, а при гомополимеризации строение всех макрорадикалов одинаково и различаются они только своей длиной.
При распаде инициатора в конденсированной фазе образуются два радикала, окруженные молекулами растворителя или мономера (при полимеризации в массе). Часть таких пар погибает в клетке (вступает в реакции рекомбинации или диспропорционирования), а часть выходит в объем. Если с мономером реагируют все вышедшие в обьем радикалы, то скорость инициирования равна скорости генерирования радикалов: vi = 2ekd [I]. Если часть радикалов инициатора, вышедших в обьем, реагирует с макрорадикалами, то vi растет с ростом [M], пока не достигает значения 2 ekd [I]. В литературе описаны такого рода примеры. На выход радикалов в объем концентрация мономера практически не влияет, так как рекомбинация радикальных пар в клетке протекает неизмеримо быстрее, чем реакция радикала с мономером.
In 
Реакция продолжения цепи определяет как скорость полимеризации, так и строение образующегося полимера. Виниловые мономеры полимеризуются по типу голова к хвосту (см. выше). Константа скорости продолжения цепи kp определяется активностью мономера и ведущего цепную реакцию макрорадикала. Ниже приведены константы скорости kp для ряда мономеров :
С повышением температуры заметную роль начинает играть реакция деполимеризации, т.е. распада макрорадикала на мономер и радикал
R n · 
Tmax = 
Обрыв цепей, как это видно из схемы, происходит в результате реакции между макрорадикалами. Эти радикалы вступают между собой в реакции двух типов, а именно рекомбинации:
От соотношения между константами скорости этих двух реакций зависит средняя степень полимеризации 
P = kp[M] 

Это соотношение влияет и на молекулярно-массовое распределение: M w /Mn = 1.5 при рекомбинации R · и M w /Mn = 2 при их диспропорционировании.
По-видимому, в большинстве случаев именно сегментальная подвижность лимитирует скорость и определяет величину константы скорости гибели макрорадикалов.

Молекулярная масса образующегося полимера зависит не только от скорости и способа гибели макрорадикалов, но и от реакции передачи цепи, когда рост макрорадикала прекращается, а цепная реакция полимеризации продолжается, например:
Такая передача цепи на мономер характеризуется константой передачи цепи C м =k м /kp ; Она не влияет на скорость цепной полимеризации (если все образовавшиеся в этой реакции радикалы реагируют с мономером), но, естественно, отражается, на степени полимеризации:


Накапливающийся при полимеризации полимер также может участвовать в реакции передачи цепи:
В результате возникают разветвленные макромолекулы.
В передаче цепи может принимать участие растворитель S или специальный агент (например, CСl 4 ), вступающий с макрорадикалом в реакцию отрыва, замещения или присоединения, например:
Степень полимеризации, естественно, уменьшается с ростом [S] и связана с ней соотношением:


r · + M
R · + M
r · + Z
R · + Z
Z · + M
R · + R · 
R · + Z · 
Z · + Z · 
1. Инигибитор не реагирует с радикалами инициатора, не участвует в продолжении цепи, и все цепи обрываются на молекулах ингибитора, т. е. выполняются неравенства:
В этом случае в квазистационарном режиме vi = 2kde[I] = fkZ[Z][R · ] и скорость радикальной полимеризации
v = 2kde[I](1 + 
а степень полимеризации P = 1 + 
— 
In 
Поскольку ингибитор расходуется со скоростью инициирования (а точнее, скоростью vi/f ), то скорость во времени будет нарастать в соответствии с уравнением (здесь v = v0 при t = 0):
а кинетика расходования мономера, пока в системе есть ингибитор, описывается формулой:
2. Ингибитор не участвует в продолжении цепи, и все цепи обрываются на ингибиторе, но Z реагирует с радикалами инициатора. В этом случае скорость инициирования vi = kr[M][r · ] [I]. Образующиеся из инициатора радикалы реагируют как с мономером, так и с ингибитором, так что скорость инициирования
vi = 
и скорость полимеризации (при длинных цепях) равна
v = 
или после преобразования:




где w = v/v0 в момент t, a w = w0 в момент t = 0, v0 = v при [Z]=0. Экcпериментальные данные согласуются с этой формулой.
Скорость полимеризации при длинных цепях равна:
v=kpZ[M[(1 + 

Как показал эксперимент, во многих случаях коэффициент j настолько велик, что эта зависимость приобретает достаточно простой вид:


Константы скорости реакций полимерных радикалов с хиноном kZ меняются в диапазоне 10 3 ё 10 5 л/моль с.
Нитросоединения тормозят полимеризацию таких мономеров, как стирол и винилацетат, но слабо влияют на полимеризацию таких мономеров, как метилметакрилат и метилакрилат. Механизм торможения полимеризации нитросоединениями в некоторых своих моментах остается неясным. Первичный акт заключается в присоединении нитрогруппы к макрорадикалу:
Для образовавшегося радикала предполагается четыре альтернативных реакции превращения:
Нитрозобензол, в свою очередь, также является ингибитором и реагирует с макрорадикалами:
C6H5N=O 

R · + RAr · H ® RH + RAr
Ниже приведены значения kZ/kp для ряда ArH.
| Мономер | Стирол | Метилакрилат | Винилацетат |
| Антрацен | 2.0 (317К) | 0.098 (323) | 36.5 (328) |
| 3.4-Бензпирен | 14.0 (317К) | 30.6 (323) | |
| Тетрацен | 862 (323) |
Тормозят полимеризацию, обрывая цепи, 1,3,5-трифенилвердазильные радикалы. Однако, эти радикалы могут участвовать и в инициировании, реагируя с двойной связью мономера (акрилонитрила). Кроме того, они взаимодействуют с пероксидами. Далеко не всегда по расходованию ДФПГ можно оценить скорость генерирования радикалов в системах, где идет полимеризация. винилацетата.
Как уже отмечалось (см. выше), в радикальной полимеризации существенно важна реакция передачи цепи и чем интенсивней она протекает, тем меньше молекулярная масса полимера. Передатчиками цепи являются разнообразные реагенты, которые, реагируя с макрорадикалами, расходуются. каталитическая передача цепи была открыта на порфириновых комплексах кобальта. Эти комплексы очень быстро реагируют с макрорадикалами полимеризующегося метилметакрилата (константа передачи цепи составляет 0.3 + 3.6 ґ 10 3 для порфириновых комплексов разного строения при 333К), многократно (10 4 ё 10 6 раз), участвуя в передаче цепи. Предполагается следующий (гидридный) механизм катализа порфирином (CoII):
Передача цепи через порфирин кобальта сопровождается ингибированием полимеризации. Предполагается, что обрыв цепей происходит по реакции макрорадикала с гидридом CoII
R · + HСo(II) ® RH + Co(II)
Обрыв цепей происходит многократно: f = 70 при [CH 2=C(CH3)CO2-CH3 ] = 0.5 моль/л и f = 23 при концентрации мономера 7 моль/л (333К, бензол, инициатор АИБН, глубина полимеризации 10% ).
RСo(II) ® R · + Co(II) или
RСo(II) ® R’CH=CHR” + HCo (II)
Элементарные стадии многократного обрыва цепей и обратимого ингибирования является пока гипотетическими.

В технологии получения полимерных изделий часто возникает задача регулировать полимеризацию на глубоких стадиях. Разработан ряд кинетических приемов, позволяющих стабилизировать скорость полимеризации на глубоких стадиях. Ниже дано их краткое изложение.
R · + R · и R · + Z изменяется, и главным каналом обрыва цепей становится реакция макрорадикалов с ингибитором (выполняется неравенство (2 kivi) 1/2 [Z]). В качестве малоэффективных ингибиторов можно использовать нитросоединения и ароматические углеводороды.
2. Метод фотоингибирования предусматривает воздействие света на малоэффективный ингибитор.полимеризации Z, превращающее его в высокоэффективный ингибитор. В отсутствие света такой ингибитор практически не участвует в обрыве цепей. Поглощая квант света малоэффективный ингибитор. переходит в триплетно-возбужденное состояние и в таком состоянии быстро реагирует с макрорадикалом:
Снижение скорости полимеризации на глубоких стадиях достигается включением света, который поглощается ингибитором, в результате чего усиливается обрыв цепей на ингибиторе. В качестве фотоингибиторов можно использовать многоядерные ароматические углеводороды, алкилнитриты, серу.
4. Введение кислорода в систему, содержащую акцепторы пероксидных радикалов. Такие соединения, как фенолы и ароматические амины очень медленно реагируют с макрорадикалами и практически не тормозят полимеризацию. Однако с пероксирадикалами эти соединения реагируют быстро (см. Лекцию 14). Поэтому полимеризацию на глубоких стадиях можно тормозить, введя сначала в мономер такого типа акцептор пероксирадикалов InH, а на глубокой стадии, где необходимо снизить скорость полимеризации, ввести кислород. Интенсивное торможение обусловливают реакции:
RO2 · + InH ® ROOH + In ·
In · + In · ® молекулярные продукты.

1. Бемфорд К., Барб У., Дженкинс А., Оньон П., Кинетика радикальной полимеризации винильных соединений, Москва, Изд-во иностр. лит., 1961.
2. Уоллинг Ч., Свободные радикалы в растворе, Москва, Изд-во иностр. лит., 1960.
3. Гладышев Г. П., Полимеризация винильных мономеров, Алма-Ата, Изд-во АН КазССР, 1964.
4. Бреслер С.Е., Ерусалимский Б. Л., Физика и химия макромолекул. Москва, Наука. 1965.
5. Хувинк Р., Ставерман А., Химия и технология полимеров. Москва, Химия, 1965.
6. Багдасарьян Х. С., Теория радикальной полимеризации. Москва, Изд-во АН СССР, 1966.
7. Comprehensive Chemical Kinetics. V. 14., Free-radical Polymerisation, Amsterdam, Els. Sc. Publ. Co., 1976.
8. Гладышев Г. П., Попов В. А., Радикальная полимеризация при глубоких степенях превращения. Москва, Наука, 1974.
9. Оудиан Дж., Основы химии полимеров, Москва, Мир, 1974.
10. Иванчев С. С., Радикальная полимеризация, Ленинград, Химия, 1985.
11. Денисов Е. Т., Константы скорости гомолитических жидкофазных реакций, Москва, Наука, 1971.