В результате чего образуются полипептиды
Пептиды
Пептиды (греч. πεπτος — питательный) — семейство веществ, молекулы которых построены из остатков α-аминокислот, соединённых в цепь пептидными (амидными) связями —C(O)NH—.
Это природные или синтетические соединения, содержащие десятки, сотни или тысячи мономерных звеньев — аминокислот. Полипептиды состоят из сотен аминокислот, в противоположность олигопептидам, состоящим из небольшого числа аминокислот (не более 10-50), и простым пептидам (до 10).
В 1900 году немецкий химик-органик Герман Эмиль Фишер выдвинул гипотезу о том, что пептиды состоят из цепочки аминокислот, образованных определёнными связями. И уже в 1902 году он получил неопровержимые доказательства существования пептидной связи, а к 1905 году разработал общий метод, при помощи которого стало возможным синтезировать пептиды в лабораторных условиях.
Постепенно учёные изучали строение различных соединений, разрабатывали методы разделения полимерных молекул на мономеры, синтезировали все больше и больше пептидов. На сегодняшний день известно более 1500 видов пептидов, определены их свойства и разработаны методы синтеза.
Содержание
Терминология: Олигопептиды и Полипептиды
Грань между олигопептидами и полипептидами (тот размер, при котором белковая молекула перестаёт считаться олигопептидом и становится полипептидом) достаточно условна. Часто пептиды, содержащие менее 10-20 аминокислотных остатков, называют олигопептидами, а вещества с большим числом аминокислотных звеньев — полипептидами. Во многих случаях эта грань в научной литературе не проводится вообще и небольшая белковая молекула (такая, как окситоцин) упоминается как полипептид (или просто как пептид).
История
Пептиды впервые были выделены из гидролизатов белков, полученных с помощью ферментирования.
В 1953 В. Дю Виньо синтезировал окситоцин, первый полипептидный гормон. В 1963 г., на основе концепции твердофазного пептидного синтеза (P. Меррифилд) были созданы автоматические синтезаторы пептидов. Использование методов синтеза полипептидов позволило получить синтетический инсулин и некоторые ферменты.
На сегодняшний день известно более 1500 видов пептидов, определены их свойства и разработаны методы синтеза.
Панкреатические молекулы полипептидного характера
Опиоидные пептиды
Лиганды опиоидных рецепторов были обнаружены и во многих периферических органах, тканях и биологических жидкостях. Присутствие опиоидов показано в гипоталамусе и гипофизе, плазме крови и спиномозговой жидкости, желудочно-кишечном тракте, лёгких, органах репродуктивной системы, иммунокомпетентных тканях и даже в коже. Наряду с эндорфинами обнаружены и так называемые экзорфины или параопиоиды — опиоидные пептиды, образующиеся при переваривании пищи. К настоящему времени опиоидные рецепторы и их эндогенные лиганды обнаружены практически во всех органах и тканях млекопитающих, а также у животных более низких ступеней классификации вплоть до простейших.
Основная часть опиоидных пептидов образуется путём внутриклеточного расщепления высокомолекулярных предшественников, что приводит к образованию ряда биологически активных фрагментов, в том числе и опиоидных пептидов. Идентифицированы и наиболее изучены 3 таких предшественника: проопиомеланокортин (ПОМК), проэнкефалин А и продинорфин (проэнкефалин В). В состав ПОМК (локализованного главным образом в гипофизе) входят аминокислотные последовательности b-липотропина, АКТГ, a-, b- и g-меланоцитстимулирующих гормонов, a-, b- и g-эндорфинов. В настоящее время установлено, что основным источником энкефалинов (метионин-энкефалина и лейцин-энкефалина) в организме является проэнкефалин А, локализованный преимущественно в надпочечниках. В его составе содержится 4 аминокислотные последовательности мет-энкефалина и одна лей-энкефалина, а также ряд продленных форм мет-энкефалина: меторфамид, МЕРГЛ (мет-энкефалин-Arg6-Gly7-Leu8), МЕРФ (мет-энкефалин-Arg6-Phe7), пептид Ф и группы родственных пептидов, входящих в состав пептида Е: BAM 22, 20, 18, 12, взаимодействующих с опиоидными рецепторами mu-, kappa- и delta-типа.
В структуре другого проэнкефалина — препроэнкефалина В (или продинорфина) — обнаружены последовательности a- и b-неоэндорфинов, динорфинов [динорфин 1-8, 1-17 (А), динорфин В (риморфин), 4кД-динорфин], обладающих наибольшим сродством к ОР k-типа, а также лей-энкефалина. Радиорецепторный анализ связывания эндорфинов и энкефалинов с опиоидными рецепторами показал, что сродство мет- и лей-энкефалинов к опиоидным рецепторам delta-типа выше, чем к рецепторам mu-типа; b-эндорфин имеет примерно одинаковое сродство к опиоидным рецепторам mu- и delta-типа, a- и g-эндорфины проявляют гораздо меньшее сродство к обоим типам рецепторов по сравнению с b-эндорфином. Несмотря на то, что мет-энкефалин взаимодействует преимущественно с опиоидными рецепторами d-типа, его аналоги с более длинной аминокислотной последовательностью — меторфамид и пептиды группы BAM (пептиды из мозгового вещества надпочечников) обладают противоположным профилем селективности взаимодействия с опиоидными рецепторами (mu > kappa > delta). Большинство эндогенных опиоидов в той или иной степени могут взаимодействовать с несколькими типами рецепторов. Так, b-эндорфин своим N-концевым фрагментом способен взаимодействовать с mu- и delta-опиоидными рецепторами, а С-концом с epsilon-рецепторами. В коже амфибий, а затем и в мозге и некоторых других органах теплокровных, обнаружен 4-й предшественник ОП — продерморфин, который считается источником дерморфина (mu-агониста) и дельторфина (delta-агониста). В ЦНС обнаружены эндогенные пептиды, специфически взаимодействующие с mu-опиоидными рецепторами: Tyr-Pro-Trp-Phe-NH2 и Tyr-Pro-Phe-Phe-NH2, названные эндоморфинами, а также пептид ноцицептин, оказывающий свой анальгетический эффект через опиоидоподобные орфановые рецепторы.
Свойства пептидов
Пептиды постоянно синтезируются во всех живых организмах для регулирования физиологических процессов. Свойства пептидов зависят, главным образом, от их первичной структуры — последовательности аминокислот, а также от строения молекулы и её конфигурации в пространстве (вторичная структура).
Классификация пептидов и строение пептидной цепочки
Молекула пептида — это последовательность аминокислот: два и более аминокислотных остатка, соединённых между собой амидной связью, составляют пептид. Количество аминокислот в пептиде может сильно варьировать. И в соответствии с их количеством различают:
Соединения, содержащие более ста аминокислотных остатков, обычно называются белками. Однако это деление условно, некоторые молекулы, например, гормон глюкагон, содержащий лишь двадцать девять аминокислот, называют белковым гормоном. По качественному составу различают:
Пептиды также делятся по способу связи аминокислот между собой:
Цепочка повторяющихся атомов называется пептидным остовом: (—NH—CH—OC—). Участок (—CH—) с аминокислотным радикалом образует соединение (—NH—C(R1)H—OC—), называемое аминокислотным остатком. N-концевой аминокислотный остаток имеет свободную α-аминогруппу (—NH), в то время как у C-концевого аминокислотного остатка свободной является α-карбоксильная группа (OC—). Пептиды различаются не только по аминокислотному составу, но и по количеству, а также расположению и соединению аминокислотных остатков в полипептидную цепочку. Пример: Про-Сер-Про-Ала-Гис и Гис-Ала-Про-Сер-Про Несмотря на одинаковый количественный и качественный состав, эти пептиды имеют совершенно разные свойства.
Пептидная связь
Пептидная (амидная) связь — это вид химической связи, которая возникает вследствие взаимодействия α-аминогруппы одной аминокислоты и α-карбоксигруппы другой аминокислоты. Амидная связь очень прочная, и в нормальных клеточных условиях (37 °C, нейтральный ph) самопроизвольно не разрывается. Пептидная связь разрушается при действии на неё специальных протеолитических ферментов (протеаз, пептидгидролаз).
Значение
Пептидные гормоны и нейропептиды, например, регулируют большинство процессов организма человека, в том числе, и принимают участие в процессах регенерации клеток. Пептиды иммунологического действия защищают организм от попавших в него токсинов. Для правильной работы клеток и тканей необходимо адекватное количество пептидов. Однако с возрастом и при патологии возникает дефицит пептидов, который существенно ускоряет износ тканей, что приводит к старению всего организма. Сегодня проблему недостаточности пептидов в организме научились решать. Пептидный пул клетки восполняют синтезированными в лабораторных условиях короткими пептидами.
Синтез пептидов
Образование пептидов в организме происходит в течение нескольких минут, химический же синтез в условиях лаборатории — достаточно длительный процесс, который может занимать несколько дней, а разработка технологии синтеза – несколько лет. Однако, несмотря на это, существуют довольно весомые аргументы в пользу проведения работ по синтезу аналогов природных пептидов. Во-первых, путём химической модификации пептидов возможно подтвердить гипотезу первичной структуры. Аминокислотные последовательности некоторых гормонов стали известны именно благодаря синтезу их аналогов в лаборатории.
Во-вторых, синтетические пептиды позволяют подробнее изучить связь между структурой аминокислотной последовательности и её активностью. Для выяснения связи между конкретной структурой пептида и его биологической активностью была проведена огромная работа по синтезу не одной тысячи аналогов. В результате удалось выяснить, что замена лишь одной аминокислоты в структуре пептида способна в несколько раз увеличить его биологическую активность или изменить её направленность. А изменение длины аминокислотной последовательности помогает определить расположение активных центров пептида и участка рецепторного взаимодействия.
В-третьих, благодаря модификации исходной аминокислотной последовательности, появилась возможность получать фармакологические препараты. Создание аналогов природных пептидов позволяет выявить более «эффективные» конфигурации молекул, которые усиливают биологическое действие или делают его более продолжительным.
В-четвёртых, химический синтез пептидов экономически выгоден. Большинство терапевтических препаратов стоили бы в десятки раз больше, если бы были сделаны на основе природного продукта.
Зачастую активные пептиды в природе обнаруживаются лишь в нанограммовых количествах. Плюс к этому, методы очистки и выделения пептидов из природных источников не могут полностью разделить искомую аминокислотную последовательность с пептидами противоположного или же иного действия. А в случае специфических пептидов, синтезируемых организмом человека, получить их возможно лишь путём синтеза в лабораторных условиях.
Биологически активные пептиды
Пептиды, обладая высокой физиологической активностью, регулируют различные биологические процессы. По своему биорегуляторному действию пептиды принято делить на несколько групп:
Однако такое деление условно, так как действие многих пептидов не ограничивается каким-либо одним направлением. Так, например, вазопрессин, помимо сосудосуживающего и антидиуретического действия, улучшает память.
Пептидные гормоны
Пептидные гормоны — это многочисленный и наиболее разнообразный по составу класс гормональных соединений, представляющий собой биологически активные вещества. Их образование происходит в специализированных клетках железистых органов, после чего активные соединения поступают в кровеносную систему для транспортировки к органам-мишеням. По достижении цели гормоны специфически воздействуют на определённые клетки, взаимодействуя с соответствующим рецептором.
Нейропептиды
Нейропептиды — соединения, синтезируемые в нейронах, обладающие сигнальными свойствами. Действие нейропептидов на ЦНС очень разнообразно. Они воздействуют непосредственно на мозг и контролируют сон, влияют на память, поведение, процесс обучения, обладают обезболивающим действием.
Тахикининовые пептиды (Tachykinin peptides)
Пептиды иммунологического действия
Наиболее изученные пептиды, участвующие в иммунном ответе — тафцин, тимопотин II и тимозин α1. Их синтез в клетках организма человека обеспечивает функционирование иммунной системы.
Пептидные биорегуляторы
На основе разработанной петербургскими учеными технологии из органов и тканей животных были выделены пептиды, обладающие тканеспецифическим действием, способные восстанавливать на оптимальном уровне метаболизм в клетках тех тканей, из которых они выделены. Важным отличием этих пептидов является их регулирующее действие: при подавлении функции клетки они её стимулируют, а при повышенной функции – снижают до нормального уровня. Это позволило создать новый класс лекарственных препаратов – пептидные биорегуляторы.
Первый из них – иммуномодулятор тималин – уже более 28 лет находится на фармацевтическом рынке и применяется для восстановления функции иммунной системы при заболеваниях различного генеза, включая онкологические заболевания. За ним последовали эпиталамин (биорегулятор нейроэндокринной системы), сампрост (препарат для лечения заболеваний предстательной железы), кортексин (препарат для лечения широкого спектра неврологических заболеваний), ретиналамин (препарат для лечения дегенеративно-дистрофических заболеваний сетчатки). За 25 лет широкого применения пептидных биорегуляторов их получили более 15 млн человек. При этом не было выявлено противопоказаний к их применению и побочного действия.
Неизвестные пептиды: «теневая» система биорегуляции
Автор
Редакторы
Уже давно не вызывает сомнений значимость белков для практически любого аспекта существования жизни. Однако их «младшие братья» — пептиды — привлекают незаслуженно мало внимания, обычно считаясь биологически не такими уж важными. Нет, никто не забывает про исключительную роль пептидов в эндокринной системе и антибактериальной защите. Однако ещё двадцать лет назад нельзя было и заподозрить, что пептидный «фон», присутствующий во всех тканях и традиционно воспринимаемый как «обломки» функциональных белков, также выполняет свою функцию. «Теневые» пептиды формируют глобальную систему биорегуляции и гомеостаза, — возможно, более древнюю, чем эндокринная и нервная системы.
В начале 2010 года постановлением Президиума РАН директор Института биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова — Вадим Тихонович Иванов — награждён Большой золотой медалью Российской академии наук имени М.В. Ломоносова — «за выдающийся вклад в развитие биоорганической химии». На общем собрании РАН в мае этого года В.Т. Иванов прочитал лекцию о роли пептидов в качестве универсальных биорегуляторов. По мотивам лекции Иванова написана эта статья.
Белки, как постулировано ещё классиками диалектического материализма, являются основным «рабочим телом» жизни. Недаром даже в школьном учебнике биологии отдельным списком перечисляются функции белков: каталитическая, структурная, защитная, регуляторная, сигнальная, транспортная, запасающая, рецепторная и двигательная. Первые белки описали ещё в XVIII веке — это были альбумин («яичный» белок), фибрин (один из белков крови) и глютен (запасающий белок пшеницы). Центральная роль белков во всей биологии была осознана к концу первой четверти XX века, и с тех пор ни у кого уже не вызывает сомнения, что абсолютно все жизненные процессы протекают с участием этих универсальных «молекул жизни».
Есть у белков и «младшие братья» — пептиды. Отличие между этими двумя классами молекул довольно условное — идентичные по химической природе, они различаются лишь размером (длиной полипептидной цепи): если молекула состоит более чем из 50 аминокислотных остатков — это белок, а если менее — то пептид. Перечисленные выше «классические» функции относятся главным образом к белкам, на долю пептидов же традиционно отводилась роль в эндокринной регуляции: большинство хорошо известных биологических пептидов (а их не так уж много) являются нейрогормонами и нейрорегуляторами. Основные пептиды с известной функцией в человеческом организме — пептиды тахикининового ряда, вазоактивные интестинальные пептиды, панкреатические пептиды, эндогенные опиоиды, кальцитонин и некоторые другие нейрогормоны.
Кроме этого, важную биологическую роль играют антимикробные пептиды [1], секретируемые как животными, так и растениями (встречаются, например, в семенах или в слизи лягушек), а также антибиотики пептидной природы, о которых ещё будет немного сказано далее.
И вот не так давно (не более тридцати лет назад) обнаружилось, что кроме этих пептидов, обладающих вполне определёнными функциями, ткани живых организмов содержат довольно мощный пептидный «фон», состоящий в основном из фрагментов более крупных функциональных белков. Долгое время считалось, что это не имеет принципиального значения, и что такие пептиды — всего лишь «обломки» рабочих молекул, которые организм ещё не успел «подчистить». Однако в последнее время становится понятно, что этот «фон» играет важную роль в поддержании гомеостаза (тканевого биохимического равновесия) и регуляции множества жизненно важных процессов самого общего характера — таких как рост, дифференциация и восстановление клеток. Не исключено даже, что система биорегуляции на основе пептидов — эволюционный «предшественник» более современных эндокринной и нервной систем.
Однако давайте разбираться по порядку, и, чтобы не утратить исторической перспективы, начнём с короткой экскурсии в историю изучения пептидных веществ в нашей стране.
Историческая справка: пептидная школа в СССР
В 1959 году в Академии наук СССР был создан Институт химии природных соединений, во главе которого встал академик Михаил Михайлович Шемякин (1908–1970). Сотрудники института с самого начала были ориентированы на изучение природных биорегуляторов, таких как витамины и антибиотики. Большую работу по синтезу пептидных антибиотиков вёл молодой инициативный учёный — будущий директор института и вице-президент АН СССР Юрий Анатольевич Овчинников (1934–1988).
«Визитной карточкой» Института на долгие годы стал валиномицин — депсипептидный циклический антибиотик из бактерий Streptomyces fulvissimus, — синтез которого осуществила команда под руководством Овчинникова [2], доказав заодно ошибочность существовавших ранее представлений о структуре этого вещества (рис. 1). Валиномицин оказался ионофором, то есть веществом, селективно увеличивающим проницаемость биологической липидной мембраны для определённого типа ионов. Конформационное исследование валиномицина и его комплексов с ионами калия (а именно их он и переносит через мембрану) позволило сформулировать механизм работы антибиотика [3]. Ион металла, как в браслет, помещается в центр полости, присутствующей в циклической молекуле, и без энергетических затрат переносится через клеточную мембрану, — что и приводит к «обнулению» калиевого трансмембранного потенциала и, в конечном счёте, к гибели микроорганизма.
Рисунок 1. На лабораторном коллоквиуме в Институте химии природных соединений (1965 г.). Структуру циклического антибиотика валиномицина на доске рисует В.Т. Иванов. Депсипептиды, к которым относится и валиномицин, содержат наряду с «классическими» пептидными связями также одну или несколько сложноэфирных групп.
Блестящий пример валиномицина и других ионофоров, плюс шедшие параллельно в США исследования краун-эфиров, также способных к формированию прочных комплексов с ионами металлов, породили по всему миру каскад работ, приведших к становлению контейнерной химии, основанной на концепции «хозяин-гость» [4]. За работы в этой области Дональд Крам, Жан-Мари Лен и Чарльз Педерсен в 1987 году были удостоены Нобелевской премии по химии. Кстати, пространственная структура трансмембранного калиевого канала, полученная уже в XXI веке, показала, что механизм переноса и селективности к иону K + у этого белка принципиально такой же, как и в случае валиномицина, — только в канале координационную сферу иона образуют аминокислотные остатки из субъединиц канала-тетрамера [5], а в антибиотике это остов самой циклической молекулы-депсипептида.
За огромную работу по исследованию валиномицина и других ионофоров, результаты которой суммированы в монографии «Мембрано-активные комплексоны», Ю. А. Овчинников и В. Т. Иванов — нынешний директор Института биоорганической химии РАН (ИБХ — так сегодня называется институт, созданный Шемякиным) — были в 1987 году удостоены Ленинской премии. А в память о том романтическом периоде в биоорганической химии около входа в ИБХ красуется статуя, изображающая комплекс валиномицина с ионом калия.
«Болгарская простокваша», или как пептиды стимулируют врождённый иммунитет
Пептидные антибиотики — вещь, бесспорно, интересная, однако они по большей части вырабатываются микроорганизмами и действуют на микроорганизмы же, а значит, исследования должны были двигаться дальше — в сторону изучения пептидов животных и человека. Чтобы сделать переход к рассказу о человеческих пептидах более плавным, сначала коротко расскажем о мурамилпептидах — компонентах клеточной стенки бактерий, способных стимулировать врождённый иммунитет у человека.
В 1970-е годы в ИБХ обратился болгарский врач Иван Богданов с просьбой помочь проанализировать препарат, полученный им из продуктов ферментации кисломолочной бактерии Lactobacillus bulgaricus. Дело в том, что он хотел найти действующее начало «чудотворных» болгарских кисломолочных продуктов (в первую очередь, простокваши), якобы играющих роль в знаменитом болгарском долголетии. Роль диеты в долголетии целых народов так и остаётся не до конца доказанной, но вот препарат Богданова вызвал живой интерес, поскольку обладал существенной противоопухолевой активностью. По своему составу этот экстракт представлял собой сложную смесь веществ бактериального происхождения.
В результате исследований обнаружилось, что действующим началом препарата Богданова является элементарное звено клеточной стенки бактерий — глюкозаминил-мурамил-дипептид (ГМДП), — оказывающее на организм человека иммуностимулирующее и противоопухолевое действие. Фактически, этот элемент бактерии представляет для иммунной системы как бы «образ врага», мгновенно запускающий каскад поиска и удаления патогена из организма. Кстати, быстрый ответ — неотъемлемое свойство врождённого иммунитета, в отличие от адаптивной реакции, требующей до нескольких недель, чтобы «развернуться» полностью. На основе ГМДП был создан лекарственный препарат ликопид [6], применяющийся сейчас для широкого спектра показаний, связанных в основном с иммунодефицитами и инфекционными заражениями — сепсисом, перитонитом, синуситами, эндометритами, туберкулёзом, а также при различных видах лучевой и химеотерапии.
Новые «-омики»: пептидомика — новое направление постгеномных исследований
На этом изыскания «из жизни пептидов» не закончились — на самом деле, история с «простоквашей» и многие другие работы по веществам пептидной природы сообщили толчок для рождения новой отрасли, занимающейся систематическим изучением пептидов, содержащихся в живых клетках и тканевых жидкостях.
В начале 1980-х годов стало понятно, что роль пептидов в биологии сильно недооценена — их функции много шире, чем у всем известных нейрогормонов. Прежде всего, обнаружилось, что пептидов в цитоплазме, межклеточной жидкости и тканевых экстрактах много больше, чем считалось до того — как по массе, так и по числу разновидностей. Более того, состав пептидного «пула» (или «фона») в разных тканях и органах существенно отличается, и эти отличия сохраняются у разных особей. Число «свеженайденных» в тканях человека и животных пептидов в десятки раз превышало количество пептидов «классических» с хорошо изученными функциями. В течение какого-то времени «теневые» пептиды считались просто биохимическим «мусором», оставшимся от деградации более крупных функциональных белков и ещё не «прибранным» организмом, и лишь с начала 1990-х завеса тайны начала приподниматься.
Изучением роли пептидных «пулов» стала заниматься новая дисциплина — пептидомика, — становление которой происходило не в последнюю очередь и в ИБХ. Всем известно, что реализация генетической программы, заложенной в ДНК организмов, начинается с генóма — совокупности хромосом и генов [7]. Изучением организации и работы генома занимается специальная область на стыке молекулярной биологии и биотехнологий — генóмика. Ядро клетки, подобно командному центру, отправляет в цитоплазму послания — матричные РНК (мРНК), являющиеся «слепками» генов. Этот процесс называется транскрипцией, а совокупность всех мРНК, присутствующих в данный момент в цитоплазме и отражающих активность генома, по аналогии назвали транскриптóмом, особенности которого изучает транскриптомика. Сумма всех белковых молекул, которые синтезировали рибосомы, «прочитав» кодирующие белки мРНК, называется протеóмом, и изучает эту «белковую сферу» протеомика [8].
Эти три «-омики» являются классическими, но если вспомнить о том, что белки имеют ограниченный «срок годности», после чего расщепляются протеазами на фрагменты — то есть на пептиды! — то появляется ещё одна «-омика»: пептидомика [9]. По аналогии, её роль — изучить состав и функции белковых «пулов», существующих в разных тканях и органах, а также объяснить механизмы их образования и разрушения. Пептидóм находится на самом конце информационной цепочки: Генóм → Транскриптóм → Протеóм → Пептидóм. Пептидомика — самая молодая дисциплина из перечисленных: её возраст не превышает 30 лет, а название было предложено только в районе 2000 года. К настоящему моменту экспериментальная пептидомика позволила сформулировать три самых главных закономерности, описывающие поведение совокупности «теневых пептидов» в живых организмах.
Прежде всего, биологические ткани, жидкости и органы содержат большое число пептидов, образующих «пептидные пулы», и роль их далеко не балластная. Эти пулы образуются как из специализированных белков-предшественников, так из белков с иными, своими собственными функциями (ферментов, структурных и транспортных белков и др.).
Во-вторых, состав пептидных пулов устойчиво воспроизводится при нормальных условиях и не обнаруживает индивидуальных отличий. Это значит, что у разных особей пептидóмы мозга, сердца, лёгких, селезёнки и других органов будет примерно совпадать, но между собой эти пулы будут достоверно различаться. У разных видов (по крайней мере, среди млекопитающих) состав аналогичных пулов также весьма схож.
И, наконец, в-третьих, при развитии паталогических процессов, а также в результате стрессов (в том числе, длительного лишения сна) или применения фармакологических препаратов состав пептидных пулов меняется, и иногда довольно сильно. Это может использоваться для диагностики различных патологических состояний, — в частности, такие данные есть для болезней Ходжкина и Альцгеймера.
Точный состав пептидных пулов определить сложно, — прежде всего, потому, что число «участников» существенным образом будет зависеть от концентрации, которую считать значимой. При работе на уровне единиц и десятых долей наномоля (10 −9 М) это несколько сотен пептидов, однако при увеличении чувствительности методик до пикомолей (10 −12 М) число зашкаливает за десятки тысяч. Считать ли такие «минорные» компоненты за самостоятельных «игроков», или же принять, что они не имеют собственной биологической роли и представляют лишь биохимический «шум» — вопрос открытый.
Пептидные пулы — общая черта живых организмов?
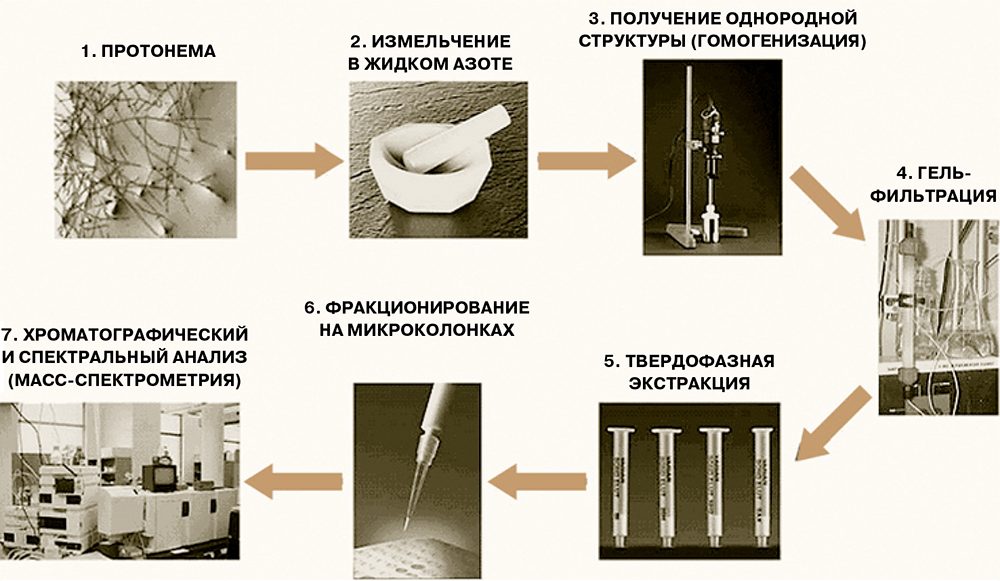
Большинство пионерских работ по пептидомике проведены на тканях животных, и во всех случаях были выявлены пептидные пулы определённого и характерного состава — у человека, быка, крысы, мыши, свиньи, суслика, гидры, дрозофилы, саранчи. Но является ли феномен наличия пептидных пулов общим, например, для растений и прокариот? В случае простейших или бактерий выяснить ситуацию ещё предстоит, но вот для растений, видимо, уже можно дать положительный ответ. В частности, для модельного растения — мха Рhyscomitrella patens, геном которого недавно был расшифрован, — было показано, что на каждой стадии развития (у нитчатой формы, протонемы и на стадии зрелой стадии, гаметофоров) в растении присутствует большое число эндогенных пептидов — фрагментов клеточных белков, набор которых индивидуален для каждой формы растения. (Схема экспериментального анализа пептидов из мха показана на рисунке 2.)
Рисунок 2. Схема анализа пептидов мха
Даже если у прокариот не обнаружится ничего похожего, уже можно сделать вывод, что большое число многоклеточных организмов культивирует внутри себя пептидные «пулы». Но для чего они служат и как образуются?
Пептиды: «теневая» система биорегуляции
Механизм образования пептидных пулов проще всего выяснить на культурах клеток, потому что, в отличие от целых тканей и органов, в этом случае появляется уверенность, что пептиды генерируются именно этим типом клеток, а не каким-то другим (или вообще не являются артефактом выделения из тканей). Наиболее подробно в этом смысле изучены эритроциты человека [10] — клетки тем более интересные, что они лишены ядра, а, следовательно, большинство биохимических процессов в них сильно заторможено.
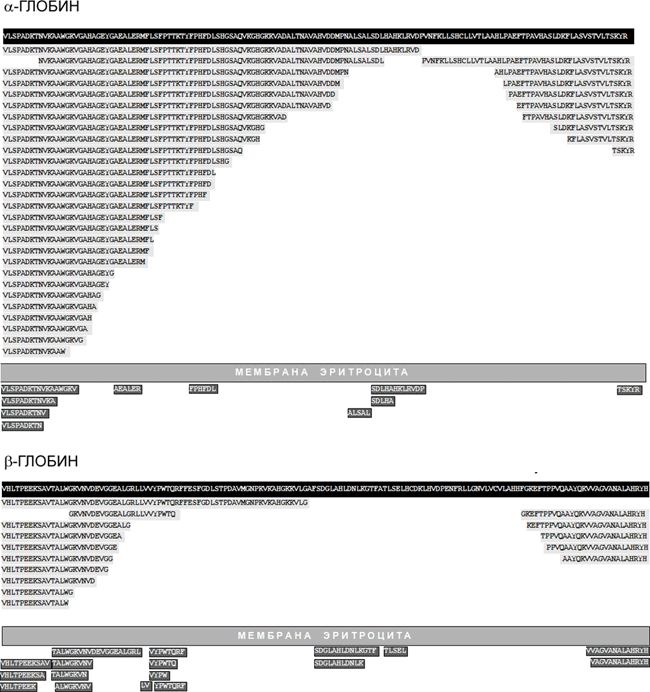
Установлено, что внутри эритроцитов происходит «нарезание» гемоглобиновых α- и β-цепей на серию крупных фрагментов (всего выделено 37 пептидных фрагментов α-глобина и 15 — β-глобина) и, кроме того, эритроциты выделяют в окружающую среду множество более коротких пептидов (рисунок 3). Пептидные пулы образуются и другими культурами клеток (трансформированными миеломоноцитами, клетками эритролейкемии человека и др.), т. е. продукция пептидов культурами клеток — широко распространённый феномен. В большинстве тканей 30–90% всех идентифицированных пептидов являются фрагментами гемоглобина, однако идентифицированы и другие белки, порождающие «каскады» эндогенных пептидов, — альбумин, миелин, иммуноглобулины и др. Для части «теневых» пептидов предшественников пока не найдено.
Даже беглый взгляд на перечень пептидных фрагментов гемоглобина (рис. 3) приводит к выводу, что разнообразие эндогенных пептидов значительно превосходит традиционный набор пептидных гормонов, нейромодуляторов и антибиотиков. Несмотря на множество разрозненных данных об активности отдельных компонентов пептидных пулов, ключевой вопрос о биологической роли пептидных пулов в целом оставался не решённым. Представляет ли основная масса пептидов в пулах просто нейтральные промежуточные продукты разрушения белковых субстратов на пути к аминокислотам, вновь используемым для ресинтеза белков, или эти пептиды играют самостоятельную биологическую роль?
Рисунок 3. Образование пептидов в культуре эритроцитов человека. На чёрном фоне показаны аминокислотные последовательности α- и β-глобина, а на сером — последовательности пептидов, идентифицированных как фрагменты этих белков.
Для ответа на этот вопрос было изучено действие более 300 пептидов — компонентов пептидных пулов тканей млекопитающих — на набор культур опухолевых и нормальных клеток. В результате оказалось, что более 75% этих пептидов оказывают выраженное пролиферативное или антипролиферативное действие хотя бы на одну культуру (то есть, ускоряют или замедляют деление клеток) [11]. Были обнаружены и другие виды биологической активности, более или менее пересекающиеся с активностями гормонов, парагормонов и нейротрансмиттеров. В результате ряда таких работ было сделано несколько выводов:
По-видимому, один из главных механизмов действия коротких биологических пептидов — работа через рецепторы хорошо известных пептидных нейрогормонов. Сродство «теневых» пептидов к рецепторам очень низкое — в десятки или даже тысячи раз ниже, чем у их «основных» лигандов, но нужно принимать во внимание и тот факт, что концентрация «теневых» пептидов примерно в такое же число раз выше. В результате оказываемый ими эффект может иметь ту же величину, а, учитывая широкий «биологический спектр» пептидного пула, можно сделать вывод об их важности в регуляторных процессах.
В то же время, мишени действия большинства «теневых» пептидов неизвестны. По предварительным данным, некоторые из них могут влиять на работу рецепторных каскадов и даже участвовать в «управляемой гибели» клетки — апоптозе.
Кстати, фрагменты более крупных белков, обладающие своей собственной функцией, никак не связанной с функцией «родителя», получили название криптеинов («спрятанные» белки). Криптеины сейчас довольно активно изучаются и выявляются в последовательностях «не секретных» белков в надежде обнаружить у них особые биологические (например, лекарственные) свойства.
Полифункциональный и полиспецифичный «биохимический буфер», который образует пептидный пул, «смягчая» метаболические колебания, позволяет говорить о новой, ранее неизвестной системе регуляции на основе пептидов (см. таблицу 1). Этот механизм дополняет всем известные нервную и эндокринную системы, поддерживая в организме своеобразный гомеостаз и устанавливая равновесие между ростом, дифференцировкой, восстановлением и гибелью клеток. Изменение пептидного «фона» почти наверняка обратит внимание на протекающий патологический процесс, а восстанавливающее и стимулирующее действие многих пептидных веществ, видимо, можно объяснить как раз восстановлением нарушенного равновесия.
Учитывая сказанное, можно даже высказать предположение, что пептидная биорегуляторная система является эволюционным предшественником более совершенных и современных нервной и эндокринной систем. Эффекты, оказываемые пептидным «фоном», могут проявляться уже на уровне отдельной клетки, в то время как невозможно себе представить работу нервной или эндокринной системы в одноклеточном организме.
| Свойство | Регуляторная система | ||
|---|---|---|---|
| Нервная | Эндокринная / паракринная | Тканеспецифичные пептидные пулы | |
| «Рабочее тело» | Нейротрансмиттеры | Гормоны | Пептиды — фрагменты функциональных белков |
| Предшественник | Специфический белковый предшественник | Специфический белковый предшественник | Функциональные белки |
| «Порождающий» процесс | Сайт-специфическое расщепление | Сайт-специфическое расщепление | Действие набора клеточных протеаз |
| Концентрация (нМ/г ткани) | 0,001–1.0 | 0,001–1.0 | 0,1–100 |
| Тип регуляции | Синаптическая секреция | Внеклеточная секреция | Изменение концентрации в ткани |
| Механизм действия | Связывание с рецепторами синаптической мембраны | Связывание с рецепторами клеточной мембраны | Связывание с рецепторами «родственных» гормонов |
| Константа связывания с рецептором (Kd, нМ) | 1–1000 | 0,1–10 | 100–10000 |
| Период активности | Секунды–минуты | Минуты–часы | Часы–дни |
| Биологическая роль | Передача нервного импульса | Регуляция физиологических процессов в ткани или всём организме | Поддержание тканевого гомеостаза |
Будущие приложения пептидомики
Лекарственные препараты, по существу являющиеся вариациями на тему пептидных пулов различных тканей животных, уже достаточно широко представлены на рынке (таблица 2), хотя они и не входят в число «блокбастеров», приносящих концернам максимальные барыши. Основная область их применения — состояния, связанные с дегенерацией или трансформацией клеток и тканей, а также необходимостью регенерации (заживления ран). Однако такие препараты не являются чистыми химическими веществами, а, следовательно, не удовлетворяют требованиям современной доказательной молекулярной медицины. (Дело в том, что современные фармакологические стандарты — такие как Good Clinical Practice — подразумевают проведение клинических испытаний, в которых совершенно чётко было бы доказано действие того или иного лекарственного компонента.)
| Препарат | Источник | Показание |
|---|---|---|
| Солкосерил (Швейцария) | Депротеинизированный гемодериват из телячьей крови | Заживление ран, трансплантация, ишемия |
| Актовегин (Дания) | Пептиды плазмы крови | Заживление ран, трансплантация, ишемия |
| Вирулизин (Канада) | Экстракт желчного пузыря крупного рогатого скота | Иммунодефициты, онкология |
| Тимулин (Россия) | Экстракт тимуса крупного рогатого скота | Иммунодефициты |
| Церебролизин (Австрия), Кортексин (Россия) | Экстракт головного мозга крупного рогатого скота/свиньи | Инсульт, болезнь Альцгеймера |
| Раверон (Швейцария) Простатилен (Россия) | Экстракт предстательной железы крупного рогатого скота | Простатит, аденома предстательной железы |
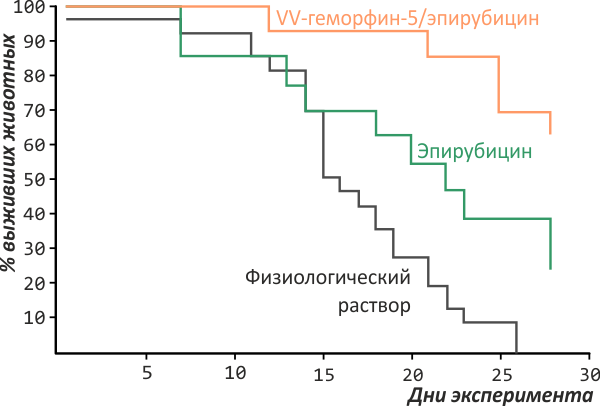
Одно из перспективных направлений здесь — использование упоминавшейся уже антипролиферативной активности пептидов. Так, в опытах на карциноме молочной железы мышей один из фрагментов гемоглобина (так называемый VV-геморфин-5) удваивал выживаемость животных при совместном применении со стандартным цитостатиком эпирубицином по сравнению с применением одного только эпирубицина [12] (рис. 4). Этот эксперимент даёт основания полагать, что на основе природных пептидных пулов возможно создание вспомогательных и поддерживающих препаратов для онкологической терапии.
Рисунок 4. Средняя продолжительность жизни мышей с карциномой молочной железы при интраперитонеальном введении эпирубицина и комбинированной терапии эпирубицином с VV-геморфином-5. Выживаемость во втором случае была выше в два раза.
Однако разработка и тестирование новых лекарств — чрезвычайно долгий и затратный процесс, осложняемый конкурентной борьбой фармацевтических гигантов [13]. Более близкая перспектива использования пептидных пулов — это диагностика заболеваний и прочих патологических состояний. Выше уже не раз было сказано, что пептидный состав образца сильно зависит от состояния, в котором находился организм — донор ткани. Уже есть примеры использования пептидомного подхода для выявления маркеров тех или иных заболеваний, в том числе — онкологических.
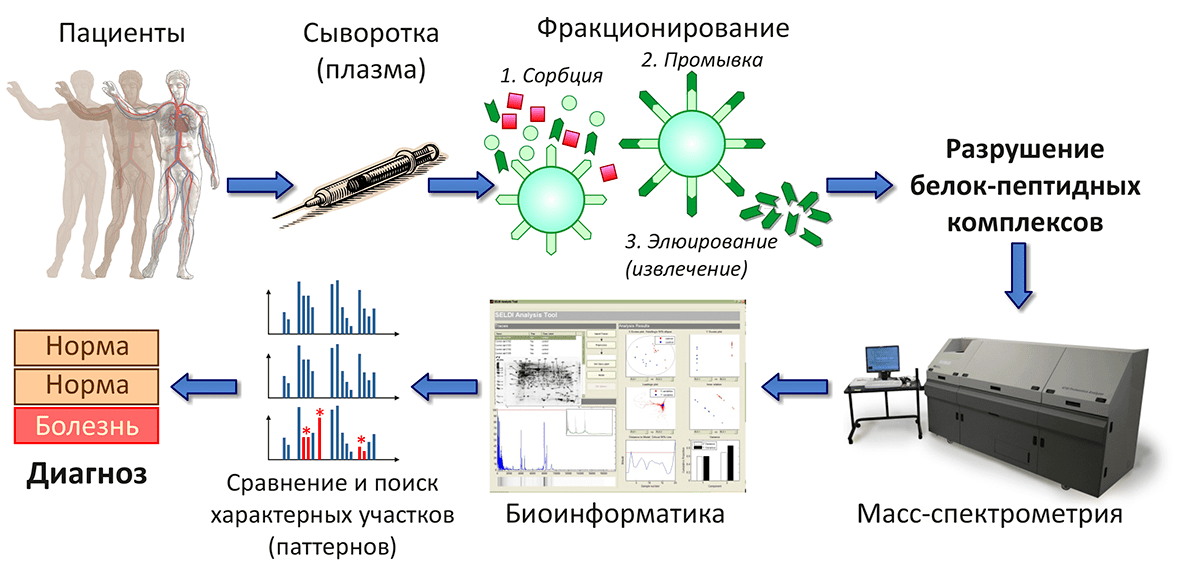
В Институте биоорганической химии разработана методика масс-спектрометрического анализа пептидного профиля образцов крови и выявлены статистически достоверные различия, по которым можно диагностировать рак яичников, колоректальный рак или сифилис (рис. 5). Масс-спектр, отражающий состав пептидного пула образца тканей, в случае больного человека будет иметь характерные отличия, по которым исследователи — а в перспективе и врачи — смогут ставить точный диагноз.
Рисунок 5. Медицинская диагностика на основе пептидного профилирования образцов крови. Сочетание масс-спектрометрических и биоинформатических методов позволяет выявить различия между пептидным составом крови больных и здоровых пациентов.
Эти примеры не оставляют сомнения, что «теневые» пептиды из тканевых пулов хранят массу практически полезной информации — от диагностики до лечения социально-значимых заболеваний.
Статья написана с использованием материалов и иллюстраций, любезно предоставленных В.Т. Ивановым. Упрощённая версия этой статьи была первоначально опубликована в журнале «Наука и жизнь» [14]; в 2011 году она заняла первое место в конкурсе научно-популярных статей «Наука — это понятно!», проводимом Советом молодых ученых РАН.