Перемежающаяся хромота
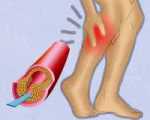
Перемежающаяся хромота – это дискомфорт, судороги, боли и другие неприятные ощущения, которые появляются в мышцах ног вследствие недостаточного кровоснабжения при физических нагрузках и исчезают в состоянии покоя. Развивается на фоне облитерирующих заболеваний артерий нижних конечностей. Является промежуточной стадией между бессимптомным течением и тяжелой ишемией, сопровождающейся трофическими расстройствами. Наличие, причину и тяжесть перемежающейся хромоты устанавливают на основании опроса, осмотра, тестов и дополнительных исследований. Лечение – специальные комплексы ЛФК, медикаментозная терапия, оперативные вмешательства.
МКБ-10
Общие сведения
Перемежающаяся хромота (ПХ) – проявление целого ряда облитерирующих болезней артерий. Распространенность таких патологий, в среднем, составляет 2-3%, увеличивается с возрастом. Наличие симптома отмечается лишь у 11-33% больных. Половина людей, страдающих перемежающейся хромотой, не обращаются за медицинской помощью, поскольку расценивают нарушение, как естественное следствие старения или других заболеваний. У мужчин ПХ обнаруживается вдвое чаще, чем у женщин.
Причины
Перемежающаяся хромота провоцируется следующими патологиями нижних конечностей:
Патогенез
Перемежающаяся хромота появляется при перекрытии 60-70% диаметра артерий. В норме при физической нагрузке кровоток в мышцах увеличивается. При появлении симптома сосуды, напротив, спазмируются. Это объясняется сопутствующими нарушениями функций вегетативной нервной системы и гуморальными воздействиями (изменением уровня адреналина). Окклюзия и спазм взаимно усугубляют друг друга, что обуславливает появление боли и неприятных ощущений после прохождения некоторого расстояния.
Классификация
Перемежающаяся хромота рассматривается в рамках классификации ишемии нижних конечностей. Наиболее популярными вариантами являются систематизации Фонтейна и Покровского, которые почти полностью совпадают друг с другом. Различают следующие степени ишемии:
Из-за незначительной выраженности симптоматики больные редко обращаются к специалисту на этапе легкой перемежающейся хромоты. В большинстве случаев диагноз облитерирующего заболевания впервые выставляется на IIб, III или IV стадиях.
Симптомы
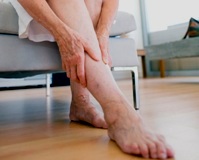
Признаками перемежающейся хромоты являются боли, дискомфортные ощущения или судороги в мышцах, возникающие на фоне движения и исчезающие в покое. Чаще страдают икроножные мышцы, реже – мускулатура стопы, бедра, ягодичной зоны. Вначале симптом развивается только после прохождения значительных дистанций, в последующем «безболевое» расстояние постепенно сокращается, пациент вынужден останавливаться через каждые 50 или 100 метров. Проявление усиливается при повышении интенсивности нагрузки на ноги, например, подъеме на лестницу, ходьбе в гору.
Еще до появления перемежающейся хромоты больного какое-то время могут беспокоить ранняя усталость ног при ходьбе, онемение пальцев, парестезии, зябкость, судороги в мышцах. Кожа на начальных этапах становится более бледной, на поздних стадиях – багрово-синюшной. Объем конечностей в зоне поражения постепенно уменьшается из-за атрофии подкожно-жировой клетчатки.
Волосы на голенях и бедрах выпадают. Кожа утолщается. Ногтевые пластины гипертрофируются, становятся слоистыми. При дальнейшем прогрессировании патологии боли возникают в покое. В области дистальных отделов конечностей образуются трофические язвы. Их развитие может сопровождаться тромбофлебитом и лимфангитом. Раны, царапины и ссадины крайне плохо заживают, любое повреждение кожи может спровоцировать развитие гангрены.
Перемежающаяся хромота не обязательно переходит в глубокую декомпенсированную ишемию. У ряда больных, особенно, при надлежащем лечении, изменения стабилизируются или незначительно усугубляются с течением времени. Быстрое нарастание симптомов и высокая вероятность гангрены более характерны для облитерирующего эндартериита и сахарного диабета, могут встречаться при облитерирующем атеросклерозе.
Диагностика
Диагностические мероприятия проводятся сосудистым хирургом. При наличии сопутствующей ИБС, обусловленной системным атеросклерозом, пациенту необходима консультация кардиолога. Больным сахарным диабетом показано комплексное обследование с участием диабетолога, эндокринолога, невролога, кардиолога. В ходе опроса устанавливают момент появления симптома, скорость его прогрессирования.
В процессе осмотра оценивают пульс на периферических артериях. Измеряют артериальное давление, определяют лодыжечно-плечевой индекс. Производят специальные пробы (термометрическую, Самюэлса, Гольдфлама и пр.), обнаруживают симптомы, свидетельствующие об ишемии конечности (прижатия пальца, плантарной ишемии Опеля). Выявляют трофические нарушения. План дополнительных диагностических мероприятий включает следующие процедуры:
Лечение перемежающейся хромоты
Программа терапевтических мероприятий составляется с учетом выраженности перемежающейся хромоты, локализации и тяжести поражения артерий, сопутствующих заболеваний и других факторов. Основными методами являются лечебная физкультура, медикаментозное лечение, воздействие на провоцирующие и усугубляющие обстоятельства. По показаниям проводятся открытые и эндоваскулярные операции на сосудах.
Традиционно при асимптомном течении ишемии и на легкой стадии перемежающейся хромоты применяются консервативные методики. При переходе болезни на более тяжелые стадии консервативные способы дополняют реваскуляризирующими хирургическими вмешательствами. При этом практикуется индивидуальный подход. Так при быстром прогрессировании болезни и стремительном развитии предкритических форм ишемии оптимальным вариантом может быть раннее начало оперативного лечения. И, напротив, при стабильном течении болезни лучшие перспективы открываются при использовании консервативных методик.
Немедикаментозные методы
Устранение предрасполагающих и провоцирующих факторов включает коррекцию режима. Пациентам следует отказаться от курения. При избытке массы тела необходима консультация диетолога для составления рациона питания, предусматривающего снижение веса. Состояние сосудов и общие метаболические процессы улучшаются при достаточной подвижности, поэтому частью немедикаментозных мероприятий становится борьба с гиподинамией.
Лечебная физкультура играет ведущую роль среди консервативных методов, является обязательной частью терапии перемежающейся хромоты. Больным рекомендуют ходить в таком темпе, при котором симптом появляется через 3-5 минут от момента начала движения. Затем следует продолжать ходьбу до умеренной боли или дискомфорта, после чего останавливаться до исчезновения неприятных ощущений, а потом идти снова.
Общая продолжительность одного занятия на начальном этапе составляет не менее 35 минут, в последующем постепенно увеличивается до 1 часа. Занятия проводят 3 или более раза в неделю. Для достоверной оценки эффективности метода в лечении конкретного больного курс ЛФК должен составлять не менее 3 месяцев. При наличии трофических язв на пальцах и подошвах ходьбу заменяют педальным тренажером или велотренажером.
Медикаментозная терапия
Поскольку абсолютное большинство случаев перемежающейся хромоты связано с системным атеросклерозом, на первый план выходят средства, влияющие на проявления и скорость прогрессирования атеросклеротического процесса. Больным назначают препараты следующих групп:
Медикаментозная терапия проводится в постоянном режиме, корректируется врачом при выявлении факторов риска или недостаточной результативности лечения. Самовольное прекращение приема после улучшения состояния недопустимо. Кроме перечисленных препаратов пациенты с сахарным диабетом должны получать инсулинотерапию. Для обеспечения наиболее полной компенсации используются пролонгированные инсулины в сочетании с медикаментами короткого и промежуточного действия.
Для улучшения кровообращения в зоне поражения применяют ингибиторы фосфодиэстеразы, вазодилататоры. При незначительных и умеренных проявлениях ишемии эффективны простаноиды. В рамках метаболической терапии назначаются средства на основе гемодиализатов крупного рогатого скота, однако мнения относительно этого метода лечения варьируются из-за недостатка масштабных клинических исследований. Перспективным направлением считается разработка генотерапевтических препаратов для стимуляции ангиогенеза.
Хирургическое лечение
Критерии желательности и необходимости оперативного лечения несколько разнятся. Наиболее распространен подход, при котором стадия умеренной перемежающейся хромоты считается относительным показанием для вмешательства, а боли покоя и трофические нарушения – абсолютным. В пользу применения оперативного пособия при наличии относительных показаний свидетельствуют жалобы больного на ограничение трудоспособности. Представителям профессий, предусматривающих длительную ходьбу, операции иногда проводят при легкой степени ПХ.
В зависимости от клинической ситуации и других обстоятельств могут применяться открытые и эндоваскулярные хирургические вмешательства для реваскуляризации пораженного сегмента.
Шунтирующие методики включают аорто-бедренное, бедренно-подколенное другие варианты шунтирования. В рамках паллиативного лечения для стимуляции коллатерального кровообращения выполняются реваскуляризирующая остеотрепанация, поясничная или периартериальная симпатэктомия. При развитии гангрены показана ампутация конечности.
Прогноз
Исход в определенной степени зависит от причины ПХ. Так, атеросклероз зачастую протекает более благоприятно, чем эндартериит. В большинстве случаев при адекватном лечении и соблюдении рекомендаций лечащего врача прогноз относительно благоприятный. У 75% пациентов даже при продолжении курения заболевание протекает достаточно стабильно, прогрессирование до критической ишемии отмечается у 25% больных. При отказе от курения этот показатель снижается до 8%. Операции требуются в 12% случаев, ампутация конечности – в 2,4%.
Профилактика
Первичные профилактические мероприятия включают нормализацию веса, отказ от курения, достаточную двигательную активность, контроль уровня холестерина, адекватную терапию сахарного диабета. Пациентам с перемежающейся хромотой важно выполнять все врачебные рекомендации, в том числе – относительно приема лекарств и занятий ЛФК. Необходимо носить удобную обувь, предупреждать травмы стопы, регулярно осуществлять профилактический и гигиенический уход за ногами.
Перемежающаяся хромота: лечебная тактика практикующего врача
Рассмотрены направления комплексного лечения пациентов с перемежающейся хромотой атеросклеротической этиологии и ее осложнением в виде критической ишемии нижних конечностей, в том числе с применением генно-терапевтических ангиогенных препаратов.
The directions of the complex treatment of patients with the intermittent lameness of atherosclerotic etiology and its complication in the form of critical ischemia of lower limbs are examined, including application of the henna-therapeutic angyo-genic preparations.
В текущем 2013 г. вышел в свет новый пересмотр Национальных рекомендаций по ведению пациентов с заболеваниями периферических артерий. Важное место в нем уделено заболеваниям сосудов ног. Несмотря на отсутствие полноценных статистических данных можно констатировать, что расчетное число страдающих данным заболеванием исходя из распространенности (0,9–7% от популяции в зависимости от возрастной группы) в России не менее 1,5 млн, значит, у 100 000 граждан выявляют терминальную (критическую) форму заболевания; что ежегодно приводит только по данному показанию к выполнению 20 000–40 000 ампутаций.
Перемежающаяся хромота (ПХ) — основной клинический синдром атеросклеротического поражения артерий нижних конечностей [1]. К сожалению, большая часть специалистов забывает об актуальности данного заболевания; возможно, на фоне драматического течения других проявлений атеросклероза данная форма незаслуженно не приковывает пристального внимания. Вместе с тем распространенность ПХ в зависимости от возраста составляет от 0,9% до 7,0%. Согласно авторитетным изданиям и крупным популяционным исследованиям (группа SAGE, 2010; Российский согласительный документ, 2013; исследование PANDORA, 2012) распространенность заболеваний периферических артерий является высокой, варьируя от 5,8% в США и 7% в России до 12,2% и 22,9% во Франции и Италии соответственно. Важно, что до 50% больных с ПХ никогда не обращались к врачам по поводу этих симптомов, но при этом они испытывают дискомфорт из-за болей в ногах. Медицинские специалисты при осмотре таких пациентов в случае их обращения в лечебно-профилактические учреждения по поводу других жалоб не опрашивают их на наличие ишемических болей в ногах при ходьбе [2].
Установлено, что именно атеросклероз является причиной поражения периферических артерий в 80–90% случаев [3], остальную часть составляет «чистая» диабетическая ангиопатия (без фонового значимого атеросклероза сосудов нижних конечностей) и поражение сосудов аутоиммунного генеза. Давно известно, что у больных с ПХ существует высокий риск развития инфаркта миокарда (ИМ) и острого нарушения мозгового кровообращения. Так, по сравнению с обычной популяцией, риск ИМ у них повышен от 20% до 60%, а риск смерти от коронарной патологии от 2 до 6 раз. При ПХ риск развития острого нарушения мозгового кровообращения повышается на 40% [2].
Больше чем у половины больных с заболеваниями периферических артерий уже на момент обращения регистрируется IIБ (хирургическая) стадия заболевания по классификации А. В. Покровского–Фонтейна, что соответствует перемежающейся хромоте, возникающей при прохождении 50–200 м [4]. Такие пациенты являются кандидатами для проведения эндоваскулярного открытого либо гибридного оперативного лечения [5]. Тем не менее, высокий уровень развития современной реконструктивной хирургии артерий нижних конечностей не может решить всех проблем у данной группы пациентов. Успех реконструктивных вмешательств напрямую зависит от состояния т. н. путей оттока — сосудов, расположенных ниже паховой складки [6]. По некоторым данным, до 40% пациентов, нуждающихся в оперативном лечении, не может быть выполнена артериальная реконструкция вследствие дистального либо распространенного мультифокального поражения артериального русла [7].
Появление болей покоя и язвенно-некротических изменений кожных покровов вплоть до гангрены у пациентов с ПХ свидетельствует о развитии критической ишемии нижних конечностей (КИНК), состояния декомпенсации артериального кровотока. Лечение КИНК требует более активного подхода как в отношении фармакотерапии, так и хирургических вмешательств. Динамика и статистика КИНК такова, что в течение первых 6 месяцев после диагностирования КИНК конечность удается сохранить лишь в 40% случаев, так как 20% больных умрут, а остальным будет выполнена большая ампутация. В результате к концу первого года после верификации диагноза лишь 45% больных имеют шанс сохранения конечности, около 30% продолжают жить после ампутации бедра или голени, четверть пациентов не переживут этот временной рубеж (рис. 1) [2].
Признано (А. В. Гавриленко и др., 2010), что при установлении диагноза заболеваний периферических артерий у пациента с ПХ или КИНК консервативная терапия показана вне зависимости от локализации и распространенности сосудистого поражения и назначается пожизненно [9]. После выполнения эндоваскулярных или оперативных вмешательств на артериях необходимость в консервативном лечении также сохраняется. В случаях, когда нет возможности достигнуть адекватной компенсации кровообращения хирургическими методами, изолированное использование терапевтического лечения остается единственной лечебной тактикой врача.
Современные подходы к консервативной терапии
Согласно руководству Американской ассоциации кардиологов (2005) основная цель консервативной терапии у пациентов с ПХ и КИНК — это улучшение качества жизни и снижение риска развития фатальных сердечно-сосудистых событий [10]. Для этого лечебная тактика врача должна включать как коррекцию факторов риска, так и назначение эффективных лекарственных препаратов. Одним из ведущих направлений коррекции факторов риска является отказ от курения, что включает в себя модификацию поведения, никотин-заместительную терапию, терапию бупропионом) (класс доказательности I) [2] (рис. 2).
Всем пациентам с ПХ показана эффективная физическая нагрузка — дозированная ходьба, то есть ходьба до появления почти максимальной ишемической боли (класс доказательности I). Программа лечебной физкультуры рекомендуется в качестве первоначальной формы лечения пациентов с перемежающей хромотой как основного проявления хронической ишемии нижних конечностей (ХИНК) (уровень доказательности A). Продолжительность занятий лечебной физкультурой составляет от 30 до 45 мин минимум, занятия проходят 3 раза в неделю, минимальный курс — 12 недель. Максимальная эффективность дозированной ходьбы проявляется через 1–2 месяца и сохраняется через 3 и более месяцев. Благоприятный эффект объясняется улучшением метаболизма скелетной мускулатуры, увеличением мышечной массы, а также улучшением функции эндотелия и, в меньшей степени, формированием коллатерального кровообращения [2].
Важным направлением является контроль за уровнем липидов в крови. Лечение ингибиторами гидроксиметилглутарил-ацетил-коэнзим А-редуктазы (статины) показано всем пациентам с заболеваниями периферических артерий (ЗПА) для достижения целевого уровня липопротеинов низкой плотности (ЛПНП) менее 100 мг/дл (класс доказательности I). Лечение дислипидемии снижает риск развития нежелательных сердечно-сосудистых событий у пациентов с атеросклерозом. Однако клиническая картина тяжелого поражения артериального русла нижних конечностей не всегда строго коррелирует с изменениями липидного спектра крови и уровнем холестерина и ЛПНП [2].
Всем пациентам с ЗПА, как с ПХ, так и КИНК, показан контроль уровня глюкозы крови (уменьшение уровня гликозилированного гемоглобина до 7%), а при наличии сахарного диабета — интенсивная терапия антигипергликемическими препаратам либо инсулином, а также тщательный уход за кожей стоп и голеней (класс доказательности I) [2].
Помимо контроля за уровнем глюкозы, важным направлением в коррекции факторов риска ЗПА является контроль уровня артериального давления (АД). Оптимальным у пациентов без сопутствующей патологии следует считать уровень АД менее 140/90 мм рт. ст., в то время как наличие таких состояний, как артериальная гипертензия, ишемическая болезнь сердца, хроническая сердечная недостаточность, сахарный диабет и почечная недостаточность, обусловливают необходимость поддержания цифр АД на уровне менее 130/80 мм рт. ст. (класс доказательности I). Целевыми препаратами являются ингибиторы ангиотензинпревращающего фермента (АПФ), достоверно снижающие риск развития ИМ, инсульта и смерти из-за сердечно-сосудистых событий у пациентов с ЗПА [2].
Антиагрегантная (антитромбоцитарная) терапия в виде приема Аспирина в дозировке 75–325 мг/сутки либо клопидогреля 75 мг/сутки показана пациентам с атеросклерозом артерий нижних конечностей для снижения риска сердечно-сосудистых событий (класс доказательности I). Практическому врачу следует помнить, что у пациентов с ЗПА пероральные антикоагулянты с целью профилактики нежелательных сердечно-сосудистых ишемических событий применяться не должны [2].
Целесообразным является назначение пациентам с ПХ ингибитора фосфодиэстеразы III — цилостазола, обладающего вазодилатирующим, метаболическим и дезагрегантным эффектом (класс доказательности I). В дозировке 100 мг два раза в день препарат увеличивает дистанцию безболевой ходьбы (ДБХ) на 40–60% по сравнению с плацебо после 12–24 недель лечения [2, 10]. Цилостазол, однако, на территории Российской Федерации не зарегистрирован. Другим препятствием к его широкому применению служит необходимость отсутствия у пациента сопутствующей патологии в виде хронической сердечной недостаточности любого класса по классификации Нью-Йоркской ассоциации кардиологов (New York Heart Association, NYHA) [12], а также ограничения, введенные европейским медицинским агентством на его использование в 2013 г. в связи с высокой вероятностью побочных эффектов [13].
Пентоксифиллин в дозе 1200 мг в сутки может рассматриваться как один из основных препаратов для увеличения максимально проходимой дистанции (МПД) у пациентов с ПХ (класс доказательности IIB). Пентоксифиллин улучшает микроциркуляцию и реологические свойства крови, оказывает сосудорасширяющее действие, блокирует фосфодиэстеразу и способствует накоплению циклического аденозинмонофосфата в клетках, что приводит к минимальному, но статистически значимому увеличению ДБХ на 21–29 метров и максимально проходимой дистанции на 43–48 метров [2, 14, 15].
Сулодексид (250 ЛЕ перорально 2 раза в день), ранее рекомендованный к применению у пациентов с КИНК, в настоящее время рекомендован пациентам с ПХ. У данной когорты пациентов сулодексид увеличивает ДБХ до 95% при курсовом применении в сочетании с парентеральным введением (класс доказательности IIА). Эффективность препарата объясняется комплексным воздействием на основные звенья патогенеза заболевания: коррекция дисфункции эндотелия, нормализация реологии крови и микроциркуляторного русла, повышение фибринолитической активности.
Перспективным направлением в комплексном лечении пациентов с ПХ атеросклеротической этиологии является коррекция дисфункции эндотелия, направленная на стимуляцию синтеза оксида азота (NO) клетками эндотелия. Дисфункция эндотелия выражается в повышенной проницаемости и адгезивности, а также в увеличенной секреции прокоагулянтных и сосудосуживающих факторов, что может рассматриваться в качестве раннего этапа развития сосудистого поражения [16]. NO является важным регулятором метаболизма клеток и играет важную роль в патогенезе эндотелиальной дисфункции [17]. Положительное влияние, направленное на коррекцию дисфункции эндотелия, может иметь интермиттирующая пневмокомпрессия, в том числе у пациентов с критической ишемией нижних конечностей [18–20]. Другим вектором коррекции эндотелиальной дисфункции является применение препаратов группы ингибиторов ангиотензинпревращающих ферментов, преимущественно периндоприла, блокаторов рецепторов ангиотензина II, преимущественно лозартана [21–23], а также бета-адреноблокаторов, преимущественно небиволола [24–26]. Это особенно важно, учитывая высокую распространенность артериальной гипертензии, а также ишемической болезни сердца и хронической сердечной недостаточности у пациентов с ХИНК. Бета-адреноблокаторы являются эффективными антигипертензивными препаратами и не противопоказаны пациентам с заболеванием артерий нижних конечностей, как это представляется большинству практических врачей [2].
Коррекция дисфункции эндотелия также возможна за счет стимуляции секреции NO экзогенными факторами системы L-аргинин — NO — гуанилатциклазы, в частности, при использовании предшественника оксида азота L-аргинина [27–29]. Терапия, направленная на коррекцию эндотелиальной дисфункции, является чрезвычайно перспективной, однако в настоящее время находится большей частью на стадии клинических исследований.
Как указано в Национальных рекомендациях (2013), к высокому классу доказательности IIA относится применение генно-терапевтических препаратов [2]. Данная группа препаратов активно исследуется последние два десятилетия. Они являются агентами т. н. «терапевтического ангиогенеза» — новой лечебной тактики, призванной путем введения генно-терапевтических препаратов, кодирующих синтез различных короткоживущих и короткодистантных молекул (факторов роста, транскрипционных факторов) индуцировать развитие микрососудистой сети, а в дальнейшем привести к образованию коллатералей. Считается, что развитие микроциркуляторного русла в ишемизированном мышечном массиве нижних конечностей способствует оксигенации тканей, снижает общее периферическое сосудистое сопротивление, а образованные на уровне окклюзии новые сосуды способны эволюционировать в функциональные коллатерали. В качестве потенциальных лекарственных средств испытываются неинтегрирующиеся в геном плазмидные и аденовирусные генные конструкции. Большим количеством клинических исследований показана их безопасность, в том числе онкологическая [30, 31]. На уровне II фазы клинических исследований значимые результаты по увеличению дистанции безболевой ходьбы были получены с генами, кодирующими эндотелиальный cоcудистый фактор роста (vascular endothelial growth factor, VEGF165), основный фактор роста фибробластов (basic fibroblast growth factor, bFGF), фактор роста гепатоцитов (hepatocyte growth factor, HGF) и др. [30–34]. Однако на этапе III фазы эффективность для лечения была установлена не для всех конструкций. В частности, применение препарата на основе гена bFGF у пациентов с IV стадией заболевания (по А. В. Покровскому–Фонтейну) не влияло на продолжительность жизни и сохранность конечности [35]. В то же время плазмидная конструкция с геном HGF, примененная по тем же показаниям, достоверно снижала выраженность болевого синдрома, положительно влияла на качество жизни, способствовала заживлению язв, что явилось основанием к признанию ее эффективности [36].
В настоящее время в Государственный реестр лекарственных средств России включен генно-терапевтический препарат Неоваскулген, активным веществом которого является сверхскрученная плазмида с геном VEGF165. Его безопасность и эффективность были исследованы в ходе мультицентровых контролируемых рандомизированных исследований, показавших достоверное увеличение дистанции безболевой ходьбы, а также ряд иных эффектов, включающих увеличение тканевого напряжения кислорода, в некоторой степени — линейной скорости кровотока, лодыжечно-плечевого индекса [37, 38]. Препарат предназначен для включения в комплексную терапию пациентов с IIa-III степени ПХ (по Покровскому–Фонтейну) атеросклеротического генеза. Препарат вводится по 1,2 мг местно внутримышечно двукратно с интервалом в 14 суток. Возможности препарата реализуются в составе комплексной терапии. В рамках клинических исследований эффективность препарата была оценена у пациентов, которым не выполнялись хирургические методы реваскуляризации и которым не назначалась терапия препаратами группы простагландинов. Установлено, что в течение полугода у пациентов детектировали прирост дистанции безболевой ходьбы в среднем на 110,4%, а через год на 167,2%. В большей степени отвечали на терапию больные с более тяжелой стадией процесса — III, для них установлены приросты 231,2 и 547,5% соответственно. Также статистически значимые сдвиги регистрируются при контроле чрескожно определяемого напряжения кислорода. В меньшей степени меняются показатели макрогемодинамики — лодыжечно-плечевой индекс и линейная скорость кровотока. Немаловажно, что при оценке качества жизни у таких пациентов установлен значимый прирост по шкале «физический компонент здоровья» (p = 0,001).
При лечении КИНК, в случае невозможности выполнения эндоваскулярной или открытой артериальной реконструкции, терапевтический подход отличается от лечения ПХ. Простаноиды, препараты простагландина Е1 (PGE1) и простациклина I2 (PGI2), наиболее изучены при лечении КИНК. Многочисленные исследования показали, что парентеральное их введение в течение 7–28 дней может уменьшить боли в покое и способствовать заживлению трофических язв и, в ряде случаев, позволяет избежать или отсрочить ампутацию конечности (класс доказательности IIB, уровень доказательности А) [2].
Генно-терапевтические ангиогенные препараты, рекомендованные к применению в лечении ПХ, считаются потенциально эффективными в лечении больных КИНК. Показана их роль в комплексном лечении пациентов с КИНК в плане улучшения отдаленных результатов реконструктивных вмешательств [39]. Появляются первые данные (И. Н. Бродский, 2013) об успешном сочетании препаратов простациклинового ряда с индукцией развития микроциркуляторного русла Неоваскулгеном у тяжелых пациентов с КИНК.
Данные по эффективности гипербарической оксигенации, спинальной нейростимуляции, а также применяемых на территории России традиционных видов физиотерапии (лазеротерапия, магнитотерапия) в лечении КИНК являются противоречивыми, в связи с чем четких рекомендаций в отношении их применения не существует [2]. Обнадеживающие данные получены в отношении проведения регионарного катетерного тромболизиса в комплексной терапии КИНК при диабетической ангиопатии. Целью локального тромболизиса у данной когорты пациентов служит лечение и профилактика микротромбообразования, стабилизация коагуляционных свойств крови [2].
Эффективное лечение пациентов с перемежающейся хромотой и ее грозным осложнением в виде критической ишемии нижних конечностей является актуальной проблемой практической медицины в связи с недостаточно уделяемым вниманием, высокой морбидностью, трудностями лечения. Авторы статьи надеются, что приведенный в работе материал будет полезен в работе не только ангиохирургов, но и врачей других медицинских специальностей.
Литература
* ГБОУ ВПО РязГМУ МЗ РФ, Рязань
** ОАО Институт стволовых клеток человека, Москва


.jpg)
.gif)



