на чем основана кислотно основная классификация катионов
Кислотно-основная классификация катионов по группам
Данная классификация катионов по группам основана на использовании в качестве групповых реагентов водных растворов кислот и оснований — хлороводородной кислоты НС1, серной кислоты H2SО4, гидроксидов натрия NaOH или калия КОН (в присутствии пероксида водорода Н2О2) и аммиака NН3. Хотя эта классификация менее совершенна, чем сероводородная, однако используется чаще, т.к. при ее использовании не требуется получение и применение токсичного сероводорода.
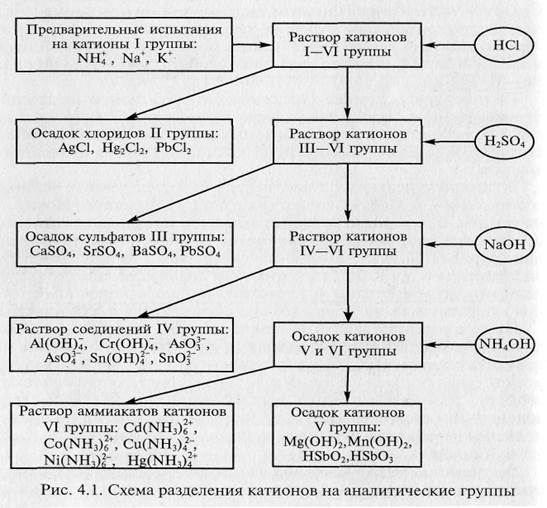
В соответствии с кислотно-основной классификацией систематический ход качественного анализа смеси катионов может быть представлен следующей схемой (рис. 4.1) [3].
В результате получается шесть фракций раствора, содержащих катионы только своей аналитической группы. После этого на последующих стадиях анализа каждый катион может быть обнаружен «внутри» группы с помощью характерных (уже не обязательно специфичных) реакций.
Полная схема систематического анализа катионов по этой классификации (как и по любой другой) практически никогда не применяется при контроле ОС, качества лекарств и минерального сырья, однако отдельные элементы ее все же иногда используются в анализе.
Катионы, открываемые в рамках кислотно-основной классификации, подразделяют на шесть аналитических групп.
Сульфаты кальция, стронция и бария практически нерастворимы в разбавленных кислотах и щелочах. Сульфат бария заметно растворяется в концентрированной серной кислоте с образованием кислой соли Сa(HS04)2. Сульфат кальция растворим в водном растворе сульфата аммония (NH4)2S04 с образованием комплекса (NH4)2[Ca(S04)2], сульфаты стронция и бария — вообще не растворяются.
Даже если бы исходное вещество и содержало формально мышьяк в виде катионов, например, АsС13, As2O3, As2O5 и т.д., то в водной среде оно гидролизуется с дальнейшим образованием анионной формы мышьяка(III) или мышьяка(V):
В соответствии с изложенным при проведении анализа по кислотно-основному методу обычно используют аналитические реакции на арсенит- или арсенат-анионы, а не на катионы мышьяка(III) или мышьяка(V).
На воздухе гидроксиды марганца(II) и железа(III) постепенно окисляются кислородом:
При действии группового реагента в присутствии пероксида водорода происходит окисление железа(II) до железа(III), марганца(II) – до марганца(IV), сурьмы(III) – до сурьмы(V):
Осадки основных солей меди(II), никеля(II) и гидроксида кадмия растворяются в избытке группового реагента с образованием соответствующих аммиачных комплексов:
Осадки, выпавшие из растворов солей кобальта(II) и ртути(II) при действии группового реагента, растворяются в избытке аммиака в присутствии солей аммония с образованием аммиачных комплексов:
Аммиачный комплекс кобальта(II) грязно-желтого цвета окисляется на воздухе до аммиачного комплекса кобальта(III) вишнево-красного цвета.
Контрольные вопросы и задания
1. Какие бывают аналитические классификации катионов и на чем они основаны?
2. Охарактеризуйте подробнее кислотно-основную классификацию катионов (нарисуйте схему разделения на группы).
3. Дайте подробную характеристику какой-нибудь одной группы катионов и напишите их реакции с групповыми реагентами.
4. Перечислите характерные реакции катионов одной из групп и напишите их уравнения для одного из них.
(Воспользуйтесь для этого электронными текстами: «Качественный анализ S- P- и D-катионов»)
Рекомендуемая литература:
1. Харитонов Ю.Я. Аналитическая химия (аналитика). Кн. 1. Общие теоретические основы. Качественный анализ. Учеб. для вузов. – М.: Высш. шк., 2001. – с. 288-291, 320-324.
2. Бессероводородные методы качественного полумикроанализа. /Под ред. А.П. Корешкова. – М.: Высш. школа, 1979.
3. Голубков Ю.М., Головачева В.А., Ефимова Ю.А. и др. Аналитическая химия. Учебник. /Под ред. А.А. Ищенко. – М.: Издательский центр «Академия», 2004. – с. 80.
Кислотно–основная классификация катионов
Кислотно–основная классификация катионов
Кислотно-основная классификация катионов основана на различии в свойствах их гидроксидов (основные или амфотерные, растворимые или не растворимые в NH3) и на различной растворимости в воде их хлоридов и сульфатов (хорошо или мало растворимые).
Деление катионов на группы по кислотно-основной классификации, групповые реагенты, а также свойства их хлоридов, сульфатов и гидроксидов даны в табл.2.
Кислотно-основная классификация катионов
Хлориды, сульфаты и гидроксиды растворимы в воде
Хлориды малорастворимы в воде
Сульфаты малорастворимы в воде
Al3+, Cr3+, Zn2+, As(III), As(V), Sn(II), Sn(IV)
2 моль/л NaOH (избыток) в присутствии H2O2
Гидроксиды растворимы в избытке NaOH
Bi3+, Fe2+, Fe3+, Mg2+, Mn2+, Sb(III), Sb(V)
Гидроксиды нерастворимы в избытке NaOH и NH3
Гидроксиды нерастворимы в избытке NaOH, но растворимы в избытке NH3
Систематический анализ смеси катионов I–IV аналитических групп, основанный на кислотно-основной классификации, начинают обычно с дробного обнаружения катионов I аналитической группы, а затем разделяют смесь на группы с помощью групповых реагентов.
Вначале осаждают хлориды катионов II аналитической группы, а затем переводят в осадок сульфаты катионов III аналитической группы. При обработке полученного раствора, содержащего катионы I, IV, V и VI аналитических групп, избытком раствора гидроксида натрия в присутствии пероксида водорода в осадок переходят основные по своей природе гидроксиды или гидратированные оксиды катионов V и VI аналитических групп. При этом катионы I и IV аналитических групп остаются в растворе. Гидроксиды катионов IV аналитической группы являются амфотерными и поэтому растворимы в избытке раствора гидроксида натрия. Осадок гидроксидов катионов V и VI аналитических групп растворяют действием разбавленного (2 моль/л) раствора азотной кислоты в присутствии пероксида водорода. Добавление к полученному раствору концентрированного раствора аммиака позволяет выделить в осадок гидроксиды катионов V аналитической группы, тогда как катионы VI аналитической группы остаются в растворе в виде комплексных амминов.
После разделения смеси катионов на группы с помощью групповых реагентов проводят обнаружение отдельных ионов внутри каждой группы с использованием их специфических реакций.
ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
Катионы I аналитической группы не имеют группового реагента, так как нет соединения, которое одновременно осаждало бы все катионы данной группы.
Гидроксиды, а также почти все соли лития, натрия, калия и аммония хорошо растворимы в воде. Поэтому известно очень ограниченное число реакций, которые могут быть использованы в качестве аналитических при определении этих ионов. Некоторые из них представлены в табл.3.
Катионы лития, натрия, калия и аммония в водных растворах бесцветны. Соли, в состав которых входят катионы лития, натрия и калия, широко используются в медицине, входят в состав многих лекарственных препаратов. Например, гидрокарбонат натрия NаНСО3 содержится в минеральных водах и применяется для понижения кислотности желудочного сока, для ингаляций и полосканий. Сульфат натрия Nа2SО4·10Н2О (глауберова соль) используется в качестве слабительного и как противоядие при отравлении солями свинца, бария и производными бензола. Раствор хлорида натрия (0,9 %) используется в качестве изотонического раствора и как противоядие при отравлении нитратом серебра. Хлорид калия используется как антиаритмическое средство, бромид натрия или калия – как успокаивающее и снотворное средство, иодид натрия и калия – при лечении ряда заболеваний. Соли лития применяют в урологической практике и при лечении нарушений обмена веществ.
Некоторые аналитические реагенты и продукты их взаимодействия с катионами
Определение катионов кислотно-основным методом анализа
Разделы: Химия
Ключевые слова: химия
Для обнаружения ионов при их совместном присутствии в растворе, каком-либо природном или промышленном объекте применяют дробный или систематический методы анализа. Дробный метод анализа заключается в обнаружении иона посредством специфической реакции. Применение этого метода ограничено, поскольку таких реакций немного. В процессе систематического анализа проводится предварительное разделение всех ионов на так называемые аналитические группы и обнаружение того или иного иона осуществляется в присутствии ограниченного числа других ионов. Систематический ход анализа обычно проводят «мокрым» путем, так как реакции между ионами обычно протекают в водных растворах. Существуют разные схемы систематического анализа, основанные на различном отношении групп ионов к действию определенных реагентов. Наиболее распространены кислотно-щелочная и сероводородная схемы анализа катионов. Сероводородный метод анализа катионов является классическим. Он основан на различной растворимости сульфидов, гидроксидов, карбонатов и хлоридов. В этом методе катионы делят на пять аналитических групп. У каждой из них есть свой групповой реагент, за исключением первой группы катионов. В качестве группового реагента используется такой реактив, который реагирует со всеми катионами данной группы в одних и тех же условиях и дает возможность отделить катионы данной группы. Групповыми реагентами являются хлороводородная кислота, сероводород, сульфид аммония, карбонат аммония. Кислотно-щелочной метод анализа катионов основан на различной растворимости в воде хлоридов и сульфатов и на различной растворимости гидроксидов в воде, избытке щелочи и водном растворе аммиака. Групповыми реактивами являются хлороводородная и серная кислота, щелочь и водный раствор аммиака. В кислотно-щелочном методе катионы делят на шесть аналитических групп.
В соответствии с кислотно-щелочной схемой анализа принята следующая классификация катионов:
На чем основана кислотно основная классификация катионов
Цель: познакомить учащихся с аналитической классификацией катионов, освоить на практике реакции с групповыми реагентами и частные реакции на катионы I–III аналитических групп.
Для удобства обнаружения все катионы делят на аналитические группы. Существует несколько классификаций катионов. Наибольшее распространение получили классификации в сероводородном, аммиачно-фосфатном и кислотно-основном методе. В основу данного пособия положена кислотно-основная классификация (табл. 1).
Кислотно-основная классификация основана на использовании основных свойств элементов: отношение их к кислотам и щелочам, амфотерность гидроксидов и способность элементов к комплексообразованию.
Практичес-ки все соединения растворимы в воде
Хлориды нераствори-мы в воде и разбавлен-ных кислотах
Сульфаты нераствори-мы в воде и кислотах
Гидроксиды растворимы в избытке щелочи и в кислотах
Гидроксиды нераствори-мы в щелочах, растворимы в кислотах
Гидроксиды растворимы в избытке водного раствора аммиака
Периодичность химических свойств явно проявляется в отношении кислотно-основных свойств элементов. Так, основные свойства гидроксидов усиливаются по мере увеличения электроположительного характера образующих их элементов. Наиболее сильными основаниями являются гидроксиды наиболее электроположительных элементов, то есть элементов A подгрупп I и II групп периодической системы (также I и III аналитических групп). Электроположительный характер в пределах одной группы усиливается с увеличением радиусов ионов. Таким образом, гидроксиды, образованные элементами с законченным 2- и 8-электронным внешним слоем (I, III гр.), обладают основным характером более сильным, чем гидроксиды, образованные катионами такого же заряда, но с законченным 18-электронным внешним слоем. Поэтому с увеличением номера группы основный характер заметно ослабевает и переходит в амфотерный, а затем и в кислотный. Кислотный характер возрастает по мере увеличения электроотрицательности элемента.
Растворимость гидроксидов также зависит от степени электроположительности элемента, то есть от величины потенциала ионизации. Чем он меньше, тем лучше растворимость гидроксидов. Так, катионы I аналитической группы образуют сильные и легко растворимые основания (наименьший потенциал ионизации), катионы III аналитической группы образуют основания менее сильные и менее растворимые и, наконец, катионы IV группы образуют основания средней силы и амфотерного характера, трудно растворимые в воде. Тип диссоциации ROH зависит от заряда и радиуса иона. Чем больше заряд и меньше радиус иона, тем больше гидроксосоединение склонно диссоциировать по типу кислот, и наоборот, основные свойства наиболее выражены в соединениях с меньшим зарядом и большим радиусом иона. У амфотерных гидроксидов соотношение заряда и радиуса таково, что они примерно в одинаковой степени проявляют склонность диссоциировать как по кислотному, так и основному типу. Так, все амфотерные гидроксиды имеют соотношения zi/ri в пределах 3–6, в то время как у основных это отношение лежит в пределах 0,6–2,5, а у кислотных – больше 10.
Таким образом, кислотно-основные свойства гидроксидов (характер и растворимость) определяются величинами потенциалов ионизации, которые возрастают при переходе от основных гидроксидов (Ip 8,6 эV), а также от структуры внешнего электронного слоя. А эти функции находятся в прямой зависимости от расположения элементов в периодической системе.
В кислотно-основной классификации элементы, обладающие окислительно-восстановительными свойствами, расположены в IV и V группах (Cr, Sn, As, Bi, Sb, Fe, Mn). Восстановительные свойства элементов находятся в прямой зависимости от потенциалов ионизации. Чем меньше потенциал ионизации, тем лучше выражены восстановительные свойства. Так, наилучшие восстановители – ионы щелочных металлов. По мере увеличения номера групп (т.е. в периодах) увеличиваются ионизационные потенциалы и уменьшается восстановительная способность атомов. В группах снизу вверх по мере возрастания ионизационных потенциалов восстановительная способность падает. Окислительные свойства элементов, атомы которых имеют во внешнем слое ≥ 4 электронов, растут в периодах по мере увеличения порядковых номеров, а в группах – снизу вверх. Так, окислительные свойства соединений Bi выше, чем у Sb и As.
Таким образом, размещение катионов по аналитическим группам основано на свойствах их соединений, которые в значительной степени обусловлены положением элементов в периодической системе. Однако следует отметить, что при тщательном анализе свойств элементов и их соединений можно наблюдать многие отклонения от выявленных тенденций, что является следствием наложения многих факторов и, скорее всего, характеризует сложную, многомерную картину химического процесса, а не отсутствие каких-либо закономерностей.
Основные характеристики аналитических групп в связи с положением катионов
в периодической системе
Первую группу составляют катионы щелочных металлов, расположенных в А-подгруппе первой группы периодической системы. Соли этих катионов представляют собой бесцветные ионные кристаллические вещества, в большинстве своем хорошо растворимые в воде. Указанные атомы обладают единственным s-электроном (s-элементы) на внешнем подуровне, который они легко отдают, образуя ионные структуры. Катионы I группы обладают законченным 2- или 8-электронным внешним слоем. Эти элементы обладают минимальным значением потенциалов ионизации Ip и ионных потенциалов Pi = Z/ri, где Z – заряд иона, ri – ионный радиус. Pi имеет смысл плотности заряда. Также в качестве химико-аналитической характеристики можно пользоваться величиной lg(Ip 2. ri), которая для I группы также имеет минимальное значение 1,35–1,40. Элементы I группы обладают слабой поляризующей способностью и потому, как правило, химические связи обычно имеют ионный характер без смещения электронных оболочек. Вследствие небольших потенциалов ионизации гидроксиды имеют ярко выраженный основной характер и хорошую растворимость в воде.
После знакомства с классификацией катионов учащиеся приступают к выполнению реакций на катионы I–III групп по виртуальному лабораторному практикуму. Все результаты необходимо оформить в виде отчета (табл. 2).
Анализ катионов. Классификация катионов на группы
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Анализ катионов
При систематическом анализе принято деление катионов и анионов на аналитические группы. Наиболее удобная, применяемая и в настоящее время классификация катионов, разработана Н.А. Меншуткиным в 1871 г. Все существующие ныне классификации предусматривают разделение катионов на 5 или 6 аналитических групп на основании следующих их свойств:
1.На различии растворимости хлоридов, карбонатов, сульфатов или гидроксидов.
2. На амфотерных свойствах некоторых гидроксидов.
3. На способности ряда гидроксидов образовывать комплексные аммиакаты.
Классификация катионов на аналитические группы
характеристика
реактив
раствор
Почти все соли калия, натрия, аммония и большинство солей магния хорошо растворимы в воде. Поэтому группового реактива, осаждающего все четыре катиона, нет.
Калий и натрий относятся к 1 группе периодической системы элементов и образуют сильные щелочи. Гидроксид аммония является слабым основанием, но катион аммония близок по свойствам к катиону калия и образует несколько аналогичных малорастворимых солей. Соли аммония разлагаются при нагревании и могут быть удалены прокаливанием. Гидроксид магния – слабое основание, плохо растворимое в воде. Труднорастворимы также фосфат магния и карбонат. Гидроксокарбонат магния растворяется в избытке солей аммония и при действии карбонатом аммония в присутствии хлорида аммония в осадок не выпадает. Поэтому при систематическом анализе ион магния остается в растворе с катионами 1 группы. По этой причине он и отнесен к этой группе.
Ионы калия, магния, аммония необходимы для минерального питания растений. Большое содержание солей натрия указывает на засоленность почв.
Анализ водных вытяжек из почвы на наличие этих катионов используют для определения пригодности почв для возделывания различных культур.
Оценка качества природных вод включает пробы на присутствие ионов аммония. Наличие в воде аммиака и солей аммония служит признаком загрязненности, так как эти соединения образуются при гниении белков.
Продукты детского и диетического питания также подвергаются обязательному исследованию на содержание натрия, калия и магния.
Катионы 2 группы, в отличии от катионов 1 группы, образуют малорастворимые в воде карбонаты. Поэтому их осаждают действием карбоната аммония, который является групповым реактивом.
Сульфиды этих элементов, в отличие от катионов 3,4 и 5 групп, хорошо растворимы в воде.
В водных растворах катионы 2 группы бесцветны.
Соли кальция используют для улучшения почв: в сильно кислые почвы для нейтрализации вводят известняк СаСО3; а в солонцеватые – гипс CaS04•2H2O. Кальций входит в состав минеральных удобрений: фосфоритной муки Са3(РО4)2, суперфосфата Са(Н2РО4)2 + CaS04, кальциевой селитры Са(НСО3)2 и т.д.
Растворимый гидрокарбонат кальция Са(НСО3)2 находится в природных водах, сообщая им временную жесткость. Арсенит и арсенат кальция используют как сельскохозяйственные яды.
Ионы бария ядовиты. Карбонат и хлорид бария используют в сельском хозяйстве как яды. Поэтому обнаружение ионов бария проводят при распознавании ядохимикатов.
Радиоактивный изотоп стронция 90 Sr, образующийся при ядерных реакциях, представляет большую опасность для здоровья и жизни.
Реакции катионов второй группы
| Реактивы | Катионы | ||
| Са 2+ | Ba 2+ | Sr 2+ | |
| (NH4 )2СО3, Nа2СО3, К2СО3 | СаСО3↓ белый | ВаСО3↓ белый | SrСО3↓ белый |
| Na2HP04 | СаНРО4↓ белый | ВаНРО4↓ белый | SrHP04↓ белый |
| (NH4)2C204 | СаС2Н4↓ белый | ВаС2О4↓ белый | SrC204↓ белый |
| H2S04 и растворимые сульфаты | CaS04↓ белый | BaS04↓ белый | SrS04↓ белый |
| К4[Fe(CN)6]+NH4Cl | Ca(NH4)2 [Fe(CN)6] ↓ белый | Ba(NH4)2•Fe(CN)6]↓, белый | ──── |
| CaS04 | BaS04↓ выпадает сразу | SrS04↓ выпадает не сразу | |
| К2Сr207 | ВаСrО4↓ желтый | ───── | |
| Окрашивание пламени | Кирпично- красное | Желто-зеленое | Карминово-красное |
К третьей аналитической группе относят катионы алюминия, железа(II), железа(III), марганца (II), цинка, хрома(III). Они характеризуются большим разнообразием свойств.
Изменение валентности этих элементов осуществляется сравнительно легко, поэтому для них характерны окислительно-восстановительные реакции.
Гидроксиды железа и марганца обладают слабоосновными свойствами, растворяются в кислотах, но не растворяются в щелочах. Гидроксиды всех катионов третьей группы не растворимы в воде, но могут переходить в коллоидное состояние.
Соли большинства элементов этой группы образуют окрашенные растворы.
Окраска растворов солей элементов третьей аналитической группы
зеленая
фиолетовая
Катионы третьей аналитической группы образуют сульфиды, нерастворимые в воде, но растворимые в кислотах. В отличие от них сульфиды первой и второй группы растворимы в воде, а сульфиды четвертой и пятой группы катионов нерастворимы в кислотах. Поэтому в качестве группового реактива используют сульфид аммония. Другие растворимые сульфиды, так же осаждающие катионы третьей группы, не могут быть использованы как групповой реактив, так как с ними в раствор будут введены катионы первой и второй групп. Присутствие катиона аммония в ходе систематического анализа определяется до введения сульфида аммония, а в дальнейшем катион аммония легко удаляется из раствора в виде аммиака. Катионы третьей группы в зависимости от воздействия на них гидр оксида аммония в присутствии хлорида аммония подразделяют на две подгруппы:
катионы аллюминия, хрома(III), железа (III), осаждаемые водным аммиаком в присутствии хлорида аммония.
катионы железа(II), марганца(II), цинка не осаждаемые таким образом.
Катионы третьей группы, подобно катионам второй группы и магния, образуют труднорастворимые карбонаты и гидрофосфаты. Кроме того, они обладают способностью образовывать комплексные соединения.
Обнаружение и количественное определение катионов третьей группы связано главным образом с анализом почв, микроудобрений, растительного и животного материала, продовольственного сырья и продуктов питания (особенно детских и диетических), так как эти катионы имеют важнейшее биологическое значение.
Алюминий в больших количествах содержится в кислых подзолистых почвах, снижая урожайность многих культур. Соли алюминия применяют для очистки природных вод.
Железо содержится в тканях всех растений и животных. Оно входит в состав гемоглобина крови животных, участвует в синтезе хлорофилла зеленых растений. При недостатке железа в почве у растений развивается хлороз, т.е. отсутствие зеленой окраски из-за пониженного содержания хлорофилла. Избыток железа в почве так же вреден для растений. Многие соли железа (лактат, сульфат, глицерофосфат) применяют в ветеринарии как антианемические средства.
Марганец, цинк, хром – микроэлементы, необходимые для нормального течения обменных процессов у растений и животных. Недостаток марганца в почве способствует развитию у них различных заболеваний; в крови – приводит к возникновению „марганцевого рахита”. Нехватка цинка ведет к нарушению синтеза хлорофилла, витаминов, ауксинов у растений, витаминов и ферментов у животных и человека.
Избыток цинка в почвах, продуктах питания, сырье является токсичным для человека, животных и растений. Согласно гигиеническим нормативам качества и безопасности продовольственных продуктов и сырья предельно допускаемое содержание цинка: в мясе- 70,0 мг/кг., в молоке – 5,0 мг/кг., в яйце-50,0 мг/кг.
Реакции катионов третьей группы
| Реактивы | Катионы | |||||
| A1 3+ | Cr 3+ | Fe 3+ | Fe 2+ | Mn 2+ | Zn 2+ | |
| (NH4)2S в щелочной среде | Аl(ОН)3 | Сr(ОН)3↓ | ↓Fе2S3 | ↓FeS | ↓MnS | ↓ZnS |
| NaOH, КОН, NН4ОH | АI(ОН)3 | Сr(ОН)3↓ | ↓Fе(ОН)3 | ↓Fе(ОН)2 | ↓Мn(OН)2 | ↓Zn(ОН)2 |
| NaOH, КОН | Р-р А102 – | Р-р Cr02 – | ↓Fе(ОН)3 | ↓Fе(ОН)2 | ↓Мn(ОН)2 | р-р ZnО2 2- |
| NH4Cl в щел. среде | ↓Аl(ОН)3 | ↓Сr(ОН)3 | ↓Fе(ОН)3 | |||
| Na2HP04 | ↓AlP04 | ↓CrPО4 | ↓FePО4 | ↓Fе3(РО4) | ↓Мn3(РО4) | ↓Zn3(РО4) |
| K4[Fe(CN)6] | ↓Fe4[Fe(CN)6]3 | ↓Fe2[Fe(CN)6] | ↓Мn2[Fе(CN)6] | ↓К2Zn3[Fе(CN)6]2 | ||
| К3[Fе(СN)6] | ↓Fe3[Fe(CN)6] | ↓Мn3[Fе(CN)6]2 | Zn3[Fе(CN)6]2 | |||
| KCNS | Fе(СNS)3 | |||||
| Алюминон | Красный | Красный | Красный | |||
| (NH4)2S208 | Cr207 2- р-р | МnО4 – р-р | ||||
| Дитизон | Красный | |||||
| Cо(NО3)2 | CoZn02 | |||||
| Н2О2 в щелочной среде | Cr204 р-р | Fе(ОН)3 | ||||
Четвертая аналитическая группа объединяет катионы серебра, свинца, и ртути(I). Общим свойством этих катионов является способность осаждаться под действием разбавленной соляной кислоты и ее солей в виде хлоридов-осадков белого цвета. Поэтому соляная кислота является групповым реактивом для катионов этой группы.
Кроме того, катионы четвертой аналитической группы образуют нерастворимые сульфиды черного цвета, которые в отличие от катионов 5 группы, не растворяются в сульфидах натрия, калия, аммония. Мало растворимы в воде также фосфаты и карбонаты катионов четвертой группы. Растворимые соли подвергаются гидролизу и их растворы имеют кислую реакцию. В окислительно-восстановительных реакция катионы четвертой группы выступают в роли окислителей и восстанавливаются до свободных металлов. В водных растворах катионы серебра, свинца и ртути (I) бесцветны.
Соединения катионов четвертой группы имеют важное биологическое значение. Ионы серебра обладают бактерицидным действием. Нитрат серебра применяют в медицине и ветеринарии при эрозиях, язвах, экземах, а также в офтальмологии и стоматологии. Металлическая ртуть и большинство ее соединений очень ядовиты. Наиболее токсичны для животных и человека: хлорид (сулема) и йодид ртути (II) и органические ртутные препараты, применяемые для протравливания семян: гранозан, этилмеркурхлорид, этилмеркурфосфат. Эти соединения нарушают углеводный и кальциевый обмен, функции почек, печени, эндокринных желез, центральной нервной системы вследствие блокады сульфгидрильных групп ферментов. Хлорид ртути (I) или каломель (Hg2CI2) не ядовита и используется в медицине и ветеринарии как слабительное, антисептическое и мочегонное средство.
Соединения свинца также ядовиты. К наиболее токсичным относятся нитрат, ацетат и гидроксохлорид свинца, а так же тетраэтилсвинец. Загрязнение воздуха, почвы и воды соединениями свинца происходит в результате выброса их промышленными предприятиями, выхлопными газами автотранспорта. В соответствии с санитарными нормами содержание свинца в 1 л воды не должно превышать 0.1 мг. В основных сельскохозяйственных продуктах допускается следующее содержание свинца и ртути:
Гигиенические нормативы содержания свинца и ртути в основных продовольственных продуктах, (в мг/кг)
| Мясо | Молоко | Яйца | |
| Свинец | 0,5 | 0,1 | 0.3 |
| Ртуть | 0,03 | 0,005 | 0,02 |
Ацетат свинца и оксид свинца используются в медицине, ветеринарии как вяжущие и противовоспалительные средства в форме примочек, компрессов, мазей и пластырей.
Реакции катионов четвертой группы
| Реактивы | Катионы | |||
| Ag + | Pb 2+ | Нg2 2+ | ||
| HCl и хлориды | AgCl↓ – белый, растворимый в NH4ОH | PbC12↓- белый, растворимый в горячей воде | Hg2C12↓ – белый, чернеющий в NH4ОH | |
| KOH, NaOH | Аg2O↓ – бурый | Pb(OH)2↓- белый, растворимый в кислотах и избытке щелочей. | Hg2О↓- черный | |
| NH40H (избыток) | [Аg(NН3)2] + раствор | Рb(ОН)↓-белый | (NН2Нg)NО3↓- белый + ↓Hg | |
| K2Cr04 | Аg2СrО4↓ кирпично- красный | PbCr04↓ – желтый | Hg2CrО4↓ – красный | |
| H2S04 | ───── | PbS04↓ – белый | ───── | |
| Na2HP04 | Аg3РО4↓ – желтый | ───── | ───── | |
| НI, (KI) | AgI↓- желтый | РbI2↓- желтый, растворимый в горячей воде, NaOH, избытке КI | Hg2I2↓- грязно-зеленый, растворимый в избытке КI | |
| Сu металлич. | ───── | ───── | Hg↓ | |
Катионы пятой группы образуют нерастворимые в воде сульфиды, гидроксиды и основные соли. Гидроксид аммония, который используется как групповой реактив, образует с катионами пятой группы, ярко окрашенные основные соли, которые, кроме солей висмута, растворимы в избытке аммиака. Образующиеся при этом комплексные соли – аммиакаты, также имеют характерную окраску.
Катионы меди, кадмия и висмута, кроме того, образуют комплексные соединения с цианидами и йодидами. В реакциях окисления-восстановления катионы пятой группы ведут себя как окислители и восстанавливаются до свободных металлов.
В водных растворах почти все катионы пятой группы окрашены.
Окраска растворов солей катионов пятой аналитической группы
| Ион | Cu 2+ | Co 2+ | Ni 2+ | Cd 2+ | Bi 3+ |
| Окраска раствора | голубая | розовая | зеленая | бесцветная | бесцветная |
Объектом качественного анализа на присутствие катионов меди, кобальта, никеля, кадмия и висмута являются удобрения, почвы, растения, биологические жидкости, сельскохозяйственное сырье, продовольственные продукты. Медь входит в состав удобрений и сельскохозяйственных ядов, например: медного купороса, парижской зелени Сu(СН3СОО)23Сu(АsО2)2, бордосской жидкости. Медь необходима для нормальной жизнедеятельности растений и животных, так как входит в состав ферментов, влияет на белковый и углеводный обмен. Сульфат и карбонат меди используют в ветеринарии как антгельминтики. Медь отнесена к токсичным элементам. Предельно допустимое содержание меди в некоторых продуктах питания приведено в таблице N29. Кобальт входит в состав витамина В12. Пониженное содержание этого микроэлемента в почвах, растениях, кормах и пищевых продуктах отрицательно сказывается на росте сельскохозяйственных культур, продуктивности животных и развитии человека. Избыточное содержание кобальта, как и меди, и кадмия считается токсичным.
Гигиенические нормативы содержания меди и кадмия в основных продовольственных продуктах, (в мг/кг)
| Мясо | Молоко | Яйца | |
| Медь | 5.0 | 1.0 | 3.0 |
| Кадмий | 0.05 | 0.03 | 0.01 |
Мышьяк /III/, сурьма/III/ и олово /III/ в щелочной среде ведут себя как восстановители. Мышьяк /V/, cурьма /V/ в кислой среде проявляют свойства окислителей.
Характерной реакцией для катионов 6 группы является образование нерастворимых в воде сульфидов при взаимодействии с сероводородом в кислой среде. Сульфиды катионов 6 группы растворяются в сульфидах натрия, калия, аммония, образуя сульфосоли (тиосоли). Например:
Сульфосоли по своему составу подобны кислородосодержащим кислотам тех же элементов с той разницей, что роль кислорода здесь играет элемент, ему аналогичный – сера.
Использование сероводорода в качестве группового реактива сопряжено с многочисленными трудностями.
Бессероводородный метод качественного анализа предусматривает осаждение катионов 6 группы (олова и сурьмы) едкими щелочами. При этом образуются соединения нерастворимые в воде, обладающие способностью растворяться в избытке щелочей.
В ветеринарии соединения мышьяка применяют в качестве противопаразитарных средств и веществ, улучшающих обмен (осарсол, новарсенол, натрия арсенат).
Продовольственные продукты и сельскохозяйственное сырье подлежат обязательному анализу на присутствие мышьяка. Предельно допустимое содержание мышьяка составляет: в мясе- 0.1 мг/кг, в молоке- 0.05 мг/кг, в яйце – 0.1 мг/кг.
Биологическая роль сурьмы и олова выяснена недостаточно. В ветеринарии используют сульфиты сурьмы /III/ и /V/ в качестве отхаркивающих средств, арсенат олова как антгельминтик.