О компании BIOCAD
Компания BIOCAD создана в 2001 году. Это одна из крупнейших международных инновационных биотехнологических компаний в России, объединившая научно-исследовательские центры мирового уровня, современное фармацевтическое и биотехнологическое производство, доклинические и клинические исследования, соответствующие международным стандартам. В штате компании около 2700 человек, почти треть — научные сотрудники и исследователи.
BIOCAD ведет полный цикл создания лекарственных препаратов: от поиска молекулы до массового производства и маркетинга. Компания фокусируется на препаратах для терапии онкологических, аутоиммунных и инфекционных заболеваний, также ведет разработки в области терапии других социально значимых заболеваний. Продуктовый портфель в настоящее время состоит из 61 лекарственного препарата, из которых 9 — оригинальные, а 22 продукта — биологические. Еще более 40 продуктов находятся на разных стадиях разработки.
ПОРТФЕЛЬ
61 продукт, 22 из которых — биологические
РАЗРАБОТКА
Более 40 препаратов находятся в разработке
СОТРУДНИКИ
2700 человек, треть — ученые и исследователи
НАШИ
ВЗГЛЯ
ДЫ
Миссия
Улучшение и продление жизни людей посредством предоставления эффективных, безопасных и доступных комплексных решений в области лекарственного обеспечения
Видение
BIOCAD – российская инновационная биотехнологическая компания полного цикла с преобладанием экспортной выручки, являющаяся лидером в странах присутствия на рынке лекарственных препаратов для лечения тяжелых хронических заболеваний
Станьте частью нашей компании
НАШИ ЦЕН НОС ТИ
Команда
В BIOCAD принято говорить: «Мы вместе достигли результатов», признавая участие и роль каждого и силу синергии команды
Вовлеченность
Вовлеченность в свое дело – это то, что отличает сотрудников BIOCAD, это основа удовольствия от работы и удивительных результатов, которые достигает команда
Саморазвитие
BIOCAD – компания, построенная на экспертизе. Для нас задачи каждого дня – это непрерывное повышение профессионального уровня
Честность
Говорить правду не всегда просто, но только открытое обсуждение и корректная обратная связь могут продвинуть нас в решении сложных задач и сделать нас лучше
Целеустремленность
Каждый из нас ориентируется на результат и имеет привычку считать, что все возможно. Мы умеем преодолевать возникшие преграды и никогда не опускаем руки, решая задачи
Ответственность
Наша ответственность – в рациональном использовании ресурсов нашей компании, готовности каждого брать ответственность на себя, принимать решения и быть внимательным к деталям
Осознанность
Строительство производства готовых лекарственных форм
Создание R&D центра на базе советского института инженерной иммунологии
Вывод на рынок препарата Лейкостим (филграстим) – первого российского гранулоцитарного колониестимулирующего фактора
Открытие второго R&D центра
Реализация программы «Организация опытно-промышленного производства субстанций и лекарственных средств на основе моноклональных антител
Вывод на рынок первого в России оригинального препарата для лечения гепатита С
– Альгерон. (цепэгинтерферон альфа-2b)
Вывод на рынок первого российского препарата на основе моноклональных антител
BIOCAD завершил регистрацию лекарственных препаратов Бевацизумаб и Трастузумаб, был открыт новый R&D центр в Санкт-Петербурге, включающий восемь современных лабораторий
Многовекторная международная экспансия в регионы ЮВА, МЕНАТ, ЛАТАМ. Создание нового научного комплекса – отдела перспективных исследований
Строительство производственных площадок в России и Финляндии. Открытие международных офисов в Египте и во Вьетнаме. Расширение продуктового портфеля для лечения аутоиммунных заболеваний
Зарегистрирован первый отечественный биоаналог инфликсимаба. Строительство четырех производственных площадок. Старт продаж на семи новых международных рынках
Зарегистрирован первый российский оригинальный препарат на основе моноклональных антител для лечения псориаза. BIOCAD занимался его разработкой 8 лет.
К 20-летию BIOCAD рассказываем историю становления компании
BIOCAD —
развитие
в мире
BIOCAD поддерживает высокое качество продукции, совершенствует технологии и оптимизирует процессы, расширяя свою деятельность за пределами России. BIOCAD создал международную группу компаний в ОАЭ, Бразилии, Вьетнаме и Китае (совместное предприятие), продукты компании реализуются в более чем 30 странах. Синергия знаний в области R&D, управления, качества и продаж позволяет не только укреплять лидерскую позицию в России но и продолжать активную географическую экспансию.
Глобальная стратегия BIOCAD по расширению бизнеса ориентирована на выбор формата, наиболее подходящего для конкретного рынка: локальный офис, дистрибуция, технический трансфер или совместное предприятие. Биоаналоги и инновационные продукты на основе моноклональных антител в портфеле BIOCAD востребованы как на активно развивающихся рынках, так и в развитых странах. Наибольший интерес представляют страны Ближнего Востока и Северной Африки, СНГ и Юго-Восточной Азии, некоторые страны Южной Америки, Китай и Европа.
BIOCAD
Ведущая российская инновационная компания с международным присутствием, объединившая научно-исследовательский центр мирового уровня, ультрасовременное фармацевтическое и биотехнологическое производство, доклинические и международные клинические исследования, соответствующие современным стандартам.
Показать полностью.
BIOCAD — одна из немногих в мире компаний полного цикла создания лекарственных препаратов: от поиска молекулы до массового производства и маркетинговой поддержки. Компания фокусируется на препаратах для терапии онкологических, аутоиммунных и инфекционных заболеваний, также ведет разработки в области терапии других социально значимых заболеваний.
Штат компании — 2500 человек, около 40% — научные сотрудники и исследователи.



BIOCAD запись закреплена
Дмитрий Морозов стал лучшим топ-менеджером 2021 года по версии газеты «Деловой Петербург»!
Традиционно ближе к концу года «Деловой Петербург» проводит награждение лауреатов проекта «Топ-100». Это рейтинг самых эффективных топ-менеджеров ведущих компаний Санкт-Петербурга и Ленинградской области.
Наш генеральный директор Дмитрий Морозов одержал победу в главной номинации и был признан «Лучшим топ-менеджером» 2021 года. Поздравляем!
Также оставляем ссылку на интервью Дмитрия Валентиновича, где он рассказал, как компания росла вместе с фармацевтической отраслью, почему ее успех нельзя повторить и как управлять командой: https://www.dp.ru/a/2021/11/18/Menshe_riskov__menshe_do
BIOCAD запись закреплена
Проект нашей компании занял II место в специальной номинации премии «За верность науке»
28 ноября наших коллег наградили в Государственном Кремлевском дворце всероссийской премией «За верность науке», которая ежегодно вручается за выдающиеся достижения в области научной коммуникации, популяризации науки и поддержки престижа деятельности ученых и инженеров в нашей стране.
Показать полностью.
Наш проект «Цикл лекций для школьников и студентов от BIOCAD» занял второе место в специальной номинации «Стратегии научно-технологического развития». Прикрепляем ссылки на курсы проекта:
Как один из лидеров фармацевтической индустрии, мы осознаем важность популяризации и продвижения знаний: от быстрого развития биотехнологий зависит не только успех нашего бизнеса, но и качество и доступность лекарственных препаратов для пациентов в ближайшем будущем. Для нашей команды большая честь одержать эту победу, так как популяризация науки — одно из ключевых направлений BIOCAD.
Отдельное спасибо всем коллегам-авторам лекций и образовательному центру «Сириус», который выступил площадкой для наших курсов. Вместе мы повышаем научный потенциал нашей страны!
BIOCAD запись закреплена
BIOCAD запись закреплена
Наше совместное предприятие с Shanghai Pharmaceuticals Holding включило первого пациента в III фазу международного многоцентрового клинического исследования нашего оригинального препарата Фортека® (МНН пролголимаб) в Китае.
«Китайский рынок является очень важным для нас по многим причинам, прежде всего из-за усилий китайских властей по обновлению и модернизации системы здравоохранения, — говорит Дмитрий Морозов. — Программы помощи гражданам по лечению онкозаболеваний в этой стране открывают широкие перспективы для наукоемких бизнесов по всему миру. Для нас также принципиально, что это наш первый опыт интеграции продуктов компании в Китае, и мы благодарны нашим китайским партнерам за слаженную работу и искреннюю заинтересованность в сотрудничестве».
BCD-100-3/DOMAJOR — международное клиническое исследование нашего оригинального чекпойнт-ингибитора PD1 у пациентов с немелкоклеточным раком легких (НМРЛ). Ожидается, что препарат будет доступен для китайских пациентов уже в 2026 году.
BIOCAD запись закреплена
Псориаз — хроническое воспалительное заболевание, влияющее на качество жизни человека. Несмотря на то, что характерные проявления псориаза — это бляшки на коже, заболевание не считают только дерматологическим. У пациентов велик риск поражения нескольких систем органов, а значит, это системное заболевание.
Показать полностью. Нередко псориаз сопровождают псориатический артрит, сердечно-сосудистые заболевания и депрессия. В мире насчитывается около 125 миллионов пациентов с псориазом, в России около 1% населения страдают от этого заболевания.
Почему возникает псориаз? Невозможно назвать одну-единственную причину, это всегда совокупность различных факторов. Начало болезни может быть вызвано стрессом, травмой, перенесенным ранее заболеванием. Например, известно, что триггером может стать стрептококковая инфекция: стрептококковые М-белки очень похожи на человеческий кератин-17, белок клеток кожи (кератиноцитов). В результате болезни иммунная система начинает распознавать белки организма как чужие и идет в атаку. В коже может начаться хроническое воспаление, в результате которого кератиноциты бесконтрольно и бесцельно делятся, в итоге развивается псориаз.
Также обнаружена связь с факторами генетики, окружающей средой, образом жизни. Более высокий риск развития болезни у людей с лишним весом, у тех, кто курит и в больших количествах употребляет алкоголь.
Псориаз — хроническое заболевание, способа окончательно победить его до сих пор нет, но возможно взять проявления болезни под контроль. Выбор терапии зависит от состояния пациента, степени тяжести и клинических проявлений. Для средней и тяжелой степени тяжести псориаза применяют: традиционные системные препараты, ПУВА-терапию и таргетные препараты, включающие синтетические таргетные средства, малые молекулы или генно-инженерные биологические препараты (ГИБП). Последние направлены на блокирование сигнальных путей, которые вызывают аномальную активацию иммунных клеток, приводящую к хроническому воспалению. Например, интерлейкин-17 (IL-17) играет важную роль в патогенезе псориаза: он привлекает иммунные Тh17-клетки к месту воспаления, взаимодействуя с рецептором IL-17R на их поверхности. Препараты на их основе действуют избирательно и минимально вмешиваются в работу иммунной системы.
BIOCAD: взгляд изнутри
BIOCAD: взгляд изнутри
Офис компании BIOCAD в особой экономической зоне Нойдорф (Санкт-Петербург)
Автор
Редакторы
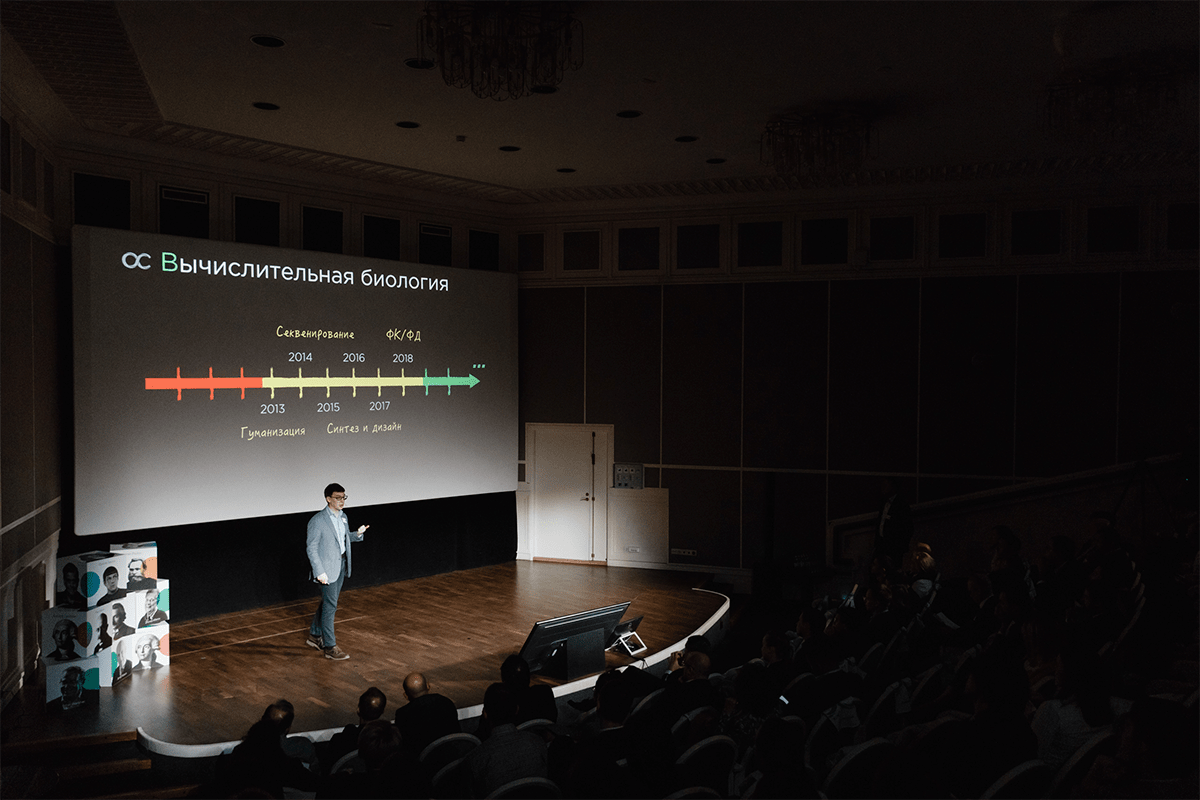
Сегодня BIOCAD — одна из крупнейших российских фармацевтических компаний, специализирующаяся в том числе на разработке терапевтических моноклональных антител. Департамент вычислительной биологии (ДВБ) занимается биоинформатическим моделированием этих молекул, тем самым оптимизируя их разработку. Тому, как устроена компания в целом и ДВБ в частности, посвящена заключительная статья спецпроекта о терапевтических антителах.
Терапевтические антитела
Спецпроект об антителах, истории их изучения, методах работы с ними, а также о применении антител в современной медицине и биотехнологии.
Партнер спецпроекта — Департамент вычислительной биологии одной из крупнейших российских биотехнологических компаний — BIOCAD. BIOCAD заслужил серьезные позиции на мировом фармацевтическом рынке благодаря выпуску лекарственных препаратов на основе антител.
Эта статья закрывает наш цикл публикаций, посвященных моноклональным антителам. Партнер спецпроекта — департамент вычислительной биологии (ДВБ) компании BIOCAD, являющейся пионером в разработке терапевтических препаратов на основе моноклональных антител в России. В этом материале мы расскажем о деятельности компании в целом и ДВБ в частности.
История BIOCAD
BIOCAD, одна из крупнейших российских биотехнологических компаний, появилась почти 20 лет назад, в 2001 году, открыв производство лекарственных средств в поселке Ильинское (Московская область). R&D-центр компании открылся лишь в следующем (2002) году на базе Института инженерной иммунологии в Москве. В нем начались работы по разработке, апробации и продвижению новых продуктов компании на фармацевтический рынок.
R&D — исследования и разработки (от англ. Research & Development). Русский аналог — НИОКР (научно-исследовательские и опытно-конструкторские работы). — Ред.
Лекарства, производящиеся BIOCAD, мы выделили в тексте зеленым шрифтом. — Ред.
Чтобы начать уверенно развиваться, разрабатывать и производить оригинальные препараты, BIOCAD сделал ставку на оптимизацию рутинных процессов путем внедрения роботов и автоматизации различных процедур. С одной стороны, такой подход позволил «разгрузить» исследователей, существенно ускорив разработку препаратов. С другой — автоматизация породила получение больших объемов данных, которые стало необходимо быстро и грамотно анализировать. В том числе этим и занимается Департамент вычислительной биологии, о котором мы подробнее расскажем чуть позже.
Моноклональные антитела — визитная карточка BIOCAD, благодаря чему компания и стала партнером спецпроекта о терапевтических антителах, заключительный материал которого вы читаете в данный момент. Что собой представляют и зачем нужны моноклональные антитела, вы можете прочесть в других статьях спецпроекта: «Краткая история открытия и применения антител» [2], «Антитело: лучший способ распознать чужого» [3], «Биотехнология антител» [4] и «Терапевтические моноклональные антитела» [5]. — Ред.
Три года работы — и в 2014 году BIOCAD зарегистрировал «Ацеллбию®» — первый препарат на основе моноклональных антител. Это биоаналог знаменитого ритуксимаба — терапевтического антитела против белка CD20 на поверхности В-лимфоцитов, предназначенного для лечения В-клеточных лимфом [4].
Годом позже компания выпустила сразу два препарата на основе моноклональных антител — «Авегру®» и «Гертикад®» (биоаналоги бевацизумаба и трастузумаба, соответственно). Бевацизумаб — антитело к эндотелиальному фактору роста А (VEGF-A), блокирующее ангиогенез (рост сосудов) в опухоли; трастузумаб — антитело к молекуле Her2/neu, избыточное накопление которой в клетках ведет к развитию рака молочной железы [2].
Итак, расширив производство и обзаведясь двумя R&D-центрами, BIOCAD постепенно смещает фокус разработок с биоаналогов и дженериков на производство оригинальных препаратов по трем направлениям:
На фармацевтическом рынке в условиях жесткой конкуренции BIOCAD стремится к расширению продуктовой линейки, и сейчас выпускает около 60 препаратов, основные действующие вещества которых — моноклональные антитела, рекомбинантные колониестимулирующие факторы, антиметаболиты и алкалоиды, а также производные платины, таксаны (рис. 1). На стадии разработки находятся, в том числе, лекарства против наследственных заболеваний, например, гемофилии (см. врезку). BIOCAD планирует также пополнить портфель препаратами для лечения сердечно-сосудистых, офтальмологических заболеваний и анемии.
Рисунок 1а. Продуктовый портфель BIOCAD
Рисунок 1б. Продуктовый портфель BIOCAD
Лечение гемофилии: опыт BIOCAD
Гемофилия — генетическое заболевание, связанное с мутациями в различных факторах свертываемости крови, в результате которых любое пустяковое кровотечение может оказаться летальным [6]. Как правило, терапия гемофилии заключается во введении пациентам факторов свертываемости крови, находящихся у них в дефиците.
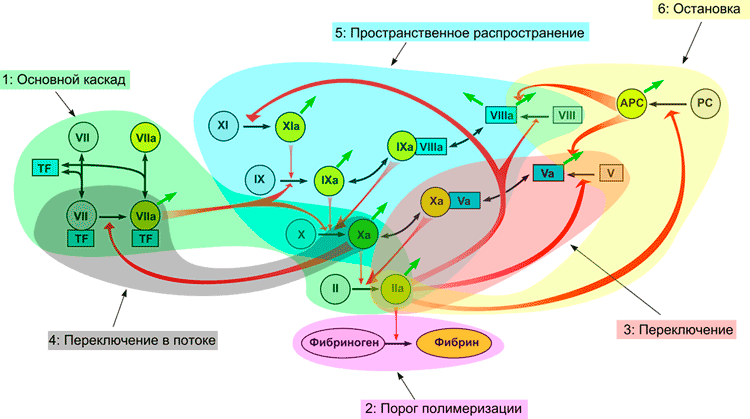
На рисунке 2 показан полный механизм свертывания крови, и любой из белков, в нем участвующих, может быть поврежден. Выделяют три типа гемофилии. При типе А дефектен фактор VIII, при типах В и С — факторы IX и XI соответственно.
Рисунок 2. Модульная структура системы свертывания: роль отдельных реакций свертывания в функционировании системы. Отсутствие факторов свертывания VIII, IX и XI вызывает гемофилию типов A, B или C соответственно.
Идея компании BIOCAD — создать геннотерапевтический препарат на основе аденоассоциированных вирусных векторов, которые будут доставлять «правильный» вариант сломанного фактора свертываемости непосредственно в клетки пациента с гемофилией. Сложность такого подхода заключается в том, что некоторые гены, кодирующие факторы свертываемости (например фактор VIII) настолько велики, что их очень сложно упаковать в вирусную частицу. В связи с этим в компании BIOCAD создана научная группа, которая работает над увеличением размера капсида, внося изменения в структуру вирусного белка, формирующего капсид.
Продукты BIOCAD в первую очередь реализуются в России, что чрезвычайно важно в условиях импортозамещения. В 2018 году компания заняла первое место в рейтинге российских быстрорастущих высокотехнологичных компаний. Однако BIOCAD активен и на международных рынках, что редкость для российских фармацевтических компаний. Сейчас у компании открыты представительства в восьми странах, а продукция экспортируется в более чем 20 стран. В 2018 году выручка компании составила 21,7 миллиардов рублей. Интересно, что почти 80% выручки компании приносят противоопухолевые препараты, такие как «Гертикад®», «Ацеллбия®» и «Авегра®» (рис. 1).
Обеспечивают такие масштабы оборота четыре производственные площадки, находящиеся в Стрельне (Санкт-Петербург), пос. Любучаны (Московская область) и селе Петрово-Дальнее (Московская область). В ближайшие годы ожидается появление еще четырех новых производств.
Расширение производства влечет за собой и увеличение кадрового состава компании (рис. 3): сегодня это более 2000 человек (из которых около 40% — ученые и исследователи), и тенденция к росту сохраняется.
Рисунок 3а. Стратегическая сессия руководителей компании BIOCAD (Сочи, май 2019 г.)
Рисунок 3б. Стратегическая сессия руководителей компании BIOCAD (Сочи, май 2019 г.)
BIOCAD — компания полного цикла: здесь происходит и разработка, и производство лекарств. За каждый этап работы отвечает свой департамент. Так, разработка лекарства начинается в Департаменте вычислительной биологии; in vivo влияние препарата на организм исследуется в Департаменте доклинических испытаний; а Департамент клинических исследований проводит все их стадии как силами самой компании, так и с привлечением CRO (contract research organization, контрактная исследовательская организация ).
Подробнее о том, как устроены клинические исследования, можно прочитать в статьях одноименного спецпроекта. В частности, в статье «Клинические испытания в России — истории успеха» [7] рассказано о наиболее ярких представителях отечественных CRO. — Ред.
Социальные инициативы BIOCAD
Успешный в долгосрочной перспективе бизнес зависит не только от уровня продаж, но и от ценностей, которые он транслирует обществу. В случае BIOCAD это увеличение продолжительности и улучшение качества жизни. Популяризация науки и инвестиции в образование — основные направления социальной активности компании.
Привлечение и подготовка молодых ученых — одно из долгосрочных стратегических направлений развития научной и технологической базы BIOCAD. В 2017 году компания открыла факультет молекулярной и клеточной биологии в Пущинском государственном естественнонаучном институте (ПущГЕНИ). Годом позже на базе Московского физико-технического института (МФТИ) BIOCAD создал лабораторию вычислительной биологии, в которой ведутся научные проекты под руководством опытных менторов из Вычислительного центра РАН, Института вычислительной математики, Института системного анализа и других профильных учреждений. Для обеспечения успешного роста кадрового состава BIOCAD также проводит стажировки внутри компании для студентов старших курсов, по результатам которых предлагает дальнейшее трудоустройство. Кроме того, сотрудники компании читают лекции в ведущих вузах страны, таких как МГУ имени М.В. Ломоносова, КФУ, РНИМУ имени Н.И. Пирогова и других.
BIOCAD планирует участвовать и в школьном образовании. В 2018 году в Парке науки и искусств образовательного центра «Сириус» компания открыла лабораторию генно-инженерных технологий, на базе которой проводит образовательные программы по молекулярной биологии.
Налаживание контактов между представителями науки и бизнеса — еще одна стратегическая цель BIOCAD. Для этого с 2017 года компания организует конференцию BiotechClub, где обсуждаются вопросы медицины, биоинформатики и биотехнологий (см. врезку и рис. 3).
Конференция BiotechClub
BiotechClub — это не только ежегодная научная конференция, организованная компанией BIOCAD, но и сообщество ведущих российских ученых и предпринимателей, готовых к диалогу, обмену опытом и знаниями.
Задача компании BIOCAD в рамках конференции — создать продуктивную платформу для взаимодействия и тесной кооперации между наукой и бизнесом, предоставить комфортные условия для презентации новых знаний в сфере биотехнологий и способствовать популяризации науки и научных профессий.
Конференция проходит третий год, тема этого года — «Генетические технологии: вызовы и возможности». В 2018 году в мероприятии приняли участие более 600 очных и более 2000 онлайн-слушателей, 50 спикеров выступили с докладами в области биотехнологии, биоинформатики, онкологии и генетики.
Мы знаем интересы и запросы научного сообщества России, поэтому и программу конференции всегда формируем так, чтобы каждый участник нашел пользу для себя. На BiotechClub 2019 мы обсудим основные актуальные вопросы, касающиеся генетических технологий.
На сессии «Генодиагностика и генотерапия» — применение генодиагностики, генной и клеточной терапий в области гематологии, онкологии и орфанных заболеваний.
В рамках сессии «Редактирование генома» будут представлены доклады, посвященные различным аспектам геномного редактирования и его применения в терапии заболеваний.
В сессию «Генетическая инженерия в фармацевтике» включены доклады о применении технологий генной и клеточной инженерии в разработке лекарственных препаратов, подходах к созданию инновационных клеточных моделей, регенеративной медицине, генной терапии тяжелых наследственных заболеваний и онколитических вирусов.
И, наконец, задача сессии «Геномная биоинформатика» — ёмко осветить современные тенденции применения биоинформатики и вычислительной биологии в различных аспектах анализа генетических данных. Доклады коснутся современных методов диагностики, анализа микробиома, глубокого изучения соматического мутагенеза иммунных рецепторов, а также конструктивных методов создания лекарственных средств, основанных на накопленных данных и развивающемся математическом моделировании.
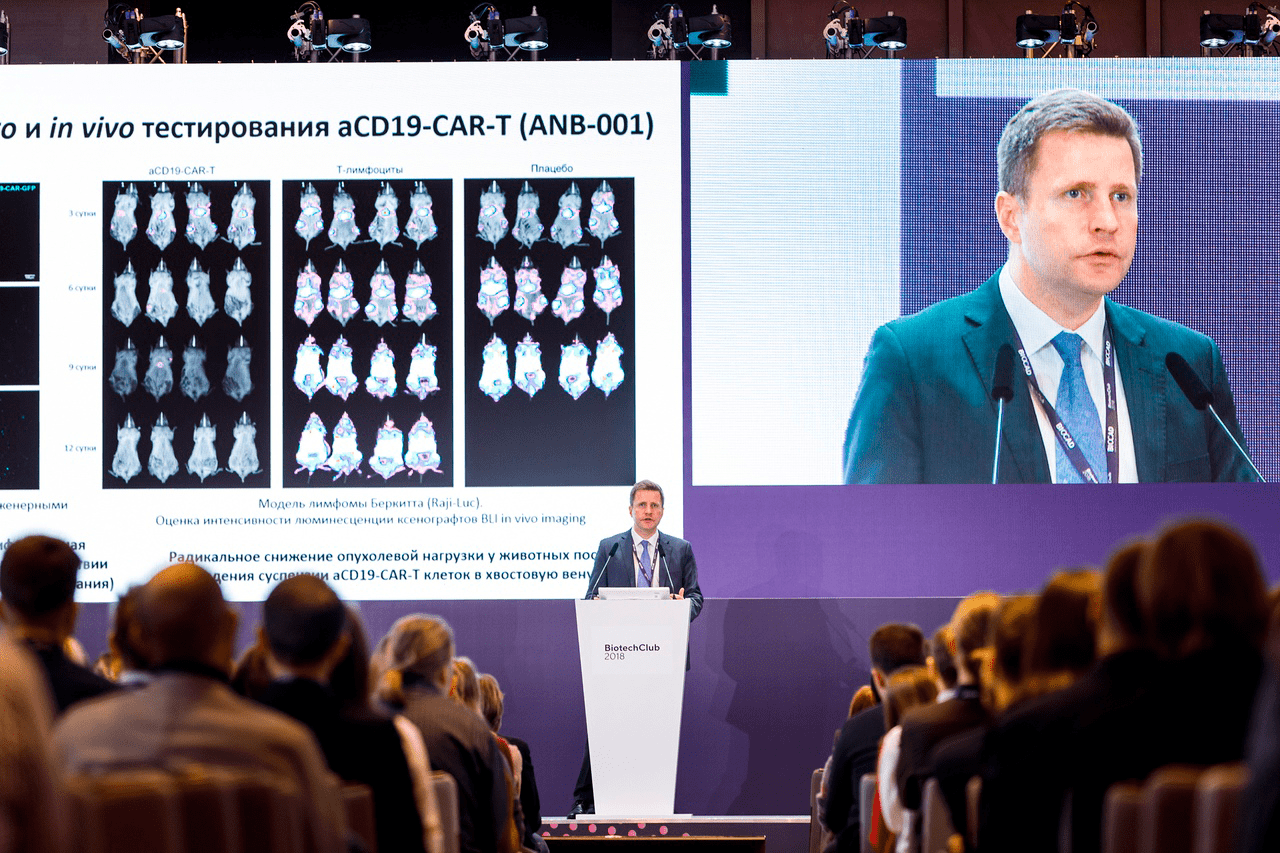
Рисунок 4а. Фотографии с конференции BiotehClub 2018. На фото — пленарное заседание From Systems Biology to Systems Medicine. Выступление академика Сергея Лукьянова.
Рисунок 4б. Фотографии с конференции BiotehClub 2018. На фото — пленарное заседание From Systems Biology to Systems Medicine. Выступление вице-президента компании BIOCAD Романа Иванова.
Рисунок 4в. Фотографии с конференции BiotehClub 2018. На фото — пленарное заседание From Systems Biology to Systems Medicine. Выступление вице-президента компании BIOCAD Романа Иванова.
Материал предоставлен партнёром — Департаментом вычислительной биологии компании BIOCAD
Помимо вовлеченности компании в образовательную деятельность, на базе BIOCAD проходят программы для пациентов и практикующих врачей, основной фокус которых — ранняя диагностика онкологических заболеваний и современные методы их лечения.
Департамент вычислительной биологии — не только биоинформатика
Несомненно, каждый департамент в компании важен и незаменим. Однако, как и в любом деле, начальные этапы являются зачастую ключевыми для успеха всей дальнейшей работы. В Департаменте вычислительной биологии (ДВБ) осуществляют дизайн молекулы, моделирование ее взаимодействия с мишенью, а также последующие этапы компьютерной доработки молекул, которые составляют основу будущего лекарственного препарата (рис. 5).
Рисунок 5а. Рабочие будни департамента вычислительной биологии BIOCAD
Рисунок 5б. Рабочие будни департамента вычислительной биологии BIOCAD
Рисунок 5в. Рабочие будни департамента вычислительной биологии BIOCAD
Рисунок 5г. Рабочие будни департамента вычислительной биологии BIOCAD
Изначально биоинформатикой в BIOCAD занималось лишь несколько человек, перед которыми ставили задачи по компьютерному моделированию конкретной молекулы и ее взаимодействию с клетками организма. Однако с расширением продуктовой линейки и добавлением в нее моноклональных антител появилась необходимость в увеличении вклада биоинформатиков в деятельность компании, что и привело к появлению ДВБ как отдельного подразделения. Молекулярная генетика, системная биология [8] и биомоделирование — основные фокусы деятельности ДВБ. Помимо этого, департамент помогает разрабатывать программное обеспечение для роботизации производства лекарственных препаратов.
Методы вычислительной биологии, использующиеся в ДВБ BIOCAD
ДВБ использует множество вычислительных методов, позволяющих не только улучшать уже существующие препараты, но и конструировать новые, а также совмещать прикладную и фундаментальную науки, внося вклад в понимание структурных особенностей антител и ферментов (рис. 6). Эта глава расскажет о «внутренней кухне» ДВБ — тех методах и подходах, которые ему удается эффективно использовать в работе.
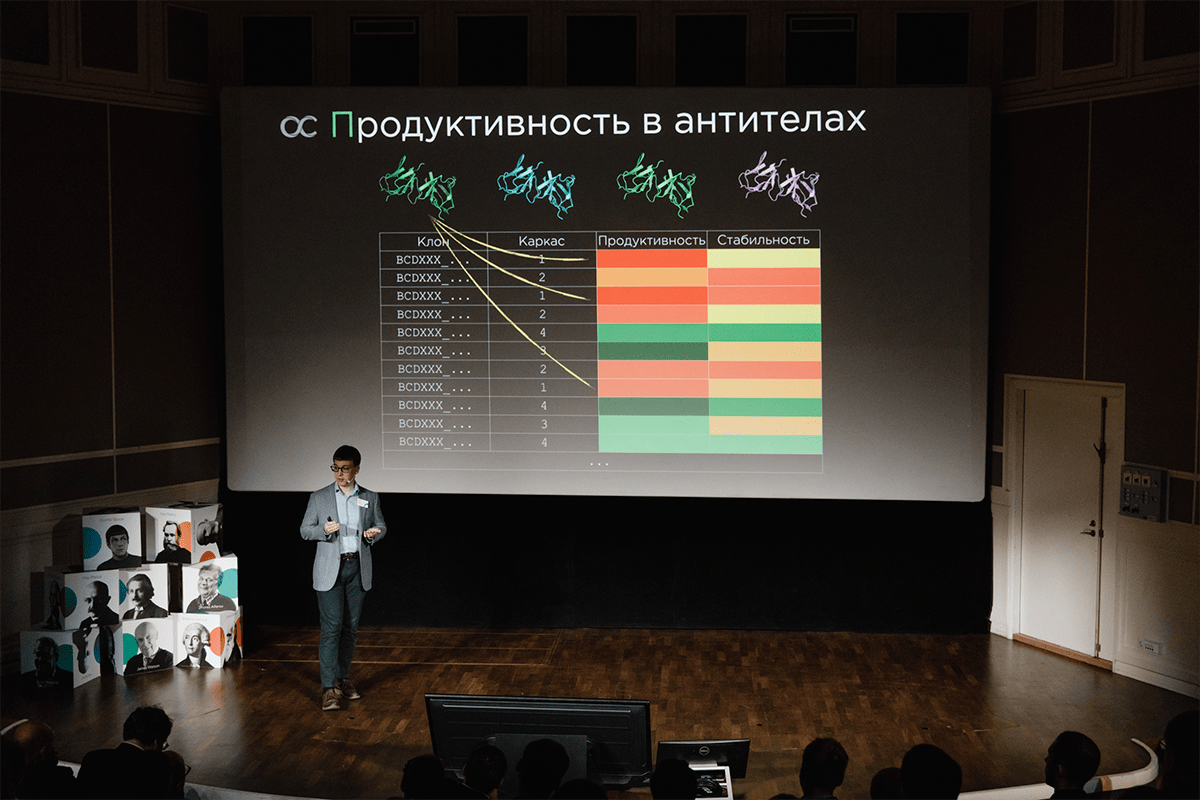
Рисунок 6а. Лекция руководителя департамента вычислительной биологии Павла Яковлева в рамках стратегической сессии руководителей компании о перспективах развития биоинформатики в BIOCAD (Сочи, май 2019 г.)
Рисунок 6б. Лекция руководителя департамента вычислительной биологии Павла Яковлева в рамках стратегической сессии руководителей компании о перспективах развития биоинформатики в BIOCAD (Сочи, май 2019 г.)
Рисунок 6в. Лекция руководителя департамента вычислительной биологии Павла Яковлева в рамках стратегической сессии руководителей компании о перспективах развития биоинформатики в BIOCAD (Сочи, май 2019 г.)
Рисунок 6г. Лекция руководителя департамента вычислительной биологии Павла Яковлева в рамках стратегической сессии руководителей компании о перспективах развития биоинформатики в BIOCAD (Сочи, май 2019 г.)
Гуманизация антител
Самым первым способом получения моноклональных антител стал метод гибридом — слияние мышиных специфичных В-лимфоцитов и клеток миеломы (о нем мы подробно рассказывали в первой статье спецпроекта [12], а также в публикации «Моноклональные антитела» [9] и комиксе «Открытие моноклональных антител» [10]). Одна из основных проблем антител, полученных таким образом, — их иммуногенность: фрагменты антител животных распознаются иммунной системой человека как чужеродные антигены, а развивающийся против них иммунный ответ может повредить собственные органы и ткани пациента.
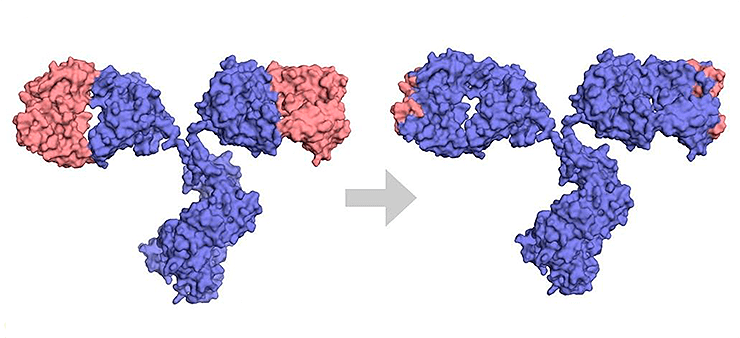
Чрезвычайно важно минимизировать иммуногенность терапевтических антител, не ослабив при этом их способность распознавать антиген. Это можно сделать за счет изменения аминокислотных последовательностей антител животного на другие, не распознающиеся иммунной системой человека, без потери целевых качеств. Соответственно, долгое время при создании терапевтических антител ученые постепенно заменяли части молекулы на человеческие (рис. 7). Так появились типы антител, различающиеся по степени их «очеловечивания» [4]:
Рисунок 7. Разница между химерными и гуманизированными антителами. Синим показаны человеческие последовательности, оранжевым — мышиные.
Ранее считалось, что безопасность антител возрастает в ряду животные → химерные → гуманизированные → полностью человеческие. Однако в ходе анализа результатов клинических исследований препаратов на основе моноклональных антител было показано, что такая прямая связь существует далеко не всегда. Полученные результаты BIOCAD представил на конференции ВОЗ в 2017 году [11], что заставило организацию пересмотреть свою позицию касательно данной темы.
Один из перспективных подходов к снижению иммуногенности терапевтических антител — их направленная гуманизация: внесение некоторого количества мутаций, которые не влияют на работоспособность, но делают молекулы «невидимыми» для иммунной системы пациента. Для решения этой задачи в ДВБ был создан и постоянно совершенствуется вычислительный алгоритм, подбирающий мутации в ходе дизайна каждого конкретного терапевтического антитела.
В ДВБ разработали протокол для предсказания структуры вариабельных фрагментов антител. Применение знаний о принципах их трехмерной укладки и внутримолекулярных взаимодействий привело к достижению гораздо более высокой точности моделирования, чем при использовании стандартного докинга для произвольных белков. Именно поэтому в департаменте ведут работы по предсказанию трехмерной структуры антитела даже без использования рентгеноструктурного анализа! Добавив к этому разнообразные подходы для предсказания посттрансляционных модификаций белков и моделирования их агрегации, можно получить максимально приближенную к реальности модель терапевтического антитела, существенно сократив и удешевив этим его производство и дальнейший анализ.
Направленный дизайн антител
Одной из сложнейших задач современной биологии является проблема фолдинга (образования третичной структуры) белка [12]. Укладка аминокислотной цепочки определяет основные функции молекулы и, значит, критически важна для предсказания ее свойств. Хотя в общем случае проблема фолдинга до сих пор не решена, для определенных групп белков (например антител) можно найти частные решения. Поскольку получение моноклональных терапевтических антител является для компании BIOCAD одной из важнейших задач, в ДВБ разрабатывают и постоянно улучшают вычислительные алгоритмы, позволяющие по аминокислотной последовательности антитела предсказывать его 3D-структуру и судить о потенциальных мишенях и силе связывания с ними.
Виртуальное моделирование каркаса молекулы позволяет не только анализировать уже готовую аминокислотную цепочку антитела, но и добавлять к ней функциональные группы (например, фосфатные, ацильные или гликозидные), обеспечивающие требуемые свойства. Предсказание же сайтов посттрансляционных модификаций и уровня их активности помогает понять, как замена той или иной аминокислоты в одном белке влияет на его связывание с другими белками, что критически важно для антитела.
Метод белок-белкового докинга позволяет моделировать взаимодействие белковых молекул для поиска и изучения сайтов, в которых оно происходит [13]. Ноу-хау ДВБ является метод гибкого белок-белкового докинга. Он отличается от стандартного подхода тем, что здесь белки представляют собой не жесткие каркасы, а гибкие модели. В этой технологии применяются графические процессоры (GPU), что позволяет существенно ускорить вычисления.
Сотрудники ДВБ разработали собственную методику эпитопного картирования, которая состоит из одновременного конструирования моноклонального антитела и прогнозирования его взаимодействия с белком-мишенью. Это чрезвычайно удобно, поскольку от того, в каком именно месте моноклональное антитело распознает молекулу-мишень, зависит его терапевтический эффект (например, блокировка или активация рецептора, фактора роста, цитокина или иной мишени), а также возможные побочные реакции.
Для анализа взаимодействия антитела с мишенью в ДВБ также используют метод вычисления изменения свободной энергии связывания, который, как правило, применяют при работе с малыми молекулами. Поскольку такой подход уникален, зачастую существующее программное обеспечение не подходит для решения поставленных задач, и ДВБ разрабатывает собственные биоинформатические решения как для молекулярного моделирования, так и для составления протоколов мутаций, влияющих на изменение свободной энергии.
Применив совокупность методов по биоинформатическому моделированию антител, ДВБ буквально собрал из частей других антител препарат BCD132, который будет использоваться для лечения рассеянного склероза и уже прошел первую фазу клинических испытаний.
Синтез полинуклеотидов
Первый этап получения белкового терапевтического препарата — это выделение или синтез соответствующего ему гена и встраивание его в плазмиду (экспрессионный вектор). Как правило, гены — это достаточно длинные цепочки нуклеотидов, которые могут содержать трудные для химического синтеза фрагменты (например, «шпильки», АТ-богатые регионы или длинные области гомологии). Соответственно, такой ген проще синтезировать по частям, уже после собирая из них полноразмерную последовательность. Еще одна трудность при сборке экспрессионного вектора — различие количества каждой тРНК в различных клетках-продуцентах, из-за чего нуклеотидную последовательность необходимо оптимизировать с учетом кодонного предпочтения конкретной системы экспрессии для максимального выхода белка.
Для учета всех этих параметров на стадии конструирования потенциального терапевтического препарата в ДВБ был создан специальный вычислительный алгоритм, подбирающий оптимальные кодоны к заданной последовательности белка, а затем находящий лучший способ разделения последовательности на олигонуклеотиды для их дальнейшего синтеза.
Разработка малых молекул
Малые небелковые молекулы, которые могут эффективно связываться с белком-мишенью, также используются в качестве терапевтических агентов. Разработка лекарственных препаратов такого типа начинается с in silico скрининга миллионов соединений с дальнейшим синтезом кандидатов и экспериментальной проверкой параметров их взаимодействия с мишенями [14].
У такой методики есть значительный недостаток. Процесс можно сравнить с поиском единственной нужной песчинки в бескрайней пустыне из малых молекул. Для увеличения полезного выхода в ДВБ постоянно ведут разработки для скрининга молекул in silico (то есть не в лаборатории, а на компьютере). Взаимодействие тех или иных молекул с клеточными мишенями моделируют на компьютере, и далее отбирают наиболее успешные варианты, что сильно сужает круг поиска. Результаты in silico экспериментов используют для создания новых виртуальных библиотек, отбора лучших молекул и их дальнейшего синтеза, что в конечном итоге увеличивает полезный выход.
Команда департамента вычислительной биологии
Проблемы, которые решают в департаменте, зачастую находятся на стыке различных дисциплин и требуют привлечения специалистов из смежных областей. Поэтому крайне важно сформировать команду, которая могла бы быстро решать неординарные задачи.
В основном набираются люди из IT-области или физических и химических специальностей: им влиться несколько легче, чем людям, пришедшим из области академической биологии. Однако у них могут возникать сложности с биологической составляющей проектов. В качестве вступительных испытаний кандидату предлагается решить какую-то небольшую задачу, связанную с тематикой группы. Например — ввести мутации в последовательность белка, повышающие сродство с другим белком, или же предсказать показатели растворимости для молекулы, исходя из информации о другой схожей с ней молекуле. Конечно же, при проверке оценивают не только итоговый результат, но и ход решения. Чем он интереснее и многограннее — тем больше шансов попасть в команду ДВБ.
Для «удержания» новых сотрудников и облегчения их интеграции в коллектив есть ряд мероприятий, нацеленных на ускоренное их вовлечение в работу команды. За 3–4 первых месяца работы с новоиспеченным сотрудником проводят несколько встреч, на которых проверяется его понимание и вовлеченность в проект. Далее человек пускается в свободное плавание, которое, тем не менее, предполагает постоянное обучение у коллег.
Характерная черта ДВБ — командное деление департамента: у каждой команды своя область задач. Поэтому с приходом нового человека более опытные члены группы вводят его в курс дела. Регулярные встречи сотрудников для совместного разбора новых публикаций или проектов не только позволяют «влиться» в коллектив, но и способствуют общению между проектными группами.
Для обмена знаниями внутри департамента придумано несколько форматов мероприятий. Так, внутри ДВБ издается «Дайджест ДВБ» — информационный листок, регулярно рассылаемый всем работникам департамента. Еженедельно проводится общее собрание департамента, на котором все проектные команды презентуют свою работу за неделю. Раз в квартал проходит более масштабное мероприятие — однодневная конференция, на которой представляются уже не локальные результаты, а стратегические планы департамента.
С момента образования ДВБ его штат вырос примерно в шесть раз. Вначале в нем было лишь шесть человек, сейчас же в ДВБ работает около 35 сотрудников. Темпы увеличения состава ДВБ высоки: в 2018 году департамент принял на работу около двадцати человек, за счет чего увеличился более чем в два раза.
Сотрудники ДВБ активно участвуют в конференциях. Так, в 2019 году каждый второй сотрудник департамента уже был на международных конференциях или планирует их посетить. Это связано как с бурным ростом ДВБ и необходимостью обучения, так и с желанием презентовать собственные материалы на крупных международных научных мероприятиях. В перечень конференций, посещаемых сотрудниками департамента, входят Protein Engineering Summit (PEGS), профильные конференции по антителам и малым молекулам (например Antibody Engineering & Therapeutics), а также конференции по высокопроизводительным вычислениям (такие как NVIDIA’s GPU Technology Conference и ICFP).
Департамент вычислительной биологии BIOCAD, как, впрочем, и компания в целом, стремится показать, что наиболее перспективные и эффективные фармацевтические решения лежат на стыке прикладной и фундаментальной наук. Именно поэтому такое большое внимание уделяется не просто решению частных задач моделирования и синтеза определенных молекул, а поиску новых методов анализа данных, оптимизации существующих подходов и актуализации текущей научной повестки. Пожалуй, именно это можно назвать основной «изюминкой» ДВБ, которая, надеемся, принесет свои плоды.