Что такое нитрат железа
Нитрат железа (III)
| Нитрат железа (III) | |
|---|---|
| Систематическое наименование | Нитрат железа (III) |
| Хим. формула | Fe(NO3)3 |
| Состояние | гигроскопичные кристаллы |
| Молярная масса | |
| RTECS | NO7175000 |
| ChemSpider | 23584 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Нитрат железа (III) — неорганическое химическое соединение, соль азотной кислоты и трехвалентного железа.
Содержание
Физические свойства
При обычной температуре в зависимости от концентрации и содержания в растворе кислоты нитрат железа (III) кристаллизуется в виде почти бесцветных кубиков, имеющих состав Fe(NO3)3·6H2O, или в моноклинных кристаллах состава Fe(NO3)3·9H2O.
Гексагидрат нитрата железа (III) Fe(NO3)3·6H2O — светло-фиолетовые гигроскопичные кристаллы с кубической решёткой. Образуется при кристаллизации из водных растворов с содержанием HNO3 не менее 57 % и 28 % Fe(NO3)3.
Нонагидрат нитрата железа (III) Fe(NO3)3·9H2O — очень гигроскопичные светло-фиолетовые кристаллы с моноклинной решёткой (a = 0,140 нм, b = 0,970 нм, c = 1,103 нм, β=95,52°, пространственная группа P21/с). Хорошо растворяются в воде. При нагревании плавится при 50,1 °C. Процесс сопровождается частичным разложением исходного продукта с выделением HNO3 и последующим кипячением раствора при 125 °C.
Таблица растворимости нитрата железа (III) в воде (в пересчете на безводную соль):
| Температура, °С | Концентрация, г/100 г воды | Концентрация, % |
| 0 | 67,08 | 40,15 |
| 20 | 82,48 | 45,2 |
| 40 | 104,83 | 51,18 |
Растворяется также в ацетоне, эфире, этаноле.
Безводный нитрат железа (III) получить не удалось.
В растворе бледно-фиолетовый гексааквакатион [Fe(H2O)6] 3+ преобладает только в том случае, если pH
0. При более высоких значениях pH раствор желтеет из-за гидролиза, а если pH выше 2-3, происходит дальнейшая конденсация и начинается образование коллоидных гелей, и в конечном итоге образуется красновато-коричневый осадок гидратированного оксида железа (III).
Получение
Химические свойства
Равновесие можно сместить в обратную сторону сильно подкислив раствор HNO3.
— Выступает в роли окислителя с металлами, например, с медью:
Нитрат железа(III)
| Нитрат железа(III) | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Нитрат железа(III) |
| Химическая формула | Fe(NO3)3 |
| Физические свойства | |
| Состояние (ст. усл.) | гигроскопичные кристаллы |
| Молярная масса | (ангидрид) 241.86 г/моль |
(нонагидрат) 403.999 г/моль
Нитрат железа(III) — неорганическое химическое соединение, соль азотной кислоты и железа III с формулой 
Содержание
Физические свойства
Нонагидрат нитрата железа(III) Fe(NO3)3·9H2O — очень гигроскопичные светло-фиолетовые кристаллы с моноклинной решёткой (a = 0,140 нм, b = 0,970 нм, c = 1,103 нм, β=95,52°, пространственная группа P21/с). Хорошо растворяются в воде. При нагревании плавится при 50,1 °C с частичным разложением и выделением HNO3.
Гексагидрат нитрата железа(III) Fe(NO3)3·6H2O — бесцветные гигроскопичные кристаллы с кубической решёткой. Образуется при кристаллизации из раствора с содержанием HNO3 около 50%.
Безводный нитрат железа(III) получить не удалось.
Получение
Нитрат железа(III) получают взаимодействием железной стружки с 20-30% раствором азотной кислоты:
В производстве этот процесс проводят продувая через раствор воздух:
В лабораторной практике нитрат железа(III) можно получить обменной реакцией:
Добавив к гидроксонитрату церия азотную кислоту и сульфат железа(II) получим следующие продукты реакции:
Химические свойства
В водных растворах нитрат железа(III) подвергается сильному гидролизу:
равновесие можно сместить в обратную сторону сильно подкислив раствор HNO3.
Разрушается разбавленными щелочами:
При нагревании разлагается:
Применение
Применяется как коагулянт при очистке сточных вод.
При окраске тканей используют нитрат железа(III) как протраву.
Нитрат железа(III) является катализатором для синтеза амида натрия из раствора натрия в аммиаке:
Некоторые глины, пропитанные нитратом железа(III), являются полезными окислителями в органическом синтезе. Также он используется ювелирами и кузнецами для протравки серебра и его сплавов.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | — | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | — | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Нитрат железа(III)» в других словарях:
Нитрат актиния(III) — Общие Систематическое наименование Нитрат актиния (III) Традиционные названия Нитрат актиния Химическая формула Ac(NO3)3 Эмпирическая формула Ac(NO3)3 … Википедия
Нитрат железа(II) — Нитрат железа (II) это соль образованная реакцией нейтрализации гидроксида железа(II) и азотной кислоты с общей молекулярной формулой Fe(NO3)2. Насыщенность его водного р ра составляет 86,95г при температуре 24 °С (при t=0°С равна 71,03г,… … Википедия
железа(III) нитрат — geležies(III) nitratas statusas T sritis chemija formulė Fe(NO₃)₃ atitikmenys: angl. ferric nitrate; iron(III) nitrate rus. железа(III) нитрат; железо азотнокислое окисное ryšiai: sinonimas – geležies tris(trioksonitratas) … Chemijos terminų aiškinamasis žodynas
Сульфат железа(III) — У этого термина существуют и другие значения, см. Сульфат железа. Сульфат железа(III) … Википедия
Хлорид железа(III) — У этого термина существуют и другие значения, см. Хлорид железа. Хлорид железа(III) … Википедия
Оксид железа(III) — Оксид железа(III) … Википедия
Бромид железа(III) — У этого термина существуют и другие значения, см. Бромид железа. Бромид железа(III) Общие Традиционные названия Трибомид железа Химическая формула FeBr3 Физические свойства Сос … Википедия
Фторид железа(III) — У этого термина существуют и другие значения, см. Фторид железа. Фторид железа(III) Общие Систематическое наименование Фторид железа(III) Традиционные названия Фтористое железо Химическая формула FeF3 … Википедия
Гидроксид железа(III) — Общие Систематическое наименование Гидроксид железа(III) Традиционные названия Гидроокись железа Химическая формула Fe(OH)3 Физические свойства Состояние ( … Википедия
Фосфат железа(III) — Фосфат железа(III) … Википедия
Нитрат железа (II)
| Нитрат железа (II) | |
|---|---|
 | |
| Систематическое наименование | Нитрат железа (II) |
| Хим. формула | FeN2O6 |
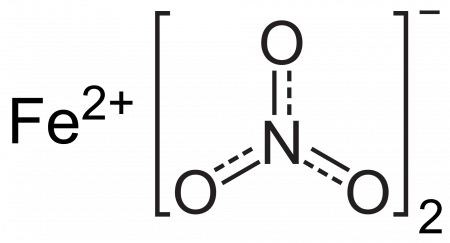
| Рац. формула | Fe(NO3)2 |
| Состояние | твёрдое |
| Молярная масса | |
| Температура | |
| • плавления | (гексагидрат) 60,5°C |
| Рег. номер CAS | 14013-86-6 |
| PubChem | 9815404 |
| SMILES | |
| RTECS | NO7175000 |
| ChemSpider | 7991154 и 32867051 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Нитрат железа (II) — соль азотной кислоты и двухвалентного железа.
Содержание
Физические свойства
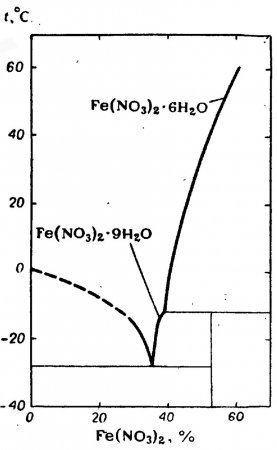
Нитрат железа (II) существует в основном в виде кристаллогидратов Fe(NO3)2·6H2O и Fe(NO3)2·9H2O.
График растворимости представлен на рисунке.
| Состояние | Температура, °С | Концентрация, % |
| Лед+Fe(NO3)2·9H2O | -28 | (35) |
| Fe(NO3)2·9H2O+Fe(NO3)2·6H2O | (39) | |
| Fe(NO3)2·6H2O | 60,5 | 62,5 |
Безводный нитрат железа (II) и его кристаллогидраты неустойчивы, поэтому легко окисляются на воздухе.
Получение
Нитрат железа (II) образуется при растворении железа в разбавленной азотной кислоте на холоде:
В чистом состоянии его лучше получать обменной реакцией сульфата железа (II) с нитратом свинца (II):
Химические свойства
Проявляет восстановительные свойства. Гидролиз практически не проявляется.
Железо. Свойства железа и его соединений.
Железо
Положение в периодической системе химических элементов
Элемент железо расположен в побочной подгруппе VIII группы (или в 8 группе в современной форме ПСХЭ) и в четвертом периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение атома железа
Электронная конфигурация железа в основном состоянии :
+26Fe 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6
Железо проявляет ярко выраженные магнитные свойства.
Физические свойства
Железо – металл серебристо-белого цвета, с высокой химической активностью и высокой ковкостью. Обладает высокой тепло- и электропроводностью.

Температура плавления 1538 о С, температура кипения 2861 о С.
Нахождение в природе
Железо довольно распространено в земной коре (порядка 4% массы земной коры). По распространенности на Земле железо занимает 4-ое место среди всех элементов и 2-ое место среди металлов. Содержание в земной коре — около 8%.
В природе железо в основном встречается в виде соединений:

Магнитный железняк Fe3O4 или FeO·Fe2O3 (магнетит).
(изображение с портала emchi-med.ru)
В природе также широко распространены сульфиды железа, например, пирит FeS2.

Встречаются и другие минералы, содержащие железо.
Способы получения
Железо в промышленности получают из железной руды, гематита Fe2O3 или магнетита (Fe3O4или FeO·Fe2O3).
В печь загружают руду, кокс и флюсы.
Шихта – смесь исходных материалов, а в некоторых случаях и топлива в определённой пропорции, которую обрабатывают в печи.
Каменноугольный кокс – это твёрдый пористый продукт серого цвета, получаемый путем коксования каменного угля при температурах 950—1100 °С без доступа воздуха. Содержит 96—98 % углерода.
Флюсы – это неорганические вещества, которые добавляют к руде при выплавке металлов, чтобы снизить температуру плавления и легче отделить металл от пустой породы.
Шлак – расплав (а после затвердевания – стекловидная масса), покрывающий поверхность жидкого металла. Шлак состоит из всплывших продуктов пустой породы с флюсами и предохраняет металл от вредного воздействия газовой среды печи, удаляет примеси.
В печи кокс окисляется до оксида углерода (II):
2C + O2 → 2CO
Затем нагретый угарный газ восстанавливает оксид железа (III):
Процесс получения железа – многоэтапный и зависит от температуры.
Наверху, где температура обычно находится в диапазоне между 200 °C и 700 °C, протекает следующая реакция:
Ниже в печи, при температурах приблизительно 850 °C, протекает восстановление смешанного оксида железа (II, III) до оксида железа (II):
Встречные потоки газов разогревают шихту, и происходит разложение известняка:
Оксид железа (II) опускается в область с более высоких температур (до 1200 o C), где протекает следующая реакция:
FeO + CO → Fe + CO2
Углекислый газ поднимается вверх и реагирует с коксом, образуя угарный газ:
CO2 + C → 2CO

2. Также железо получают прямым восстановлением из оксида водородом:
При этом получается более чистое железо, т.к. получаемое железо не загрязнено серой и фосфором, которые являются примесями в каменном угле.
3. Еще один способ получения железа в промышленности – электролиз растворов солей железа.
Качественные реакции
Качественные реакции на ионы железа +2.
2NaOH + FeCl2 → Fe(OH)2 + 2NaCl
Видеоопыт взаимодействия раствора сульфата железа (II) с раствором гидроксида натрия (качественная реакция на ионы железа (II)) можно посмотреть здесь.
Гидроксид железа (II) на воздухе буреет, так как окисляется до гидроксида железа (III):
– ионы железа +2 окрашивают раствор в светлый желто-зеленый цвет.
– взаимодействие с красной кровяной солью K3[Fe(CN)6] – также качественная реакция на ионы железа +2. При этом образуется синий осадок «турнбулева синь».
Видеоопыт взаимодействия раствора хлорида железа (II) с раствором гексацианоферрата (III) калия (качественная реакция на ионы железа (II)) можно посмотреть здесь.
Качественные реакции на ионы железа +3

3NaOH + FeCl3 → Fe(OH)3 + 3NaCl
Видеоопыт взаимодействия раствора хлорида железа (III) с раствором гидроксида натрия (качественная реакция на ионы железа (III)) можно посмотреть здесь.
– ионы железа +3 окрашивают раствор в светлый желто-оранжевый цвет.
– взаимодействие с желтой кровяной солью K4[Fe(CN)6] ионы железа +3. При этом образуется синий осадок «берлинская лазурь».
Видеоопыт взаимодействия раствора хлорида железа (III) с раствором гексацианоферрата (II) калия (качественная реакция на ионы железа (III)) можно посмотреть здесь.
В последнее время получены данные, которые свидетельствуют, что молекулы берлинской лазури идентичны по строению молекулам турнбулевой сини. Состав молекул обоих этих веществ можно выразить формулой Fe4[Fe2(CN)6]3.
– при взаимодействии солей железа (III) с роданидами раствор окрашивается в кроваво-красный цвет.
FeCl3 + 3NaCNS → Fe(CNS)3 + 3NaCl
Видеоопыт взаимодействия раствора хлорида железа (III) с раствором роданида калия (качественная реакция на ионы железа (III)) можно посмотреть здесь.
Химические свойства
1.1. Железо реагирует с галогенами с образованием галогенидов. При этом активные неметаллы (фтор, хлор и бром) окисляют железо до степени окисления +3:
2Fe + 3Cl2 → 2FeCl3
Менее активный йод окисляет железо до степени окисления +2:
1.2. Железо реагирует с серой с образованием сульфида железа (II):
Fe + S → FeS
Fe + P → FeP
1.4. С азотом железо реагирует в специфических условиях с образованием нитрида дижелеза:
1.5. Железо реагирует с углеродом и кремнием с образованием карбида и силицида:
3Fe + C → Fe3C
1.6. При взаимодействии с кислородом железо образует окалину – двойной оксид железа (II, III):
При пропускании кислорода через расплавленное железо возможно образование оксида железа (II):
2Fe + O2 → 2FeO
2. Железо взаимодействует со сложными веществами.
2.1. При обычных условиях железо с водой практически не реагирует. Раскаленное железо может вступать в реакцию при температуре 700-900 о С с водяным паром:
3 Fe 0 + 4 H2 + O → Fe +3 3O4 + 4 H2 0
В воде в присутствии кислорода или во влажном воздухе железо медленно окисляется (корродирует):
2.2. Железо взаимодействуют с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой). При этом образуются соль железа со степенью окисления +2 и водород.
Fe + 2HCl → FeCl2 + H2↑
2.3. При обычных условиях железо не реагирует с концентрированной серной кислотой из-за пассивации – образования плотной оксидной пленки. При нагревании реакция идет, образуются оксид серы (IV), сульфат железа (III) и вода:
2.4. Железо не реагирует при обычных условиях с концентрированной азотной кислотой также из-за пассивации. При нагревании реакция идет с образованием нитрата железа (III), оксида азота (IV) и воды:
С разбавленной азотной кислотой железо реагирует с образованием оксида азота (II):
При взаимодействии железа с очень разбавленной азотной кислотой образуется нитрат аммония:
Fe + CuSO4 → FeSO4 + Cu
Еще пример : простое вещество железо восстанавливает железо до степени окисления +2 при взаимодействии с соединениями железа +3:
2FeCl3 + Fe → 3FeCl2
Оксид железа (II)
Оксид железа (II) – это твердое, нерастворимое в воде вещество черного цвета.
Способы получения
Оксид железа (II) можно получить различными методами :
1. Частичным в осстановлением оксида железа (III).
Или частичным восстановлением оксида железа (III) угарным газом:
Еще один пример : восстановление оксида железа (III) железом:
2. Разложение гидроксида железа (II) при нагревании :
Химические свойства
1. При взаимодействии оксида железа (II) с кислотными оксидами образуются соли.
FeO + SO3 → FeSO4
FeO + 2HCl → FeCl2 + H2O
3. Оксид железа (II) не взаимодействует с водой.
4. Оксид железа (II) малоустойчив, и легко окисляется до соединений железа (III).
При взаимодействии с разбавленной азотной кислотой образуется оксид азота (II). Реакция идет при нагревании:
FeO + CO → Fe + CO2
Оксид железа (III)
Оксид железа (III) – это твердое, нерастворимое в воде вещество красно-коричневого цвета.
Способы получения
Оксид железа (III) можно получить различными методами :
1. Окисление оксида железа (II) кислородом.
2. Разложение гидроксида железа (III) при нагревании :
Химические свойства
1. При взаимодействии оксида железа (III) с кислотными оксидами и кислотами образуются соли.
3. Оксид железа (III) не взаимодействует с водой.
4. Оксид железа (III) окисляется сильными окислителями до соединений железа (VI).
Нитраты и нитриты в щелочной среде также окисляют оксид железа (III):
Также оксид железа (III) восстанавливается водородом:
Железом можно восстановить оксид железа только до оксида железа (II):
Оксид железа (III) реагирует также с некоторыми другими сильными восстановителями.
Fe2O3 + 3NaH → 3NaOH + 2Fe
6. Оксид железа (III) – твердый, нелетучий и амфотерный. А следовательно, он вытесняет более летучие оксиды (как правило, углекислый газ) из солей при сплавлении.
Оксид железа (II, III)
Оксид железа (II, III) (железная окалина, магнетит) – это твердое, нерастворимое в воде вещество черного цвета.
Фото с сайта wikipedia.ru
Способы получения
Оксид железа (II, III) можно получить различными методами :
1. Горение железа на воздухе:
2. Частичное восстановление оксида железа (III) водородом или угарным газом :
3. При высокой температуре раскаленное железо реагирует с водой, образуя двойной оксид железа (II, III):
Химические свойства
Свойства оксида железа (II, III) определяются свойствами двух оксидов, из которых он состоит: основного оксида железа (II) и амфотерного оксида железа (III).
1. При взаимодействии оксида железа (II, III) с кислотными оксидами и кислотами образуются соли железа (II) и железа (III).
Еще пример : оксид железа (II, III) взаимодействует с разбавленной серной кислотой.
2. Оксид железа (II, III) взаимодействует с сильными кислотами-окислителями (серной-концентрированной и азотной).
Разбавленной азотной кислотой окалина окисляется при нагревании:
Также оксид железа (II, III) окисляется концентрированной серной кислотой:
Также окалина окисляется кислородом воздуха :
3. Оксид железа (II, III) не взаимодействует с водой.
4. Оксид железа (II, III) окисляется сильными окислителями до соединений железа (VI), как и прочие оксиды железа (см. выше).
Также железная окалина восстанавливается водородом:
Оксид железа (II, III) реагирует также с некоторыми другими сильными восстановителями (йодидами и сульфидами).
Гидроксид железа (II)
Способы получения
1. Гидроксид железа (II) можно получить действием раствора аммиака на соли железа (II).
2. Гидроксид железа (II) можно получить действием щелочи на соли железа (II).
FeCl2 + 2KOH → Fe(OH)2↓ + 2KCl
Химические свойства
Гидроксид железа (II) взаимодействует с пероксидом водорода:
При растворении Fe(OH)2 в азотной или концентрированной серной кислотах образуются соли железа (III):
4. Г идроксид железа (II) разлагается при нагревании :
Гидроксид железа (III)
Способы получения
1. Гидроксид железа (III) можно получить действием раствора аммиака на соли железа (III).
2. Окислением гидроксида железа (II) кислородом или пероксидом водорода:
3. Гидроксид железа (III) можно получить действием щелочи на раствор соли железа (III).
FeCl3 + 3KOH → Fe(OH)3↓ + 3KCl
Видеоопыт получения гидроксида железа (III) взаимодействием хлорида железа (III) и гидроксида калия можно посмотреть здесь.
Например: бромид железа (III) реагирует с карбонатом натрия. При этом выпадает осадок гидроксида железа (III), выделяется углекислый газ и образуется бромид натрия:
Взаимодействие хлорида железа (III) с сульфитом, например, калия — очень интересная реакция. Во-первых, в некоторых источниках указывается, что в ней таки может протекать необратимый гидролиз. Но для ЕГЭ лучше считать, что при этом протекает ОВР. Во-вторых, ОВР можно записать в разных видах:
Также допустима такая запись:
Химические свойства
3. Гидроксид железа (III) взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—ферриты, а в растворе реакция практически не идет. При этом гидроксид железа (III) проявляет кислотные свойства.
4. Г идроксид железа (III) разлагается при нагревании :
Видеоопыт взаимодействия гидроксида железа (III) с соляной кислотой можно посмотреть здесь.
Соли железа
Нитраты железа
Нитрат железа (II) при нагревании разлагается на оксид железа (III), оксид азота (IV) и кислород:
Нитрат железа (III) при нагревании разлагается также на оксид железа (III), оксид азота (IV) и кислород:
Гидролиз солей железа
Растворимые соли железа, образованные кислотными остатками сильных кислот гидролизуются по катиону. Гидролиз протекает ступенчато и обратимо, т.е. частично:
I ступень: Fe 3+ + H2O ↔ FeOH 2+ + H +
II ступень: FeOH 2+ + H2O ↔ Fe(OH )2 + + H +
Однако сульфиты и карбонаты железа (III) и их кислые соли гидролизуются необратимо, полностью, т.е. в водном растворе не существуют, а разлагаются водой:
При взаимодействии соединений железа (III) с сульфидами протекает ОВР:
2FeCl3 + 3Na2S → 2FeS + S + 6NaCl
Более подробно про гидролиз можно прочитать в соответствующей статье.
Окислительные свойства железа (III)
Соли железа (III) под проявляют довольно сильные окислительные свойств. Так, при взаимодействии соединений железа (III) с сульфидами протекает окислительно-восстановительная реакция.
Например : хлорид железа (III) взаимодействует с сульфидом натрия. При этом образуется сера, хлорид натрия и либо черный осадок сульфида железа (II) (в избытке сульфида натрия), либо хлорид железа (II) (в избытке хлорида железа (III)):
2FeCl3 + 3Na2S → 2FeS + S + 6NaCl
2FeCl3 + Na2S → 2FeCl2 + S + 2NaCl
По такому же принципу соли железа (III) реагируют с сероводородом:
2FeCl3 + H2S → 2FeCl2 + S + 2HCl
2FeCl3 + 2KI → 2FeCl2 + I2 + 2KCl
Однако, соли железа со степенью окисления +3 в этом ряду являются небольшим исключением. Ведь для железа характерны две степени окисления: +2 и +3. И железо со степенью окисления +3 является более сильным окислителем. Таким образом, условно говоря, железо со степенью окисления +3 расположено в ряду активности после меди. И соли железа (III) могут реагировать еще и с металлами, которые расположены правее железа! Но до меди, включительно. Вот такой парадокс.
И еще один момент. Соединения железа (III) с этими металлами реагировать будут, а вот соединения железа (II) с ними реагировать не будут. Таким образом, металлы, расположенные в ряду активности между железом и медью (включая медь) при взаимодействии с солями железа (III) восстанавливают железо до степени окисления +2. А вот металлы, расположенные до железа в ряду активности, могут восстановить железо и до простого вещества.
А вот реакция нитрата железа (III) с цинком протекает уже по привычному механизму. И железо восстанавливается до простого вещества: