Что такое нити фибрина в цитологии желудка
Цитология биопсийного материала на Helicobacter pylori
Цитологическое исследование биопсийного материала на Helicobacter pylori

Тип биоматериала: ткань желудка, пищевода
Синонимы (rus): Биопсия на H.Pylori, эндоскопия на H.Pylori, мазок-отпечаток на H.Pylori, HP-тест, уреазный тест
Синонимы (eng): Biopsy for H. Pylori, endoscopy for H. Pylori, smear mark on H. Pylori, HP-test, urease test
Методы исследования: ФГДС
Сроки выполнения: 5-7 дней
Что такое цитологический анализ на хеликобактер пилори?
Хеликобактер пилори (Helicobacter Pylori) – жгутиковая бактерия, обитающая на слизистой оболочке органов желудочно-кишечного тракта. Эта бактерия обладает высокой активностью и сегодня ею заражены более 60% населения индустриальных стран и до 90% развивающихся стран.
Инфицирование Хеликобактер является основной причиной язвы желудка. Передается бактерия контактным путем. Сегодня выявлено, что мужчины болеют язвой в 4 раза чаще, чем женщины, а люди с первой группой крови на порядок чаще, чем все остальные. Инфицирование бактерией является кофактором возникновения аденокарциномы желудка (рак желудка).
Цитология является наиболее точным методом определения бактерий в желудке. При правильной подготовке к обследованию ложный результат практически исключен. Анализ предназначен для пациентов, с подозрением на заболевания органов пищеварения, вызванные бактериями Хеликобактер: гастрит, язва желудка, рак.
В качестве материала используется мазок-отпечаток, полученный по время фиброгастродуоденоскопии. Биопсийный материал извлекается из подозрительных участков слизистой желудка, исключая грубоповрежденные области, поскольку Хеликобатер не обитают в язвах и эрозиях. Материал наносится на стекло и поставляет в лабораторию для исследования.
Расшифровка результатов цитологии биопсии желудка
При получении низких значений рекомендуется подтвердить анализ иными методами: анализ кала на антигены, хелик-тесты, анализ крови. При подтверждении результатов стоит пройти серьезное лечение, поскольку Хеликобактер пилори достаточно опасная бактерия, способная вызывать сильные повреждения внутренних пищеварительных органов.
Что такое нити фибрина в цитологии желудка
Изучение заболеваний желудочно-кишечного тракта, в частности желудка и двенадцатиперстной кишки, является основой узкого направления медицины – гастроэнтерологии. Причин возникновения заболеваний желудка множество: неправильное питание, стрессы, нарушение режима труда и отдыха, воздействие вредных веществ, активность бактерий Helicobacter pylori и т.д. [1–3]. Желудок – важный орган, отвечающий за общее состояние организма, из-за желудочных состояний страдают все системы. Поэтому важно знать причины болезней желудка, основные его заболевания. Если рассматривать заболевания желудка с ракурса онкологии, то предвестниками данной патологии могут стать часто встречающиеся в повседневной практике гастроэнтерологов язвенная болезнь желудка, острый и хронический гастрит, дуоденогастральный рефлюкс, полипы, а также эрозия желудка. В ходе мониторинга пациентов стационарного и амбулаторного лечения данная группа заболеваний желудочно-кишечного тракта занимает лидирующее положение среди расстройств, которые в совокупности различных факторов окружающей среды, а также индивидуальных особенностей чаще других приводят к канцерогенной активности. Любое предраковое заболевание развивается поэтапно с нарастанием и углублением отрицательных изменений, происходящих в желудке. На некоторых стадиях любой процесс полностью обратим, то есть болезнь излечима. По мере углубления деструкции возможность обратимости снижается, наступает стойкая хронизация процесса, а болезнь становится неизлечимой. Переходу в предрак или рак способствуют наиболее глубокие стадии, когда болезнь развивается внутри клеток. Гастрит – это одно из наиболее распространенных желудочно-кишечных заболеваний воспалительного или воспалительно-дистрофического характера, поражающих слизистую оболочку желудка [4]. В связи со множеством разновидностей этой болезни термин «гастрит» является собирательным и служит для обозначения различных по происхождению воспалительных и дистрофических изменений в слизистой этого органа. Гастриты классифицируют по нескольким показателям – по типу, локализации воспалительного процесса, этиологическому фактору, эндоскопической картине, морфологическим изменениям слизистой оболочки желудка. Все эти показатели очень важны для диагностики и выбора способа лечения заболевания. Особого внимания заслуживает атрофический гастрит – длительно текущая форма хронического заболевания, при которой происходят деструктивные изменения в слизистой оболочке желудка. В результате патологического процесса ее площадь и количество функционирующих клеток резко уменьшаются. Многие специалисты считают [5–7], что этот подвид хронического гастрита является предраковым состоянием, как следствие угроза развития злокачественного процесса очень велика. При атрофическом гастрите запускается механизм перерождения нормальных клеток желудка; главные и добавочные клетки, принимающие участие в выработке пепсиногена и хлороводородной кислоты – основных составляющих желудочного сока, перестают функционировать в оптимальном режиме. Вместо него добавочные клетки желудка в большем объеме начинают продуцировать мукополисахариды – слизь. В результате резко снижается кислотность желудочного сока. То, что клетки меняют свою специализацию и перестают выполнять основную функцию, свидетельствует о том, что в организме есть сбой в системе гормональных, иммунных, ферментных и прочих регуляторов физиологических процессов. Язвенная болезнь желудка является одной из основных причин заболеваемости и смертности среди более семи миллионов ежегодно диагностируемых патологий желудочно-кишечного тракта [8]. Диагностика язвенной болезни желудка и двенадцатиперстной кишки предполагает наличие таких симптомов, как потеря веса, перенасыщенность, боли в эпигастральной области, чувство переполнения, вздутие живота, тошнота. К сожалению, наличие данных симптомов также вписывается в клиническую картину гастроэзофагеальной рефлюксной болезни, диспепсии и гастрита, в связи с чем диагностирование язвенной болезни желудка затруднено. Бессимптомное протекание данной патологии часто не позволяет провести диагностику на ранних стадиях развития болезни, заболевание остается незамеченным вплоть до клинических проявлений, а именно кровотечений желудочно-кишечного тракта [9]. Слизистая оболочка желудка выстлана одним слоем эпителиальных клеток, который поддерживается тонкими элементами рыхлой соединительной ткани, покрытой тонким слоем гладких мышечных волокон. У многих людей желудочный эпителий, помимо собственных кислых и ферментативных выделений желудка, подвергается воздействию Helicobacter pylori. Маленькие грамотрицательные палочки Helicobacter pylori обладают уникальной приспособленностью к колонизации желудка человека [10]. Наличие данных микроаэрофильных микроорганизмов приводит к возникновению ряда субклинических и клинических показателей, которые зависят от свойств заражающего штамма, хозяина и окружающей среды [11]. Ряду пациентов с язвенной болезнью желудка или развивающейся лимфомой желудка, которые ранее подвергались лечению с использованием нестероидных противовоспалительных препаратов, показана эрадикационная терапия. Но нельзя игнорировать тот факт, что данная терапия может ухудшить гастроэзофагеальную рефлюксную болезнь и увеличить риск развития рака пищевода [12]. Желудочные полипы представляют собой аномально растущую массу клеток, которые образуются на слизистой оболочке желудка. Наличие данной патологии является редкостью, и чаще всего заболевание протекает бессимптомно [13]. Большие полипы вызывают кровотечение, анемию, боль в животе или редко могут приводить к обструкции из-за своей локализации. Только определенные типы полипов способны обладать канцерогенной активностью и увеличивать риск развития онкологии в будущем, и в зависимости от этого выбирается дальнейшая стратегия лечения, которая может включать как хирургическое удаление полипа, так и мониторинг его изменений, и консервативное лечение [14].
Оценка морфологической структуры клеток возможна с помощью цитологического исследования, которое широко применяют в клинической практике как исключительно чувствительный, точный, эффективный метод диагностики злокачественных опухолей и ряда неопухолевых поражений всех органов пищеварительной трубки у больных с симптомами заболевания органов ЖКТ, а также при скрининге в группах высокого риска по развитию рака этих органов [15]. Микроскопически злокачественные клетки выстилают желудочные железы и крипты и представляют собой эпителиальные клетки, прорывающиеся через базальную мембрану и вторгающиеся в подслизистую оболочку и мышечный слой. Отдельные клетки теряют свою дифференцированность по отношению к соседним клеткам и представлены многочисленными митотическими фигурами [16]. Для предупреждения развития онкологических заболеваний важно раннее выявление таких состояний, а также их качественное обследование. Внедрение и максимальное использование современной эндоскопической техники значительно расширило возможности цитологической диагностики органов ЖКТ и, более того, открыло перспективы применения метода, поскольку цитологический материал пригоден для проведения имеющих неоценимое дифференциально-диагностическое значение иммуноморфологических, молекулярно-биологических и генетических исследований [17, 18].
Провести сравнительный анализ и выявить характерные морфологические цитологические признаки при различных доопухолевых заболеваниях желудка.
Материал и методы исследования
Результаты исследования и их обсуждение
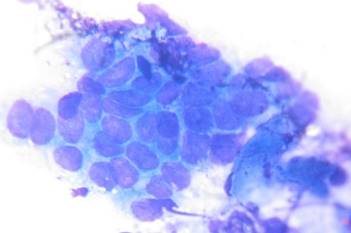
Рис. 1. Клетки покровно-ямочного эпителия с признаками гиперплазии
В случаях кишечной метаплазии в мазках-отпечатках обнаруживались высокие клетки цилиндрической, призматической или бокаловидной формы (рис. 2).
Рис. 2. Клетки покровно-ямочного эпителия с признаками кишечной метаплазии по тонкокишечному типу
Наблюдаются ядра больших и средних размеров, их расположение в клетках эксцентричное, окрашены интенсивно. Цитоплазма характеризуется базофильной окраской, у ядра и апикальной части почти прозрачная, широкая в апикальной части и узкая, более вытянутая в базальной. В исследуемых тканях имеются скопления лимфоидных элементов, а также плазматические клетки и сегментоядерные нейтрофилы. Эндоскопическая картина заживающей язвы характеризуется уменьшенной гиперемией слизистой оболочки, отсутствием некротических тканей и гнойных масс. Исчезает глубина язвы, воспаленные края язвы сглаживаются, формируется «красный рубец» – гиперемированная ткань слизистой оболочки, которая впоследствии после втяжения стенок формирует соединительнотканный «белый рубец» [23, 24]. Микроскопическое строение слизистой оболочки зависит от периода развития язвы. В цитологических мазках определяли десквамированные клетки эпителия, лейкоциты и эритроциты, фибробласты, гистиоциты, плазматические клетки и лимфоциты. Непосредственно по краю хронической язвы слизистая оболочка желудка подвергается значительному утолщению за счет интенсивной пролиферации ямочного эпителия. В цитологических препаратах можно найти все упомянутые выше клеточные элементы. В материале, полученном с краев хронической язвы, обычно обнаруживали полиморфные, различной степени зрелости клетки покровно-ямочного эпителия. Преобладание незрелых крупных клеток с большими ядрами и базофильной цитоплазмой может свидетельствовать об интенсивной пролиферации эпителия. В период обострения язвы в большом количестве встречаются дегенеративно измененные эпителиальные клетки без четких границ с укрупненными ядрами. Рисунок хроматина в них разреженный, в виде грубых волокон. В связи с большим клеточным распадом и явлениями цитолиза в материале, особенно полученном со дна язвы, можно видеть много «голых» ядер. В этих препаратах преобладали сегментоядерные лейкоциты и в значительном количестве встречаются элементы грануляционной ткани. В период рубцевания язвы в мазки попадают очень полиморфные клетки гистиоцитарного типа, которые бывает трудно отличить от атипических эпителиальных клеток [25]. В ходе эндоскопического исследования полипов оценивались количество, форма, размеры, поверхность, цвет, консистенция, воспалительные процессы и локализация новообразований. Цитологические препараты характеризовались большим количеством пластов и скоплений покровно-ямочного эпителия. При аденоматозных полипах встречаются также и железистоподобные структуры. По сравнению с цитологическими описаниями гастритов при этих заболеваниях отмечалось преимущество незрелых клеток, ядра светлые, укрупнены, рисунок хроматина нежно-сетчатый. Клетки эпителия желез и лимфоидные элементы определяются в небольшом количестве. В случаях грануляционных полипов с обильными воспалительными инфильтратами в их строме в цитологические препараты могут попадать в значительном количестве нейтрофильные лейкоциты.
В ходе проведенных исследований выявлены изменения в составе и морфологии клеток слизистой оболочки желудка, которые наблюдаются при гастрите, полипозе и язве, не являются строго специфическими. При всех этих заболеваниях может определяться различная степень пролиферации покровно-ямочного эпителия: в одних наблюдениях отмечается только незначительный полиморфизм эпителиальных клеток, в других – явно преобладают молодые элементы с некоторыми признаками атипии. Для установления диагноза необходимо применять дополнительные методы исследования, так как на основании только цитологических данных не представляется возможным диагностировать эти процессы.
Что такое нити фибрина в цитологии желудка
Одной из причин или последствий развития острых эрозивно-язвенных поражений является нарушение микроциркуляции [1] парасимпатической и симпатической нервной системы в слизистой оболочке желудка у больных с острыми изъязвлениями различной этиологии [2]. При этом не ясно, что первично: 1) острые изъязвления слизистой оболочки желудка и двенадцатиперстной кишки (ДПК), которые приводят к нарушению плотности холинергических и адренергических волокон, или 2) нарушения и особенности вегетативной иннервации слизистой оболочки желудка и ДПК, которые обусловливают развитие острых язв и эрозий при воздействии различных факторов острого изъязвления. Несомненно одно — не у каждого встречаются острые изъязвления слизистой желудка и ДПК даже при воздействии множественных факторов язвообразования.
Цель настоящей работы — морфологическое и гистохимическое изучение патогенеза развития острых изъязвлений желудка и ДПК при различных этиологических факторах острой гастропатии.
Материал и методы
В основу работы положен клинико-морфологический анализ обследования и лечения 120 больных, находившихся в клинике факультетской и эндоскопической хирургии КБГУ на базе Республиканской клинической больницы по поводу острых изъязвлений гастродуоденальной зоны пищеварительного тракта.
Всем пациентам проведено общеклиническое физикальное обследование органов и систем, а также выполнены общепринятые лабораторные и инструментальные исследования.
Результаты исследования
Базу исследований составили 120 человек, у которых гистологическое изучение гастробиоптатов показало наличие острых язв или эрозий. Предварительно не анализируя этиопатогенез этих изъязвлений, мы сочли возможным дать общую морфогистологическую характеристику состояния слизистой оболочки желудка этих больных на том основании, что во всех гастробиоптатах отмечалось:
1) наличие острых язв или острых эрозий;
2) нарушение микроциркуляции;
3) снижение плотности и флуоресценции адренергических нервных волокон и повышение активности ацетилхолинэстеразы (АХЭ) в холинергических нервных волокнах;
4) наличие Helicobacter pylori (H. pylori);
5) хроническое воспаление;
6) нарушение клеточного обновления.
Указанные признаки (2—6) позволяют диагностировать у данной группы больных хронический, чаще хеликобактерный, активный гастрит.
Гистологический анализ гастробиоптатов показал, что в исследуемой группе больных острые язвы и эрозии нередко развивались на фоне хронического хеликобактерного активного гастрита с умеренной атрофией фундальных желез. Последнее обстоятельство, при отсутствии других гистологических признаков хронической язвы, свидетельствует в пользу наличия острых язв и эрозий у обследованных больных.
Острые язвы в наших исследованиях определялись в 25% случаев, острые эрозии — в 55%. В 20% случаев изъязвления слизистой оболочки желудка диагностировались по очаговой лейкоцитарной (нейтрофильной) инфильтрации собственного слоя слизистой и прилежащего покровного или ямочного эпителия, которая является, хотя и косвенным, но диагностическим признаком эрозивного поражения желудка (табл. 1). 
При острых язвах (рис. 1) 
Ткань желудка, прилежащая к язвенному дефекту, обильно инфильтрирована полиморфно-ядерными лейкоцитами. Отмечались выраженные микроциркуляторные нарушения. Подэпителиальные капилляры резко расширены, зияют, другие — полнокровны, с признаками стаза или агрегации эритроцитов. Встречались пристеночное стояние нейтрофилов и миграция их за пределы сосудистой стенки. Прилежащая строма отечна. Определялись мелкие кровоизлияния или геморрагическая инфильтрация небольших фрагментов слизистой оболочки, что свидетельствовало о нарушении кровообращения и проницаемости сосудистой стенки.
Гораздо чаще регистрировались острые эрозии желудка (рис. 2). 
Таким образом, проведенные гистологические исследования подтвердили наличие острых язв в 25,0%, острых эрозий в 55,0% случаев. В 20,0% случаев острые изъязвления слизистой оболочки желудка диагностировались по общеклиническим косвенным признакам, что свидетельствовало о соответствии исследуемого материала изучаемой проблеме.
Дистрофические, а порой и некробиотические, изменения покровного эпителия, сопровождающиеся вакуолизацией цитоплазмы и пикнозом ядра, обычно сочетались с резко выраженным расширением прилежащих сосудов и нарушением микроциркуляции в них, что, вероятно, и обусловливало предэрозивные изменения покровного эпителия (рис. 3). 
При эрозиях расширение сосудов сочеталось с отеком собственного слоя слизистой оболочки и очаговой геморрагической инфильтрацией стромы, чаще в поверхностных отделах, хотя в нескольких (10) случаях наблюдались обширные кровоизлияния на всю толщину слизистой оболочки. Отдельные сосуды содержали большое количество полиморфно-ядерных лейкоцитов. Таким образом, гистологическое изучение гастробиоптатов в этой группе больных показало, что наличие острых язв и эрозий в желудке тесно связано с состоянием микроциркуляции и сочетается с резким расширением и неравномерным кровенаполнением сосудов, преимущественно поверхностных отделов слизистой оболочки.
Активность АХЭ значительно увеличивалась во всех исследованных случаях. Холинергические волокна в значительном количестве располагались вокруг желез (рис. 4). 
Однако ближе к поверхности слизистой оболочки плотность их расположения, толщина волокон и интенсивность окрашивания нередко существенно очагово снижались, что обычно сочеталось с расположением этих «гипохолинергических» зон рядом с изъязвленными участками, которые выявлялись в параллельных срезах, окрашенных гематоксилином и эозином.
При изучении препаратов этой группы, обработанных по методу Фалька—Хилларпа, обнаружено резкое уменьшение концентрации адренергических волокон, вплоть до полного очагового исчезновения мелких нервных проводников, а чаще — их терминалей. Кроме того, уменьшение плотности расположения нервных волокон, снижение, а очагово и отсутствие люминесценции, наблюдались в прилежащих к изъязвлениям или эрозиям зонах и в местах выраженных дистрофических изменений эпителия и подлежащей стромы, определяемых на параллельных препаратах, окрашенных гематоксилином и эозином. Некоторые варикозные утолщения терминальной сети становились нечеткими, расплывчатыми. Резкое падение катехоламинового свечения, местами вплоть до полного исчезновения наблюдалось также в адренергических волокнах подэпителиального сплетения. Менее значительно снижалась люминесценция периваскулярных адренергических сплетений.
Таким образом, проведенные гистологические исследования холинергических и адренергических составляющих вегетативной иннервации слизистой оболочки желудка показали, что при изъязвлениях последней отмечается резкое уменьшение плотности распределения и люминесценции адренергических волокон вплоть до полного очагового исчезновения мелких проводников и их терминалей, особенно в области подэпителиального сплетения. Примечательно повышение активности АХЭ за исключением зон, расположенных рядом с изъязвлениями слизистой оболочки желудка.
При гистологическом изучении препаратов больных этой группы, окрашенных по Гимзе, было определено наличие H. pylori в 78,4% случаев. Степень обсемененности этим микробом определялась полуколичественным методом на +, ++, +++ и на нашем материале встречалось в 21,6, 41,7 и 15,0% соответственно (табл. 2). 
В изученных нами гистологических препаратах H. pylori определялся в просвете желудочных ямок, в слизи на поверхности желудка и на покровно-ямочном эпителии в случае адгезии (рис. 5). 
Хронический хеликобактерный гастрит, будучи всегда активным, в соответствии с тремя степенями активности (+, ++, +++) характеризовался распространенностью нейтрофильной инфильтрации, которая определялась в собственной пластинке слизистой, в эпителии или нейтрофилы выявлялись в просвете желез, формируя так называемые ямочные абсцессы (табл. 3). 
Как следует из табл. 3, у значительного большинства обследованных больных была высокая активность хеликобактерного гастрита, которая соответствовала степени ++ и +++.
Межэпителиальные лимфоциты встречались редко. Лимфоидные фолликулы при хеликобактерном хроническом гастрите имели реактивные центры.
Таким образом, хеликобактерный активный гастрит был диагностирован у 78,4% обследуемых со степенью обсемененности + в 21,6% случаев, ++ в 41,7%случаев, +++ в 15,0% случаев, причем степень активности гастрита соответствовала + в 23,4% случаев, ++ в 40,42%, +++ в 36,17% случаев, что, вероятно, свидетельствует о достаточной значимости этой патологии как фонового заболевания при изучаемой нами гастропатии.
Нарушение клеточного обновления у обследуемых больных проявлялось атрофией слизистой оболочки с уменьшением количества собственных желез, что встречалось в 92% изученных случаев, и связано, вероятно, с пожилым возрастом подавляющего числа обследованных нами больных. Кроме того, в этой группе больных была обнаружена полная кишечная метаплазия в 15,38% случаев и неполная — в 30,76% случаев. Пролиферация покровного эпителия определялась в 61,5% случаев, тогда как дисплазии I—III степени — в 15% случаев (табл. 4). 
Анализ табл. 4 позволяет предположить, что нарушение клеточного обновления у данной группы больных является, скорее, дисрегенераторным, чем пренеопластическим, что подтверждается низким процентом и степенью дисплазий.
Таким образом, проведенные гистологические исследования показали, что острые язвы и эрозии развивались на фоне хронического хеликобактерного (в 78,4% случаев) активного гастрита, который осложнялся неполной кишечной метаплазией в 30% случаев и дисплазией I—III степени в 15% случаев, причем из 18 больных с дисплазиями лишь у 1 больного определена дисплазия III степени. Неполная кишечная метаплазия и дисплазия по выраженности и распространенности не внушали серьезных опасений, а высокий процент их наличия, вероятно, связан с контингентом обследуемых лиц, преимущественно пожилого возраста. Значение хронического гастрита в развитии острых язв и эрозий, на наш взгляд, основанный на изученных биоптатах, может быть определено как и значение других, нарушающих трофику слизистой оболочки или стрессирующих организм заболеваний, которые вызывают в слизистой желудка нейродистрофические изменения адренергического сплетения, провоцируют микроциркуляторные нарушения и обусловливают развитие дистрофических и дегенеративных или некротических изменений (эрозий, язв) в слизистой оболочке желудка.
Заключение
Не претендуя на окончательное решение механизма возникновения острых изъязвлений слизистой оболочки желудка и ДПК, можно считать, что в основе развития острых гастропатий лежат нарушения микроциркуляции в слизистой оболочке желудка, которые определяются в значительной степени характером нарушения вегетативной иннервации желудка, степенью нарушения клеточного обновления слизистой оболочки, которая, в свою очередь, напрямую коррелирует со степенью активности хронического или активного, чаще хеликобактерного гастрита и конечно относительного или абсолютного повышения кислотности желудка как непосредственного альтеративного фактора морфологической манифестации острых язв и эрозий слизистой оболочки желудка и ДПК.
Во всех изученных случаях у больных с острыми изъязвлениями гастродуоденальной зоны (ГДЗ) имеются нарушения вегетативной иннервации, морфологически проявляющиеся изменением плотности содержания адренергических волокон, а именно отмечается резкое уменьшение плотности распределения и люминесценции адренергических волокон, вплоть до полного очагового исчезновения мелких проводников и их терминалей, особенно в области подэпителиального сплетения. Примечательно повышение активности АХЭ, за исключением зон, расположенных рядом с изъязвленными участками слизистой оболочки желудка.
Нарушение микроциркуляции в слизистой оболочке желудка является одним из основных факторов развития острых изъязвлений, поскольку во всех изученных случаях такое нарушение имело место и проявлялось микротромбозами в капиллярах, особенно в зоне острой альтерации слизистой оболочки желудка.
Несомненна значительная роль нарушения клеточного обновления слизистой оболочки желудка и ДПК в развитии острых изъязвлений, и эти нарушения носят скорее дисрегенаторный характер, чем неопластический.
У значительного числа больных (более 70%) с острыми изъязвлениями желудка и ДПК выявляется обсеменение слизистой оболочки Н. рylori. Данный факт приводит к развитию активного хеликобактерного гастрита как одного из предикторов возникновения острых изъязвлений при наличии различных этиологических факторов язвообразования. Подобные изменения коррелируются со степенью активности активного хеликобактерного гастрита.
Данное исследование имеет не только научное, но и практическое значение, поскольку при выявлении у больных острых язв и эрозий слизистой оболочки желудка и ДПК необходимо выполнение морфологических и гистохимических исследований биоптатов из краев язв и отдаленных от язв и эрозий участков слизистой ГДЗ с последующим изучением вегетативной иннервации, что позволит дифференцировать базовую терапию при лечении острых изъязвлений желудка и ДПК. У больных с острыми изъязвлениями ГДЗ изучение обсемененности Н. рylori является обязательным в целях определения необходимости эрадикационной терапии.
Авторы заявляют об отсутствии конфликта интересов.