Маркеры метаболизма костной ткани. Остеопороз
Костная ткань играет роль каркаса (скелета) организма человека. Для сохранения скелета как структурного и функционального органа, костная ткань находится в процессе непрерывного ремоделирования, или обновления, за счёт двух противоположных процессов – разрушения (резорбции) старой кости и образования новой. Обновление – сложный процесс, в нём участвует множество компонентов. По концентрации в крови некоторых из них, мы можем выявить нарушения процессов метаболизма костной ткани, оценить эффективность лечения болезней опорно-двигательного аппарата. Исследуемые компоненты называют маркёрами метаболизма костной ткани.
Маркёры формирования костной ткани – остеокальцин и общий амино-терминальный пропептид проколлагена I типа (P1NP). Остеокальцин высвобождается остеобластами – клетками, синтезирующими компоненты межклеточного вещества. А P1NP отделяется от проколлагена I типа – предшественника коллагена.
Показания к исследованию остеокальцина:
Показания к исследованию P1NP:
В регуляции метаболизма костной ткани также играют роль минеральные вещества, входящие в состав кости, гормоны и витамины. Изменение их концентрации отражается на состоянии костной системы, а значит, мы можем использовать их для диагностики болезней и мониторинга лечения.
Например, гормон паращитовидных желез – паратгормон и гормон щитовидной железы – кальцитонин, участвуют в поддержании нормального уровня кальция (Ca). Кортизон – гормон надпочечников подавляет синтез коллагена, а половые гормоны оказывают анаболическое действие, то есть способствуют строительству органической основы кости.
Остеопороз
Остеопороз – это заболевание, характеризующееся общей прогрессирующей потерей костной массы и нарушением микроархитектоники (качества) костной ткани, следствием чего является хрупкость костей и повышение риска переломов. Около 75 миллионов человек в мире страдают остеопорозом. Наиболее распространено данное заболевание у женщин в постменопаузе. Это связано с изменением гормонального фона, в частности, после менопаузы снижается продукция эстрадиола – полового гормона, который помогает «удерживать» кальций в кости. Помимо постменопаузального в развитых странах встречается сенильный остеопороз, который с почти одинаковой частотой развивается у мужчин и женщин после 70 лет, а также вторичный остеопороз, обусловленный различными заболеваниями или связанный с длительным приемом некоторых лекарственных препаратов. К симптомам остеопороза относятся боль в позвоночнике, костях рук и ног, частые переломы, могут быть судороги мышц нижних конечностей, и др. Однако длительное время остеопороз никак не проявляет себя. Изредка может беспокоить ноющая боль в пояснице, которую с заболеванием не связывают.
В лаборатории CMD доступна комплексная услуга для диагностики остеопороза:
Что такое маркеры остеопороза
Комплексное обследование, включающее исследование маркеров метаболизма костной ткани и маркеров состояния минерального обмена и его регуляции. Обследование будет полезно как для ранней диагностики остеопороза, так и для выбора метода адекватной терапии и оценки ее эффективности.
Электрохемилюминесцентный иммуноанализ (ECLIA):
Кинетический колориметрический метод:
Твердофазный хемилюминесцентный иммуноферментный анализ:
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Остеопороз – метаболическое заболевание, характеризующееся снижением костной массы и микроструктурной перестройкой костной ткани, в связи с чем снижается прочность кости и повышается риск переломов.
Кость формируется остеобластами. Основная их функция – синтез остеоида (протеинового матрикса), который на 90-95 % состоит из коллагена 1-го типа, на 5 % – из белка остеокальцина и затем минерализуется кальцием и фосфатом из внеклеточной жидкости. Остеобласты содержат фермент щелочную фосфатазу, несут рецепторы к паратиреоидному гормону и кальцитриолу и способны к пролиферации. Минеральная часть кости состоит из гидроксиапатита и аморфного фосфата кальция, которые связаны с белками органического матрикса.
В костях непрерывно происходят процессы ремоделирования, включающие в себя резорбцию (разрушение) существующей костной ткани и образование новой. Резорбция кости осуществляется остеокластами. Это подвижные клетки, которые выделяют протеолитические ферменты и кислую фосфатазу, вызывая деградацию коллагена, разрушение гидроксиапатита и выведение минералов из матрикса. Ежегодно в организме человека обновляется 8-10 % всей костной ткани.
В детстве формирование костей происходит значительно интенсивнее процессов резорбции. Максимальная костная масса достигается в возрасте 25-30 лет. Затем начинают преобладать процессы резорбции и костная масса постепенно уменьшается. Метаболизм костной ткани регулируется витамином D, кальцием, эстрогенами, андрогенами, паратиреоидным гормоном, кальцитонином. Дисбаланс между разрушением и восстановлением плотности костей может возникнуть при гормональных или диетических изменениях, недостаточном употреблении кальция. Преобладание процессов резорбции приводит к остеопении (снижении плотности костей), которая прогрессирует и переходит в остеопороз.
Костная щелочная фосфатаза и остеокальцин отображают активность остеобластов в костной ткани. Стимуляция остеобластов происходит при интенсивных процессах деструкции костей, которые сопровождают остеопороз, болезнь Педжета, переломы, опухоли костей. При остеопорозе уровни остеокальцина и щелочной фосфатазы увеличиваются согласованно, причем нарушения метаболизма костной ткани возникают раньше первых изменений плотности костей, которые можно выявить при денситометрии (метод лучевой диагностики). В костях щелочная фосфатаза играет важную роль в формировании и обновлении костной ткани. Чем выше активность остеобластов, тем выше активность щелочной фосфатазы в крови, поэтому у детей и лиц, перенесших переломы костей, активность щелочной фосфатазы на высоком уровне.
Витамин D и его активные метаболиты являются компонентами гормональной системы, регулирующей фосфорно-кальциевый обмен, и участвуют, с одной стороны, в минерализации костной ткани, с другой – в поддержании гомеостаза кальция. Биологическое действие активных метаболитов витамина D заключается, главным образом, в стимуляции кишечной абсорбции кальция и фосфора, активации обмена и усилении экскреции кальция с мочой. При дефиците витамина D уровень кальция компенсируется за счет его мобилизации из костной ткани, что может привести к остеомаляции, рахиту у детей и остеопорозу у взрослых.
Уровень паратиреоидного гормона (ПТГ) тесно связан с количеством кальция, витамина D, фосфора и магния в организме. Регуляция его секреции осуществляется по принципу обратной связи, поэтому важно одновременно с ПТГ оценивать уровень свободного или ионизированного кальция в крови, учитывать клинические проявления и результаты других лабораторных и инструментальных исследований. При снижении концентрации кальция в крови (гипокальциемии) выделение ПТГ паращитовидными железами усиливается, а при повышении (гиперкальциемии) – снижается. Данные механизмы направлены на поддержание стабильного уровня кальция в крови. Повышение ПТГ способствует активации остеокластов, резорбции костной ткани и высвобождению кальция из костей, усиливает всасывание кальция из кишечника, задерживает выделение кальция почками и ингибирует обратную реабсорбцию фосфора. Антагонистом ПТГ является гормон кальцитонин, секретируемый С-клетками щитовидной железы. В норме при достижении нормальной концентрации кальция в крови продукция ПТГ снижается.
Ионизированный кальций – катион, свободно циркулирующий в крови и составляющий 46-50 % от всего кальция крови. Его уровень возрастает при понижении pH крови и снижается при защелачивании. На каждые 0,1 единицы понижения pH ионизированный кальций отвечает повышением на 1,5-2,5 %. Так как уровень ионизированного кальция не зависит от количества белка крови, он иногда является более надежным показателем первичного гиперпаратиреоза для людей с низким уровнем альбумина, чем уровень общего кальция крови.
Несмотря на то что показателя общего кальция крови часто хватает для предварительной оценки кальциевого обмена, так как часто баланс между связанным и свободным кальцием – величина стабильная и достаточно предсказуемая, у некоторых людей это соотношение нарушено, поэтому уровень общего кальция не является критерием для оценки всего кальциевого обмена. В таких случаях проверка ионизированного кальция становится необходимой.
Раннее выявление остеопороза и лечение позволяют предотвратить прогрессирование заболевания и переломы, что значительно улучшает качество жизни людей старших возрастных групп.
Для чего используется исследование?
Когда назначается исследование?
При хронических заболеваниях почек;
При лечении глюкокортикоидами (выявление супрессии костного метаболизма).
Что означают результаты?
N-Остеокальцин:
Диагностика остеопороза
Остеопороз – метаболическое заболевание костей, при котором снижается количество кости и происходит микроструктурная перестройка костной ткани. В связи с этим снижается прочность кости и повышается риск переломов. В Юсуповской больнице ревматологи проводят обследование на остеопороз с помощью современных инструментальных и лабораторных методов исследования. Для лечения пациентов врачи индивидуально подбирают эффективные лекарственные препараты, зарегистрированные в РФ. Они обладают высокой эффективностью и минимальным спектром побочных эффектов.
Потеря массы костной ткани при остеопорозе происходит исподволь и часто диагностируется только после переломов. После наступления менопаузы у женщин отмечается максимальная скорость потери костной массы. Она достигает 2–5 % в год. В итоге женщина к семидесяти годам теряет от 30 до 50 % массы костной ткани, мужчина – от 15 до 30 %. Ранняя диагностика остеопороза позволяет врачам Юсуповской больницы предотвратить грозные осложнения заболевания.
Как определить остеопороз
Диагностировать остеопороз порой бывает сложно, поскольку в большинстве случаев заболевание протекает бессимптомно и пациенты не обращаются за медицинской помощью. Наиболее постоянный симптом остеопороза – боли в крестцовом и поясничном отделах позвоночника, в области тазобедренных суставов. Пациенты иногда предъявляют жалобы на боли в области голеностопных суставов, костях таза, рёбра. Болевой синдром. усиливается при перемене погоды и атмосферного давления, физической нагрузке.
В дальнейшем боли становятся постоянными в связи с перенапряжением связок позвоночника и мышц спины. В период возникновения перелома рёбер или позвонков острая боль локализуется в месте перелома. При наличии этих симптомов врачи Юсуповской больницы проводят обследование на остеопороз с помощью денситометрии.
Клиническая картина остеопороза характеризуется следующими особенностями:
Наиболее демонстративный симптом остеопороза – перелом костей. При остеопорозе в постменопаузе преимущественно происходит потеря губчатой костной массы. Чрезвычайно характерны переломы тел позвонков. Диагноз перелома тела позвонка травматологи устанавливают на основании появления острой боли в соответствующем отделе позвоночника, которые резко усиливаются при движениях и постукивании по позвоночнику, и данных рентгенографии позвоночника в двух проекциях.
У женщин старше 45 лет возникают также переломы луча в типичном месте. В более поздних стадиях остеопороза происходят переломы шейки бедра. Множественные переломы ребер часто возникают при остеопорозе, который развился вследствие длительного применения глюкокортикоидов.
У пациентов с возрастным остеопорозом наблюдаются потери как губчатой, так и кортикальной костной массы. Возникают переломы шейки, связанные с кортикальным остеопорозом, и межвертельные переломы по причине потери губчатого вещества. В этом случае диагноз остеопороза устанавливают во время рентгенологических исследований.
Как диагностировать остеопороз
Начальный этап диагностики остеопороза – выявление факторов риска на основе данных пациента. Вероятность развития остеопороза повышается у пациентов с низким содержанием кальция в рационе, дефиците витамина D, страдающих заболеваниями желудочно-кишечного тракта (вследствие снижения всасываемости кальция). Риск развития остеопороза повышается при наличии следующих факторов:
Врачи Юсуповской больницы широко используют в диагностике остеопороза рентгенологические методы. При рентгенографии можно обнаружить наличие нарушения плотности кости только при потере более 30 % костной массы. С помощью данного метода чаще выявляют поздние признаки остеопороза – переломы трубчатых костей или деформацию позвонков.
Информативным методом обследования на остеопороз является денситометрия – измерение плотности костной ткани, основанное на определении кальция. Для ранней диагностики остеопороза используют различные методы костной денситометрии. Они позволяют выявить уже 2–5 % потери массы кости, оценить динамику плотности костной ткани в процессе развития заболевания или эффективность проводимой терапии.
Врачи применяют изотопные методы исследования (монофотонную и двухфотонную абсорбциометрию), рентгеновские (моноэнергетическую и двухэнергетическую абсорбциометрию, количественную компьютерную томографию) и ультразвуковые. Двухэнергетическая рентгеновская абсорбциометрия – золотой стандарт, позволяющий измерять содержание костного минерала в любом участке скелета, определять содержание солей кальция, мышечной массы и жировой ткани во всём организме. С помощью денситометров проводят исследование поясничных позвонков, костей предплечья, проксимальных отделов бедра и всего тела.
Анализы при остеопорозе у женщин и мужчин
С целью оценки метаболизма костной ткани ревматологи Юсуповской больницы применяют лабораторные методы диагностики. Целью лабораторной диагностики является исключение заболеваний, проявлением которых может быть остеопения (остеомаляции, болезни Педжета, костных метастазов, миеломной болезни), установление причин вторичного остеопороза и метаболическая характеристика заболевания. Последняя важна для постановки диагноза и выбора метода адекватной терапии, оценки ее эффективности.
Как называется анализ на остеопороз? Для оценки интенсивности костного обмена используют специальные биохимические маркеры, которые разделяют на 3 группы. К маркерам формирования костной ткани относится остеокальцин, кальцитонин и костный фермент щелочной фосфатазы – остаза.
Остеокальцин является основным неколлагеновым белком костного матрикса, который продуцируют остеобласты. Выработка остеокальцина зависит от витаминов К и D. Это до некоторой степени снижает чувствительность и специфичность определения остеокальцина как маркера метаболизма костной ткани.
Именно концентрация кальцитонина в крови отражает метаболическую активность остеобластов костной ткани, поскольку это вещество является результатом нового синтеза, а не высвобождения его при разрушении кости. При первичном остеопорозе выявляют нормальный или слегка повышенный уровень остеокальцина. Его повышение при первичном остеопорозе происходит у лиц с высоким уровнем костного обмена. Повышенный уровень декарбоксилированного остеокальцина может являться прогностическим параметром увеличения риска переломов бедра при остеопорозе у лиц пожилого возраста.
Выработка кальцитонина происходит в парафолликулярных клетках щитовидной железы. Кальцитонин оказывает следующее влияние на костную ткань, обмен кальция и фосфора:
Костный фермент щелочной фосфатазы (остаза) является показателем состояния костной ткани. Его исследование назначают для диагностики обменных заболеваний кости и контроля эффективности лечения остеопороза. Активность остазы повышается при патологии костей с повышением активности остеобластов или распадом костной ткани, гиперпаратиреозе, рахите, остеосаркоме и раковых метастазах в кости, при заживлении переломов.
Физиологическое повышение активности остазы наблюдается в период быстрого роста, у женщин в последнем триместре беременности и после менопаузы. Активность остазы снижается при гипотиреозе, наследственной гипофосфатаземие, нарушении роста кости, недостатке магния и цинка в пище. Маркер формирования костного матрикса определяют с целью оценки эффективности анаболической и антирезорбтивной терапии остеопороза, других видов патологии костной ткани.
Анализ на остеопороз
В диагностике остеопороза используют маркеры состояния обмена:
Паратгормон участвует в регулировании восстановления структуры костной ткани. Этот маркер исследуют при наличии повышения уровня кальция или понижении содержания фосфора в крови. При постменопаузальном остеопорозе уровень паратгормона чаще нормальный или пониженный, а у пациентов со стероидным или возрастным остеопорозом немного повышен.
Показатели содержания кальция в крови при первичном остеопорозе не выходят за пределы физиологической нормы. Гиперкальциемия определяется у больных сенильным остеопорозом при длительной иммобилизации после перелома шейки бедра. Повышенное содержание кальция в крови наблюдается при первичном остеопорозе, сопровождающемся повышенным костным обменом.
При первичном остеопорозе уровень фосфора в крови в большинстве случаев не выходит за пределы нормы. Он снижается у пожилых людей при сочетании остеопороза с остеомаляцией (размягчением костей). Для оценки почечного обратного всасывания фосфора концентрацию определяют в утренней моче.
Витамин D общий – это показатель, который отражает статус витамина D в организме. Уровень витамина D может варьировать в зависимости от возраста (у пожилых людей он снижается), характера принимаемой пищи, сезона (выше в конце лета, ниже зимой). Снижение содержания в крови витамина D наблюдается при беременности.
Маркеры резорбции костной ткани
Для оценки эффективности лечения остеопороза используют маркеры резорбции (повторного всасывания). Их снижение под влиянием терапии начинается уже через 2–3 недели и достигает нормы через 3–6 месяцев. Вeta-CrossLaps (С-концевые телопептиды), образуются при деградации коллагена первого типа, который составляет более 90 % органического матрикса кости. Его измерение позволяет оценить темпы деградации относительно «старой» костной ткани. При патологическом увеличении обратного всасывания при остеопорозе и в пожилом возрасте коллаген первого типа деградирует в большом объеме. Это приводит к увеличению уровня его фрагментов в крови.
В настоящее время существуют данные о влиянии полиморфизма генов на минеральную плотность костной ткани. Аллельный полиморфизм сети генов костного ремоделирования изучают для выявления генотипов предрасположенности к остеопорозу. Широко распространёнными ферментами являются кислые фосфатазы. Их уровень анализируют с целью определение степени обратного всасывания кости, мониторинга антирезорбтивной терапии.
Чтобы выполнить современную и качественную диагностику остеопороза в лаборатории Юсуповской больницы, запишитесь на приём к ревматологу, позвонив по телефону контакт центра. Врач после первичного осмотра назначит те анализы на остеопороз и инструментальные методы исследования, которые наиболее информативны для установления пациенту точного диагноза. Обследование на остеопороз методом денситометрии позволяет выявить снижение минерализации костной ткани на доклиническом этапе развития патологического процесса.
Что такое маркеры остеопороза
Современная лабораторная диагностика остеопороза.
Значимость заболевания в современном обществе и медицине определяется его распространённостью среди населения, тяжестью течения и исходов, экономическими потерями больного, семьи и общества в целом. Остеопороз (ОП) — системное метаболическое заболевание скелета, характеризующееся снижением массы костной ткани и нарушением микроархитектоники её строения, что снижает прочность кости и увеличивает риск переломов. По мнению экспертов ВОЗ, ОП сегодня — одно из наиболее распространённых заболеваний, которое наряду с инфарктом миокарда, инсультом, раком и внезапной смертью занимает ведущее место в структуре заболеваемости и смертности населения.
Результаты многочисленных исследований убедительно доказали, что костная масса является главной детерминантой механических свойств костной ткани и определяет 75-80% её крепости. Риск переломов прямо связан с абсолютными значениями минеральной плотности костной ткани (МПКТ) позвоночника и шейки бедра, а костная денситометрия — единственный достоверный метод, позволяющий установить степень снижения костной массы. Риск перелома увеличивается с возрастом, который главным образом связан у пожилых людей с низкой МПКТ. Риск перелома бедра возрастает в 2-3 раза при каждом снижении МПКТ шейки бедра на одно стандартное отклонение в соответствии с критериями ВОЗ.
Патогенез остеопороза.
ОП сегодня широко используется как модель фундаментальных исследований в изучении молекулярных механизмов межклеточного взаимодействия. ОП – многофакторное заболевание, в основе которого лежат процессы нарушения костного ремоделирования с повышением резорбции костной ткани и снижением костеобразования. Ремоделирование костной ткани начинается с резорбции, осуществляемой в процессе остеокластогенеза с образованием полости резорбции. Остеобласты (ОБ) «атакуют» полость резорбции, где строят новый костный матрикс для последующей минерализации. Оба процесса костеобразования тесно связаны. Образование кости превышает резорбцию в течение роста скелета, и наоборот, резорбция превалирует в течение последующего периода жизни человека. Оба процесса костеобразования являются результатом тесного клеточного взаимодействия ОБ иостеокластов (ОК), которые берут начало от предшественников различных клеточных линий, а именно: ОБ — из мезенхиальных стволовых клеток, ОК — из макрофагально-моноцитарных клеток крови.
Кость формируется остеобластами. Основная их функция – синтез остеоида (протеинового матрикса), который на 90-95% состоит из коллагена 1 типа, на 5% из белка остеокальцина и впоследствии минерализуется кальцием и фосфатом из внеклеточной жидкости. ОБ содержат фермент щёлочную фосфатазу, несут рецепторы к паратиреоидному гормону (ПТГ) и кальцитриолу и способны к пролиферации. Минеральная часть кости состоит из гидроксиапатита и аморфного фосфата кальция, которые нековалентно связаны с белками органического матрикса
Резорбция кости осуществляется остеокластами. Это подвижные клетки. Выделяя протеолитические ферменты и кислую фосфатазу, вызывают деградацию коллагена, разрушение гидроксиапатита и выведение минералов из матрикса. Имеется корреляция между активностью тартратрезистентной кислой фосфатазы в сыворотке крови и выраженностью резорбтивных процессов в кости.
В норме оба процесса – образование и разрушение уравновешены.
Сроки физиологического ремоделирования кости.
| Фаза резорбции кости | 14-30 дней |
| Switch-over фаза (простагландин Е2 ответственен за апоптоз остекластов) | 10 дней |
| Фаза формирования кости | 90 дней |
| Фаза отдыха | 900 дней |
Биологический смысл феномена ремоделирования кости состоит в приспособлении механических свойств кости к постоянно меняющимся условиям окружающей среды. Рост и обновление скелета сопровождается регенерацией микроповреждений и поддержанием возможности перехода минералов в кровь и обратно. У взрослых людей остеобласты продуцируют чуть меньше костной ткани, чем требуется. Следствием этого является отрицательный баланс кости, который составляет 0,5-1% ежегодно. Данный феномен известен как «ассоциированная с возрастом остеопения».
OPG-остеопротегерин – остеокластингибирующий фактор, гликопротеин, широко экспрессированный в различных тканях, является мощным ингибитором костной резорбции. OPG действует для RANKL как «мнимый» рецептор, блокирует взаимодействие с RANK и таким образом ингибирует формирование зрелых ОК, нарушает процесс остеокластогенеза и резорбцию костной ткани. Баланс между RANKL и OPG фактически определяет количество резорбированной кости.
Недавно были получены данные, что Т-клетки принимают участие в регуляции костного метаболизма. При индукции интерлейкина-17 (IL-17),который в эксперименте индуцировал экспрессию СОХ-2-зависимого простагландина Е2 и RANKL в ОБ, авторы пришли к заключению, что IL-17 — важный цитокин для остеокластной резорбции. Однако наиболее важными медиаторами для действия различных систем в процессе ремоделирования костной ткани как в норме, так и при ОП является в настоящее время система RANKL-RANK-OPG.
Факторы, играющие важную роль в патогенезе ОП и его переломов: генетические, формирование низкого пика костной массы, потеря минеральной плотности кости, ассоциированная с возрастом и постменопаузой, нарушение архитектоники строения кости, особенности геометрии кости (бедра), травмы и падения, питание с низким содержанием кальция и витамина D, белка и др., низкая двигательная активность, вредные привычки (курение, алкоголь). При вторичном ОП к перечисленным факторам присоединяются факторы заболевания, отрицательного действия лекарственных препаратов (глюкокортикостероиды, иммунодепрессанты и др.), которые вызывают потерю костной массы и ОП.
Снижение костной массы при ОП, которое является основным фактором его патогенеза, рассматривается сегодня как следствие формирования неадекватно низкого пика костной массы в молодом возрасте и интенсивной потери кости, связанной с возрастом, в пожилом возрасте. Генетические факторы — главные детерминанты пика костной массы. Вклад генетических факторов составляет 60-80% в зависимости от методов исследования (близнецы, семьи). Различные гены рассматриваются в качестве кандидатов, участвующих в сложном процессе ремоделирования, формирования и эволюции костной массы, приводящих к ОП и переломам. Многочисленные комплексные исследования различных лабораторий мира направлены на поиск конкретных генов, изучение их полиморфизма, функции и взаимодействия в процессе костного ремоделирования и ОП.
Первичный остеопороз
Остеопороз, развивающийся в периоде постменопаузы, относится к классу первичных остеопорозов. Известно, что снижение секреции половых гормонов в период климактерия оказывает прямое и опосредованное влияние на состояние костного метаболизма. Снижение содержания эстрогенов приводит к нарушению кальциевого обмена, что сопровождается уменьшением минеральной плотности костной ткани. Кроме того, имеет место подавление активности остеобластов, что приводит к преобладанию резорбции над процессами формирования костной ткани. Постменопаузальный остеопороз составляет 85% общего количества первичного остеопороза.
Сенильный остеопороз — так называемый второй тип остеопороза, в патогенезе которого важную роль играет снижение всасываемости кальция в кишечнике, чему также способствует дефицит витамина D, вызванный уменьшением поступления его с пищей, замедлением образования его в коже из провитамина D. Наибольшее значение в патогенезе сенильного остеопороза имеет дефицит активных метаболитов витамина D вследствие снижения его синтеза в почках. При сенильном остеопорозе определённую роль играет развитие резистентности к витамину D — т.е. дефицит рецепторов 1,25(ОН)2D. Указанные факторы вызывают развитие транзиторной гипокальциемии, что приводит к усилению продукции паратиреоидного гормона. В результате вторичного гиперпаратиреоза усиливается резорбция костной ткани, в то время как костеообразование к старости снижено.
Вторичный ОП
Серьёзной медицинской проблемой является и вторичный ОП, возникающий при различных заболеваниях: ревматологических, эндокринологических, онкологических, обструктивных заболеваниях лёгких и бронхиальной астмы, заболеваниях почек, щитовидной железы, органов пищеварения, при иммобилизации и длительном приёме ряда медикаментов (кортикостероиды, иммунодепрессанты, антиконвульсанты, тиреоидные гормоны и др.).
Снижение МПКТ при вторичном ОП часто достигает критериальных величин ОП (-2,5 SD и более по Т-критерию) и даёт основание поставить диагноз.
У больных ревматоидным артритом (РА) в постменопаузе развитие ОП имело место в поясничном отделе позвоночника и шейке бедра у 36%, в предплечье у 40%, а у пациентов с сохранённым менструальным циклом — у 7 и 10% соответственно. Возраст больных и длительность менопаузы, наличие факторов риска, активность и длительность заболевания, степень функциональной недостаточности суставов, проводимая терапия (особенно назначение глюкокортикоидов — ГК) оказывают влияние на величину потери МПКТ и развитие остеопении. При обследовании больных с эндогенным гиперкортицизмом (синдром и болезнь Иценко-Кушинга) ОП обнаружен у 91%, переломы тел позвонков или рёбер — у 58%. ОП у больных бронхиальной астмой значительно утяжеляет течение основного заболевания, увеличивает стоимость лечения. По данным доктора И.А.Барановой, снижение МПКТ было выявлено у 42,8% больных бронхиальной астмой 20-49 лет, ранее не получавших гормональную терапию, и потеря МПКТ увеличивалась в 5 раз при среднетяжёлом течении (53,5%) по сравнению с легким (11%). У больных молодого и среднего возраста, принимавших ГК в средней дозе 10,20±5,99 мг/сут на протяжении 8-14 лет, снижение МПКТ обнаружено у 85%, у 13% зарегистрированы переломы скелета. В качестве причины развития ОП при РА, ряде воспалительных заболеваний, бронхиальной астме обсуждается непосредственное влияние самого заболевания на костную ткань, поскольку известно большое число общих цитокинов, принимающих участие в патогенезе хронического воспалительного процесса и костного ремоделирования, а также ГК, которые наиболее эффективны для базисной терапии при ряде системных заболеваний и в то же время занимающих ведущее место в индукции вторичного ОП. Изучение переломов при вторичном ОП остаётся актуальной задачей.
Стероидный остеопороз также относится к классу вторичных остеопорозов и вызывается патологическим повышением эндогенной продукции глюкокортикоидов надпочечниками или возникает при введении синтетических аналогов кортикостероидов, применяемых для лечения ревматологических, аллергических, гематологических, глазных болезней, заболеваний кожи, желудочно-кишечного тракта (ЖКТ), почек, печени. Стероидный остеопороз возникает при заболеваниях, характеризующихся повышенной секрецией кортикостероидов надпочечниками (Иценко-Кушинга).
Биохимические маркеры костного метаболизма
Их исследуют для оценки скорости протекания процессов костного ремоделирования и диагностики остеопороза с высоким или низким темпом костного обмена, разобщённости или дисбаланса его составляющих: костной резорбции и костеобразования. Разделение показателей на маркеры образования и резорбции кости является условным. Совместно они отражают итоговые изменения резорбции и костеобразования, направленные в ту или иную сторону.
Наиболее точными маркерами костного образования в настоящее время признают исследование содержания остеокальцина, коллагена 1 типа, остеопротегерина (OPG), Интерлейкина 17 в крови.
Исследование маркеров костного ремоделирования целесообразно для:
1. Динамической оценки костного метаболизма;
2. Прогноза потери костной массы (вторичная профилактика при выявленной остеопении);
3. Прогноза перелома костей;
4. Отбора пациентов для проведения терапии;
5. Быстрого мониторинга терапии.
Процесс костного ремоделирования регулируется многими системными гормонами, цитокинами, факторами роста, идентифицированы многие локальные факторы костного ремоделирования. При изучении ОП важна оценка параметров минерального кальций-фосфор-магниевого обмена (уровень общего и ионизированного кальция, фосфора, магния, меди, цинка, витаминов С и К), которые вовлечены в процесс костеобразования.
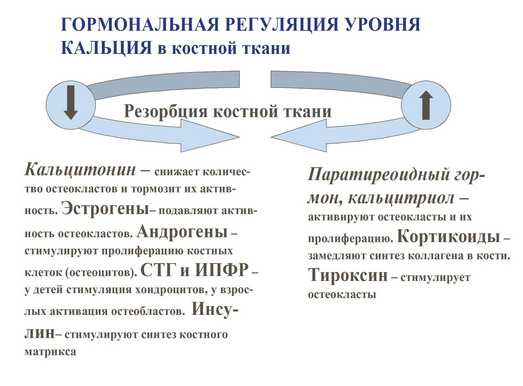
Гормональная регуляция уровня кальция в кости.
— паратиреоидный гормон – стимулирует резорбцию кости опосредованно воздействуя на остеокласты;
— кальцитонин – снижает количество остеокластов и тормозит их активность;
— эстрогены – подавляют активность остеокластов;
— андрогены – стимулируют пролиферацию остеоцитов и усиливают процессы костного синтеза;
— гормон роста и инсулинподобный фактор роста 1 (соматомедин-С) – активируют процесс синтеза кости за счёт стимуляции остеобластов;
— инсулин – стимулирует синтез костного матрикса;
— тироксин – стимулирует остеокласты, усиливая резорбцию костной ткани;
— кортикостероиды – замедляют синтез коллагена в костной ткани;
Из вышеперечисленного следует, что изучение уровня этих гормонов и маркеров костного ремоделирования на ранней стадии развития остеопении, особенно при вторичном ОП, позволит спрогнозировать и оценить вероятность дальнейшей резорбции костной ткани, провести профилактику ОП, назначить лечение.
Алгоритм лабораторной оценки костного ремоделирования.