Что такое ледяная уксусная кислота
Характеристика и свойства уксусной кислоты
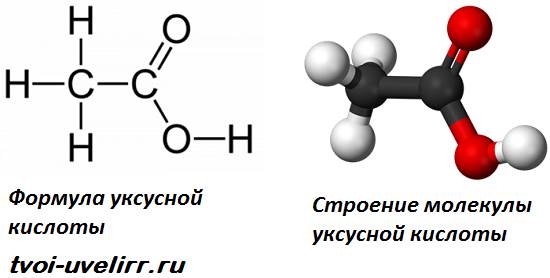
Уксусная кислота (или этановая) – органическое химическое соединение, относящееся к карбоновым кислотам (в состав их формулы входит карбоксильная группа – COOH). Это вещество известно человечеству с древних времен. Без нее невозможно производство многих пищевых продуктов и получение органических веществ.
Общая характеристика, формула
Химическая формула вещества СН3СООН. При нормальных условиях это бесцветная жидкость, обладающая резким характерным запахом и кислым вкусом. Попадание концентрированного вещества на слизистые оболочки вызывает химический ожог. «Ледяная» уксусная кислота 99 процентов обладает высокой гигроскопичностью, т.е. она способна поглощать водяной пар из атмосферного воздуха.
В уксусе могут растворяться не только жидкости, но и газы. Например, в нем растворяются фтороводород HF, хлористый водород HCl и бромистый водород HBr.
Соли рассматриваемого химического вещества называются ацетатами. Такое же наименование имеют и сложные эфиры. В качестве пищевой добавки применяется раствор уксусной кислоты с концентрацией 3 – 9%. В составе уксусной кислоты не может быть никаких примесей.
История открытия уксусной кислоты
Рассматриваемое вещество известно человеку с первобытных времен. СН3СООН образуется при скисании вина (отсюда и другое название – винный уксус). Впервые химические свойства уксуса описано в Древней Греции в 3 веке до н.э. В то время это вещество применялось для получения красителей. В Древнем Риме большой популярностью пользовался так называемый свинцовый сахар – ацетат свинца. Эта соль была причиной хронических отравлений и болезней римской аристократии.
Химическое строение уксуса впервые начал исследовать французский химик Дюма: он опубликовал труд о замещении атома водорода в органических соединениях атомом хлора. Так он получил хлоруксусную кислоту.
В середине 19 века немецкий химик А. Кольбе синтезировал уксус путем хлорирования сероуглерода CS2 до тетрахлометана CCl4, который путем пиролиза превращался в тетрахлорэтилен C2Cl4. Дальнейшее воздействие хлором водного раствора тетрахлорэтилена дало возможность получить трихлоруксусную кислоту. После электролитического восстановления ученый получил СН3СООН.
Еще в начале ХХ века значительное количество уксуса проводилось путем перегонки древесины.
Получение и производство
На ранних этапах развития индустрии вещество уксусная кислота получали путем окисления бутана и ацетатальдегида. Этот альдегид окислялся в присутствии катализатора ацетата марганца при высоком давлении и температуре. Реакция имела такой вид: 2СН3СНО + О2→2СН3СООН.
Окисление же бутана проходило при высоком давлении и в присутствии катализатора ацетата кобальта. Реакция имела такой вид: 2С4Н10 + 5О2→ 2СН3СООН.
В результате подорожания нефти (а рассмотренные способы базировались на окислении продуктов ее крекинга) сделали такие химические реакции экономически невыгодными. Более совершенный способ получения уксусной кислоты – это каталитическое карбонилирование метанола (древесного спирта) путем воздействия на него окисью углерода. Реакция имеет такой вид: СН3СОН + СО → СН3СООН. Катализатором служит йодистая соль кобальта.
С 1970 г. компания Монсанто предложила использовать в качестве катализатора родиевые соли. В результате производство уксусной кислоты заметно возросло.
В процессе биохимического производства применяется окисление этилового спирта микроорганизмами. Реакция проходит при участии фермента алькогольдегидрогеназы.
Также пищевую добавку уксусную кислоту можно получить путем окисления этилового спирта: С2Н5ОН + О2→ СН3СООН + Н2О.
Химические и физические свойства
Физические свойства уксусной кислоты следующие:
В следующих примерах показаны кислотные свойства уксусной кислоты.
Качественной реакцией на наличие ацетатов является их взаимодействие с сильными кислотами. Уксус вытесняется из водных растворов солей. При этом появляется характерный запах.
Хранение и транспортировка
Промышленная уксусная кислота наливается в транспортную тару (оцинкованные металлические бочки или канистры из полимерных материалов). В магазины раствор поступает в стеклянных или пластиковых бутылках с навинчивающимися крышками или пробками.
Хранить это вещество нужно в плотно закрытой таре в помещениях, которые специально приспособленные для хранения воспламеняющихся веществ. Места хранения уксусной кислоты должны быть защищенными от попадания прямых солнечных лучей и осадков.
Класс опасности уксусной кислоты – 8: едкие и коррозийные вещества.
Перевозку нужно осуществлять в цистернах из нержавеющей стали. Они не должны иметь нижнего слива. Наливные отверстия, люки оборудуются герметичными резиновыми, полиэтиленовыми прокладками, которые предотвращают расплескивание жидкости в процессе перевозки.
ООО «Эверест» осуществляет оптовые поставки уксусной ледяной (этановой) кислоты по выгодным ценам. Подробнее по телефону: +7 (812) 448-47-55.
Уксусная кислота. Свойства и применение уксусной кислоты
Спиртовой, яблочный, бальзамический, винный, солодовый, — все это пищевой уксус. Он становится итогом деятельности уксуснокислых бактерий.
Название создано по аналогии с молочнокислыми. Превратить в уксус, как видно, микроорганизмы могут многое.
Так, в Японии производят пшеничный, ячменный и рисовый настой. В США изготавливают острый уксус из ореха Пекан.
Бальзамическая жидкость из белого винограда популярна в странах Средиземноморья. Основное содержимое продукта – уксусная кислота.
Свойства уксусной кислоты
Уксусная кислота относится к карбоновым. На то указывает карбоксильная группа COOH. Перед ней идет метиловый фрагмент CH3.
Хотя, есть и синтетический метод получения. Об этом поговорим в отдельной главе.
Легко проходит взаимодействие и с неорганическими соединениями, у которых нет углеродного скелета.
Из веществ, в которых уксусная кислота не растворяется, упомянем сероуглерод. Это бесцветная жидкость с приятным ароматом.
То есть, жидкость ужимается. Это указывает на увеличение плотности. Максимум для уксусной кислоты – 1, 074 грамма на кубический сантиметр.
Уксусом признают водные растворы от 3-ех до 15-ти процентов. Наиболее популярна уксусная кислота 9, то есть, 9-процентная.
Если же речь идет об эссенции, — это 80-процентный раствор. Реже встречаются уксусная кислота 70 и 40.
Из всех эссенций можно сделать столовую добавку путем разбавления. Как развести уксусную кислоту, поведаем в специальной главе.
Пока же, ознакомимся со свойствами соединения в чистом 100-процентном виде.
Если нет сторонних примесей, растворителей, перед нами ледяная уксусная кислота.
При низких температурах она преобразуется в массу, напоминающую лед. Если градусы, напротив, зашкаливают, кислота самовоспламеняется.
Достаточно 454-ех по шкале Цельсия. Закипает же кислота при 118-ти градусах. Это в случае, если давление держится на 10-ти миллиметрах ртутного столба.
Если отметка поднимется до 42-ух миллиметров, температура кипения составит уже 42 градуса, а при 100-та миллиметрах ртутного столба процесс начнется на 62-ой отметке шкалы Цельсия.
Из химических реакций для уксусной кислоты типична не только диссоциация, то есть растворение, но и взаимодействие с активными металлами.
Так именуют элементы, проще остальных расстающиеся со своими электронами.
Применяясь в быту, героиня статьи является опасным соединением. Не зря в пищу добавляют слабые растворы вещества, причем, в малых количествах.
Эссенций требуется 20-40 миллилитров, в зависимости от концентрации. Речь о попадании реагента в пищевод.
Соединение сжигает его стенки, приводя к нестерпимым болям и отказу функций органов.
Ожог уксусной кислотой может быть и наружным. Он менее опасен, чем внутренний, есть шанс снизить вредоносное действие реагента в первые минуты его попадания на тело.
Добыча уксусной кислоты
Бактериальная закваска – не единственный ответ на вопрос, как получить уксусную кислоту. Кроме биогенного, есть синтетический способ.
Это выделение реагента из древесины, или нефтепродуктов. Из них получают ацетилен, а из него – уксусный альдегид.
Метод разработан русским ученым Михаилом Кучеровым. Этот химик работал в Лесотехнической академии Санкт-Петербурга в конце 19-го – начале 20-го столетий.
В ряде реакций получался уксусный альдегид. В итоге, Кучеров решил поместить в сосуд ацетилен и пропускать окись через него. Образование альдегида не заставило себя ждать.
Нюанс состоит в том, что уксусная кислота образуется в природе, а ацетилен – нет. Тем не менее, добыча кислоты из него выгоднее, чем ее извлечение из растений, плодов.
Поэтому, сначала проводят синтез ацетилена. Он не содержится в воздухе и не формируется в земле, может быть лишь побочным продуктом разложения углеводородов.
Ограничение прописано законодательно. Обоснование – недостаточные вкусовые качества и отсутствие дополнительных полезных веществ, образующихся при скисании винограда, зерновых, яблок.
Хороший уксус приравнивают к вину, точно так же выдерживают и коллекционируют.
Во Франции, к примеру, годовое потребление продукта на душу населения приближается к 4-ем литрам.
Не удивительно, что население страны волнуют нюансы вкуса и пользы съедаемого уксуса. В России же годовая норма на человека – 200 миллиграммов.
Столь незначительное участие продукта в кухне не вызывает интереса, 6-уксусная кислота стоит в холодильнике, или 15-ти, синтезирован продукт, или получен естественным путем.
Применение уксусной кислоты
В хозяйстве столовая уксусная кислота пригождается не только для готовки. Соединение используют в качестве пятновыводителя.
Особенно хорошо он устраняет следы от фруктов и ягод. Устранить реагент способен и неприятные запахи, в частности, затхлый.
Такой может появиться в хлебнице. Протрешь ее стенки раствором уксуса и избавишься от проблемы.
Сделав уксус из уксусной кислоты, можно протереть им пятна на стеклах и зеркалах. Приятным бонусом станет особый блеск поверхностей.
Эфир уксусной кислоты способен сделать нити и кожу более эластичными. Поэтому, перчатки, шелковые и замшевые вещи вымачивают в метановой воде из расчета 3 столовых ложки на 1 литр жидкости.
Если нужно счистить налет с душевой лейки, стоит, опять же, купить уксусную кислоту.
Деталь помещают в ее раствор на ночь. Утром лейку промывают под сильным напором воды.
Промыть, точнее, ополоснуть уксусным раствором рекомендуют и волосы. Они становятся шелковистыми, приобретают бриллиантовый блеск.
Цена уксусной кислоты
Речь об оптовых поставках. 70-процентный раствор стоит столько же. По сути, выгоднее брать ледяную и разводить уксус самостоятельно.
Здесь уж, как говориться, вопрос времени, наличия оборудования и, главное, желания.
Теперь, рассмотрим таблицу уксусной кислоты 9-процентной. За половину литра в стеклянной бутылке просят всего 14-18 рублей.
Однако, это ценник за продукт на основе синтетического соединения. Если рассматривать уксус яблочный, 500 миллилитров будут стоить уже 250-400 рублей.
За такой же объем винного уксуса просят около 100 рублей, а за половину килограмма бальзамического, и вовсе, 900-1500 рублей.
Порой, полторы тысячи просят всего за 250 миллилитров продукта. Точный ценник зависит от концентрации и производителя.
Уксус из стран Евросоюза и США, как правило, дороже предложений из бывших республик СССР.
Как разбавить уксусную кислоту
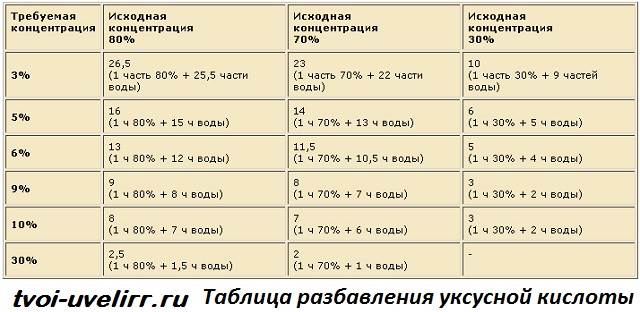
Прибавить нужно 7 частей питьевой воды. Соответственно, чтобы получить 9 уксус из 70-ти уксусной кислоты, нужно взять 10 миллилитров реагента и 70 миллилитров жидкости.
Если нужно уксусную кислоту развести не до уксуса 9, а до 6-процентного, следует на 10 миллилитров реагента взять 11 частей, то есть, 110 миллилитров, жидкости.
Иногда, требуется 8-процентный раствор. Его создают из столовой ложки кислоты и 80-ти миллилитров воды. 90 миллилитров жидкости идут на 7-процентный уксус.
Наиболее редко требуются 10-ти и 30-процентные растворы. Первый складывают из 10-ти миллилитров уксусной кислоты и 60-ти миллилитров жидкости.
30-процентная эссенция составляется из столовой ложки реагента и всего 15-ти миллилитров воды. Последняя концентрация используется для очистки тканей и металлических деталей.
10-процентный уксус еще подходит для готовки. Жидкость нужна кипяченая, желательно очищенная, пропущенная через фильтры.
Работать необходимо в резиновых перчатках, а в качестве емкостей использовать лишь керамическую, или стеклянную посуду.
Кислота уксусная 70%, 80%, 99,8%


Вещество бесцветно, отличается очень резким запахом. В чистом виде практически не применяется – это опасные для здоровья и жизни людей соединения. Перед использованием в промышленности, кулинарии или быту ледяная кислота обязательно должна быть разбавлена водой.
Что такое ледяная уксусная кислота
Ледяная уксусная кислота (ЛУК) представляет собой органическое соединение, одноосновную кислоту, относящуюся к классу карбоновых кислот.
Это регулятор кислотности, стабилизатор, зарегистрированная официально пищевая добавка Е260, нормы — ГОСТ 61-75.
Области применения:
Хранить дома жидкую ледяную кислоту опасно, так как даже небольшое ее количество при неосторожном применении может вызвать летальный исход.
Формула
Синонимы ледяной уксусной кислоты (формула СН3СООН или С2Н4О2) — этановая кислота, уксусная кислота, ЛУК. Acetic acid glaciad — международное название. Это эффективный растворитель органических соединений, который прекрасно смешивается с большинством растворителей, гигроскопична, хорошо растворяется в воде.
Квалификация вещества — «хч», то есть химически чистый (высшая степень чистоты реактива, то есть основной компонент содержится в количестве 99% и более).
ЛУК можно приобрести в аптеке без рецепта в виде:
Получение
Вещество получают микробиологическим (брожение содержащих спирт жидкостей) или химическим (перегонка древесины) способами.
ЛУК получают следующими способами:
Рекомендуем: Уксус против вредителей: особенности обработки капусты
Свойства уксусной кислоты напрямую зависят от ее концентрации, то есть от содержания воды или примесей.
Концентрация
Применяется в быту и пищевой промышленности как эссенция или уксус. Объясняется подобное легкостью разбавления вещества то нужной концентрации при знании правильных пропорций.
Названия кислоты разные и зависят от концентрации основного вещества:
Свойства
Ледяная кислота представляет собой кристаллы или жидкость без цвета, имеет очень резкий запах, на вкус кислая. Закипает при температуре +118,1 градуса Цельсия, плавится (то есть кристаллы становятся жидкостью) при +16,75 градуса Цельсия. Очень высокая температура обуславливает самовозгорание ЛУК.
Физические свойства
Ледяная уксусная кислота
Уксусная кислота представляет собой бесцветную жидкость с характерным резким запахом и кислым вкусом. Гигроскопична. Неограниченно растворима в воде. Смешивается со многими растворителями; в уксусной кислоте хорошо растворимы неорганические соединения и газы, такие как HF, HCl, HBr, HI и другие. Существует в виде циклических и линейных димеров.
Абсолютная уксусная кислота называется ледяной
, ибо при замерзании образует льдовидную массу.
Уксусная кислота образует двойные азеотропные смеси со следующими веществами.
Влияние уксуса на организм человека
Опасной для человека дозой служит 1 стакан (200 миллилитров) даже обыкновенного столового уксуса, если его выпить. Ледяной уксусной кислоты хватит 15 г или 20 мл, эссенции — от 20 до 40 мл. При попадании вовнутрь вещество сжигает стенки пищевода, что сопровождается невыносимой болью.
К химическому ожогу приведет попадание на кожу вещества с концентрацией от 30% и больше. Причем поражения могут быть разной степени тяжести. ЛУК при контакте с кожными покровами и слизистой провоцирует необратимый некроз тканей вследствие коагуляции.
Нейтрализовать разрушающее действие поможет незамедлительное и обильное промывание поврежденного участка большим количеством воды с обычным мылом, которое впитает кислоту с образованием хлопьев. Так происходит из-за щелочной реакции среды мыла. После промывания потребуется обработать обожженное место фурацилином или любым другим антисептиком.
Внимание! Пары ледяной кислоты крайне опасны. Нейтрализовать раздражение дыхательных путей поможет полоскание горла, носа, ингаляцией раствором кальцинированной соды (2%).
Сколько допускается употреблять уксусной кислоты человеку, науке до сих пор не известно. Случаи ухудшения здоровья человека в результате дефицита в рационе этого вещества медицине не известны.
Людям, страдающим язвой, гастритом или другими заболеваниями пищеварительного тракта продукты, содержащие вещество, употреблять не рекомендуется, так как оно раздражает, а иногда и разрушает слизистую. Что обуславливает появление изжоги, а в тяжелых случаях— ожог пищеварительного тракта. Редко, но встречается индивидуальная непереносимость.
Рекомендуем: Как избавиться от тли в саду — горчица и уксус помогут
Опасность передозировки
Чаще всего в быту появление ожогов провоцирует 80% эссенция, но иногда достаточно концентрации 30%. Повредить глаза можно 2% раствором. Для органов дыхания опасны пары с концентрацией уксусной кислоты 2%. Ядовитый пар вдыхается легкими, после чего выделяется ими же, что обуславливает возникновение пневмонии.
Передозировка приводит:
При вскрытии умершего человека кислота легко обнаруживается благодаря специфическому запаху.
Особенности применения ледяной уксусной кислоты
ЛУК применяется как водный раствор с разной концентрацией при печатании книг, производстве текстиля, в качестве реагента и растворителя.
Использование:
В быту вещество используется для удаления с одежды пятен от ягод, фруктов, неприятного, затхлого запаха в хлебнице (достаточно протереть ее стенки раствором), загрязнений на зеркалах и стеклах. После протирания ватными дисками, смоченными в разведенной кислоте засаленных участков на шерстяных вещах, волокна ткани восстанавливаются, а жирность исчезает. Стеклянные и зеркальные поверхности после обработки раствором начинают блестеть.
В народной медицине
ЛУК применяется в качестве прижигающего и мумифицирующего средства при удалении мозолей, бородавок и других доброкачественных поражений кожного покрова.
Разведенная ледяная кислота оказывает действие:
Уксусные компрессы в народной медицине широко применяются как средство, снижающее температуру тела.
Водный раствор применяется:
Важно! Лечиться ледяной кислотой самостоятельно категорически запрещено! План мероприятий должен назначить доктор.
Как лекарственное средство ЛУК внутрь не принимается. До ХХ века 5% раствор использовался в борьбе с ожирением. Действие основывалось на раздражении органов пищеварения (вплоть до ожога), в результате чего питательные вещества не усваивались. Люди действительно худели, но за это они расплачивались здоровьем.
Рекомендуем: Как избавиться от плесени с помощью уксуса
В косметологии
Благодаря свойству уничтожать микробы вещество используется при лечении прыщей. Кроме того, оно эффективно:
Важно! Употребление большого количества уксуса запрещено. Концентрированные растворы вообще противопоказано принимать внутрь, так как доза 20 мл уже является смертельной для человека.
Существуют правила предосторожности при использовании и хранении уксусной кислоты:
Кислота разъедает резиновые части бытовых приборов. Например, если в стиральную машинку залить концентрированный раствор, то резинка, находящаяся рядом с барабаном порвется.
Использование уксусной кислоты
Использование уксусной кислоты много и разнообразно. Эта кислота используется в производстве товаров, в пищевой промышленности, в индустрии чистоты, в медицине и в качестве пищевой добавки. Уксусная кислота также является биохимическим незаменимым в форме ацетильной группы, где это имеет основополагающее значение для конструирования аминокислот и поэтому невозможно существовать без. Давайте посмотрим на некоторые из этих применений уксусной кислоты более подробно.
Уксусная кислота в производстве товаров
Уксусная кислота является важным химическим реагентом, используемым для производства ацетата, клеев, клеев и синтетических тканей. Уксусная кислота также используется в гальванических покрытиях, когда металлическое покрытие наносится на объект путем помещения его в раствор, который содержит определенную соль металла. Раствор должен быть проводящим, а кислоты, которые отдают ионы водорода, создают идеальные условия. Кроме того, гальваническое покрытие может происходить только внутри раствора, а соли металлов растворяются только в растворах с низким (кислотным) значением рН.
Уксусная кислота является сырьем, используемым для производства ацетат целлюлозы, уксусный ангидрид (пластмассы) и хлоруксусная кислота, используемые в производстве красителей и пестицидов, а также некоторые лекарства.
Уксусная кислота в пищевой промышленности
Уксусная кислота используется в пищевой промышленности для регулирования уровня кислотности или щелочности пищевых продуктов. Свод федеральных правил (CFR) классифицирует уксусную кислоту как пищевую добавку общего назначения, которая безопасна при использовании в соответствии с надлежащей производственной практикой. В Европе правила использования электронных номеров распространяются на все пищевые добавки. Уксусная кислота имеет код E260 и считается безопасным ингредиентом, который контролирует бактериальную колонизацию и может использоваться без ограничений. Это не новая находка. Говорят, что древние вавилоняне использовали уксус в качестве пищевого консерванта.
Уксус используется для производства заправок для салатов, приправ, которые включают горчицу, кетчуп и майонез, а также в соусах и солениях.
Уксусная кислота для очистки
Уксусная кислота использовалась в качестве моющего средства и дезодоратора веками, если не тысячелетиями; губки уксуса были помещены в дорогие филигранные кольца, которые носили богатые, когда они шли по грязным и вонючим улицам восемнадцатого века. Дезодорирующие свойства уксуса также использовались в течение нескольких поколений. Моряки использовали уксус, чтобы вычистить палубы кораблей, на которых они работали и жили. Принципы микробного контроля, возможно, не были понятны в то время, но характеристики этого органического раствора, пахнущие, чистые и предотвращающие заболевания, были, безусловно, хорошо известны.
Добавление щелочного продукта к кислоте вызывает бурлящую, шипящую реакцию. Некоторые традиционные чистящие средства считают, что этот эффект обеспечивает более глубокую очистку устойчивых поверхностей. Например, очистка заднего двора щелочной едкой натрией (гидроксид натрия) и последующее использование смеси уксуса поверх этого вызовут реакцию, которая, безусловно, выглядит так, как будто она обладает эффектом глубокой очистки; однако, это очень мало увеличивает гигиенический эффект, а скорее противодействует щелочной моющей способности каустической соды с кислотными свойствами уксуса.
Сегодня многие преданные поклонники белого уксуса рекламируют экологические преимущества использования разбавленной уксусной кислоты для чистки ванных комнат, стирки белья, удаления запахов и придания чистоте и безопасности поверхностям приготовления пищи. Уксусная кислота также удаляет ржавчину и известковые отложения.
Уксусная кислота в медицине
Уксусная кислота или уксус, вероятно, использовались в медицине еще до написания слова. Если вы пострадали от открытой раны на острове Кос в четвертом веке до нашей эры, возможно, Гиппократ назначил вам ежедневную стирку уксуса. Если у вас болит горло, он мог бы также попросить вас смешать мед и уксус, чтобы сделать Oxymel, древнегреческое лекарство от кашля; Если вы служили в Европе во время Первой мировой войны, вы могли иметь только доступ к чистому уксусу и оставаться свободным от инфекции.
Сегодня растворы уксусной кислоты используются в лаборатории. кровь тестирование процессов как мойка слайдов. Они удаляют бактериальные биопленки в ранах и пищеварительная система и часто использовались при инфекциях наружного уха, поэтому избегайте применения антибиотиков. Проглатывание уксуса повышает уровень ацетата в толстой кишке и способствует усвоению кальция с более низким кровяным давлением и более высокой плотностью кости в результате. Исследования изучают использование ацетата в качестве противоопухолевого препарата.
Уксусная кислота как пищевая добавка
Уксусная кислота является популярной пищевой добавкой и употребляется в форме уксуса, чаще всего яблочного уксуса. Когда связано с коэнзим А, ацетильная группа уксусной кислоты занимает центральное место в углеводном и жировом обмене.,
Много исследований было сделано в отношении связи между потреблением уксуса и снижением уровня глюкозы в крови. В тех случаях, когда продукты с высоким гликемическим индексом потребляются после приема двух-трех столовых ложек яблочного уксуса, их гликемическая ценность снижается на 35%. Для диабетиков это может означать снижение пикового уровня глюкозы в крови после приема пищи и улучшение гликемического контроля, а также для пациентов, не страдающих диабетом. меньший риск развития резистентности к инсулину, Замена штатного огурца маринованным огурцом показали снижение общего гликемического индекса на 30%.
На следующем изображении показан эффект продукты с низким и высоким гликемическим индексом (GI) на уровень глюкозы в крови. Продукты с высоким ГИ вызывают быстрый пик уровня глюкозы в крови, что увеличивает выработку инсулина, что позволяет клеткам метаболизировать глюкозу. Это означает, что уровень глюкозы в крови быстро падает, вызывая чувство голода. Продукты с низким ГИ вызывают более мягкий рост сахара в крови и не заставляют поджелудочную железу вырабатывать такое большое количество инсулина. В результате получается плавная кривая, которая остается стабильной и не опускается, увеличивая уровень сытости после еды. Когда пища с высоким GI и пищей с низким GI съедается одновременно, они частично компенсируют друг друга, создавая эффект плато. Уксус, как известно, имеет тот же эффект, что и пища с очень низким ГИ.