Бутанол что это такое
Бутанол (бутиловый спирт)
Бутиловый спирт (бутанол) — бесцветная, чуть маслянистая жидкость с характерным запахом сивушного масла. Ограниченно растворим в воде.
Существуют 4 изомера бутанола:
Н-бутанол используется как растворитель для красок, лаков и олиф, натуральных и синтетических смол, каучуков, растительных масел, красок и алкалоидов. Он играет роль промежуточного звена в производстве фармацевтических препаратов и химикалий, и используется в отраслях промышленности, производящих искусственную кожу, текстиль, небьющееся стекло, резиновый клей, шеллак, плащи, фотографические пленки и духи.
Вторичный бутанол также используется как растворитель и химический промежуточный продукт; он входит в состав тормозных жидкостей, промышленных моющих средств, политур, средств для удаления краски, агентов для флотации руды, фруктовых эфирных масел, духов, красителей.
Изобутанол является растворителем поверхностных покрытий и клеев; он входит в состав лаков, средств для удаления краски, духов, чистящих средств и гидравлической жидкости.
Трет-бутанол используется для удаления воды из различных материалов, как растворитель в производстве лекарств, духов и ароматических веществ, а также в качестве химического промежуточного продукта. Он также входит в состав промышленных моющих средств, применяется для денатурации этилового спирта и добавляется в бензин для повышения его октанового числа.
Информация о токсичности
Токсичность бутанола относительно невелика (LD50 составляет 2290–4360 мг/кг), но наивысшая среди младших спиртов.
При употреблении внутрь возникает эффект, сходный с эффектом от употребления Этанола.
Бутанол содержится в небольших количествах в различных алкогольных напитках.
Иногда бутанол, полученный из технических жидкостей, используется в качестве суррогатного алкогольного напитка.
Концентрация в 0.01% в воздухе ни как не влияет на организм, в то время как 0.02% вызывает воспаление роговой оболочки глаза.
Спецификация на бутанол, согласно ГОСТ 5208-81:
Массовая доля основного вещества, %, не менее
. 99,5
Массовая доля кислот, %, не более
. 0,005
Массовая доля воды, %, не более
. 0,1
Показатель преломления
. 1,407-1,409
Бутанол (бутиловый спирт) фасуется производителем в 200-литровые бочки, при необходимости производиться фасовка в канистры.
По типу материала
По области применения
Полуфабрикатные материалы, Химическая промышленность
Бутиловый спирт — химическое сырье, растворитель и добавка к автомобильному топливу
Бутиловый спирт — органическое вещество, углеводород бутанол, первичный спирт. 
Бутиловые спирты
В группу бутиловых спиртов входит сам бутиловый спирт или 1-бутанол, н-бутанол (нормальный), а также его три изомера:
— изобутиловый спирт;
— 2-бутанол (втор-бутанол, втор-бутиловый спирт, нормальный вторичный бутиловый спирт);
— трет-бутанол (трет-бутиловый спирт).
Изомеры различаются структурой молекул, и, соответственно, физическими свойствами.
Свойства
Н-бутанол — это маслянистая жидкость, без цвета, прозрачная, с характерным запахом. В воде растворяется, но в небольших пропорциях, менее 8 г в 100 мл воды. Хорошо смешивается с органическими растворителями. Втор- и трет-бутиловый спирты смешиваются с водой в любых пропорциях. Трет-бутанол при нормальных условиях может быть твердым веществом, которое плавится при 25 °С, или жидкостью при более высоких температурах.
Бутиловый спирт обладает более высокой энергоэффективностью, чем бензин, этиловый и метиловый спирты, поэтому его выгодно добавлять в топливо, в том числе в дизельное. При этом топливо с добавками бутанола оказывается более безопасным для окружающей среды.
Бутиловый спирт — менее агрессивный химический реактив, чем этиловый спирт. Он менее летуч, его допускается использовать в топливных трубопроводах, тогда как этанол перевозится только в цистернах.
Токсичность бутилового спирта
При попадании внутрь воздействие бутанола на человеческий организм сходно с воздействием этилового спирта. Наибольшую опасность представляют пары бутанола при длительном их вдыхании. Они могут вызвать головные боли, раздражение глаз и органов дыхания, угнетение центральной нервной системы, поэтому при работе с бутанолом надо использовать средства защиты.
При попадании бутилового спирта в глаза существует риск потери зрения, поэтому глаза следует немедленно промыть водой и обратиться к врачу.
Применение
Н-бутиловый спирт:
— сырье в органическом синтезе полигликолей, бутиленгликолей, бутилацетата и некоторых других органических веществ, в том — числе фармацевтических препаратов;
— добавка в автомобильное топливо;
— научные и лабораторные исследования;
— востребован в микроэлектронике, в производстве кожезаменителей, плащей, ударопрочного стекла, фотопленки, резинового клея, парфюмерных изделий;
— для получения керамических покрытий;
— в топливных элементах;
— для получения водорода.
Изобутиловый спирт применяется для изготовления:
— присадок для смазочных масел;
— фармацевтических препаратов, пищевых эссенций, как основа для отдушек и парфюма;
— пестицидов.
Бутиловый и изобутиловый спирты используют:
— в качестве промышленных и бытовых растворителей для лаков и красителей, жиров и масел, полиакрилатов;
— как модификатор при производстве синтетических органических смол;
— при изготовлении нескольких видов химических пластификаторов, например, дибутилфталата.
Втор-бутиловый спирт используется:
— в качестве растворителя, средства для полировки, удаления краски;
— как высококалорийная добавка в топливо;
— как составная часть тормозных и гидравлических жидкостей; производственных моющих средств;
— для стабилизации бензинометиловых смесей;
— в качестве сырья при производстве втор-бутилацетата, метилэтилкетона;
— для алкилирования и дегидратации в органическом синтезе;
— для получения красителей, эфирных масел, отдушек.
Трет-бутиловый спирт используется в качестве:
— растворителя, антисептика;
— химического сырья для получения искусственного мускуса, изобутена и некоторых других органических соединений;
— для алкилирования и дегидратации в органическом синтезе.
Необходимый для лабораторий и производства химический реактив бутиловый спирт, бутилацетат, а также другие химреактивы, лабораторное оборудование и средства защиты по хорошим ценам и с доставкой по Москве и области можно купить в «ПраймКемикалсГрупп». Интернет-магазин примечателен широчайшим ассортиментом товаров для химиков, медиков и специалистов в области различных производств. У нас хороший сервис, есть система скидок.
Бутанол
Бутиловый спирт (бутанол) C4H9OH — бесцветная жидкость с характерным запахом сивушного масла. Известны нормальный первичный бутиловый спирт СН3(СН2)3ОН, нормальный вторичный бутиловый спирт СН3СН2СН(ОН)СН3, изобутиловый спирт (СН3)2СНСН2ОН, триметилкарбинол (СН3)3СОН. Ядовит.
Содержание
Производство
В промышленности бутанол получают оксосинтезом из пропилена с использованием никель-кобальтовых катализаторов при 1,0-1,5 МПа. Из ацетальдегида через ацетальдоль и кротоновый альдегид, который гидрируют на медных, меднохромовых или никелевых катализаторах. Ацетоно-бутиловым брожением пищевого сырья.
Бутанол начал производиться в 10-х годах XX века с использованием бактерии Clostridia acetobutylicum. Сырьём для производства могут быть сахарный тростник, свекла, кукуруза, пшеница, маниока, а в будущем и целлюлоза.
В 50-х годах из-за падения цен на нефть начал производиться из нефтепродуктов.
В США ежегодно производится около 1,39 млрд литров бутанола.
Применение
Бутанол применяют как растворитель в лакокрасочной промышленности, в производстве смол и пластификаторов, в синтезе многих органических соединений.
Применение в качестве автомобильного топлива
Может, но не обязательно должен, смешиваться с традиционными топливами. Энергия бутанола близка к энергии бензина. Бутанол может использоваться в топливных элементах, как сырьё для производства водорода.
В 2007 году в Великобритании начнутся продажи биобутанола в качестве добавки к бензину.
Ссылки
Этанол · Пропанол · Бутиловый спирт/Изобутанол · Пентанол · Гексанол · Гептанол
Жирные спирты: Октанол (C8) · Нонанол (C9) · Деканол (C10) · Ундеканол (C11) · Додеканол (C12) · Тетрадеканол (C14) · Цетиловый спирт (C16)
Полезное
Смотреть что такое «Бутанол» в других словарях:
бутанол — сущ., кол во синонимов: 1 • растворитель (67) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
бутанол — бутан ол, а … Русский орфографический словарь
бутанол — іменник чоловічого роду … Орфографічний словник української мови
бутанол — бутиловый спирт … Cловарь химических синонимов I
Butanol — Бутанол … Краткий толковый словарь по полиграфии
бутиловый спирт — бутанол … Cловарь химических синонимов I
Многокомпонентные растворители — растворители, в состав которых входят два или более компонента, именно такое сочетание веществ обуславливает большие функциональные возможности этого раствора и его потребительские свойства. Растворители Растворитель 645: толуол 50%, бутилацетат… … Википедия
Бутиловый спирт — н бутанол … Википедия
Спирты — Отличительная особенность спиртов гидроксильная группа при насыщенном атоме углерода на рисунке выделена красным (кислород) и серым цветом (водород). Спирты (от лат. … Википедия
Бутиловый спирт
| н-бутанол | |
.jpg) | |
.jpg) | |
| Общие | |
|---|---|
| Систематическое наименование | 1-бутанол |
| Сокращения | BuOH |
| Традиционные названия | бутанол |
| Химическая формула | С4H9OH |
| Эмпирическая формула | С4H10O |
| Рациональная формула | CH3(CH2)3OH |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Молярная масса | 74,12 г/моль |
| Плотность | 0,81 г/см³ |
| Динамическая вязкость (ст. усл.) | 33,79 м Па·с (при 20 °C) |
| Термические свойства | |
| Температура плавления | -90,2 °C |
| Температура кипения | 117,4 °C |
| Температура вспышки | 34 °C |
| Температура самовоспламенения | 345 °C |
| Молярная теплоёмкость (ст. усл.) | 2,359 Дж/(моль·К) |
| Удельная теплота испарения | 591,2 к Дж/кг |
| Химические свойства | |
| pKa | 16 |
| Растворимость в воде | 7,9 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,399 |
| Классификация | |
| Рег. номер CAS | 71-36-3 |
| SMILES | ССССО |
| Безопасность | |
| ЛД50 | 2290–4360 мг/кг |
Бутиловый спирт (н-бутанол) C4H9OH — представитель одноатомных спиртов. Известны нормальный первичный бутиловый спирт СН3(СН2)3ОН и его изомеры: нормальный вторичный бутиловый спирт СН3СН2СН(ОН)СН3, изобутиловый спирт (СН3)2СНСН2ОН, третбутиловый спирт (триметилкарбинол) (СН3)3СОН.
| Бутанол | ||||
| Систематическое название | 1-Бутанол | 2-Метил-1-пропанол | 2-Бутанол | 2-Метил-2-пропанол |
| Тривиальные названия | н-Бутанол | изо-Бутанол | втор-Бутанол | трет-Бутанол |
| Структурная формула |  |  | 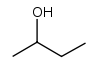 | 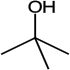 |
| Вторичные спирты (2°) | Изопропиловый спирт · 2-Бутанол · 2-Гексанол |
|---|---|
| Третичные спирты (3°) | 2-Метил-2-бутанол |
Полезное
Смотреть что такое «Бутиловый спирт» в других словарях:
бутиловый спирт — butilo alkoholis statusas T sritis chemija formulė H(CH₂)₄OH atitikmenys: angl. butyl alcohol rus. бутиловый спирт ryšiai: sinonimas – 1 butanolis … Chemijos terminų aiškinamasis žodynas
Бутиловый спирт — см. Бутильные алкоголи. Б. эфир см. Эфиры простые … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
бутиловый спирт — бутанол … Cловарь химических синонимов I
втор-бутиловый спирт — antr butilo alkoholis statusas T sritis chemija formulė CH₃CH(OH)CH₂CH₃ atitikmenys: angl. sec butyl alcohol rus. втор бутиловый спирт ryšiai: sinonimas – 2 butanolis … Chemijos terminų aiškinamasis žodynas
трет-бутиловый спирт — tret butilo alkoholis statusas T sritis chemija formulė (CH₃)₃COH atitikmenys: angl. tert butyl alcohol; trimethylcarbinol rus. трет бутиловый спирт; триметилкарбинол ryšiai: sinonimas – 2 metil 2 propanolis … Chemijos terminų aiškinamasis žodynas
вторичный бутиловый спирт — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN secondary butyl alcohol … Справочник технического переводчика
третичный бутиловый спирт — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN tertiary butyl alkohol … Справочник технического переводчика
спирт — СПИРТ, а ( у), м Спец. Горючая, богатая алкоголем жидкость, получаемая путем перегонки некоторых веществ, содержащих крахмал и сахар (применяется как сырье в производстве красителей, синтетических смол, моющих и лекарственных веществ;… … Толковый словарь русских существительных
Бутиловые спирты
Бути́ловые спирты́ (бутанолы) —это алифатические спирты, с брутто-формулой С4Н9ОН, и молекулярной массой 74,12. Существуют н-бутиловый спирт (1-бутанол, пропилкарбинол) — CH3CH2CH2CH2OH, с температурой кипения 117,4°С и плотностью 0,810 г/куб.см; втор-бутиловый спирт (2-бутанол, метилэтилкарбинол) — C2H5CH(OH)CH3, с температурой кипения 99,5°С, и плотностью 0,806 г/куб.см; изобутиловый спирт (изобутанол, 2-метил-1-пропанол, изопропилкарбинол) — (CH3)2CHCH2OH, с температурой кипения 108, 1 °С и плотностью 0,806 г/куб.см; трет-бутиловый спирт (трет-бутанол, 2-метил-2-пропанол, триметилкарбинол) — (CH3)3COH, с температурой плавления 25,5°С, температурой кипения 82,5°С и плотностью 0,789 (все плотности даны при температуре 20°С). 1-бутанол, 2-бутанол и изобутанол — бесцветные жидкости с характерным спиртовым запахом, трет-бутанол же является твердым веществом (бесцветные ромбические кристаллы).
По химическим свойствам бутанолы — типичные алифатические спирты: они этерифицируются кислотами, при взаимодействии с альдегидами (кетонами) образуют ацетали (кетали), дегидратируются в простые эфиры и олефины, окисляются (кроме трет-бутанола) в карбонильные соединения, а также при взаимодействии с аммиаком образуют моно-, ди- и трибутиламины.
Основные методы получения бутиловых спиртов
В основном промышленным методом получения н-бутанола является оксосинтез из пропилена с использованием никель-кобальтовых катализаторов. Н-бутиловый спирт получают также из ацетальдегида через ацетальдоль и кротоновый альдегид, который гидрируют на медных, меднохромовых или никелевых катализаторах, или ацетоно-бутиловым брожением пищевого сырья.
Изобутиловый спирт содержится в значительном количестве в сивушных маслах, откуда он выделяется фракционной перегонкой. Его получают также оксосинтезом (вместе с н-бутиловым спиртом) и из смеси оксида углерода и водорода по схеме, аналогичной синтезу метанола, но при других параметрах.
Втор-бутиловый спирт получают взаимодействием 70-85% серной кислоты с бутенами, содержащимися во фракциях С4 термического и каталитического крекинга нефтепродуктов, пиролиза жидких углеводородов и одностадийного дегидрирования бутана. Из бутенов предварительно удаляют изобутен и бутадиен. Образующуюся втор-бутилсерную кислоту гидролизуют. Его также можно синтезировать эпоксидированием бутенов органическими гидропероксидами с последующим гидрированием полученного эпоксида в спирт или прямой гидратацией бутенов.
Трет-бутиловый спирт синтезируют взаимодействием 40-65% серной кислоты с изобутеном, содержащимся во фракциях С4, так же, как втор-бутиловый спирт, и прямой гидратацией изобутена в присутствии сульфокатионитов.
Н-бутиловый спирт, изобутиловый спирт и их смеси применяют как растворители в лакокрасочной промышленности, модификаторы мочевино- и меламино-формальдегидных смол, для получения пластификаторов. Кроме того, н-бутанол служит сырьем для синтеза бутилацетата, бутилакрилата и эфиров с гликолями, а изобутанол — для получения изобутилацетата и изобутилксантогената (на основе изобутилксантогената калия получают кристаллические хорошо растворимые присадки к смазочным маслам), пестицидов, душистых веществ, пищевых эссенций, лекарственных средств.
Втор-бутиловый спирт — промежуточный продукт в производстве метилэтилкетона; он также служит сырьем для синтеза втор-бутилацетата; растворителем; алкилирующим и дегидратирующим агентом; высокооктановым компонентом моторных топлив (октановое число 110), обладающим в смеси с метилтрет-бутиловым эфиром синергическим эффектом; стабилизатором смесей бензина с метанолом (так называемых бензометанольных смесей); компонентом тормозных жидкостей.
Трет-бутиловый спирт — промежуточный продукт в производстве изобутена высокой степени чистоты из газов нефтепереработки; алкилирующий агент; сырье для производства трет-бутилгидропероксида, искусственного мускуса; растворитель; антисептик; денатурирующий агент для этанола-сырца.
Назначение установки получения спиртов методом оксосинтеза
Установка предназначена для получения альдегидов или соответствующих спиртов, включающего кроме собственно гидроформилирования также и стадии получения катализатора, выделения его из продуктов реакции, разделения продуктов синтеза и гидрирования альдегидов в соответствующие спирты.
Общие сведения о процессе оксосинтеза
Реакция оксосинтеза была открыта в Германии в 1938 году Роеленом из фирмы «Ruhrchemie». Роелен изучал влияние небольших добавок олефинов на процесс Фишера-Тропша в присутствии гетерогенного кобальтового катализатора. Он обнаружил в реакционной среде примеси альдегидов. Позднее Эдкинс назвал эту реакцию – реакцией гидроформилирвания.
Термином же оксосинтез в научной литературе стали пользоваться для определения технологического процесса получения альдегидов или соответствующих спиртов, включающего кроме собственно гидроформилирования также и стадии получения катализатора, выделения его из продуктов реакции, разделения продуктов синтеза и гидрирования альдегидов в соответствющие спирты.
Таким образом, термином оксосинтез обозначается не конкретная реакция, а сложный технологический комплекс.
В той или иной степени реакцию гидроформилирования катализируют многие металлы: железо, марганец, рутений, кобальт, родий. Классический комплекс – гидрокарбонил кобальта HCo(CO)4.
Основные стадии процесса «оксосинтеза»
Процесс получения масляных альдегидов и бутиловых спиртов осуществляется с использованием кобальтсодержащего катализатора. Кобальт вводится в систему в виде мало летучей термоустойчивой соли 2-этилгексаната кобальта, хорошо растворимой в органическом продукте гидроформилирования.
Весь процесс получения альдегидов и спиртов методом оксосинтеза разделяется на следующие основные стадии:
Стадия карбонилообразования заключается в получении гидрокарбонила кобальта (катализатора реакции гидроформилирования) из его органической соли взаимодействием синтез-газа, состоящего из окиси углерода и водорода, с 2-этилгексанатом кобальта, растворенным в циркулирующем по системе кубовом остатке, по реакции:
и далее идет равновесный переход дикобальтоктакарбонила в гидрокарбонил по реакции:
Свободная 2-этилгексановая кислота, выделившаяся при реакции, остается в кубовом остатке и проходит затем по всей системе до стадии окислительной декобальтизации.
Реакцию карбонилообразования проводят при температуре 140-175°C и давлении 240-305 кгс/см². Реакция протекает с незначительным выделением тепла. Эти условия обеспечивают образование и сохранение карбонилов кобальта. При увеличении температуры скорость реакции возрастает, а при температуре выше 180°С начинается термическое разложение образующихся карбонилов кобальта.
Стадия гидроформилирования заключается в получении масляных альдегидов взаимодействием пропилена с синтез-газом, состоящим из окиси углерода и водорода, в присутствии гидрокарбонила кобальта по реакции:
Реакцию гидроформилирования проводят при температуре 125-145°C и давлении 230-305 кгс/см². Реакция идет с выделением тепла, равным 30 ккал/моль пропилена.
Стадия гидроформилирования осуществляется в двух последовательно соединенных вертикальных реакторах. Съем тепла реакции производится с помощью встроенных теплоснимающих элементов (трубок Фильда) путем циркуляции через них водяного конденсата. По способу съема тепла реакторы гидроформилирования делятся на: реакторы с внутренним теплосъемом, реакторы с внешним теплосъемом, реакторы комбинированного типа. В реакторах с внутренним теплосъемом тепло реакции поглощается за счет подачи холодного сырья или продукта гидроформилирования прямо в зону реакции. Все компоненты подадаются в реактор снизу съема тепла осуществляется позонным впрыскиванием охлажденных продуктов гидроформилирования. В таких аппаратах предусматривается также циркуляция газового потока, что улучшает теплообмен между реакционной смесью и впрыскиваемым холодным продуктом. Достоинством таких аппаратов является простота конструкции, недостатоком – повышенный выход побочных продуктов. В Германии и России используются реакторы колонного типа со встроенными теплоснимающими элементами типа трубок Фильда. В качестве охлаждающей жидкости используется деминерализованная вода. Комбинированный реактор состоит из двух зон : одна зона работает как аппарат идеального перемешивания, а вторая как аппарат идеального вытеснения. В зоне идеального смешения осуществляется «первая часть реакции» гидроформилирования. В этой зоне процесс ведется до степени превращения олефина 50-70%. Затем реакционная смесь поступает в зону идеального вытеснения. Здесь реакция осуществляется наиболее рационально, с минимальным выходом побочных продуктов. Реакционный узел комбинированного типа может представлять собой как два отдельных, последовательно соединенных реактора, так и один секционный аппарат.
Ниже представлены схемы реакторов с внутренним теплосъемом и комбинированного типа.
Скорость реакции гидроформилирования пропорциональна концентрации пропилена и катализатора (гидрокарбонила кобальта), увеличивается с повышением давления водорода и снижается с повышением давления окиси углерода. Поскольку давление в процессе гидроформилирования поддерживается примерно на одном уровне, взаимное влияние на процесс давлений водорода и окиси углерода будет осуществляться через изменение их концентраций в синтез-газе, а точнее, через изменение их соотношения. Скорость реакции гидроформилирования растет также с повышением температуры проведения процесса.
Конечной целью проведения стадии гидроформилирования является более полная конверсия поступившего пропилена с минимальным выходом побочных продуктов и с максимальным выходом конечных основных продуктов (нормального и изомасляного альдегидов), при максимальном соотношении их в сторону нормального масляного альдегида, и при исключении как перерасхода синтез-газа, так и потерь кобальта.
Исходные компоненты реакции гидроформилирования подаются как в жидком виде (кубовый остаток, пропилен), так и в газообразном виде (синтез-газ), поэтому распределение пропилена между газовой и жидкой фазами в значительной степени влияет на скорость и степень превращения пропилена в целевые продукты. Скорость реакции в газовой фазе примерно на два порядка ниже, чем в жидкой, а при снижении скорости реакции требуется большее время контакта для обеспечения требуемой конверсии.
Степень превращения пропилена, особенно близкая к 100%, значительным образом влияет на соотношение выхода основных и побочных продуктов. Поэтому очень важно держать ее в оптимальном интервале 92-95%. Степень превращения определяется по содержанию пропилена в сбросном газе. Снижение содержания пропилена в сдувке ниже 5% об. приводит к значительному увеличению выхода побочных продуктов. Повышение содержания пропилена в сдувке говорит о снижении конверсии, и при содержании более 10% об. приводит к его потере.
Подача кубового остатка в качестве растворителя 2-этилгексаната кобальта влияет на суммарную скорость процесса гидроформилирования как своим составом, так и изменением фазового распределения в системе (увеличивает объем жидкой фазы и соответственно пропилена в ней).
Увеличение расхода подаваемого кубового остатка увеличивает степень конверсии пропилена через увеличение концентрации кобальта в системе и через увеличение объема жидкой фазы. Увеличивается при этом и выход побочных продуктов. Поддерживая расход кубового остатка в оптимальном интервале (1,4-3,0 м3/ч), в зависимости от нагрузки по пропилену, требуемую концентрацию кобальта в системе (0,07-0,15% масс. в пересчете на металлический) поддерживают путем изменения расхода подпитки свежего раствора 2-этилгексаната кобальта в подаваемый кубовый остаток.
Процесс приготовление раствора солей кобальта
С целью поддержания требуемой концентрации кобальта осуществляют процесс приготовления раствора солей кобальта высших органических кислот, который состоит из двух стадий.
На первой стадии производится экстракция кобальта из кубового остатка, выводимого из процесса оксосинтеза, водным раствором уксусной кислоты. Кобальт в кубовом остатке находится в виде солей высших органических кислот С8 (2-этилгексановой и 2-этилгексеновой) и бутиратов.
В процессе регенерации кобальта из кубового остатка водным раствором уксусной кислоты соли кобальта кислот С8 и С4 в результате обменной реакции превращаются в ацетат кобальта, переходящий в водную фазу, с выделением высших органических кислот и масляной кислоты, которые выводятся с органической фазой, содержащей кубовый остаток.
Водный раствор ацетата кобальта используется для приготовления солей кобальта высших органических кислот.
С целью восполнения потерь кобальта в процессе гидроформилирования и ректификации масляных альдегидов используют сухой ацетат кобальта или карбонат кобальта.
На второй стадии осуществляется получение раствора солей кобальта высших органических кислот взаимодействием раствора ацетата кобальта с 2-этилгексановой кислотой.
Реакция протекает при температуре 180-200°C, давлении до 1,3 кгс/см² в присутствии кубового остатка.
Уксусная кислота при этих условиях отгоняется и равновесие реакции смещается вправо. Кубовый остаток служит в качестве растворителя образовавшихся солей кобальта высших органических кислот. Отогнанный раствор уксусной кислоты вновь используется для экстракции кобальта из кубового остатка.
Важной характеристикой процесса гидроформилирования является соотношение выхода нормального и изомасляного альдегидов.
С повышением температуры увеличивается доля изомасляного альдегида. Увеличение давления в системе в условиях процесса (240-305 кгс/см²) повышает долю нормального масляного альдегида, вследствие увеличения парциального давления как окиси углерода, так и водорода, содержащихся в синтез-газе.
Как исходное сырье, так и синтез-газ содержат различные примеси, влияющие на реакцию гидроформилирования. Основными примесями, которые может принести в процесс пропилен, являются: диеновые, ацетиленовые, сернистые и перекисные соединения. Поэтому содержание их в пропилене постоянно контролируется и строго регламентируется.
На стадии гидроформилирования может использоваться, как чистый пропилен, так и пропан-пропиленовая фракция (ППФ), с содержанием пропилена в ней не менее 90% масс. Пропан, содержащийся в этом сырье в количестве 3-10% масс., является инертным разбавителем и занимает определенную часть реакционного объема и оказывает влияние на межфазное распределение пропилена в процессе, а, следовательно, и на скорость основной реакции, и на степень конверсии.

Образующаяся малолетучая, термически устойчивая соль кобальта (2-этилгексанат кобальта), хорошо растворимая в продукте гидроформилирования (сырых альдегидах), при последующей ректификации продукта остается в кубовом остатке и возвращается на стадию гидроформилирования, карбонилообразования, где вновь переводится в карбонилы кобальта.
Заниженная подача воздуха в реактор по отношению к расходу продуктов гидроформилирования, также поступающих в реактор, приводит к неполному переводу карбонилов кобальта в 2-этилгексанат кобальта. В результате чего в дальнейшем происходит термическое разложение карбонилов кобальта в процессе ректификации, выпадение металлического кобальта, забивка трубопроводов и аппаратов.
Завышенная подача воздуха в реактор приводит к повышенному окислению альдегидов, содержащихся в продукте гидроформилирования, до масляной кислоты и образованию солей кобальта масляной кислоты (бутиратов кобальта) по реакции:
Количество органической кислоты, подаваемой на окислительную декобальтизацию, устанавливается ориентировочно 5 литров кислоты на 1 м3 пропилена, поступающего на стадию гидроформилирования.
Зависимость необходимого расхода кислоты, подаваемой в реактор, от расхода пропилена (ППФ), поступающего на гидроформилирование представлена в таблице.












