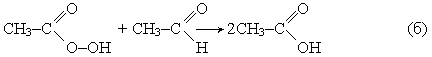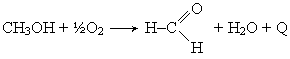неверно что под неполным окислением углеводородов подразумевают
Неверно что под неполным окислением углеводородов подразумевают
5. Процессы окисления
Неполное окисление углеводородов получило значительное распространение в современном промышленном органическом синтезе. При этом получают спирты, фенолы, альдегиды, кетоны, органические кислоты, ангидриды и эпоксисоединения.
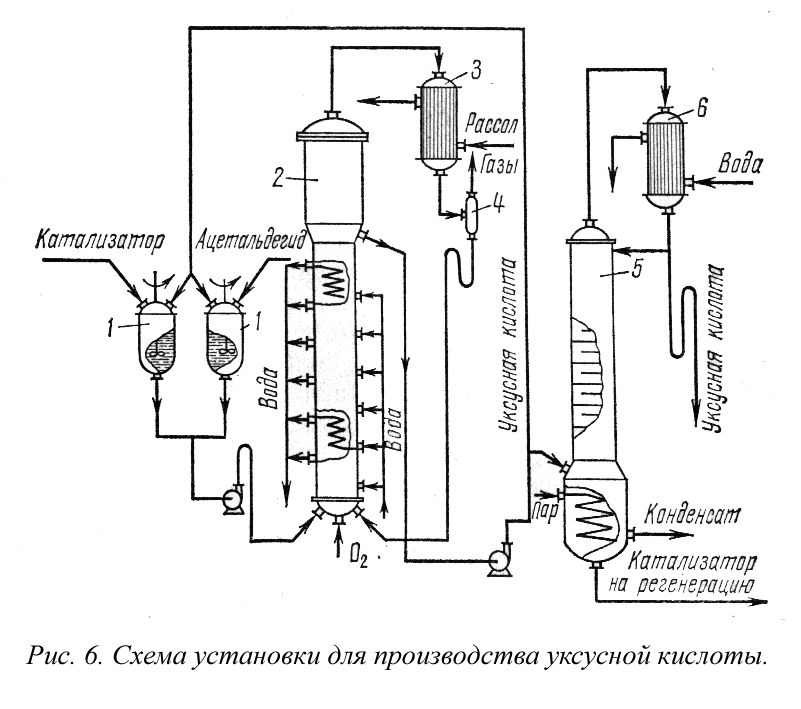
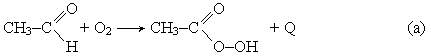
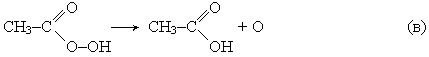
Производство уксусной кислоты. Получение уксусной кислоты окислением ацетальдегида протекает в две стадии. Сначала при окислении ацетальдегида образуется нестойкая надуксусная кислота:
которая далее вновь взаимодействует с а цетальдегидом с образованием уксусной кислоты:
Возможна побочная реакция разложения надуксусной кислоты, сопровождающаяся выделением атомарного кислорода и значительного количества тепла:
Помимо этого способа уксусную кислоту получают при сухой перегонке древесины и в процессе биохимического окисления этилового спирта под влиянием бактерий (уксусного грибка).
Уксусная кислота и ее производные широко применяются в различных отраслях промышленности и народного хозяйства. Значительное количество уксусной кислоты перерабатывается в уксусный ангидрид. В качестве ацетилирующего средства уксусная кислота используется для производства ацетилцеллюлозы, при получении полупродуктов в тонком органическом синтезе. Уксусная кислота применяется в пищевой, текстильной промышленностях. Соли уксусной кислоты применяются при крашении и печатании тканей, в промышленности тонкого органического синтеза и др. Сложные эфиры уксусной кислоты применяются в качестве растворителей, душистых веществ, фруктовых эссенций.
Производство формальдегида. Получение формальдегида окислением метанола широко распространено в промышленности. Этот технологический процесс изучен и разработан советским ученым Е. И. Орловым.
Пары метилового спирта окисляются кислородом воздуха при температурах 500-700° С в присутствии катализатора серебра, нанесенного на пемзу:
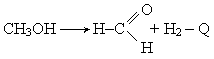
При подаче воздуха в количестве, несколько меньшем стехио-метрического, частично прогекает эндотермическая реакция дегидрирования метилового спирта:
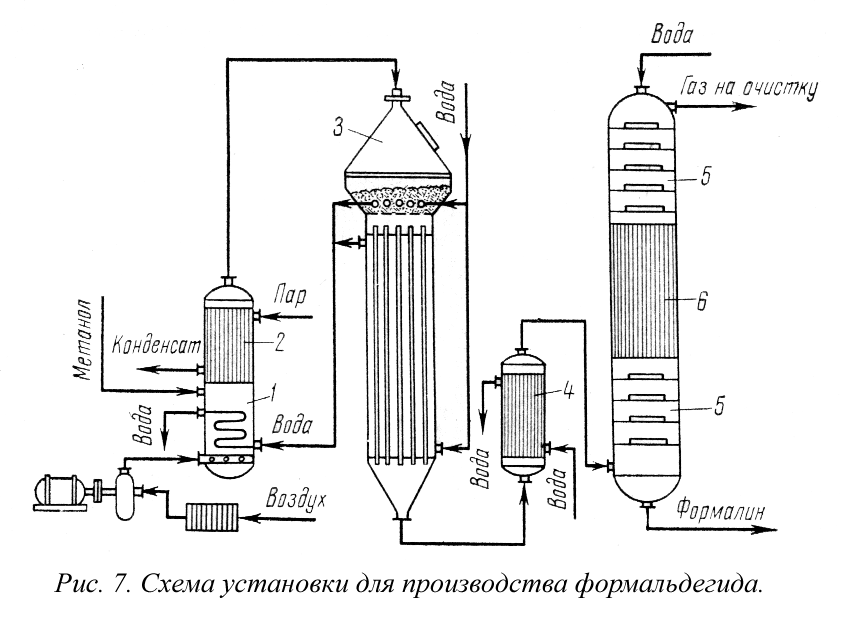
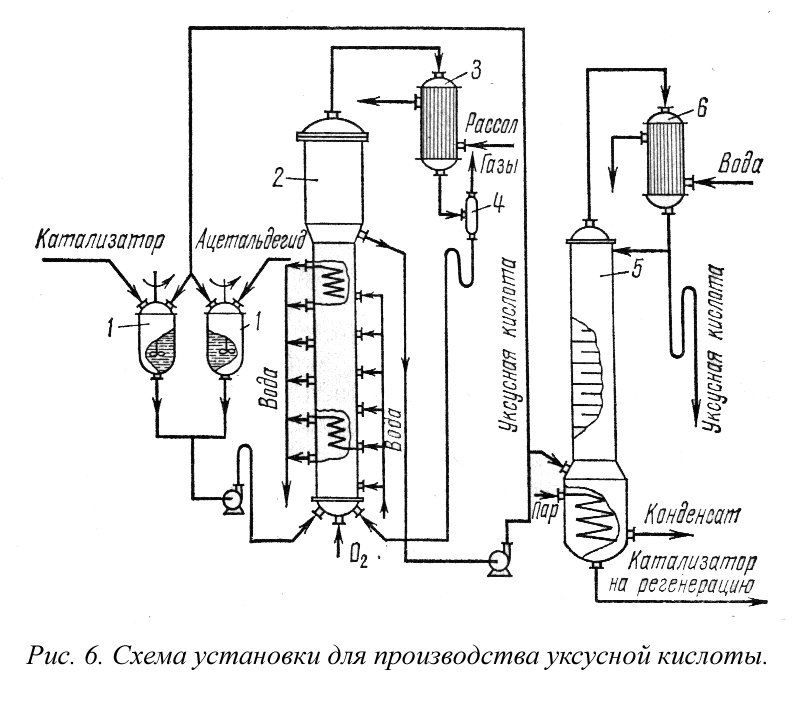
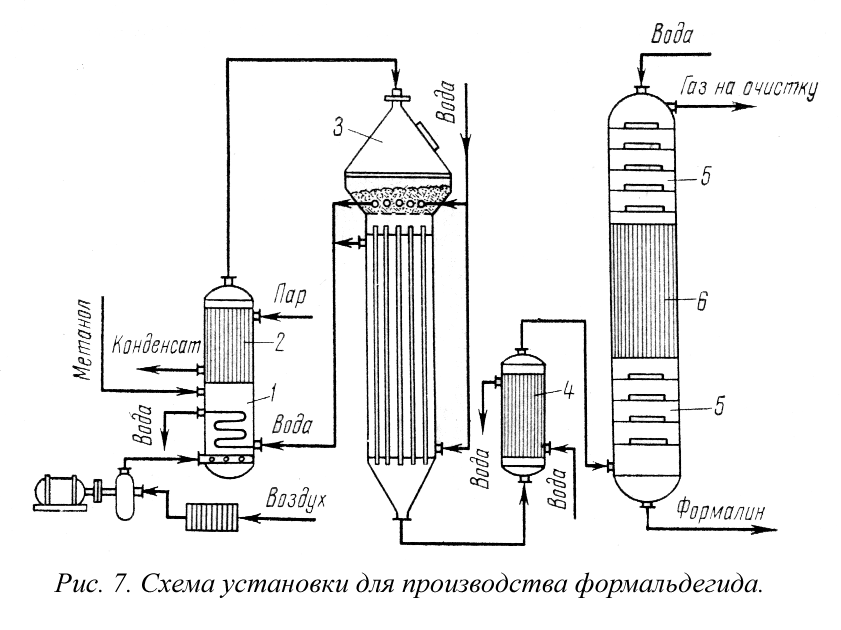
На рис. 7 представлена технологическая схема производства формальдегида окислением метилового спирта. Метанол испаряется в спиртоиспарителе 1 при нагревании горячей водой до 45-55° С. Через барботер в спиртоиспаритель вводится воздух и таким образом приготовляется спиртовоздушная смесь с содержанием 0,5 г. СН 3 ОН на 1 л спиртовоздушной смеси.
Во избежание конденсации паров спирта из спиртовоздушной смеси предусмотрен спиртоперегреватель 2, в котором смесь нагревается до 110° С. Нагретая спиртовоздушная смесь поступает в контактный аппарат 3, где в слое серебряного катализатора при 650-700° С образуется формальдегид. При установившемся процессе окисление протекает автотермично. Температурный режим в слое катализатора регулируют изменением количества и температуры спир-товоздушной смеси, подаваемой в аппарат, и воды, поступающей в трубки, находящиеся в слое.
Окисление олефинов большей частью в промышленной практике проводят для получения окисей олефинов (эпоксидов).
Неверно что под неполным окислением углеводородов подразумевают
5. Процессы окисления
Неполное окисление углеводородов получило значительное распространение в современном промышленном органическом синтезе. При этом получают спирты, фенолы, альдегиды, кетоны, органические кислоты, ангидриды и эпоксисоединения.
Производство уксусной кислоты. Получение уксусной кислоты окислением ацетальдегида протекает в две стадии. Сначала при окислении ацетальдегида образуется нестойкая надуксусная кислота:
которая далее вновь взаимодействует с а цетальдегидом с образованием уксусной кислоты:
Возможна побочная реакция разложения надуксусной кислоты, сопровождающаяся выделением атомарного кислорода и значительного количества тепла:
Помимо этого способа уксусную кислоту получают при сухой перегонке древесины и в процессе биохимического окисления этилового спирта под влиянием бактерий (уксусного грибка).
Уксусная кислота и ее производные широко применяются в различных отраслях промышленности и народного хозяйства. Значительное количество уксусной кислоты перерабатывается в уксусный ангидрид. В качестве ацетилирующего средства уксусная кислота используется для производства ацетилцеллюлозы, при получении полупродуктов в тонком органическом синтезе. Уксусная кислота применяется в пищевой, текстильной промышленностях. Соли уксусной кислоты применяются при крашении и печатании тканей, в промышленности тонкого органического синтеза и др. Сложные эфиры уксусной кислоты применяются в качестве растворителей, душистых веществ, фруктовых эссенций.
Производство формальдегида. Получение формальдегида окислением метанола широко распространено в промышленности. Этот технологический процесс изучен и разработан советским ученым Е. И. Орловым.
Пары метилового спирта окисляются кислородом воздуха при температурах 500-700° С в присутствии катализатора серебра, нанесенного на пемзу:
При подаче воздуха в количестве, несколько меньшем стехио-метрического, частично прогекает эндотермическая реакция дегидрирования метилового спирта:
На рис. 7 представлена технологическая схема производства формальдегида окислением метилового спирта. Метанол испаряется в спиртоиспарителе 1 при нагревании горячей водой до 45-55° С. Через барботер в спиртоиспаритель вводится воздух и таким образом приготовляется спиртовоздушная смесь с содержанием 0,5 г. СН 3 ОН на 1 л спиртовоздушной смеси.
Во избежание конденсации паров спирта из спиртовоздушной смеси предусмотрен спиртоперегреватель 2, в котором смесь нагревается до 110° С. Нагретая спиртовоздушная смесь поступает в контактный аппарат 3, где в слое серебряного катализатора при 650-700° С образуется формальдегид. При установившемся процессе окисление протекает автотермично. Температурный режим в слое катализатора регулируют изменением количества и температуры спир-товоздушной смеси, подаваемой в аппарат, и воды, поступающей в трубки, находящиеся в слое.
Окисление олефинов большей частью в промышленной практике проводят для получения окисей олефинов (эпоксидов).
3.4. Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола).
Химические свойства алканов
Алканами (парафинами) называют нециклические углеводороды, в молекулах которых все атомы углерода соединены только одинарными связями. Другими словами в молекулах алканов отсутствуют кратные — двойные или тройные связи. Фактически алканы являются углеводородами, содержащими максимально возможное количество атомов водорода, в связи с чем их называют предельным (насыщенными).
Ввиду насыщенности, алканы не могут вступать в реакции присоединения.
Поскольку атомы углерода и водорода имеют довольно близкие электроотрицательности, это приводит к тому, что связи С-Н в их молекулах крайне малополярны. В связи с этим для алканов более характерны реакции протекающие по механизму радикального замещения, обозначаемого символом SR.
1. Реакции замещения
В реакциях данного типа происходит разрыв связей углерод-водород
Галогенирование
Алканы реагируют с галогенами (хлором и бромом) под действием ультрафиолетового света или при сильном нагревании. При этом образуется смесь галогенпроизводных с различной степенью замещения атомов водорода — моно-, ди- три- и т.д. галогенозамещенных алканов.
На примере метана это выглядит следующим образом:
Меняя соотношение галоген/метан в реакционной смеси можно добиться того, что в составе продуктов будет преобладать какое-либо конкретное галогенпроизводное метана.
Механизм реакции
Разберем механизм реакции свободнорадикального замещения на примере взаимодействия метана и хлора. Он состоит из трех стадий:
Свободными радикалами, как можно видеть из рисунка выше, называют атомы или группы атомов с одним или несколькими неспаренными электронами (Сl•, •Н, •СН3,•СН2• и т.д.);
Эта стадия заключается во взаимодействии активных свободных радикалов с неактивными молекулами. При этом образуются новые радикалы. В частности, при действии радикалов хлора на молекулы алкана, образуется алкильный радикал и хлороводород. В свою очередь, алкильный радикал, сталкиваясь с молекулами хлора, образует хлорпроизводное и новый радикал хлора:
3) Обрыв (гибель) цепи:
Происходит в результате рекомбинации двух радикалов друг с другом в неактивные молекулы:
2. Реакции окисления
В обычных условиях алканы инертны по отношению к таким сильным окислителям, как концентрированная серная и азотная кислоты, перманганат и дихромат калия (КMnО4, К2Cr2О7).
Горение в кислороде
А) полное сгорание при избытке кислорода. Приводит к образованию углекислого газа и воды:
Б) неполное сгорание при недостатке кислорода:
Каталитическое окисление кислородом
В результате нагревания алканов с кислородом (
200 о С) в присутствии катализаторов, из них может быть получено большое разнообразие органических продуктов: альдегиды, кетоны, спирты, карбоновые кислоты.
3. Термические превращения алканов
Крекинг
Крекинг (от англ. to crack — рвать) — это химический процесс протекающий при высокой температуре, в результате которого происходит разрыв углеродного скелета молекул алканов с образованием молекул алкенов и алканов с обладающих меньшими молекулярными массами по сравнению с исходными алканами. Например:
Крекинг бывает термический и каталитический. Для осуществления каталитического крекинга, благодаря использованию катализаторов, используют заметно меньшие температуры по сравнению с термическим крекингом.
Дегидрирование
Отщепление водорода происходит в результате разрыва связей С—Н; осуществляется в присутствии катализаторов при повышенных температурах. При дегидрировании метана образуется ацетилен:
Нагревание метана до 1200 °С приводит к его разложению на простые вещества:
При дегидрировании остальных алканов образуются алкены:
При дегидрировании н-бутана образуются бутен-1 и бутен-2 (последний в виде цис- и транс-изомеров):
Дегидроциклизация
Изомеризация
Химические свойства циклоалканов
Химические свойства циклоалканов с числом атомов углерода в циклах больше четырех, в целом практически идентичны свойствам алканов. Для циклопропана и циклобутана, как ни странно, характерны реакции присоединения. Это обусловлено большим напряжением внутри цикла, которое приводит к тому, что данные циклы стремятся разорваться. Так циклопропан и циклобутан легко присоединяют бром, водород или хлороводород:
Химические свойства алкенов
1. Реакции присоединения
Поскольку двойная связь в молекулах алкенов состоит из одной прочной сигма- и одной слабой пи-связи, они являются довольно активными соединениями, которые легко вступаю в реакции присоединения. В такие реакции алкены часто вступают даже в мягких условиях — на холоду, в водных растворах и органических растворителях.
Гидрирование алкенов
Алкены способны присоединять водород в присутствии катализаторов (платина, палладий, никель):
Гидрирование алкенов легко протекает даже при обычном давлении и незначительном нагревании. Интересен тот факт, что для дегидрирования алканов до алкенов могут использоваться те же катализаторы, только процесс дегидрирования протекает при более высокой температуре и меньшем давлении.
Галогенирование
Алкены легко вступаю в реакцию присоединения с бромом как в водном растворе, так и с органических растворителях. В результате взаимодействия изначально желтые растворы брома теряют свою окраску, т.е. обесцвечиваются.
Гидрогалогенирование
Как нетрудно заметить, присоединение галогеноводорода к молекуле несимметричного алкена должно, теоретически, приводить к смеси двух изомеров. Например, при присоединении бромоводорода к пропену должны были бы получаться продукты:
Тем не менее в отсутствие специфических условий (например, наличие пероксидов в реакционной смеси) присоединение молекулы галогеноводорода будет происходить строго селективно в соответствии с правилом Марковникова:
Присоединении галогеноводорода к алкену происходит таким образом, что водород присоединяется к атому углерода с большим числом атомов водорода (более гидрированному), а галоген — к атому углерода с меньшим числом атомов водорода (менее гидрированному).
Гидратация
Данная реакция приводит к образованию спиртов, и также протекает в соответствии с правилом Марковникова:
Как легко догадаться, по причине того, что присоединение воды к молекуле алкена происходит согласно правилу Марковникова, образование первичного спирта возможно только в случае гидратации этилена:
Именно по такой реакции проводят основное количество этилового спирта в крупнотоннажной промышленности.
Полимеризация
Специфическим случаем реакции присоединения можно реакцию полимеризации, которая в отличие от галогенирования, гидрогалогенирования и гадратации, протекает про свободно-радикальному механизму:
Реакции окисления
Как и все остальные углеводороды, алкены легко сгорают в кислороде с образованием углекислого газа и воды. Уравнение горения алкенов в избытке кислорода имеет вид:
В отличие от алканов алкены легко окисляются. При действии на алкены водного раствора KMnO4 обесцвечивание, что является качественной реакцией на двойные и тройные CC связи в молекулах органических веществ.
Окисление алкенов перманганатом калия в нейтральном или слабощелочном растворе приводит к образованию диолов (двухатомных спиртов):
В кислой среде происходит полное разрыв двойной связи с превращение атомов углерода образовывавших двойная связь в карбоксильные группы:
В случае, если двойная С=С связь находится в конце молекулы алкена, то в качестве продукта окисления крайнего углеродного атома при двойной связи образуется углекислый газ. Связано это с тем, что промежуточный продукт окисления – муравьиная кислота легко сама окисляется в избытке окислителя:
При окислении алкенов, в которых атом C при двойной связи содержит два углеводородных заместителя, образуется кетон. Например, при окислении 2-метилбутена-2 образуется ацетон и уксусная кислота.
Окисление алкенов, при котором происходит разрыв углеродного скелета по двойной связи используется для установления их структуры.
Химические свойства алкадиенов
Реакции присоединения
Например, присоединение галогенов:
Бромная вода обесцвечивается.
В обычных условиях присоединение атомов галогена происходит по концам молекулы бутадиена-1,3, при этом π-связи разрываются, к крайним атомам углерода присоединяются атомы брома, а свободные валентности образуют новую π-связь. Таким образом, как бы происходит «перемещение» двойной связи. При избытке брома может быть присоединена еще одна его молекула по месту образовавшейся двойной связи.
Реакции полимеризации
Химические свойства алкинов
Алкины являются ненасыщенными (непредельными) углеводородами в связи с чем способны вступать в реакции присоединения. Среди реакци присоединения для алкинов наиболее распространено электрофильное присоединение.
Галогенирование
Поскольку тройная связь молекул алкинов состоит из одной более прочной сигма-связи и двух менее прочных пи-связей они способны присоединять как одну, так и две молекулы галогена. Присоединение одной молекулой алкина двух молекул галогена протекает по электрофильному механизму последовательно в две стадии:
Гидрогалогенирование
Присоединение молекул галогеноводорода, также протекает по электрофильному механизму и в две стадии. В обоих стадиях присоединение идет в соответствии с правилом Марковникова:
Гидратация
Присоединение воды к алкинами происходит в присутсвии солей рути в кислой среде и называется реакцией Кучерова.
В результате гидратации присоединения воды к ацетилену ообразуется ацетальдегид (укусный альдегид):
Для гомологов ацетилена присоединение воды приводит к образованию кетонов:
Гидрирование алкинов
Алкины реагируют с водородом в две ступени. В качестве катализаторов используют такие металлы как платина, палладий, никель:
Тримеризация алкинов
При пропускании ацетилена над активированным углем при высокой температуре из него образуется смесь различных продуктов, основным из которых является бензол – продукт тримеризации ацетилена:
Димеризация алкинов
Также ацетилен вступать в реакцию димеризации. Процесс протекает в присутствии солей меди как катализаторов:
Окисление алкинов
Алкины сгорают в кислороде:
Взаимодействие алкинов с основаниями
Алкины с тройной C≡C на конце молекулы, в отличие от остальных алкинов, способны вступать в реакции, в которых атом водорода при тройной связи замещается металл. Например, ацетилен реагирует с амидом натрия в жидком аммиаке:
а также с аммиачным раствором оксида серебра, образуя нерастворимые солеподобные вещества называемые ацетиленидами:
Благодаря такой реакции можно распознать алкины с концевой тройной связью, а также выделить такой алкин из смеси с другими алкинами.
Следует отметить, что все ацетилениды серебра и меди являются взрывоопасными веществами.
Ацетилениды способны реагировать с галогенпроизводными, что используется при синтезе более сложных органических соединений с тройной связью:
Химические свойства ароматических углеводородов
Ароматический характер связи влияет на химические свойства бензолов и других ароматических углеводородов.
Единая 6пи–электронная система намного более устойчива, чем обычные пи-связи. Поэтому для ароматических углеводородов более характерны реакции замещения, а не присоединения. В реакции замещения арены вступают по электрофильному механизму.
Реакции замещения
Галогенирование
Нитрование
Лучше всего реакция нитрования протекает под действием не чистой азотной кислоты, а ее смеси с концентрированной серной кислотой, так называемой нитрующей смеси:
Алкилирование
Реакция при которой один из атомов водорода при ароматическом ядре замещается на углеводородный радикал:
Также вместо галогенпроизводных алканов можно использовать алкены. В качестве катализаторов можно использовать галогениды алюминия, трехвалентного железа или неорганические кислоты.
Способ неполного каталитического окисления углеводородов
Изобретение предназначено для неполного каталитического окисления углеводородов. Способ заключается в том, что сырье, содержащее углеводородное сырье и кислородсодержащий газ, подвергают контактированию с катализатором при повышенной температуре в реакторе. Причем катализатор имеет форму пористой монолитной структуры и включает каталитически активный металл, нанесенный на носитель на основе двуокиси циркония. В процессе пуска или остановки реактора катализатор подвергают тепловому удару по меньшей мере 50 o С в секунду в температурном интервале по меньшей мере 500 o С. Изобретение обеспечивает высокий уровень селективности по окиси углерода и водорода, высокий уровень каталитической стабильности и устойчивости к тепловому удару. 15 з.п. ф-лы, 1 табл.
Настоящее изобретение относится к способу неполного каталитического окисления углеводородов, в частности к способу получения смеси окиси углерода и водорода из метана, природного газа, попутного газа или других источников легких углеводородов.
Имеется ряд сообщений об академических экспериментах, проведенных с неподвижными слоями частиц катализатора.
Так, в статье A.Т. Ashcroft et al. («Selective oxidation of methane to synthesis gas using transition metal catalysts», Nature, v. 344, N 6264, с. 319-321, 22 марта 1990) раскрыто неполное окисление метана до синтез-газа в присутствии ряда катализаторов, содержащих рутений. Целью экспериментов было установить возможность проведения процесса неполного окисления в мягких условиях и при низких температурах. С этой целью эксперименты проводились при малой объемной скорости газа 40000/ч, давлении 1 атм и температуре примерно 775 o C. Используемый катализатор содержал малое количество твердых порошкообразных частиц катализатора.
В статье P.D.F. Vernon et al. («Partial Oxidation of methane to Synthesis Gas», Catalysis Letters 6 (1990) 181-186) описан ряд экспериментов, в которых использовались катализаторы, содержащие никель, рутений, родий, палладий, иридий или платину, либо нанесенными на окись алюминия, либо присутствующие в виде смеси оксидных предшественников. Описанные эксперименты ограничивались процессом неполного каталитического окисления только в мягких условиях и с использованием малых количеств катализатора в форме гранул с неподвижным слоем. Те же эксперименты авторы опубликовали в работе «Partial Oxidation of Methane to Synthesis Gas, and Carbon Dioxide as an Oxidising Agent for Methane Conversion», Catalysis Today, 13 (1992) 417-426.
В статье R.H. Jones et al. («Catalytic Conversion of Methane to Synthesis Gas over Europium Iridate, Eu2Ir2O7«, Catalysis Letters 8 (1991) 169-174) сообщается о селективном неполном окислении метана с использованием европиум-иридиевого пирохлора Eu2Ir2O7. Реакция исследовалась в мягких условиях при давлении 1 атм и температуре 873 К (600 o C). Катализатор получали путем измельчения с последующим прессованием в таблетки. Таблетированный катализатор помещался в пористую фритту (спекшаяся масса) на основе двуокиси кремния и непосредственно использовался в экспериментах.
Патент США N 5149464 (US-A-5149464) описывает способ селективного окисления метана до моноокиси углерода и водорода путем контактирования газовой смеси реагентов при температуре приблизительно от 650 до 900 o C с твердым катализатором, который обычно может быть описан или как а) катализатор формулы MxM’yOz, где М является по меньшей мере одним из следующих элементов: Mg, B, Al, Ln, Ga, Si, Ti, Zr и Hf; Ln является по меньшей мере лантаном или одним из элементов подгруппы лантанидов; М’ представляет собой d-переходный металл, а каждое из отношений х/у, y/z и (x+y)/z независимо друг от друга принимают значения от 0.1 до 8; или b) окись d-блок-переходного металла; или с) d-блок-переходный металл на тугоплавкой подложке; или d) катализатор, образованный нагревом a) или b) в условиях реакции или в условиях, предотвращающих окисление.
В заявке США N US-A-5149464 указано, что d-блок-переходные металлы следует выбирать из тех, которые имеют атомный номер 21-29, 40-47 и 72-79, то есть металлы скандий, титан, ванадий, хром, марганец, железо, кобальт, никель, медь, цирконий, ниобий, молибден, технеций, рутений, родий, палладий, серебро, гафний, тантал, вольфрам, рений, осмий, иридий, платина и золото. В заявке США US-A-5149464 заявлено, что предпочтительными металлами являются элементы группы VIII Периодической системы элементов, такие как железо, осмий, кобальт, рений, иридий, палладий, платина, никель и рутений.
Способ, описанный в US-A-5149464, осуществляют при температурах в интервале от 650 до 900 o C с предпочтительным интервалом от 700 до 800 o C. В US-A-5149464 описан ряд экспериментов, в которых испытаны различные катализаторы, содержащие металлы группы VIII, включая окись рутения, окиси празеодима/рутения, пирохлоры, рутений на окиси алюминия, родий на окиси алюминия, палладий на окиси алюминия, платину на окиси алюминия, окись никель/алюминий, перовскиты и окись никеля.
Аналогичное общее описание катализаторов для применения в процессах неполного каталитического окисления содержится в международной заявке WO 92/11199. В WO 92/11199, в частности, описаны эксперименты, в которых использовались катализаторы, содержащие иридий, палладий, рутений, родий, никель и платину на подложке из окиси алюминия. Все эксперименты проводились в мягких условиях, причем типичными условиями были давление 1 атм, температура 1050 К (777 o C) и объемной скорости газа примерно 20000/ч.
В экспериментах, описанных как в US-A-5149464, так и в WO 92/11199, использовали катализатор в виде твердых измельченных частиц, удерживаемых в неподвижном слое путем заполнения в реакционную трубку между двумя заглушками из силикатной ваты.
В европейской заявке на патент 0303438 (EP-A-0303438) раскрыт способ неполного каталитического окисления углеводородного сырья, в котором газовая смесь углеводородного сырья, кислорода или кислородсодержащего газа, и необязательно пара вводится в зону неполного каталитического окисления для приведения в контакт с удерживаемым там катализатором. Катализатор, используемый в способе, может включать широкий спектр каталитически активных компонентов, например палладий, платину, родий, иридий, осмий, рутений, никель, хром, кобальт, церий, лантан и их смеси. Далее, в EP-A-0303438 утверждается, что материалы, которые обычно не считаются каталитически активными, также могут использоваться в качестве катализаторов, например тугоплавкие оксиды, такие как кордиоэрит, муллит, титанат алюмосиликата, циркониевая шпинель и окись алюминия. Катализатор может иметь различную форму, например форму листов рифленого металла, уложенных так, чтобы образовывать удлиненные каналы в укладке, или проволочной сетки. Однако в EP-A-0303438 предпочтение отдано катализаторам в форме экструдированных сотовых монолитов. Эти монолиты включают большое количество параллельных каналов, распространяющихся сквозь структуру в направлении потока сырья и получаемых газов.
Европейский патент 0262947 (EP-B-0262947) раскрывает способ образования водорода за счет частичного окисления углеводорода, в котором смесь углеводорода и кислорода вводится в массу катализатора. Катализатор, раскрытый в EP-B-0262947, включает платину и оксид хрома на твердой тугоплавкой подложке. Структура подложки, описанная в EP-B-0262947, представляет собой монолитные сотовые подложки того типа, который используется при очистке загрязнений от автомобилей или химических установок, предпочтительно включающая частицы с максимальным размером от 1 до 4 мм, например 1,5 мм.
В статье D. A. Hickman and L.D. Schmidt («Synthesis Gas Formation by Direct Oxidation of Methane over Pt Monoliths», Journal of Catalysis 138, 267-282, 1992) описаны эксперименты по неполному окислению метана в присутствии катализатора, включающего платину или родий. Реакции неполного окисления проводились практически при атмосферном давлении и при температуре в интервале от 600 до 1500 К (от 327 до 1227 o C). Использовались катализаторы в виде металлических сеток, покрытых металлом вспененных монолитов и покрытых металлом экструдированных монолитов. Катализаторы в виде металлической сетки содержали от 1 до 10 слоев сетки в 16 проволок на 1 см (40 меш) или 32 проволоки на 1 см (80 меш). Вспененные монолиты состояли из альфа-окиси алюминия и описаны как имеющие открытую ячеистую, губчатую структуру. Использованные образцы имели номинальную пористость от 12 до 20 пор на 1 см (от 30 до 50 пор на 1 дюйм (ppi)). Экструдированными монолитами являлись экструдированные монолиты кордиерита, имевшие 62 квадратные ячейки/см 2 (400 квадратных ячеек/дюйм 2 и состоявшие из прямых параллельных каналов, обеспечивающих ламинарное течение газов через каналы при исследованных условиях протекания газа.
В статье J. K. Hockmuth («Catalytic Partial Oxidation of Methane over a monolith Supported Catalyst», Applied Catalysis B: Environmental, 1 (1992) 89-100) сообщается о неполном каталитическом окислении метана с использованием катализатора, включающего комбинацию платины и палладия на подложке из монолитного тела кордиерита.
Европейская заявка на патент 0576096 (EP-A-0576096) раскрывает процесс неполного каталитического окисления углеводородного сырья, в котором сырье, включающее углеводородное сырье, кислородсодержащий газ и необязательно пар с молярным отношением кислорода к углероду в интервале от 0.45 до 0.75, контактирует в реакционной зоне с катализатором в адиабатических условиях. Катализатор включает металл группы VIII Периодической системы элементов, нанесенный на носитель. Катализатор находится в реакционной зоне в виде неподвижного слоя, имеющего высокую извитость (определенную как отношение длины пути, проходимого газом при протекании сквозь структуру, к длине кратчайшего возможного прямого пути сквозь структуру). В EP-A-0576096 раскрыт широкий спектр носителей и структур, в том числе частицы носителя, металлические сетки и тугоплавкие пены. Пригодные для использования в качестве носителей материалы включают тугоплавкие оксиды, такие как оксиды кремния, алюминия, титана, циркония и их смеси. Заявлено, что окись алюминия является особенно предпочтительным материалом для носителей.
В Европейской заявке на патент 0548679 (EP-A-O548679) раскрыт способ получения окиси углерода и водорода неполным каталитическим окислением метана в присутствии катализатора, полученного путем осаждения родия и/или рутения в качестве активного компонента на носитель, состоящий из двуокиси циркония или стабилизированной двуокиси циркония. В EP-A-0548679 катализатор описан как имеющий любую пригодную форму, такую как тонкодисперсный порошок, бусинки, таблетки, пластины, мембраны или монолиты. В EP-A-0549679 описан способ неполного каталитического окисления, который проводят при температуре от 350 до 1200 o C, предпочтительно от 450 до 900 o C при давлении до 300 кг/см 2 G, предпочтительно меньше чем 50 кг/см 2 G. Обычная рабочая объемная скорость газа в EP-A-0548 679 находится в области от 1000 до 10000/ч, предпочтительно от 2000 до 20000/ч. Конкретные примеры в EP-A-0548679 описывают эксперименты, проведенные при атмосферном давлении при температурах от 300 до 750 o C и объемных скоростях 16000 и 43000/ч. Во всех экспериментах, описанных в EP-A-0548679, катализатор удерживался в виде неподвижного слоя частиц.
Публикация заявки на европейский патент 0656317 (EP-A-0656317) содержит описание способа неполного каталитического окисления углеводородного сырья, в котором углеводород смешивается с кислородсодержащим газом и контактирует с катализатором. Катализатор удерживается в виде неподвижного слоя, имеющего высокую извитость (определенную как отношение длины пути, проходимого газом при протекании сквозь структуру к длине кратчайшего возможного прямого пути сквозь структуру), по меньшей мере 1.1 и имеющего по меньшей мере 750 пор на квадратный сантиметр. Катализатор предпочтительно включает каталитически активный металл, нанесенный на носитель. Пригодные носители включают тугоплавкие оксиды, такие как оксид кремния, оксид алюминия, оксид титана, оксид циркония и их смеси. Специально отмечен катализатор, включающий вспененную тугоплавкую двуокись циркония.
Привлекательный для промышленного применения способ неполного каталитического окисления должен работать при повышенном давлении, обычно превышающем 10 бар, например около 30 бар, и при высокой часовой объемной скорости газа, обычно порядка от 500000 до 1000000/ч. Из-за термодинамического поведения реакции неполного окисления необходимо вести реакцию при повышенных температурах для того, чтобы получить высокий выход окиси углерода и водорода при повышенных давлениях. Для получения выхода, пригодного для промышленного применения, необходимы температуры порядка 1000 o C или более.
Обнаружено, что наиболее подходящим типом неподвижного слоя катализатора для использования при неполном каталитическом окислении углеводородов в условиях, привлекательных для промышленности, является такой тип, в котором катализатор находится в виде монолитной структуры. Катализатор для использования в таком способе включает один или более каталитически активных компонентов, нанесенных на носитель из тугоплавкого оксида, причем носитель имеет форму монолита. Используемые здесь термины «монолит» или «монолитная структура» относятся к любой одной ячейке пористого материала, предпочтительно к любой одной ячейке пористого тугоплавкого материала, в которой поры образуют прямые или ветвистые, параллельные или случайно направленные каналы, распространяющиеся сквозь структуру ячейки, то есть имеющие связанную открытую пористость.
Меры, необходимые для предотвращения теплового удара катализатора при работе процесса в промышленном масштабе, обычно включающие подогрев, например, посредством медленной теплопередачи, весьма дороги и трудны в исполнении. Таким образом, существует необходимость в способе неполного каталитического окисления, который сочетает высокий уровень селективности до окиси углерода и водорода, высокий уровень каталитической стабильности и устойчивость к тепловым ударам.
Неожиданно обнаружено, что монолитные структуры на основе двуокиси циркония обеспечивают значительно более высокое сопротивление тепловым ударам при рабочих режимах процесса неполного каталитического окисления, чем монолиты, изготовленные из других материалов.
Таким образом, настоящее изобретение предлагает способ неполного каталитического окисления углеводородного сырья, который включает контактирование исходного сырья, содержащего углеводородное сырье и кислородсодержащий газ, с катализатором при повышенной температуре при таких условиях, при которых катализатор чувствителен к тепловому удару, причем катализатор имеет форму пористой монолитной структуры и включает каталитически активный металл, нанесенный на носитель на основе двуокиси циркония.
Преимущество способа, предлагаемого настоящим изобретением, заключается в том, что используемый катализатор, как установлено, является особенно прочным при экстремальных условиях, преобладающих при проведении реакций неполного каталитического окисления. В частности, процесс является устойчивым в условиях, когда катализатор подвержен тепловым ударам. Было обнаружено, что монолитные катализаторы на основе двуокиси циркония демонстрируют высокое сопротивление тепловому удару в конкретных условиях окисления по сравнению с обычными катализаторами, такими, как катализаторы на основе оксида алюминия.
Углеводородное сырье контактирует с катализатором в виде смеси с кислородсодержащим газом. Для использования в качестве кислородсодержащего газа подходит воздух. Однако может быть предпочтительным использование в качестве кислородсодержащего газа по существу чистого кислорода. В этом случае нет необходимости перерабатывать большой объем инертного газа, например азота, как в случае использования воздуха в качестве кислородсодержащего газа. Сырье необязательно может включать пар.
Углеводородное сырье и кислородсодержащий газ предпочтительно присутствуют в исходном сырье в таких количествах, чтобы обеспечить отношение кислорода к углероду в интервале от 0.3 до 0.8, более предпочтительно в интервале от 0.45 до 0.75. Здесь под отношением кислорода к углероду имеется в виду отношение кислорода в виде молекул (O2) к атомам углерода, присутствующих в углеводородном сырье. Предпочтительно отношение кислорода к углероду находится в интервале от 0.45 до 0.65 при стехиометрическом соотношении 0.5, что означает, что отношения в интервале от 0.45 до 0.65 особенно предпочтительны. Если в сырье присутствует пар, отношение пара к углероду находится предпочтительно в интервале приблизительно от 0.0 до 3.0, более предпочтительно от 0.0 до 2.0. Углеводородное сырье, кислородсодержащий газ и пар, если он присутствует, предпочтительно хорошо перемешиваются до приведения их в контакт с катализатором.
Способ настоящего изобретения может быть осуществлен при любом подходящем давлении. Для промышленных применений наиболее пригодны повышенные давления, то есть давления, существенно превышающие атмосферное давление. Способ может быть осуществлен при давлениях в области до 150 бар. Предпочтительно способ проводят при давлениях в области от 2 до 125 бар, в особенности от 5 до 100 бар.
Способ может быть осуществлен при любой подходящей температуре. В предпочтительных условиях высокого давления, превалирующих в процессах промышленного масштаба, сырье предпочтительно контактирует с катализатором при высоких температурах. Это необходимо для достижения высокой конверсии при предпочтительных повышенных давлениях. Таким образом, исходная смесь предпочтительно контактирует с катализатором при температуре, превышающей 950 o C, более предпочтительно при температуре в интервале от 950 до 1400 o C, особенно предпочтительно при температуре от 1000 до 1300 o C. Исходная смесь предпочтительно предварительно подогревается до контактирования с катализатором.
При проведении процесса сырье может подаваться с любой подходящей объемной скоростью. Преимуществом способа настоящего изобретения является то, что могут быть достигнуты очень высокие объемные скорости газа. Так, объемные скорости газа (выраженные в нормальных литрах газа на килограмм катализатора в час) находятся в области от 20000 до 100000000 нл/кг/ч, более предпочтительно в области от 50000 до 50000000 нл/кг/ч. Объемные скорости в интервале от 500000 до 30000000 нл/кг/ч, особенно приемлемы для использования в данном способе.
Катализатор, используемый в способе настоящего изобретения, включает каталитически активный металл, нанесенный на монолитную структуру на основе двуокиси циркония. Каталитически активные металлы для использования в катализаторе выбираются из группы VIII Периодической системы элементов. Ссылки на Периодическую систему приводятся здесь по версии CAS, опубликованной в CRC Handbook of Chemistry and Physics, 68-е издание. Предпочтительные катализаторы для применения в способе настоящего изобретения включают металл, выбираемый из рутения, родия, палладия, осмия, иридия и платины. Особенно предпочтительны катализаторы, включающие рутений, родий или иридий в качестве каталитически активного металла. Наиболее приемлемым каталитически активным металлом является иридий.
Катализатор включает каталитически активный металл на монолитном носителе на основе двуокиси циркония. Может быть использован любой пригодный материал на основе двуокиси циркония. Пригодные материалы на основе двуокиси циркония выпускаются в промышленности. Носитель предпочтительно включает по меньшей мере 70 вес.% двуокиси циркония, например выбирается из известных видов стабилизированных или частично стабилизированных оксидов циркония или по существу чистой двуокиси циркония. Стабилизированная или частично стабилизированная двуокись циркония, включающая оксиды одного или более редкоземельных элементов, элементы Периодической системы групп IIIB или IIA, являются особенно предпочтительными материалами на основе двуокиси циркония. Наиболее предпочтительны материалы на основе двуокиси циркония, стабилизированной или частично стабилизированной одним (или более) оксидом Mg, Ca, Al, Y, La или Ce. Стабилизированная или частично стабилизированная двуокись циркония может быть в любой доступной форме, такой как композиты на основе частиц, волокон или усов.
Монолитный носитель на основе двуокиси циркония может включать материал на основе двуокиси циркония, как описано выше, покрытый другим материалом с желаемыми свойствами, улучшенным сопротивлением тепловому удару (например, SiC, SiO2, Al2O3 или их смеси), улучшенной каталитической стабильностью или улучшенной термической стабильностью.
Носитель имеет форму монолитной пористой структуры. Монолитная структура, которая в наибольшем измерении может иметь размер от 1 см до 1 м и более, может включать одну или множество отдельных монолитных частей носителя. Хотя множество частей носителя обеспечивает большее сопротивление тепловому удару, чем аналогичный моноблочный носитель, удержание и хорошая поверхностная стыковка частей может быть проблематичной при больших объемных скоростях, применяемых в настоящем изобретении. Несмотря на это носитель может быть сегментированным монолитным носителем в соответствии с известными технологиями. Пористая монолитная структура может иметь любую приемлемую форму. Одной из форм монолитной структуры является экструдированная ячеистая форма, для которой пригодные материалы известны и доступны на промышленном уровне. Экструдированный ячеистый материал характеризуется тем, что он имеет множество прямых, вытянутых, параллельных каналов, проходящих сквозь структуру. Однако предпочтительными являются монолитные структуры с высокой извитостью. Термин «извитость» является общеизвестным термином в данной области и применительно к настоящему изобретению определен как отношение длины пути, проходимого газом при протекании сквозь структуру, к длине кратчайшего возможного прямого пути сквозь структуру. Из этого следует, что экструдированная ячеистая структура имеет извитость 1.0. Монолитная структура для применения в способе настоящего изобретения предпочтительно имеет высокую извитость, то есть извитость более 1.1. Монолитная структура предпочтительно имеет извитость в области от 1.1 до примерно 10.0, более предпочтительно в области от 1.1 до 5.0. Наиболее предпочтительной областью извитости для монолитной структуры является от 1.3 до 4.0.
Монолитная структура для применения в способе настоящего изобретения является пористой, как определено выше. Монолитная структура предпочтительно имеет высокую пористость. Эти поры следует отличать от микропор, которые могут иметься в материале носителя. Монолитная структура предпочтительно содержит по меньшей мере 500 пор на квадратный сантиметр, более предпочтительно по меньшей мере 750 пор на квадратный сантиметр. Предпочтительными являются монолитные структуры, имеющие от 1000 до 15000 пор на квадратный сантиметр, более предпочтительно от 1250 до 10000 пор на квадратный сантиметр.
Монолитная структура предпочтительно имеет долю пустот в пределах от 0.4 до 0.9, более предпочтительно во избежание избыточного скачка давления от 0.6 до 0.9.
Наиболее пригодной и особенно предпочтительной монолитной структурой для носителя катализатора в способе настоящего изобретения является пена. Пригодные для применения в способе настоящего изобретения пены на основе двуокиси циркония выпускаются промышленностью.
Катализаторы для способа настоящего изобретения могут быть приготовлены известными в данной области методами. Наиболее пригодным методом является пропитка материала на основе двуокиси циркония соединением каталитически активного металла.
Сырье предпочтительно контактирует с катализатором в адиабатических условиях. В настоящем описании термин «адиабатические» относится к условиям реакции, в которых практически отсутствуют тепловые потери и излучение из реакционной зоны, за исключением тепла, уносимого из реактора газовым потоком.
Другой аспект настоящего изобретения относится к окиси углерода или водороду, полученным вышеописанным способом.
Окись углерода и водород, полученные в способе настоящего изобретения, могут быть использованы в любом процессе, в котором требуется один или оба этих компонента. Смесь окиси углерода и водорода, получаемая в этом способе, особенно пригодна для использования в синтезе углеводородов, например в процессе Фишера-Тропша, или для синтеза оксигенатов, например метанола. Способы конверсии окиси углерода и водорода в такие продукты хорошо известны. С другой стороны, смесь окиси углерода и водорода может быть использована в производстве водорода путем конверсии водяного пара. Другие применения включают процессы гидроформилирования и карбонилирования.
Способ настоящего изобретения описан далее следующими иллюстративными примерами, из которых примеры 1, 2 и 3 являются примерами осуществления настоящего изобретения, а пример 4 приведен только в целях сравнения.
Промышленную пену на основе двуокиси циркония, стабилизированную алюминием (Al-PSZ, 990 пор на квадратный сантиметр) пропитывают родием с применением обычной методики пропитки для получения окончательного содержания родия 5 вес.%.
Пропитанную пену двуокиси циркония загружают в стальной реактор. Структура катализатора имеет извитость между 1.5 и 2.5. Хорошо перемешанные природный газ и кислород подают в реактор для контактирования с катализатором. Исходное сырье имеет отношение кислорода к углероду 0.54. Сырье подают с часовой объемной скоростью (ЧОС) 750000 нл/кг/ч (нормальных литров газа на килограмм катализатора в час) при давлении 1.0 бар.
Рабочая температура катализатора измеряется с использованием оптической пирометрии. Состав газа, выходящего из реактора, определяют с помощью газовой хроматографии. Определяют степень конверсии и селективность процесса по окиси углерода и водороду (из расчета на превращенный метан) Рабочие условия и результаты экспериментов обобщены в таблице.
Сырье предварительно подогревают до 250 o C. Вначале, однако, реакция не наблюдалась. Малая часть катализатора была инициирована с помощью генератора тепла сжиганием смеси пропана и кислорода. Это привело к быстрому воспламенению всей структуры катализатора, наблюдаемому как свечение, быстро распространяющееся поперек структуры катализатора от точки воспламенения в течение примерно 15 с. В это время весь катализатор быстро нагревается от исходной температуры 250 o C до конечной рабочей температуры 1240 o C. Тем самым катализатор подвергается тепловому удару более чем 60 o C в секунду в области температуры 990 o C. Описание катализатора в конце эксперимента дано в таблице.
Промышленную пену на основе друокиси циркония, стабилизированную алюминием (Al-PSZ, 990 пор на квадратный сантиметр), пропитывают иридием с применением обычной методики пропитки для получения окончательного содержания иридия 5 вес.%.
Для исследования катализатора иридий/двуокись циркония использовалась общая экспериментальная методика, описанная в примере 1. Рабочие режимы и результаты представлены в таблице.
Промышленную пену на основе двуокиси циркония, стабилизированную алюминием (Mg-PSZ, 990 пор на квадратный сантиметр), пропитывают родием с применением обычной методики пропитки для получения окончательного содержания родия 5 вес.%.
Для исследования катализатора родий/двуокись циркония использовалась общая экспериментальная методика, описанная в примере 1. Рабочие режимы и результаты представлены в таблице.
Пример 4. Сравнительный пример.
С целью сравнения промышленную пену на основе оксида алюминия (Al2O3) пропитывают родием с применением обычной методики пропитки для получения окончательного содержания родия 5 вес.%.
Для исследования катализатора родий/оксид алюминия использовалась общая экспериментальная методика, описанная в примере 1. Рабочие режимы и результаты представлены в таблице.
1. Способ неполного каталитического окисления углеводородного сырья, который включает контактирование сырья, содержащего углеводородное сырье и кислородсодержащий газ, с катализатором, при повышенной температуре в реакторе, причем катализатор имеет форму пористой монолитной структуры и включает каталитически активный металл, нанесенный на носитель на основе двуокиси циркония, отличающийся тем, что в процессе пуска или остановки реактора катализатор подвергают тепловому удару, по меньшей мере 50 o C в секунду в температурном интервале, по меньшей мере, 500 o C.
2. Способ по п.1, отличающийся тем, что проводят контактирование возможно подогретого газа в состоянии перед воспламенением или пара до или непосредственно во время контактирования сырья с катализатором, предпочтительно любого пригодного газа в состоянии перед воспламенением, который чисто воспламеняется при умеренной температуре.
5. Способ по любому из предшествующих пунктов, отличающийся тем, что кислородсодержащим газом является по существу чистый кислород.
6. Способ по любому из предшествующих пунктов, отличающийся тем, что исходное сырье включает углеводородное сырье и кислородсодержащий газ в количествах, обеспечивающих отношение кислорода к углероду от 0,3 до 0,8, предпочтительно от 0,45 до 0,75, более предпочтительно от 0,45 до 0,65.
7. Способ по любому из предшествующих пунктов, отличающийся тем, что исходное сырье контактирует с катализатором при давлении в интервале до 150 бар, предпочтительно от 2 до 125 бар, более предпочтительно от 5 до 100 бар.
10. Способ по любому из предшествующих пунктов, отличающийся тем, что катализатор включает в качестве каталитически активного металла металл VIII-ой группы Периодической системы элементов, предпочтительно металл, выбираемый из родия, иридия или рутения, более предпочтительно иридия.
11. Способ по любому из предшествующих пунктов, отличающийся тем, что монолитный носитель катализатора включает, по меньшей мере, 70 вес.% двуокиси циркония, например, выбранной из известных видов стабилизированной или частично стабилизированной двуокиси циркония или по существу чистой двуокиси циркония, предпочтительно включающей стабилизированную или частично стабилизированную двуокись циркония, содержащей оксиды одного или нескольких редкоземельных элементов, элементы группы IIIВ или группы IIА Периодической таблицы.
14. Способ по любому из предшествующих пунктов, отличающийся тем, что катализатор является пеной.
16. Способ по любому из предшествующих пунктов, отличающийся тем, что исходное сырье контактирует с катализатором практически в адиабатических условиях.