неспецифическая резистентность организма что это
ПОВЫШЕНИЕ НЕСПЕЦИФИЧЕСКОЙ РЕЗИСТЕНТНОСТИ ОРГАНИЗМА С ПОМОЩЬЮ КВЧ-ТЕРАПИИ
Военно-медицинский институт ФПС России при НГМА
Одним из таких методов является воздействие электромагнитного излучения низкой интенсивности ММ- диапазона длин волн. Каждая клетка живого организма является достаточно автономным образованием, а поскольку человеческий организм состоит из 10 15 клеток, то для обеспечения нормальной работы такой сложной системы необходим определенный механизм синхронизации функций. Гомеостаз организма связан с излучением клетками электромагнитных полей в КВ Ч- диапазоне (миллиметровых волн крайне высокой частоты), каждая клетка является автогенератором этих частот. Поскольку амплитудно-частотные характеристики излучения больного и здорового организмов разные, любую его патологию следует считать так же и патологией клеток. Внешнее излучение (аппараты КВЧ-терапии ), моделируя собственные излучения в организме в КВЧ-диапазоне и выполняя функции синхронизирующего устройства, навязывают организму утраченную в процессе болезни «здоровую» ритмику и таким образом воздействует на его собственную информационно-управляющую систему [4].
Если какие-то функции организма снижены по сравнению с нормой, то воздействие ЭМ ММВ может их нормализовать или приблизить к норме. При КВ Ч- терапии речь при воздействии идет не о том или ином конкретном заболевании или методе лечения, а о гармоничном восстановлении организма, то есть таком восстановлении организма, при котором единовременно устраняются все или, по крайней мере, значительная часть нарушений, мешающих взаимосвязанному функционированию различных систем организма.
Применение КВЧ- терапии в курортологии, реабилитологии показало, что после 5-6 сеансов отмечался выраженный иммуномодулирующий эффект, сохраняющийся в течение нескольких месяцев, повышается устойчивость организма человека к внешним вредным воздействиям, осуществляется профилактика возникновения патологических сдвигов в организме [10,11]. В опытах на животных доказана возможность использования электромагнитного КВЧ-излучения в качестве профилактического средства от летальной гриппозной инфекции [12]. Высказана возможность применения КВЧ-облучения в качестве профилактического и терапевтического средства в предэпидемические периоды и во время эпидемий гриппа.
Целью работы явилась оценка повышения неспецифической резистентности с помощью аппарата для КВЧ-терапии «АМФИТ 0,2/10-0,1» [13].
Оценка эффективности проводилась на модели гриппа и других острых респираторных заболеваний в воинских коллективах на протяжении эпидемических сезонов 1998-2000 годов.
1. КВЧ-терапия молодому пополнению.
2. КВЧ-терапия у военнослужащих, проходящих службу по контракту.
Опытная ( n = 28) и контрольная ( n = 33) группы сформированы перед началом эпидемического сезона. В октябре-ноябре регистрировалась высокая заболеваемость ОРЗ, в январе прошла вспышка гриппа. Сеансы КВЧ проведены по той же схеме, что и предыдущему коллективу в конце ноября.
При практически одинаковых исходных данных, после КВЧ-терапии в опытной группе заболеваемость оказалась ниже в 1,7 раза, в опытной группе не зарегистрировано осложнений ОРЗ и гриппа. Индекс эффективности составил 1,69, а показатель защищенности 42%.
Под наблюдением находилось два коллектива: опытный ( n = 107) и контрольный ( n = 109). Опытный коллектив, сформированный в августе-сентябре, являлся коллективом с традиционно более высокой заболеваемостью гриппом и ОРЗ. Контрольный коллектив сформирован в это же время, заболеваемость умеренно выражена.
По итогам наблюдения, общая заболеваемость за год составила в опытном коллективе 495 на 1000 военнослужащих, а в контрольном 889, то есть в опыте меньше в 1,8 раза ( р
При оценке воздействия электромагнитного излучения ММ-волн крайневысокой частоты на показатели иммунитета исследовали кровь добровольцев до КВЧ и через сутки после сеансов КВЧ. Лица, находящиеся под наблюдением относились к категории практически здоровых военнослужащих, не имели жалоб на состояние здоровья и были разделены на группы со сниженной резистентностью и без них только по данным аппаратной экспресс-диагностики с помощью аппарата «Анализатора иммунодефицита «Хелпер». Показатели числа лейкоцитов и лимфоцитов у всех наблюдаемых не отличались от показателей нормы.
Контрольная группа сформирована из того же коллектива методом случайной выборки. КВЧ контрольной группе не проводилось.
1. Установлено, что предлагаемый метод КВЧ-терапии является эффективным методом предсезонной неспецифической профилактики гриппа и других ОРЗ в воинских коллективах. Его использование среди лиц групп риска позволило в последующем снизить заболеваемость этими инфекциями в 1,8 раза.
2. При проведении КВЧ-профилактики у лиц с наличием термопризнаков снижения резистентности организма наиболее эффективным и экономичным является метод селективной профилактики.
3. Рефлексогенное воздействие ММ-волн крайневысокой частоты приводит к изменению показателей клеточного иммунитета: достоверному увеличению Т-лимфоцитов хелперов и иммунорегуляторного индекса, а следовательно к повышению неспецифической резистентности организма к инфекционным заболеваниям.
1. Воробьев А. А., Ляшенко В. А. Иммунобиологические препараты:
настоящее и будущее. // Журн. микробиологии, эпидемиологии и иммунобиологии. 1995. № 6. С. 105-111.
3. Вогралик В. Г.,Вогралик М. В. Пунктурная рефлексотерапия. Горький. 1988.
4. Девятков Н. Д., Голант М. Б., Бецкий О. В. Миллиметровые волны и их роль в процессах жизнедеятельности. М., Радио и связь. 1991.
6. Веткин А. Н. Применение миллиметровых волн в клинике. // Миллиметровые волны нетепловой интенсивности в медицине. М., ИРЭ АН СССР. 1991.С. 7-15.
8. Лян Н. В., Воторопин С. Д. Миллиметровая терапия в профилактике послеоперационных осложнений онкологических больных. // Миллиметровые волны в биологии и медицине. 1995. № 5. С. 51-54.
12. Защитный эффект низкоинтенсивного облучения при летальной гриппозной инфекции. /Рыжкова Л.В., Старик А.М., Волгарев А.П. // Миллиметровые волны нетепловой интенсивности в медицине. М., ИРЭ АН СССР. 1991. С. 374-378.
13. Корнаухов А. В., Анисимов С. И., Алябина Н. А. и др. Аппарат КВЧ-терапии с шумовым излучением «АМФИТ-0,2/10-01» и некоторые аспекты его применения в медицине. // Миллиметровые волны в биологии и медицине. 1999. №2 (14). С. 49-52.
Средства и методы, повышающие неспецифическую резистентность организма человека к гриппу и ОРВИ
Средства и методы повышения неспецифической сопротивляемости и схемы их применения
1.Лекарственные препараты растительного происхождения
3).Сироп из плодов шиповника по 1 чайной ложке в день в холодный сезон года для дошкольников. Применение в указанных дозах не требует врачебного контроля.
2.Продигиозан (бактериальный липополисахарид, рекомендуется с 3-х лет)
«Гексавит», «Ревит», «Декамевит», в возрастных дозировках 2-3 раза в день после еды в виде курса продолжительностью 20-30 дней.
5.Противогриппозный комплекс (дибазол, аскорбиновая кислота, тимоген)
Применяют в течение 4-х дней по схеме прилагаемой к препарату.
Не рекомендуется детям до 1 года.
Противовирусные препараты для экстренной профилактики при контакте с больным.
С профилактической целью по 1 табл. (0,05г) взрослым после еды ежедневно 1-2 раза от 2-7 дней (внутриочаговая профилактика), до 20 дней (внеочаговая профилактика).
Профилактически по 2 табл. (0,2г) взрослым 2 раза в неделю в течение 3 недель. При контакте с больным гриппом по 0,2г (2 табл.) в день (до еды) в течение 10-14 дней.
Противопоказан лицам с заболеваниями почек, печени, сердечно-сосудистой системы.
3.Оксолиновая мазь во время эпидемии и вспышек ОРЗ, при контакте с больным в семье (предназначена для самостоятельного применения, не имеет противопоказаний)
Ежедневное двукратное смазывание слизистой оболочки носа в течение 7-10 дней.
4.Лейкоцетарный человеческий интерферон, для экстренной защиты детей дошкольного возраста
Ежедневное закапывание или распыление 0,25 мл (5кап.) в каждый носовой ход 2 раза в сутки с интервалом не менее 6 часов. Рекомендуется проводить профилактические курсы в первые 7-10 дней пребывания ребенка в коллективе, при контакте с больным в семье или детском учреждении.
Противостояние с резистентными бактериями: наши поражения, победы и планы на будущее
Противостояние с резистентными бактериями: наши поражения, победы и планы на будущее
Эмблема Глобального плана действий по борьбе с устойчивостью к антибиотикам, подготовленного Всемирной организацией здравоохранения. Наше противостояние с резистентностью настолько важно, что с недавних пор стало активно поддерживаться даже на межгосударственном уровне.
Автор
Редакторы
На протяжении всего своего существования человечество крайне не любит задумываться о последствиях предпринимаемых действий и предпочитает жить днем сегодняшним. Неоднократно подобное поведение оборачивалось проблемами, тянущими за собой другие, и так далее. Но зачастую никакого урока из этого человечество не извлекает. Подобная история случилась и со стремительно возрастающей устойчивостью микроорганизмов к антибиотикам. Опасная ситуация создавалась «силами» человека, им же и должна быть исправлена. В решении этой проблемы задействованы представители научного мира и системы здравоохранения, прикладываются усилия на уровне государств и общественных организаций. Но ничто не остается неизменным — ни устойчивость микроорганизмов, ни наши подходы к ее преодолению. Давайте разберемся, какие шаги предпринимаются для решения проблемы антибиотикорезистентности, каких высот достигла приспособленность микроорганизмов и что с этим всем можно сделать.
Современный ученый, занимающийся исследованиями в естественнонаучной или медицинской областях и желающий быть в курсе происходящих в научном сообществе событий, еженедельно (а то и чаще) получает новостные рассылки из различных журналов. И практически ни одна такая подборка не обходится без сообщений на тему резистентности бактерий, грибов, простейших и вирусов к соответствующим лекарствам. Зарубежные научные, научно-популярные и даже обычные СМИ более чем часто говорят о вновь возникающей устойчивости каких-либо штаммов к антибиотикам и о путях решения этой проблемы. Даже неискушенный читатель не может не заметить обилия подобной информации, нарастающей с годами паники и всё более масштабно развертывающейся программы контрдействий.
Отличная статья Джулиана и Дороти Дейвис про историю устойчивости к антибиотикам: «Происхождение и эволюция антибиотикорезистентности» (англ.) [1].
В отличие от многих мировых проблем, вопрос возникающей устойчивости микроорганизмов к антибиотикам затрагивает любого человека любого возраста в любой стране. Шансы, что из-за их неправильного использования чувствительные штаммы станут устойчивыми, а (при определенных условиях) непатогенные — патогенными, равновелики для всех. Из множества бактерий, населяющих нашу планету, некоторые могут распространяться и вызывать заболевания исключительно в жарком климате, в странах с определенным уровнем гигиены. Но есть и другие, которые существуют повсеместно, не ведая границ: не стоит забывать, например, о патогенных штаммах «мирных», обычных для нашего микробиома Escherichia coli или Klebsiella pneumoniae.
Быстрая выработка антибиотикорезистентности — глобальная проблема, и небольшими спорадически возникающими инициативами ее решить не получится. Необходимы скоординированные действия всех государств. Ситуация с устойчивостью не только к единичным, но уже и ко множеству антибиотиков усугубилась до такой степени, что ее решили обсудить на ежегодной сессии Генеральной ассамблеи ООН, состоявшейся в сентябре этого года в Нью-Йорке. Важно отметить, что вопросы здравоохранения включали в повестку сессий лишь трижды — когда обсуждали ВИЧ, незаразные болезни и лихорадку Эбола. Теперь в список добавилась и резистентность микроорганизмов к антибиотикам. То, что это явление стои́т в одном ряду с важнейшими проблемами здравоохранения, не вызывает удивления.
Глобальные инициативы до сентябрьской сессии Генассамблеи ООН
Впервые на глобальном уровне тема антибиотикорезистентности обсуждалась в 2014 году в докладе Всемирной организации здравоохранения (ВОЗ). После сбора и анализа данных по 114 странам стало очевидно, что на их территории распространены устойчивые к препаратам «последней линии» — карбапенемам — штаммы Klebsiella pneumoniae и резистентные к фторхинолонам штаммы Escherichia coli. Еще тогда были предложены принципиально возможные решения, но это не быстро претворяющиеся в реальность меры, и должно пройти время, чтобы их тщательно проработать, принять и чтобы они начали действовать [2].
После этого доклада появилось множество разных инициатив. В мае 2015 года был принят Глобальный план действий по устойчивости к противомикробным препаратам [3]. С ноября 2015 года в рамках недели борьбы с резистентностью начали проводить ежегодную кампанию «Антибиотики: используйте осторожно!», которая направлена на повышение осведомленности общественности и медицинских работников. К слову, эта кампания проводилась и в ноябре 2016 года [4].
Казалось бы, предпринятые действия уже должны были придать ускорение поиску решений относительно антибиотикорезистентности. Однако в этом году проблема вновь обсуждалась на сессии Генеральной ассамблеи — значит, не всё так просто. Чтобы понять почему, нужно немного рассказать о биологических механизмах и последствиях устойчивости к антибиотикам.
Как и почему возникает резистентность
В природе резистентность появляется спонтанно из-за накапливающихся в ДНК случайных мутаций, которые повышают приспособленность микроорганизмов в среде с угнетающим веществом. Нередко это свойство приобретается и путем горизонтального переноса генов от других бактерий, поэтому детерминанты резистентности способны быстро распространяться даже между неродственными штаммами. При длительном воздействии антибиотика вначале погибает бόльшая часть популяции чувствительных к нему микроорганизмов, а та малая доля, что выживает, либо уже имеет жизненно важные для этих условий мутации, либо успевает мутировать или захватить нужные гены от бактерий-соседей и под селективным давлением антибиотика закрепить благоприобретения. В любом случае, выжившие способны нормально существовать и размножаться даже в присутствии антибиотика. То есть он больше на них не действует.
Уточняю, что «официально», потому что другие исследователи до Флеминга обнаруживали этот антибиотик; подробнее о предшественниках можно прочитать в обзоре «Эволюция наперегонки, или почему антибиотики перестают работать» [6], а о самом Флеминге — в статье «Победитель бактерий» [7].
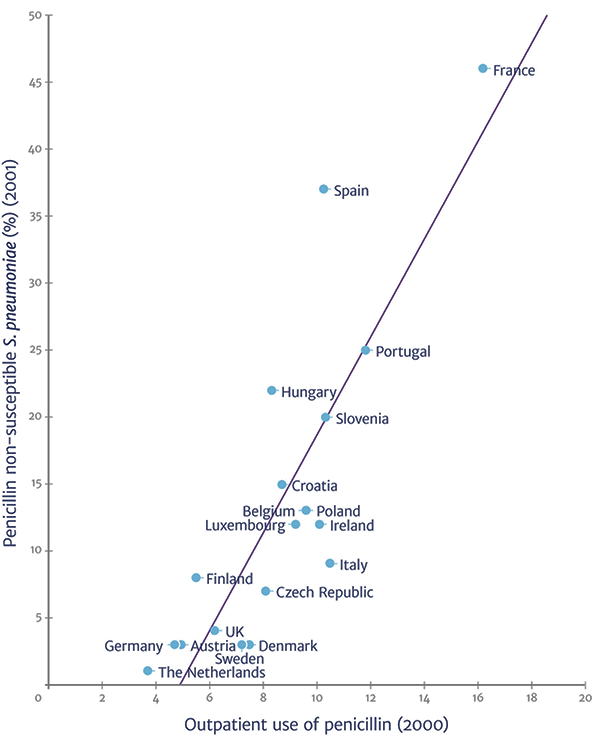
Здесь стόит оговорить один момент. Обычно в быстро развивающейся резистентности бактерий винят людей, беспричинно принимающих антибиотики в «любой непонятной ситуации». Или людей, необоснованно прерывающих курс просто потому, что «стало лучше, чего лечиться-то» (рис. 1) [8]. Тем не менее огромный вклад в это нехорошее дело вносит широкомасштабное использование антибиотиков в животноводстве: больше половины мирового объема используемых антибиотиков приходится именно на скотоводство и птицеводство [9]. Подобная тактика сильно подрывает наши «рубежи» в борьбе с патогенными микроорганизмами. Причина добавления антибиотиков в корм для домашних животных проста и обоснована: они позволяют предотвратить ряд инфекционных заболеваний, поддержать здоровье и продуктивность животных, снизить смертность, которая оборачивается крупными экономическими потерями.
Рисунок 1. Существует прямая корреляция между использованием пенициллина и ростом доли устойчивых к нему пневмококков (Streptococcus pneumoniae).
В исследовании, опубликованном в журнале PNAS, подсчитали, что в 2010 году во всём мире в корма было добавлено более 63 000 тонн антибиотиков. И это — только по скромным оценкам. Ожидается, что к 2030 году указанное число возрастет на 67%, но, что должно особенно встревожить, оно удвоится в Бразилии, Индии, Китае, Южной Африке. И в России [10].
Побочным действием чрезмерного использования антибиотиков является то, что не все они метаболизируются. После выведения из организма они проникают в почву и задерживаются в ней, впоследствии накапливаясь в растениях. Через почву антибиотики попадают в воду и распространяются на значительные расстояния, воздействуя на бόльшее число микроорганизмов, чем изначально предполагалось. Они могут вновь попадать в организм человека и животных и воздействовать в том числе на их микробиом.
Таким образом, несмотря на многочисленные предупреждения, из-за массового и неправильного использования антибиотиков устойчивость к ним распространяется среди микроорганизмов всё шире и быстрее. А значит, людей и животных с каждым годом становится всё труднее лечить от бактериальных инфекций.
Проблемы, порождаемые резистентностью
Это не то, что могло бы произойти в отдаленном будущем.
Это наша настоящая реальность в развивающихся и развитых странах,
в селах и городах, в госпиталях, на фермах.
Мы теряем способность защищать людей и животных
от опасных для жизни инфекций.
Пан Ги Мун, генеральный секретарь ООН
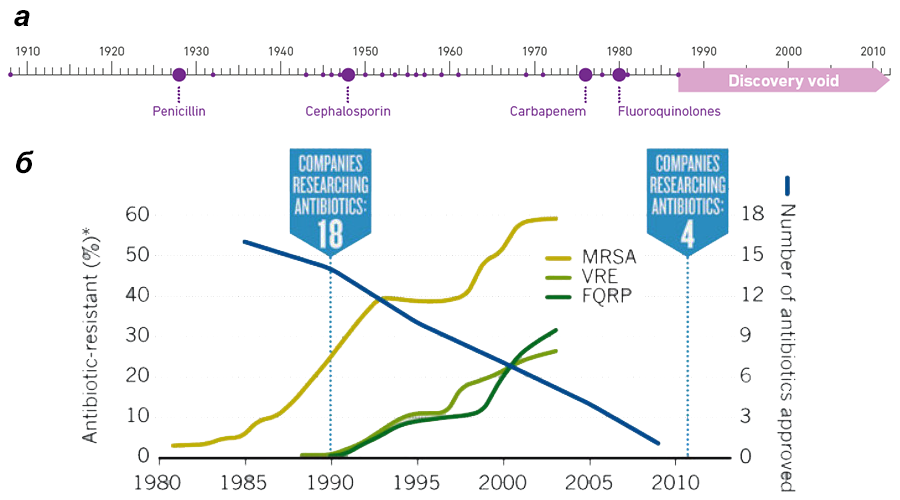
Раньше, если у возбудителя болезни вырабатывалась устойчивость к какому-то одному антибиотику, использовали комбинации из нескольких, чтобы они уж точно уничтожили патоген. Но со временем появились бактерии, резистентные сразу к нескольким химически несхожим антибиотикам, что во много раз обострило ситуацию [11]. Более того, за последние 30 лет не удалось открыть никаких новых классов антибиотиков, при этом спектр используемых антибиотиков сужается, а это повышает шансы выработки к ним устойчивости (рис. 2). Чтобы осознать масштаб происходящего, стόит перечислить некоторые заболевания и статистику по ним.
Рисунок 2. Рост бактериальной антибиотикорезистентности отбивает у фармкомпаний желание разрабатывать новые препараты. а — Уже 30 лет ничего не слышно о новых классах антибиотиков. б — По мере увеличения количества резистентных бактерий падает интерес к поиску новых антибиотиков, и число вводимых в клиническую практику препаратов стремится к нулю. Условные обозначения: * — процент клинических изолятов, устойчивых к антибиотикам; MRSA — метициллин-резистентные Staphylococcus aureus; VRE — ванкомицин-резистентные Enterococcus; FQRP — фторхинолон-резистентные Pseudomonas aeruginosa.
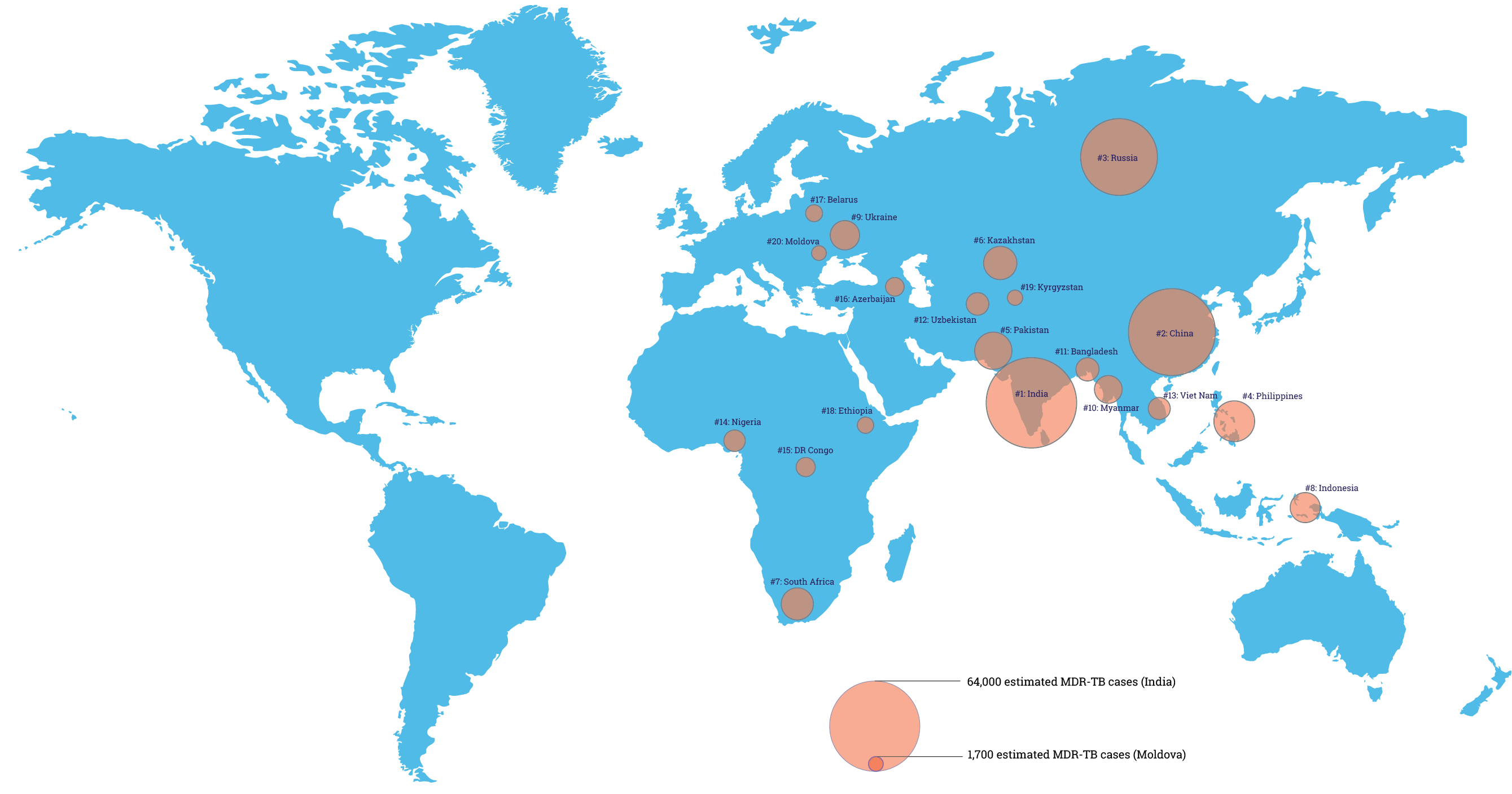
Согласно официальным оценкам, по причине резистентности к антибиотикам и невозможности вылечить различные инфекции в год умирает не менее 700 000 человек. Точно подсчитать число жертв невозможно, так что, увы, на самом деле их намного больше [12]. Особенно тревожной становится ситуация с туберкулезом: в 105 странах циркулируют возбудители, устойчивые сразу к нескольким антибиотикам, а по данным ВОЗ, такие штаммы Mycobacterium tuberculosis в 2014 году были найдены у 480 000 человек. Должен насторожить и побудить к действиям следующий факт: около половины таких случаев приходится на Индию, Китай и Россию (рис. 3) [13].
Рисунок 3. Мировая карта встречаемости мультирезистентного возбудителя туберкулеза. Карта составлена по статистическим данным за 2012 год. Диаметр круга положительно коррелирует с частотой случаев туберкулеза, устойчивого к терапии несколькими антибиотиками.
Для развивающихся стран с тропическим и субтропическим климатом, например Африки, одну из опасностей представляют эпидемии брюшного тифа, виновник которых выдерживает натиск сразу нескольких препаратов.
Всё шире распространяются неподдающиеся антибактериальной терапии инфекции, которые пациент «подхватывает» в больнице (внутрибольничные, или нозокомиальные), проходя лечение по другой причине [14]. Установлено, что у пациентов с метициллин-резистентными Staphylococcus aureus вероятность летального исхода на 64% выше, чем у людей с не резистентными к этому лекарству штаммами золотистого стафилококка [2].
О новом «оружии» в борьбе с золотистым стафилококком написано в статье «Антибиотики прямо под нашим носом» [15].
Всего за год — с 2013 по 2014 — более чем в четыре раза (с 0,6 до 2,5% среди исследованных штаммов) увеличилась устойчивость возбудителя гонореи Neisseria gonorrhoeae к антибиотику азитромицину. Комбинации препаратов — например, того же азитромицина и цефтриаксона — пока что действуют. Но, памятуя о печальном опыте с другими патогенами, уже сейчас необходимо продумывать альтернативные варианты лечения — чтобы быть готовыми к тому моменту, когда гонококк привыкнет и к этим антибиотикам [16]. Ситуация кажется не такой катастрофической по сравнению с другими, поэтому добавлю: в июне этого года Центр по контролю и профилактике заболеваний (CDC) министерства здравоохранения США сообщил, что гонококк перестал поддаваться лечению уже половиной ранее используемых антибиотиков [17].
Этот центр создал замечательную интерактивную карту распространенных в США резистентных штаммов бактерий [18].
Ожесточеннее становится борьба и с микробами-оппортунистами, которые в норме не вызывают болезнь, но для людей с ослабленным иммунитетом могут стать серьезной и даже смертельно опасной проблемой. Несмотря на то, что муковисцидоз — это наследственное заболевание, связанное с поражением желез внешней секреции и накоплением в легких вязкой мокроты (при легочной форме болезни), ему сопутствуют разные инфекции. Раньше, до начала нулевых, существовали детские лагеря для страдающих этим заболеванием, но впоследствии из-за стремительной передачи инфекций и выработки устойчивости к применяемым для лечения антибиотикам было решено отказаться от этой затеи. Пациентам теперь вообще строго не рекомендуется находиться близко друг к другу [19].
Последствия
Пациентов с заболеваниями, вызываемыми резистентными микроорганизмами, часто приходится пролечивать не одним антибиотиком, а их комбинациями, курс длится дольше обычного, что делает лечение довольно затратным и выматывающим. Более того, не всегда оно вообще доступно, поэтому повышается и смертность. Кроме целенаправленного лечения инфекции, под угрозу ставятся и стандартные врачебные вмешательства, которые впоследствии требуют использования антибиотиков — например, некоторые полостные операции или химиотерапия.
Не нужно забывать, что человек — это и биологическое, и социальное существо, и помимо выживания ему необходимо контактировать с другими представителями общества. И здесь возникает на первый взгляд неочевидная проблема: люди с инфекциями или ослабленным иммунитетом не могут полноценно общаться с другими людьми из-за опасности заражения. В пример можно привести упомянутую выше отмену летних лагерей для детей с муковисцидозом, поводом для которой стали вспышки инфекций, вызываемых резистентными штаммами Burkholderia cepacia [20]. Другое вынужденное ограничение — нахождение в отдельных боксах в инфекционных больницах. Получается, что устойчивость микроорганизмов к антибиотикам сильно влияет даже на психологическое состояние человека и его социализацию.
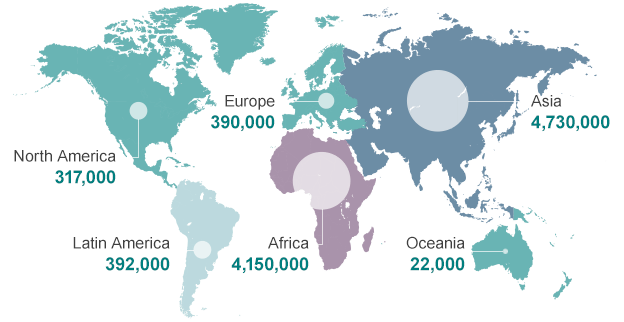
Группа под руководством британского финансиста Джима О`Нила провела подсчет экономических потерь, с которыми столкнется человечество к 2050 году, если всё останется по-прежнему и не получится продвинуться в решении проблемы резистентности. По этому сценарию потери трудоспособного населения к тому времени могут достичь 11–14 миллионов человек в год. В денежном выражении это означает, что кумулятивная потеря будет равна 100 трлн долларов, или средний годовой убыток составит 3 трлн долларов. К слову, весь годовой бюджет США лишь на 0,7 трлн превышает эту цифру (рис. 4) [9].
Рисунок 4. Если мы не сумеем притормозить всё быстрее распространяющуюся антибиотикорезистентность, то к 2050 году именно по этой причине мир будет терять до 10 миллионов человек ежегодно.
Но настоящую цену возникающей резистентности подсчитать нереально.
Что предпринимается для решения проблемы?
Темпы приобретения бактериальной резистентности превышают
мировые темпы открытия новых антибиотиков.
Маргарет Чен, генеральный директор ВОЗ
Как мы уже поняли, проблема резистентности микроорганизмов влияет не только на здравоохранение, но и на экономику государств, а в глобальном масштабе — на сохранение человечества. Микробы не знают государственных границ, поэтому проблема их устойчивости к антибиотикам должна решаться общими усилиями всех стран и как можно быстрее. Нужно не только создавать новые антибиотики, но и вводить ограничения на их продажу и использование, информировать общественность о важности разумного применения антибиотиков, а также пытаться использовать какие-то альтернативные средства. О возможных замещениях антибиотиков можно прочитать, например, в статье «Эволюция наперегонки, или почему антибиотики перестают работать» [6]. Если смотреть с биологической точки зрения, то одним из возможных решений проблемы с катастрофически быстрой выработкой устойчивости к современным противомикробным препаратам могла бы стать фаговая терапия. Однако бактериофаги имеют свои плюсы и минусы, и о них рассказывает статья «Пожиратели бактерий: убийцы в роли спасителей» [21].
Еще одним решением может стать иммунопрофилактика — например, своевременная вакцинация человека и домашних животных, благодаря которой у них вырабатывается собственный иммунитет. Сильный собственный иммунитет не позволяет организму пасовать перед патогенами и смело отражает их нападения. Чем меньше вероятность заболеть у одного, тем меньше вероятность, что он заразит других. Получается, что таким образом каждый вносит свой вклад в борьбу с патогенными микроорганизмами.
А вообще, есть базовые принципы, которых необходимо придерживаться, чтобы не позволять патогенным микроорганизмам распространяться: каждый должен соблюдать гигиену, организации — санитарные нормы, а государство — тщательнее следить за здоровьем населения (например, регулярно проводить диспансеризацию).
Как я уже упоминала в начале, стали появляться такие инициативы, как Глобальный план действий по устойчивости к противомикробным препаратам [3], неделя всемирной обеспокоенности по поводу антибиотиков [4], многолетняя кампания «Антибиотики: используйте осторожно!» [4]. Несомненно, они вносят вклад в информирование общественности и обсуждение новых путей борьбы с резистентностью.
Существуют два глобальных плана действий. Первый сформирован в 2015 году Всемирной организацией здравоохранения [22], а второй, действие которого распространяется на период 2016–2020, разработан в этом году Продовольственной и сельскохозяйственной организацией ООН (FAO) [23]. По многим пунктам они пересекаются. Планируется обеспечивать инвестиции в изучение антибиотикорезистентности, повышать осведомленность об этом явлении, усиливать контроль над развитием устойчивости, предотвращать вспышки инфекций. На сентябрьской сессии Генеральной ассамблеи страны подтвердили, что будут разрабатывать свои внутригосударственные планы, ориентируясь на принятые международные.
Соответствующие локальные мероприятия уже начали проводить. Например, Минздрав России решил ужесточить контроль над продажей антибиотиков, чтобы уменьшить масштаб их применения без врачебного назначения.
Конгресс США заложил в бюджет 2016 года 160 млн долларов, для того чтобы поддержать исследования антибиотикорезистентности и изучение человеческого микробиома [24].
Репозиторий патогенов, имеющих четко охарактеризованные признаки резистентности, был создан в июле 2015 года в США и с тех пор пополнился многими представителями Enterobacteriaceae (включая сальмонелл), Staphylococcus, Enterococcus и Streptococcus [25]. Такой банк данных можно использовать для улучшения диагностики и испытания новых антибиотиков.
Еще совсем недавно у всех на слуху была реклама антибактериального мыла, в которой говорилось, что оно «уничтожит всех микроорганизмов на ваших прекрасных руках». Рекламодатели не уточняли, для чего нужно уничтожать их всех, включая представителей нормальной кожной микробиоты. Но в сентябре 2016 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) наконец вынесло предписание о запрете с осени 2017 года продажи на территории США повседневных моющих средств с 19 антибактериальными компонентами, включая самые распространенные — триклозан и триклокарбан [26].
Во время осенней сессии Генеральной ассамблеи ООН генеральный директор FAO Жозе Грациану да Силва сказал: «Резистентность бактерий к антибиотикам — это проблема не только больниц и госпиталей, но и ферм, и нашего продовольствия. Сельское хозяйство должно взять на себя ответственность более аккуратно использовать антимикробные препараты и уменьшать их применение за счет хорошо поддерживаемой гигиены» [27]. И шаги в этом направлении уже предпринимаются.
В Великобритании было решено сократить использование антибиотиков в сельском хозяйстве на 20% [28]. Там же главы нескольких королевских медицинских колледжей и двух журналов о здоровье направили правительству письмо с призывом вообще запретить применение антибиотиков в животноводстве без надобности. Но у этого шага могут быть свои «недостатки» — придется тщательнее следить за здоровьем животных и проводить вакцинирование, в то время как добавлять антибиотики в корм проще и дешевле [29].
Заключение
Резистентность микроорганизмов к антибиотикам — серьезная и сложная проблема, которая затрагивает каждого человека. Немало решений было предложено и немало действий уже совершено на мировом и государственном уровнях, чтобы обуздать этот опасный феномен. Но еще больше только предстоит сделать. Стратегия борьбы с антибиотикорезистентностью не ограничивается сокращением использования антибиотиков и ужесточением норм их применения в медицинских целях. Она включает и информирование общественности о проблеме в целом — чтобы люди хотя бы немного понимали, почему всё это так важно и чем это грозит. И задача правительств и мировой общественности — обеспечить необходимые условия для подобных просветительских инициатив. Только так, с полным осознанием смысла и целей своих усилий, мы сможем хоть как-то продвинуться в решении проблемы антибиотикорезистентности.