неоперабельная аневризма головного мозга что это
Что такое аневризма сосудов мозга? Причины возникновения, диагностику и методы лечения разберем в статье доктора Фомина Б. Б., нейрохирурга со стажем в 13 лет.
Определение болезни. Причины заболевания
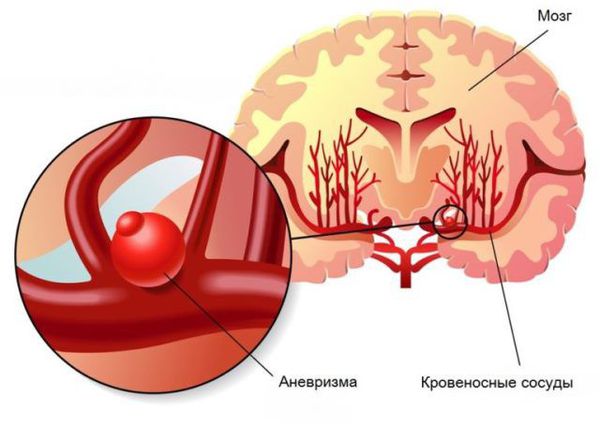
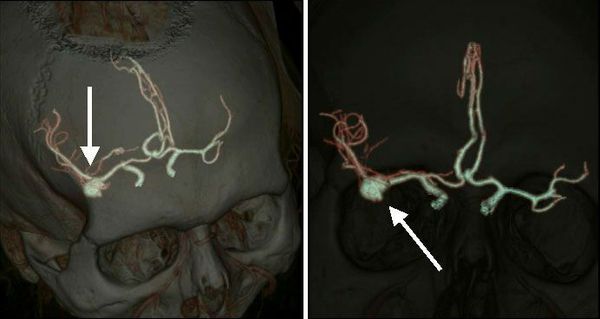
Аневризма артерий головного мозга (церебральная, внутричерепная аневризма) — это деформация церебральных артерий в виде выпячивания их стенки в месте истончения.
Артериальные аневризмы могут формироваться и на других артериях человеческого организма:
Венозные и капиллярные аневризмы не рассматриваются, так как они редко встречаются и менее опасны.
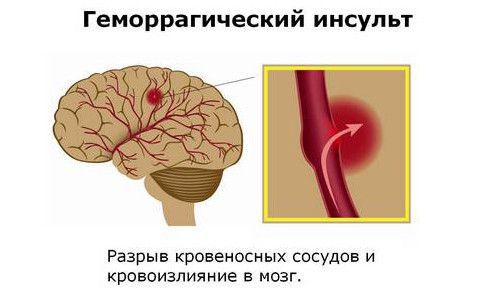
Особенностью аневризм сосудов головного мозга является то, что при их разрыве возникает внутричерепное кровотечение, повреждающее структуры головного мозга. Такие факторы, как замкнутое костями внутричерепное пространство, колоссальная функциональная значимость и одновременно с этим высокая ранимость мозговой ткани, обуславливают тяжесть состояния пациентов с разрывом церебральных аневризм.
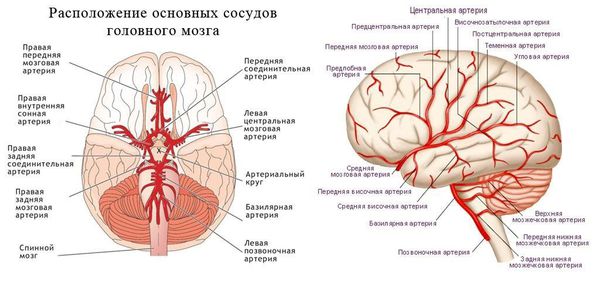
Аневризмы возникают преимущественно в местах ветвления (развилок) и изгибов артерий. Это связано с повышенным гемодинамическим воздействием постоянного тока крови на эти участки сосудов. Как говорится, «где тонко, там и рвётся». Но пусковым моментом развития аневризм сосудов головного мозга является неполноценность артериальной стенки. Она может быть связана с врождёнными аномалиями соединительной ткани. Аномалии могут быть как самостоятельными, так и ассоциированными с различными патологиями:
Насколько распространена аневризма головного мозга
Беременность при аневризме сосудов головного мозга
Физиологически и клинически беременность у пациенток с аневризмой сосудов головного мозга протекает без особенностей, так как «носительство» аневризмы никак не влияет на течение самой беременности. Но, как и у любого пациента с данной патологией, риск разрыва аневризмы сохраняется. Поэтому беременным женщинам с аневризмой требуется тщательное наблюдение и обследование с целью предупредить угрожающий здоровью и жизни пациентки и плода разрыв аневризмы, вовремя принять тактическое решение (оперировать во время беременности или уже после родоразрешения).
С учётом гормональных изменений в организме беременной женщины, в том числе, влияющих на работу сердечно-сосудистой системы (изменение тонуса сосудов, колебания артериального давления и т. д.), риск разрыва аневризмы может быть выше, чем у небеременных женщин. Следует обратить внимание на артериальное давление (особенно на резкие колебания цифр систолического давления), вести дневник учёта артериального давления. Пациенткам с выявленной аневризмой обычно рекомендуется выключить аневризму из кровотока (операция, после которой кровь перестает поступать в саму аневризму, при этом не нарушается кровоток по остальным сосудам) до планирования беременности. В случае если аневризма диагностирована уже во время беременности, пациентка обязательно консультируется и наблюдается у нейрохирурга. Решение об операции принимается индивидуально (оценивается локализация, размеры, форма аневризмы, риски её разрыва). В случае принятия решения не оперировать аневризму во время беременности, родоразрешение проводится только путём кесаревого сечения.
Симптомы аневризма сосудов мозга
В подавляющем большинстве случаев до разрыва аневризмы не проявляются специфической симптоматикой. «Немые» (т. е. нервавшиеся аневризмы) выявляются случайно, например, когда врач-невропатолог направляет пациента на обследование по поводу частых приступов головной боли для исключения внутричерепной патологии: опухоли, аномалии развития и т. д. У пациентов с «немыми» аневризмами могут отмечаться жалобы на эпизодические головокружения, головную боль, снижение работоспособности и когнитивных функций (реже).
Если аневризма разорвалась, клиническая картина представлена внезапной, резчайшей головной болью, словно по голове разлился кипяток или «вонзили кинжал»; многократной рвотой, не приносящей облегчения; повышением температуры тела до 37-38 о С; ознобом; утратой сознания; судорогами.
В зависимости от локализации, размера аневризмы и калибра несущей артерии, объём кровоизлияния бывает различным. В связи с этим симптоматика тоже может быть разной: от слабо выраженной в виде умеренной головной боли, нечёткости зрения, двоения в глазах, нарушения координации, изменения чувствительности лица и частей тела, до очень яркой — угнетение сознания, вплоть до комы, судорог, нарушения витальных функций (угнетения деятельности сердечно-сосудистой и дыхательной систем).
Патогенез аневризма сосудов мозга
Основные моменты в формировании церебральных аневризм упоминались ранее — неполноценность сосудистой стенки, постоянное воздействие гемодинамического удара потока крови, влияние факторов, способствующих повреждению и быстрому «износу» сосудов. Остановимся на процессах, происходящих при разрыве аневризмы.
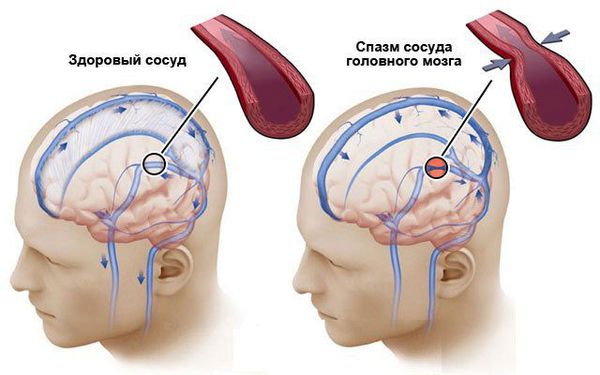
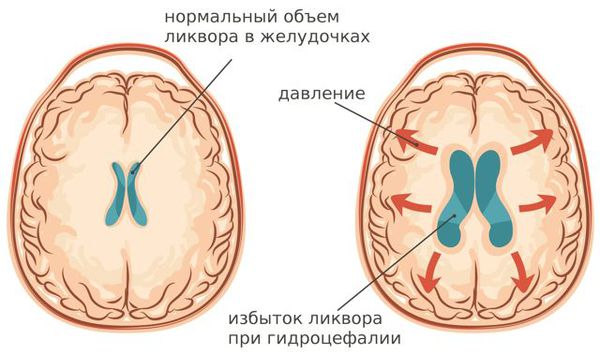
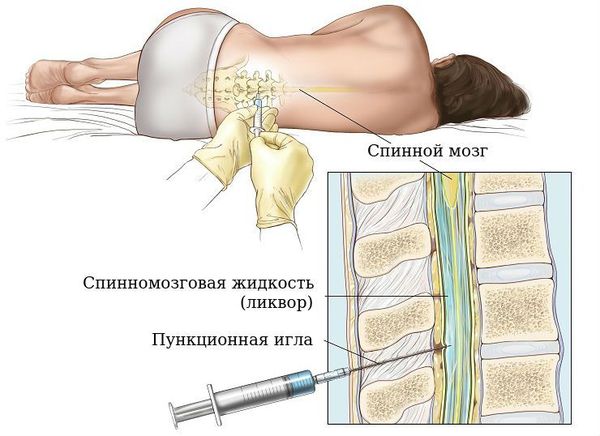
В субарахноидальном пространстве (между паутинной и мягкой оболочками мозга) в норме циркулирует прозрачная бесцветная спинномозговая жидкость — ликвор. Появление крови в этом пространстве приводит к повышению объёма ликвора, вследствие чего повышается внутричерепное давление. Также происходит механическое раздражение рецепторов и нервных стволов артерий головного мозга, что влечёт за собой развитие кратковременного сужения (спазма) мозговых артерий. Это объясняет снижение кровоснабжения головного мозга в первые часы после начала разрыва аневризмы. Как правило, это не приводит к ишемии (омертвлению) участков мозга.
Если пациент выживает, то в последующем у него развивается иммунореактивный воспалительный процесс, затрагивающий стенки артерий, формируются арахноидальные спайки (сращения), кисты, участки глиоза (рубцы на месте омертвевшей мозговой ткани). Все эти процессы нарушают нормальную работу головного мозга, приводят к разобщению функций повреждённых областей. Развивается стойкий неврологический дефицит:
Классификация и стадии развития аневризма сосудов мозга
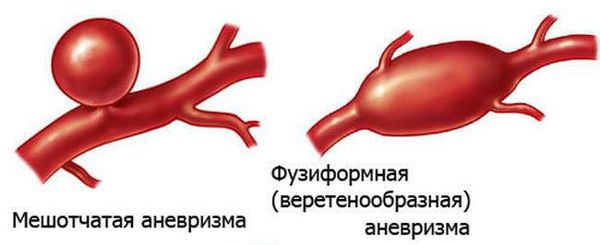
По форме выпячивания стенки сосуда выделяют мешотчатые, веретенообразные (фузиформные) и пузыреобразные аневризмы. Первая разновидность встречается в подавляющем большинстве случаев (50:1) по отношению к другим вариантам.
По величине выделяют аневризмы:
Аневризмы могут иметь один мешок или дополнительные выпячивания (дивертикулы).
По локализации церебральные аневризмы разделяются в зависимости от несущей артерии:
Шкала комы Глазко позволяет оценить степень нарушения сознания — от умеренного оглушения до запредельной комы. Шкала Hunt&Hess даёт представление о тяжести состояния больного с САК на основании выраженности клинической симптоматики и неврологических нарушений — от 1 до 5 баллов. Шкала Fisher позволяет оценить риски развития вазоспазма, основываясь на количестве крови в подоболочечных пространствах головного мозга при САК (определяется при компьютерной томографии).
Стадии САК:
Осложнения аневризма сосудов мозга
Осложнения аневризматического ОНМК могут иметь различную степень тяжести. Они зависят от калибра несущей аневризму артерии, её функциональной значимости в кровоснабжении мозга и объёма кровоизлияния. Самое угрожающее осложнение из всех — повторный разрыв аневризмы. Происходит он, как правило, в первые несколько дней после первого разрыва, когда сгусток в области дефекта аневризмы еще «рыхлый» и легко размывается потоком крови, зачастую под повышенным давлением. В 70-80 % случаев это осложнение является фатальным. Небольшой процент пациентов, переживших неоднократные разрывы церебральных аневризм — глубокие инвалиды с грубыми неврологическими нарушениями.
Диагностика аневризма сосудов мозга
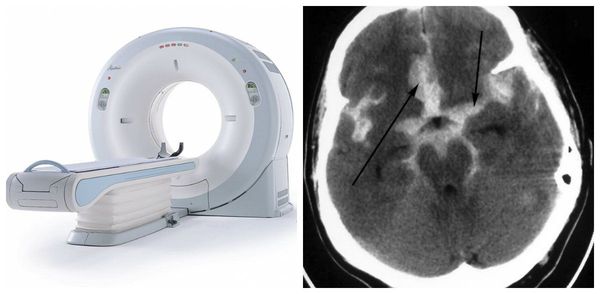
В связи с доступностью, высокой скоростью обследования, специфичностью и чувствительностью метода, КТ предпочтительнее МРТ. МРТ в режиме ангиографии (МРА сосудов головного мозга) весьма полезна в плановых ситуациях, когда врачи только подозревают у пациента наличие сосудистой патологии головного мозга.
При выявлении признаков САК проводят ангиографическое обследование:
Перечисленные методы инструментальной диагностики дают исчерпывающую информацию о локализации, форме и размерах аневризмы. Также исследования позволяют оценить анатомию артерий в области выявленной патологии для последующего планирования хирургической тактики. Для осмотра рассматриваемой категории пациентов обязательно привлекается нейрохирург, при тяжёлом состоянии больного — реаниматолог.
Для оценки степени выраженности спазма церебральных артерий назначается ультразвуковое сканирование сосудов шеи и головы. Это обследование позволяет прогнозировать ранние осложнения церебрального ангиоспазма и корректировать терапию.
Лечение аневризма сосудов мозга
Имея представление о выпячивании стенок церебральных артерий, логично предположить, что главным принципом лечения аневризмы головного мозга является её выключение из общего кровотока. Звучит довольно просто: перекрыть просвет аневризмы, устранив таким образом угрозу разрыва. Но в действительности всё намного сложнее.
Сосуды головного мозга находятся глубоко в черепе, делясь на ветки, проникают в мозг и окутывают его поверхность. В сочетании с высокой функциональной значимостью церебральных артерий этот фактор значительно осложняет и порой делает невозможным полное выключение аневризмы, особенно при сложных формах аневризматического мешка.
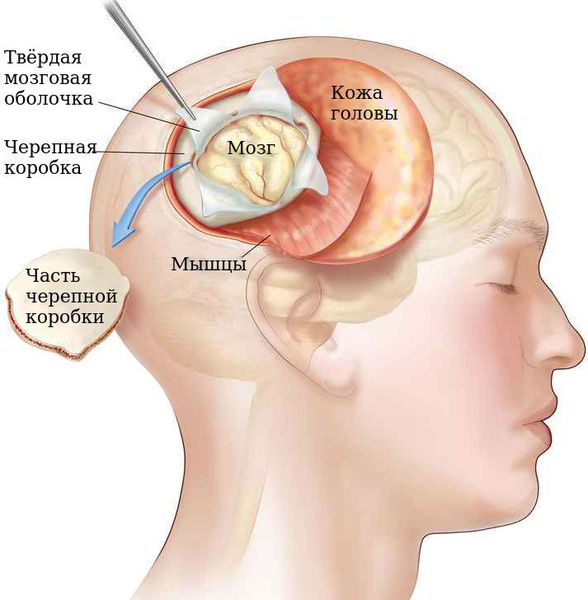
Существуют два принципиально разных метода хирургического лечения пациентов с аневризмами церебральных артерий: открытый или прямой (т. е. через трепанацию черепа) и эндоваскулярный (изнутри артерии под рентген-контролем). Оба варианта имеют свои преимущества и недостатки.
Проникая в полость черепа, нейрохирург с помощью операционного микроскопа и микроинструментов вскрывает оболочки мозга, опорожняет субарахноидальные цистерны (участки расширения субарахноидального пространства в области расхождения паутинной и мягкой мозговых оболочек), вымывая оттуда ликвор вместе со сгустками крови. В результате этого уменьшается степень выраженности и распространённости вазоспазма.
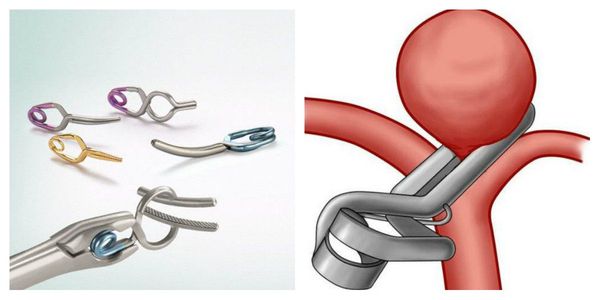
В последующем освобождаются пути ликворотока, что уменьшает риски развития гидроцефалии. Затем начинается деликатная диссекция (обнажение) мозговых артерий и поэтапный подход к аневризме по артерии, на которой она расположена. В случае мешотчатой конфигурации аневризмы выделяется её шейка (т. е. самое основание). Завершающим этапом операции является наложение сосудистого клипса, который пережимает просвет аневризмы и прекращает в ней ток крови. Сосудистые клипсы сделаны из сплава медицинского титана, они представляют собой зажимы, подобные маленьким прищепкам.
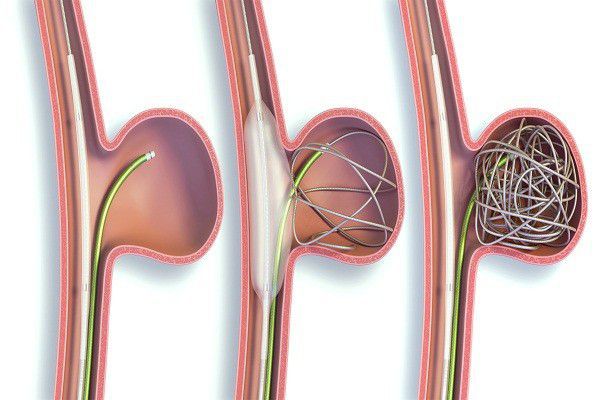
При эндоваскулярном методе пунктируется (прокалывается) бедренная артерия, в неё устанавливается интродьюсер (порт), через который вводятся проводники для дальнейшего продвижения их точно к месту расположения аневризмы. На всех этапах такой операции в артерию подаётся рентгенконтрастное вещество, благодаря чему на экране ангиографа (специального рентген-аппарата) контролируется положение проводников и анатомия артерий. Достигнув аневризмы, рентген-ангиохирург вводит в просвет аневризматического мешка платиновые микроспирали, которые, скручиваясь, формируют клубок и плотно заполняют аневризму. Также при таких операциях используются сосудистые стенты, зафиксированные на баллонах. Стент фиксируется внутри сосуда и «выключает» аневризму из кровотока, принимая на себя давление крови.
Преимущества этого вида хирургического лечения:
Лекарства
Медикаментозного лечения аневризмы сосудов головного мозга не существует. Аневризма — это в большинстве случаев мешковидное выпячивание стенки сосуда. Каким-либо из препаратов устранить этот дефект стенки не представляется возможным. Другое дело, проводить мероприятия по снижению риска разрыва аневризмы (проводить адекватное лечение гипертонической болезни, исключить вредные привычки, наблюдаться у специалистов, проводить контрольные обследования и т. д.).
Принципы оказания первой помощи при разрыве аневризмы
В случае возникновения у человека симптоматики субарахноидального кровоизлияния (которая описывалась ранее), следует незамедлительно вызвать бригаду скорой медицинской помощи и кратко описать оператору основные симптомы. Во время ожидания приезда скорой больного необходимо уложить на ровную поверхность в положении с приподнятой на 30 градусов верней частью тела (чтобы голова была выше уровня сердца) — для улучшения венозного оттока от головного мозга. Также следует обеспечить максимальный приток кислорода (освободить дыхательные пути, расстегнуть одежду). На область проекции сонных артерий (передне-боковая поверхность шеи) приложить холод (любые имеющиеся под рукой охлаждённые предметы, в т.ч. из холодильника) – для обеспечения рефлекторного сужения сосудов и ускорения процессов свёртывания крови. Если больной без сознания и возникла рвота, повернуть его на бок и предотвратить попадание рвотных масс в дыхательные пути.
Можно ли полностью вылечить аневризму сосудов головного мозга
Современные методы хирургического лечения аневризм головного мозга (как эндоваскулярные, так и прямые хирургические операции) в подавляющем числе случаев позволяют добиться полного выключения аневризмы из кровотока.
Реабилитация после операции
Реабилитация пациентов, перенесших операцию по выключению аневризмы сосудов головного мозга, проводится в различном объёме и зависит это от того в остром периоде кровоизлияния или вне разрыва оперирован больной, имелись ли осложнения во время операции или в раннем операционном периоде.
В зависимости от выраженности неврологических нарушений (расстройства речи, нарушения двигательной сферы и т.д.), назначаются занятия с логопедом, с инструктором ЛФК, массажистом и т. д. Одновременно с этими мероприятиями, как правило, назначаются медикаментозные препараты из группы ноотропов, сосудисто-метаболический комплекс с целью обеспечения максимального улучшения и восстановления утраченных функций головного мозга.
Может ли аневризма сосудов головного мозга развиться повторно
К сожалению, даже после успешно выполненной операции по выключению аневризмы сосудов головного мозга из кровотока есть риск возникновения новой аневризмы в том же месте. Это связано с тем, что стенка сосуда, на котором образовалась аневризма порой изменена не только в области самого выпячивания (аневризмы), а имеет неполноценную структуру в смежных к аневризме отделах. Также имеет значение степень выключения аневризмы во время операции, т. к. сохранение даже небольшого фрагмента шейки аневризмы может в последующем привести к формированию выпячивания в этом заведомо слабом месте сосуда.
Применяются ли народные средства
Народные средства для лечения аневризмы головного мозга неэффективны. Отсутствие своевременного адекватного лечения при разрыве аневризмы может привести к смерти пациента.
Прогноз. Профилактика
В 15-25 % случаев субарахноидальное кровоизлияние заканчивается смертельным исходом в первые сутки после разрыва аневризмы. Летальность в первый месяц у больных САК достигает 30 %. В первые две недели после разрыва у 15-20 % пациентов аневризма рвётся вновь. В первые полгода с момента САК повторный разрыв аневризмы происходит у 50 % больных с летальностью до 60-80 %. У выживших пациентов зачастую сохраняется грубый неврологический дефицит: речевые, двигательные, чувствительные, координаторные и когнитивные расстройства.
Наиболее благоприятен прогноз в случаях, когда аневризма выявлена до разрыва и есть возможность проведения операции по её закрытию в плановом порядке. Смертность и частота серьёзных осложнений в таком случае не достигает 1-2 %.
Все профилактические мероприятия при данной патологии можно разделить на две группы: профилактика образования аневризм и профилактика их разрыва. Лучшая профилактика разрыва аневризмы — раннее выявление и своевременное лечение этой патологии.
Лечение неразорвавшихся аневризм головного мозга
Общая информация
Краткое описание
Ассоциация нейрохирургов России
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ЛЕЧЕНИЮ НЕРАЗОРВАВШИХСЯ АНЕВРИЗМ ГОЛОВНОГО МОЗГА (Москва, 2015)
Клинические рекомендации утверждены на Пленуме Правления Ассоциации нейрохирургов России 14.10.2015 г. Красноярск
Введение
В последние годы число обращений пациентов с неразорвавшимися аневризмами (НА) в нейрохирургические учреждения неуклонно возрастает. Опубликованные в зарубежной литературе серии по анализу этой патологии содержат до нескольких сотен, а кооперативные исследования – до нескольких тысяч больных.
Учитывая, что неразорвавшиеся аневризмы потенциально могут стать источником внутричерепного кровоизлияния, возникла необходимость определения тактики ведения и лечения этих больных. Единой точки зрения по этому вопросу не существует, хотя в последние годы рекомендации различных клиник все более совпадают по различным позициям и становятся более конкретными. Основной проблемой при выявлении неразорвавшейся аневризмы является оценка вероятного риска ее разрыва. Несмотря на опубликованные незначительные показатели первичных кровоизлияний из ранее неразорвавшихся аневризм [28, 75, 90], существуют группы больных с высоким риском разрыва аневризм. К таким факторам риска относят как морфологические особенности выявленной аневризмы (несколько куполов, неровность тела аневризмы, соотношение размера аневризмы к диаметру несущего сосуда, расположение, большой и гигантский размеры, увеличение размеров аневризмы с течением времени и т.д.), так и семейный анамнез кровоизлияния из аневризмы, наличие ряда вредных привычек, таких как курение, присутствие сопутствующих заболеваний (артериальная гипертензия). Существенное увеличение пациентов с диагностированными неразорвавшимися аневризмами в РФ и накопление значительного опыта хирургического лечения этой патологии явилось обоснованием для создания российского рекомендательного протокола по ведению и лечению больных с НА.
Этиология и патогенез
В настоящее время этиология и патогенез НА рассматриваются в рамках этиологии и патогенеза аневризм в целом. Факторы, лежащие в основе заболевания, принято делить на немодифицируемые и модифицируемые. К первым относят: генетические факторы [12, 26, 100]; ряд наследственных заболеваний [4, 9, 13, 19, 21, 84, 85, 99, 106, 120]; возраст и пол [6, 30, 31, 35, 40, 41, 62, 66, 71, 97, 103, 114, 115]. Во вторую группу входят: артериальная гипертония, курение, алкоголь, лекарства и вещества с симптомиметическим действием, пероральные контрацептивы [31, 32, 36, 45, 52, 53, 114]. Доказательность степени влияния этих факторов на формирование аневризм, в том числе, неразорвавшихся, различна.
Эпидемиология
Факторы и группы риска
Группы повышенного риска выявления НА
Пол и возраст
Частота выявления НА увеличивается с возрастом, достигая максимума в возрастной группе от 50 до 60 лет. Чаще аневризмы выявляются у женщин, в независимости от возрастной категории [6, 30, 31, 35, 40, 41, 62, 66, 71, 97, 103, 114, 115].
Сопутствующие заболевания
Пациенты с перечисленными ниже заболеваниями входят в группу повышенного риска обнаружения неразорвавшихся аневризм [4, 9, 13, 19, 21, 84, 85, 99, 106, 120]:
— аутосомно-доминантный поликистоз почек (частота обнаружения аневризм в 3-14 раз выше по сравнению с основной популяцией)
— синдром Элерса-Данло IV типа
— синдром Марфана
— коарктация аорты
— двустворчатый аортальный клапан
— эластическая псевдоксантома
— наследственная геморрагическая телеангиэктазия
— нейрофиброматоз 1 типа
— недостаточность α1-антитрипсина
— фиброзномышечная дисплазия
— феохромацитома
— сидром Кляйнфельтера
— туберозный склероз
— Синдром Нунан (наследственное сочетание стеноза клапанов лёгочной артерии, гипертелоризма, оттопыренных ушных раковин и др. нарушений)
— недостаточность α-глюкозидазы
— первичная карликовость с микроцефалией и остеодисплазией
— внутричерепные артериовенозные мальформации
«Семейные аневризмы»
По данным различных исследований [9, 55, 56, 76-78, 83, 86, 94] частота встречаемости «семейных аневризм» составляет от 7 до 20% в зависимости от различных методов оценки семейного анамнеза и анализа полученных данных. Чаще выявляют неразорвавшиеся аневризмы среди родственников первого поколения пациента с разрывом аневризмы – около 4% [74, 94], с некоторой большей встречаемостью среди сибсов пациента, чем среди его детей.
К факторам, повышающим вероятность обнаружения аневризмы среди родственников больного, перенесшего САК, относят следующие: старший возраст, женский пол, курение, наличие в анамнезе гипертонической болезни, гиперхолестеринемия, семейный анамнез поликистозной болезни почек, семейный анамнез наличия САК или аневризмы у 2 и более родственников [74]. Частота выявления неразорвавшихся аневризм у родственников первой степени родства при наличии в анамнезе аневризм и/или САК у 2 и более членов их семей составляет от 8,7% [76] до 19,1% (старше 30 лет, наличие таких отягощающих факторов, как курение и гипертоническая болезнь) [9].
Риск разрыва аневризмы
Таблица 1. Риск разрыва НА в зависимости от ее размера и локализации (по данным ISUIA [114]).
| Пятилетний кумулятивный риск разрыва в соответствии с размером и расположением аневризмы | |||||
| 7-12 мм | 13-24 мм | 25 мм | |||
| Группа 1 | Группа 2 | ||||
| Кавернозный отдел ВСА (n=210) | 0 | 0 | 0 | 3.0% | 6.4% |
| ПСА и ПМА/СМА/ВСА | |||||
(n=1037)
средняя мозговая артерия, ВСА – внутренняя сонная артерия, ВББ – вертебробазилярный бассейн, ЗМА – задняя мозговая артерия, ЗСА – задняя соединительная артерия
Группа 1 – пациентов без САК
Группа 2 – пациенты с САК в анамнезе при разрыве другой аневризмы
Предрасполагающие факторы риска разрыва аневризмы
Рост аневризмы
К факторам, ответственным за рост аневризм с течением времени, относят повышенное АД, гемодинамический стресс в зависимости от формы аневризмы и ее расположения, изначальный размер аневризмы, воспаление в стенке аневризмы, женский пол, курение, молодой возраст, избыточное употребление алкоголя. Отмечается повышенный риск роста аневризм у пациентов с наличием инсульта или транзиторной ишемической атакой в анамнезе, и при выявлении множественных аневризм [39, 58, 89].
Проспективное исследование, проведенное в США и включавшее пациентов с аневризмами диаметром менее 7 мм и без наличия САК в анамнезе (всего 319 аневризм) не зафиксировало ни одного разрыва аневризмы за период наблюдения в течение 2,4 лет. Однако за период наблюдения был отмечен рост аневризмы как минимум на 0,75 мм у 5,4% пациентов в течение года [10].
Отмечено, что ежегодный риск разрыва «растущей» аневризмы может превышать данный показатель у аневризмы без роста в 12 раз [58, 71, 104].
Морфологические параметры и локализация
Наибольшая частота кровоизлияний характерна для аневризм в вертебробазилярном бассейне, в области ПСА и перикаллезной артерии [111,121]. Аневризмы в области СМА менее подвержены риску разрыва.
Больший риск разрыва аневризмы отмечают при выявлении следующих морфологических параметров: больший размер, неправильная форма и/или наличие дивертикулов, узкая шейка аневризмы, соотношение максимального размера аневризмы к диаметру несущей артерии более 2,05, соотношение высоты аневризмы к диаметру шейки более 1,6 [47, 80, 111, 121].
Другие факторы
Факторами риска разрыва НА являются молодой возраст, курение, артериальная гипертензия, женский пол, наличие в анамнезе САК из другой аневризмы, семейный анамнез САК [10, 61].
Клиническая картина
Cимптомы, течение
НА наиболее часто определяются в ходе обследования больных после кровоизлияния из другой аневризмы, а также при наличии у больного неврологической симптоматики или возникновения внезапной головной боли или изменения ее характера. В исследовании ISUIA неразорвавшаяся аневризма была выявлена у пациентов в ходе обследования по поводу кровоизлияния из другой аневризмы (30.4%), головной боли (23.7%), ТИА или ОНМК по ишемическому типу (10.5% и 10.6% соответственно), поражения черепных нервов (8.0%), судорожных припадков (2.9%), появления симптомов объемного образования головного мозга (2.7%), субдуральной или внутримозговой гематомы (1.2%), опухоли головного мозга (0.8%), демиелинизирующих заболеваний головного мозга (0.4%) и неопределенных “приступов” (7.1%) [114].
Характер проявления НА влияет на естественное течение заболевания и на выбор тактики лечения. Отмечено, что среди неразорвавшихся симптомных аневризм риск кровоизлияния в 4 раза выше по сравнению с асимптомными, случайно выявленными, аневризмами [111].
Диагностика
Диагностика
Возможности методов нейровизуализации аневризм резко расширились в последнее десятилетие, включая применение дигитальной субтракционной ангиографии в 2D и 3D режимах, МР-ангиографии и КТ-ангиографии.
После выявления неразорвавшейся аневризмы необходимо оценить ее анатомические особенности (и, что возможно будет доступно в широкой практике в будущем, гемодинамические параметры) как при первичном исследовании, так и при обследовании в динамике для определения дальнейшей тактики лечения [22, 63, 122].
Методы обследования
Компьютерная томография в ангиографическом режиме (КТ-ангиография)
Чувствительность, специфичность и точность КТ-ангиографии в диагностике аневризм составляет 96.3%, 100% и 94.6% соответственно. При милиарных аневризмах размером менее 3 мм эти показатели составляют 81.8%, 100% и 93.3% соответственно [108].
При проведенном в 2003 мета-анализе 21 исследования, включавших 1251 пациентов, выявлено, что чувствительность и специфичность КТ-ангиографии составляет 93.3% и 87.8% соответственно в сравнении с цифровой церебральной ангиографией [14]. Выполнение КТ-ангиографии позволяет оценить наличие кальцификатов в стенке аневризмы и тромбов в ее полости [70]. Однако 3D-реконструкция может не совсем точно отражать истинную анатомию и размеры шейки/купола/несущего сосуда, особенно при аневризмах малых размеров (менее 5 мм) [29].
Дигитальная субтракционная ангиография (ДСА)
ДСА остается «золотым стандартом» в диагностике аневризм, особенно с введением в рутинную практику 3D-ротационной ангиографии, для выявления аневризм менее 3 мм и сосудов малого диаметра (в том числе, перфорирующих артерий) [20, 29, 46, 60, 91, 95, 101, 102, 116]. ДСА не может быть использована как скриннинговое исследование в связи с необходимостью госпитализации пациентов и наличием вероятных осложнений при проведении манипуляции, таких как аллергическая реакция на контраст, ОНМК по ишемическому типу, разрыв аневризмы, повреждение артерии, гематома в области пункции артерии и другие [34, 82]. Количество осложнения при проведении ДСА, включая постоянный неврологический дефицит у пациентов с аневризмами, САК и АВМ, не превышает 0.07% [17].
Проведение ДСА нецелесообразно [рекомендация] у пациентов с аутосомно-доминатным поликистозом почек, почечной недостаточностью, синдромом Элерса-Данло.
Анализ изображений [рекомендации]
При выявлении аневризмы, независимо от того, какой метод использовался, необходимо определить ряд параметров для уточнения тактики лечения и проведения динамического наблюдения. Необходимо оценить размеры шейки аневризмы, соотношение диаметра купола к диаметру шейки, угол расположения аневризмы относительно несущего сосуда (для латеральных аневризм), соотношение максимального размера купола к диаметру несущего сосуда, размеры аневризмы в 3 плоскостях [63].
Скриннинг
Определенные группы в популяции, имеющие повышенный риск обнаружения аневризм головного мозга, подлежат проведению скрининга. Пациент перед проведением обследования должен быть информирован о возможных последствиях как проведения самого исследования, так и различных видов лечения или консервативного лечения, включая такие психологические факторы, как стресс и тревогу, если аневризма будет обнаружена. Учитывая данные эпидемиологических исследований, можно рекомендовать проводить неинвазивные методы скрининга каждому человеку в общей популяции после 30 лет в независимости от наличия или отсутствия факторов риска обнаружения аневризмы. Если при первом обследовании данных за аневризму не обнаружено, повторное обследование можно рекомендовать по достижении 50 лет.
Лечение
Хирургическое лечение пациентов с неразорвавшимися аневризмами
Отбор пациентов с неразорвавшимися аневризмами на операцию [рекомендации]
Проведение операции по поводу НА сосудов головного мозга показано при наличии одного и/или нескольких следующих факторов риска разрыва аневризмы:
• размер аневризмы 7 и более мм
• несферическая форма и наличие дивертикулов
• латеральное расположение аневризмы
• коэффициент соотношения высоты купола аневризмы к диаметру шейки аневризмы более 1,6
• коэффициент соотношения максимального размера аневризмы к диаметру несущего сосуда более 2,05
• угол отклонения латеральной аневризмы от несущей артерии более 1120
• рост размера аневризмы на 0,75 мм и более в течение 6 месяцев
• появление новых клинических проявлений (симптомы поражения черепных нервов, появление и/или изменение характера головных болей, ишемические нарушения в бассейне несущей аневризму артерии)
• незамкнутость артериального круга большого мозга
• «перианевризматическое» окружение – контакт аневризмы с ТМО, костями черепа, черепными нервами, артериями и венами
• множественные аневризмы
• наличие в анамнезе кровоизлияния из другой аневризмы
• курение
• артериальная гипертензия
При выявлении у больного НА размерами 3 мм и менее хирургическое лечение не показано, больному необходимо проведение динамического наблюдения с повторными обследованиями через 6, 12 месяцев и затем каждые 2 года [стандарт]. Подобному же наблюдению подлежат пациенты, отказавшиеся от хирургического лечения [стандарт].
При выявлении аневризм размерами от 3 до 7 мм необходимо измерение морфологических параметров аневризмы, вопрос о проведении хирургического лечения принимается индивидуально с учетом факторов риска (возраст, пол, наличие в анамнезе курения, гипертонической болезни, наличие «семейного» анамнеза, наличие генетических заболеваний) [рекомендации].
Больной с НА должен быть информирован о характере болезни, возможных вариантах течения, возможных осложнениях хирургического вмешательства [стандарт].
Обследование в нейрохирургическом стационаре [рекомендации]
После поступления больного в специализированный нейрохирургический стационар, помимо общих клинических исследований, необходимо провести:
— подробный неврологический осмотр;
— КТ-АГ или МР-АГ головного мозга при поступлении в том случае, если: с момента предыдущего исследования прошло более 6 месяцев; отмечено изменение в неврологическом статусе больного за время с момента выявления аневризмы до госпитализации; качество ранее выполненных КТ и/или МРТ низкое.
— проведение ДСА (в 2D и 3D режимах) показано пациентам со «сложными» аневризмами для оценки их морфологических особенностей и выбором тактики хирургического лечения; также больным с аневризмами размерами менее 7 мм для оценки их морфологических параметров и уточнения рисков разрыва.
Хирургические вмешательства у пациентов с неразорвавшимися церебральными аневризмами [рекомендации]
1) Микрохирургическое лечение:
— пациенты в возрасте до 60 лет
— аневризмы доступной локализации
— аневризмы большого и гигантского размера, оказывающие объемное воздействие на окружающие структуры
— частично тромбированные аневризмы
— при необходимости выполнения комбинированных (микрохирургическое выключение аневризмы из кровотока и реваскуляризирующие вмешательства) операций.
2) Эндоваскулярное лечение:
— пациенты в возрасте старше 60 лет
— локализация аневризм в вертебробазилярном бассейне, в области кавернозного отдела или офтальмического сегмента ВСА
— наличие декомпенсированных соматических заболеваний
Интраоперационный контроль эффективности прямого хирургического вмешательства [рекомендации]
Для подтверждения радикальности клипирования аневризмы и состоятельности кровотока по несущей артерии и функционально значимым ветвям выполняют следующее:
— пункция аневризмы и/или вскрытие просвета аневризмы
— визуальная оценка области клипирования (через микроскоп и/или эндоскоп)
— контактная интраоперационной допплерографии/флуометрия
— интраоперационная ангиография с использованием индоцианина зеленого
Оценка результатов операции и исходов лечения больных, динамическое наблюдение за пациентами после выключения аневризмы из кровотока
Окончательную оценку исходов проводят в сроки не ранее 6 месяцев после операции. Более раннюю оценку (при выписке больного) выполняют как промежуточный этап. Оценку исходов лечения проводят по шкале исходов Глазго.
Пациентам с оперированными церебральными аневризмами, вне зависимости от типа хирургического вмешательства, необходимо проведение контрольных обследований для исключения повторного заполнения аневризмы, оценки остаточной заполняющейся части аневризмы, а также для выявления аневризм de novo [63] [стандарт].
Для проведения динамического наблюдения за пациентами после операции возможно выполнение МР-ангиографии, КТ-ангиографии или ДСА.
Несмотря на то, что применение МР-ангиографии и КТ-ангиографии ограничивается наличием возможных артефактов от металлических имплантов, таких как клипсы, стенты и спирали, эти методы остаются достаточно эффективными для послеоперационного контроля [1, 2, 48, 88, 92]. Напряженность поля при выполнении контрольной МР-ангиографии должна быть 1,5 Тесла [опция].
Применение КТ-ангиографии для динамического наблюдения может быть ограничено в связи с нежелательностью рентгеновского облучения у ряда пациентов [70, 79, 98, 107].
Использование ДСА в качестве контрольного обследования у пациентов с оперированными аневризмами ограничено в связи с инвазивностью обследования и наличием радиационной нагрузки [24, 76].
После проведенного хирургического лечения контрольную ДСА в ранние сроки (до 2 недель после операции) выполняют в том случае, если аневризма не была полностью выключена, при сомнении хирурга в радикальности проведенной операции, или при подозрении на миграцию наложенного клипса. Повторное исследование после микрохирургической операции необходимо провести в течение 6-12 месяцев после вмешательства [рекомендация].
После выполнения эндоваскулярного вмешательства необходимо выполнение контрольного обследования (ДСА) в период от 6 до 12 месяцев после операции [1, 2, 3, 48, 72, 87, 92] [рекомендации]. Время последующих контрольных обследований зависит от характера окклюзии аневризмы при вмешательстве и первом контрольном обследовании, а также от состояния пациента. При наличии резидуальной аневризмы после эмболизации или стентирования обязательно проведение обследований в отдаленном периоде, так как возможны кровоизлияния и рост остаточной части аневризмы. Показано проведение серии контрольных обследований при аневризмах с широкой шейкой, больших и гигантских аневризмах, так как у них имеется высокий риск повторного заполнения [10, 93].
Всем пациентам, входящим в популяционные группы риска по формированию аневризм, независимо от вида оперативного вмешательства, после завершения периода наблюдения можно рекомендовать выполнение неинвазивных методов обследования (МР- или КТ-ангиографии) 1 раз в 5 лет для исключения формирования аневризм de novo [рекомендация].
Динамическое наблюдение за пациентами с неразорвавшимися церебральными аневризмами, не получавшими хирургического лечения [рекомендации]
Пациентам с неразорвавшимися аневризмами сосудов головного мозга, которые не получали хирургического лечения, необходимо проведение нейровизуализационного обследования в динамике для исключения роста аневризмы, изменения ее формы и появление других факторов риска ее разрыва [4, 11, 24, 25, 37, 42, 59, 64].
1) При отсутствии противопоказаний основной методикой для проведения динамического наблюдения является TOF MRA (времяпролётная магнитно-резонансная ангиография), а также у пациентов с почечной недостаточностью и тем, у кого имеет значение доза полученного рентгеновского облучения.
2) КТ-ангиография головного мозга является методом выбора у пациентов с противопоказаниями к проведению МРТ или при наличии аневризм, которые не могут быть правильно оценены с помощью МРТ (милиарные аневризмы менее 3 мм, «сложные» аневризмы).
3) Первое динамическое обследование после выявления неразорвавшейся аневризмы необходимо проводить в период от 6 до 12 месяцев [8, 33, 56, 112, 113]. Затем рекомендуется проводить обследование 1 раз в год или каждые 2 года при отсутствии признаков роста аневризмы и/или изменения ее других морфологических параметров (формы, расположение относительно несущего сосуда и т.д.) [113].
Госпитализация
Больного с неразорвавшейся аневризмой сосудов головного мозга, при наличии показаний к хирургическому лечению, необходимо госпитализировать в плановом порядке в стационары, где имеются:
— нейрохирургическое отделение;
— специалисты, владеющие опытом прямых микрохирургических операций по поводу церебральных аневризм;
— специалисты, владеющие опытом эндоваскулярного выключения аневризм;
— отделение лучевой диагностики, оснащенное аппаратурой для проведения КТ или МРТ, спиральной КТ-ангиографии, МР-ангиографии, ангиографическая операционная для проведения ДСА и выполнения эндовазальных операций;
— операционная, оснащенная оборудованием для микрохирургии церебральных аневризм (операционный микроскоп, микрохирургический инструментарий, съемные и постоянные немагнитные клипсы);
— отделение нейрореанимации.
Информация
Источники и литература
Информация
| Крылов Владимир Викторович | академик РАН, профессор, доктор медицинских наук, заведующий научным отделением неотложной нейрохирургии НИИ скорой помощи им. Н.В. Склифосовского, заведующий кафедрой нейрохирургии и нейрореанимации Московского государственного медико-стоматологического университета им. А.И. Евдокимова, главный внештатный специалист нейрохирург Министерства Здравоохранения Российской Федерации |
| Элиава Шалва Шалвович | Доктор медицинских наук, профессор, заведующий отделением сосудистой нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Яковлев Сергей Борисович | Доктор медицинских наук, заведующий отделением эндоваскулярной нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Хейреддин Али Садек | Доктор медицинских наук, врач отделения сосудистой нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Белоусова Ольга Бенуановна | Доктор медицинских наук, ведущий научный сотрудник отделения сосудистой нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Полунина Наталья Алексеевна | Кандидат медицинских наук, научный сотрудник отделения неотложной нейрохирургии НИИ СП им. Н.В. Склифосовского |
Определение понятий
Стандарт
Общепринятые принципы диагностики и лечения, которые могут рассматриваться в качестве обязательной лечебной тактики (эффективность подтверждена несколькими рандомизированными исследованиями, мета-анализами или когортными клиническими исследованиями).
Рекомендация
Лечебные и диагностические мероприятия, рекомендованные к использованию большинством экспертов по данным вопросам. Могут рассматриваться как варианты выбора лечения в конкретных клинических ситуациях (эффективность подтверждена отдельными рандомизированными исследованиями или когортными клиническими исследованиями).
Опция
Лечебные и диагностические мероприятия, которые могут быть полезны (эффективность подтверждена мнением отдельных экспертов, в отдельных клинических случаях).
Не рекомендуется
Лечебные и диагностические мероприятия, не имеющие положительного эффекта или могущие принести вред (любой уровень подтверждения).