Особенности диагностики нейроэндокринных опухолей
Нейроэндокринные опухоли (НЭО) — это гетерогенная группа новообразований, развивающихся из нейроэндокринных клеток. Такие клетки расположены в различных органах и секретируют биологически активные вещества, эффекты которых обуславливают многообразие клинической картины и трудности диагностики. Прежде чем попасть на прием к онкологу, пациентам зачастую бывают проведены консультации различных специалистов, обращение к которым вызвано симптоматикой новообразования. Ранняя диагностика НЭО в значительной мере зависит от онконастороженности непрофильных клиницистов и, конечно же, от морфологической верификации диагноза — «золотого правила» в онкологии, своеобразной точки отсчета онкологической истории.
Локализация НЭО крайне разнообразна, но чаще всего они обнаруживаются в органах пищеварительной системы (более 50 %): прямая (17,2 %) и тонкая кишка (13,4 %), желудок (6,0 %), поджелудочная железа (6–7 %). НЭО занимают второе место в общей структуре онкологической патологии ЖКТ, уступая лидерские позиции лишь колоректальному раку. Около 27 % случаев НЭО возникают в легких (согласно базе данных Surveillance, Epidemiology, and End Results (SEER) 1975-2016) [1].
Еще недавно обсуждались вопросы включения НЭО в список орфанных заболеваний. Но в настоящее время отмечается увеличение частоты встречаемости этой патологии, в том числе из-за улучшения диагностических возможностей (в частности, распространение гастроскопии, колоноскопии, капсульной эндоскопии).
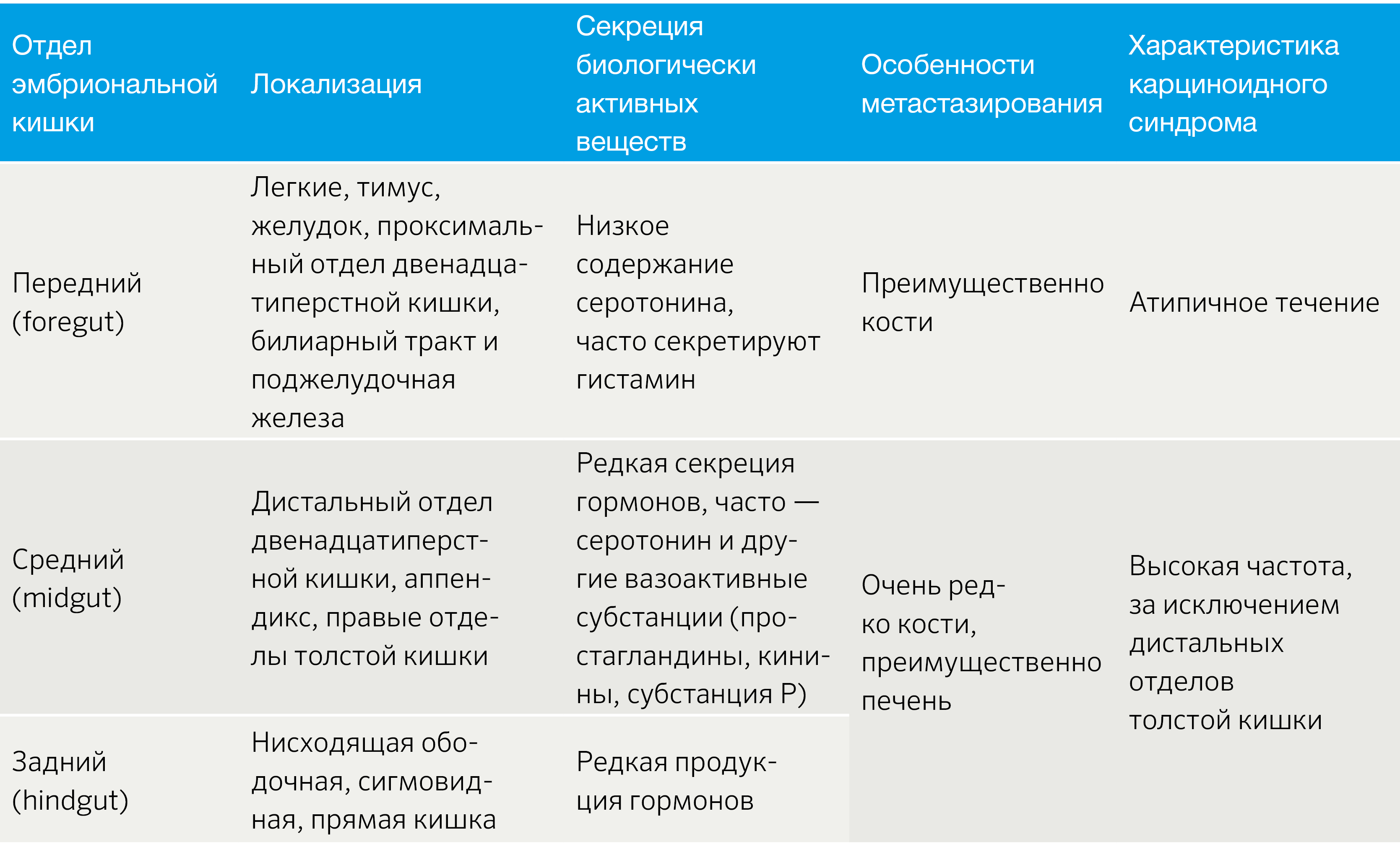
НЭО классифицируют в зависимости от отдела эмбриональной кишечной трубки: из передней, средней и задней кишки (табл. 1) [2].
Табл.1 | Классификация НЭО по эмбриогенезу [2].
Карциноидный синдром — важный клинический признак. В основном, он обусловлен эффектами серотонина, а также брадикинина, гистамина, дофамина и в меньшей степени других биологически активных веществ (БАВ).
Клинические проявления карциноидного синдрома разнообразны. Наиболее часто у пациентов отмечается гиперемия кожи лица, приливы, диарея, боль в животе. У 60 % пациентов отмечают формирование карциноидной болезни сердца, с нарушением работы преимущественно клапанного аппарата правых отделов (стеноз и/или недостаточность легочного и трехстворчатого клапанов). Серьезным осложнением является декомпенсация нарастающей сердечной недостаточности. Морфологическим субстратом служит выраженный диффузный фиброэластоз эндокарда. Возможны появления телеангиоэктазий, одышки, пеллагры, бронхоспазма. Усиливается продукция соединительнотканных компонентов, в частности, коллагена. Это ведет к фиброзированию и стенозу брыжеечных артерий, фиброзирующему стенозу уретры. Ввиду склонности к развитию спаечного процесса в брюшной полости нарастает риск формирования кишечной непроходимости.
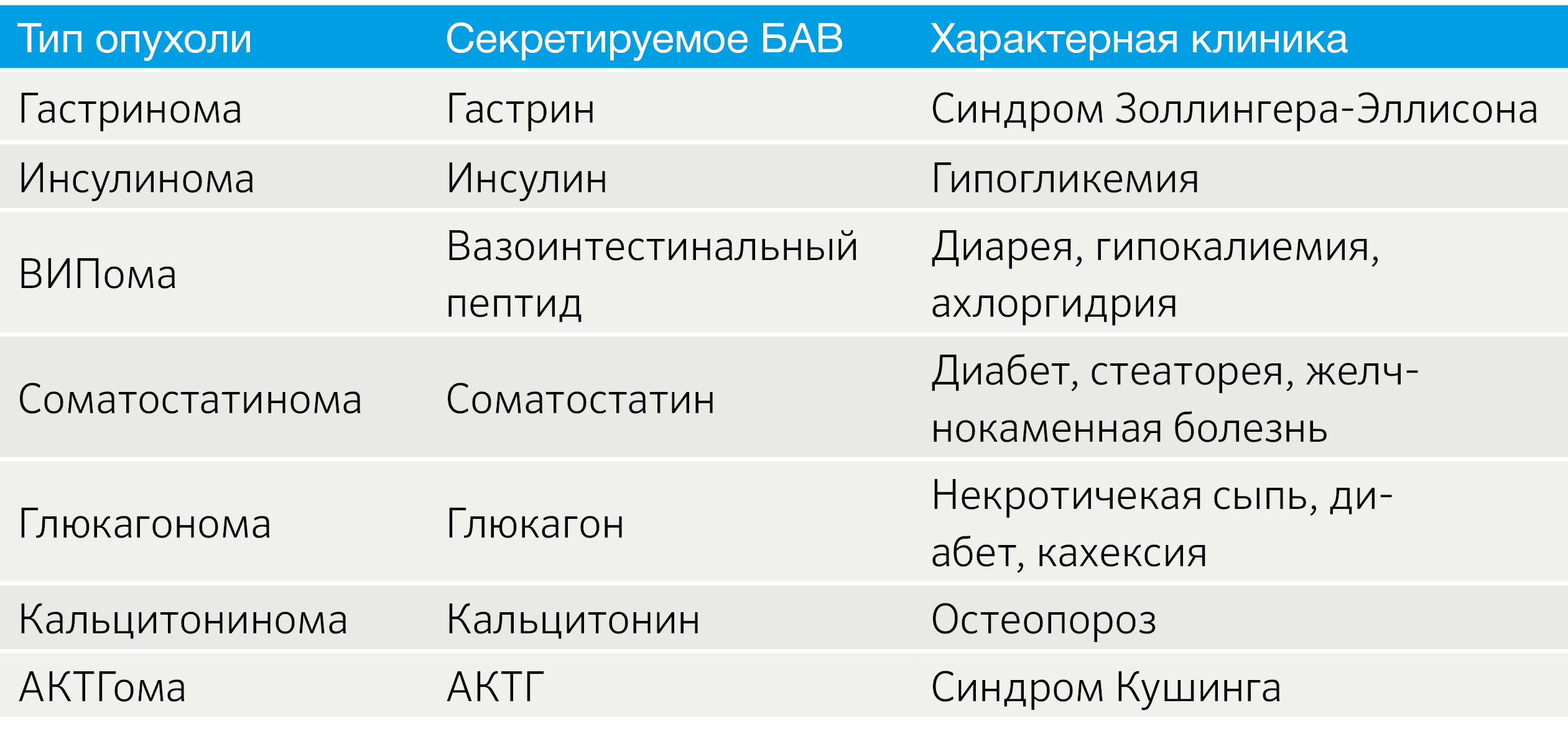
Важным аспектом является функциональный статус опухоли. В зависимости от наличия продукции БАВ выделяют функционирующие (табл. 2) и нефункционирующие новообразования [3].
Табл.2 | Функционирующие НЭО [3].
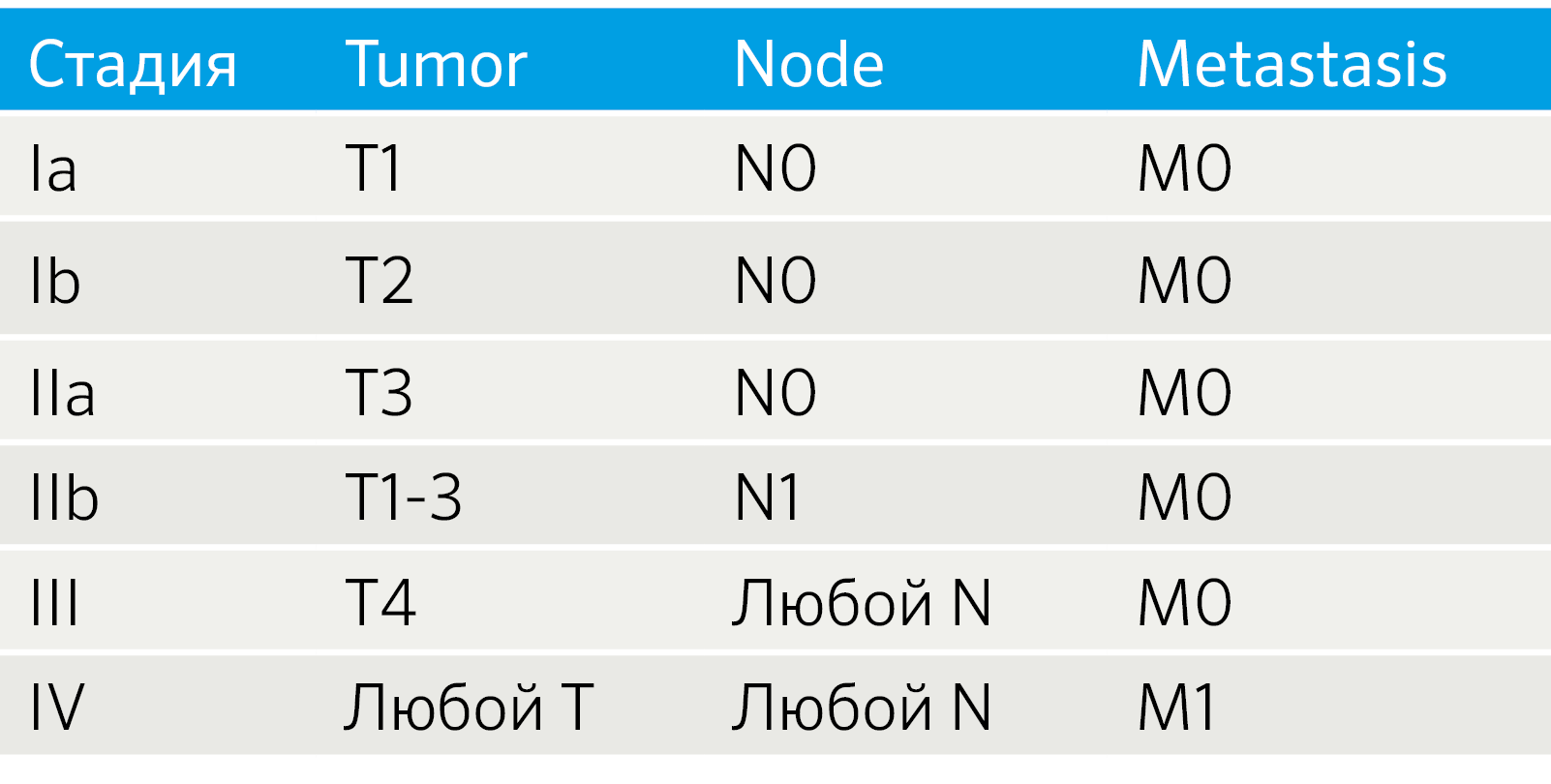
Особенности TNM-классификации определяются локализацией НЭО. НЭО легких стадируются как немелкоклеточный рак легких, для НЭО ЖКТ и поджелудочной железы разработаны рекомендации Европейского общества по изучению НЭО (ENETS) [4]. Также установление стадии TNM для всех анатомических локализаций регламентируется руководством, созданным Американским объединенным комитетом по раковым заболеваниям (the American Joint Committee on Cancer, AJCC) [5, 6]. Так как эти системы не идентичны, возникают вопросы унификации подходов к стадированию. Например, была создана модифицированная система ENETS (mENETS), для диагностики НЭО поджелудочной железы (pNET) (табл. 3) [7].
Табл.3 | Стадирование НЭО поджелудочной железы согласно модифицированной системе ENETS (mENETS) [7].
И вот мы подходим к той черепахе, на которой стоят киты онкологической диагностики. Это, несомненно, гистологическая верификация диагноза. Как и многие опухолевые заболевания, морфологические градации НЭО подвергались различным модификациям, уточнениям, дополнениям. Дискуссии в этой области в итоге привели к созданию 4-ой редакции классификации ВОЗ (2017 год) [8]. Именно она является актуальной на настоящий момент и заключение при проведении патологоанатомическом исследовании должно отвечать введенным в ней понятиям и требованиям.
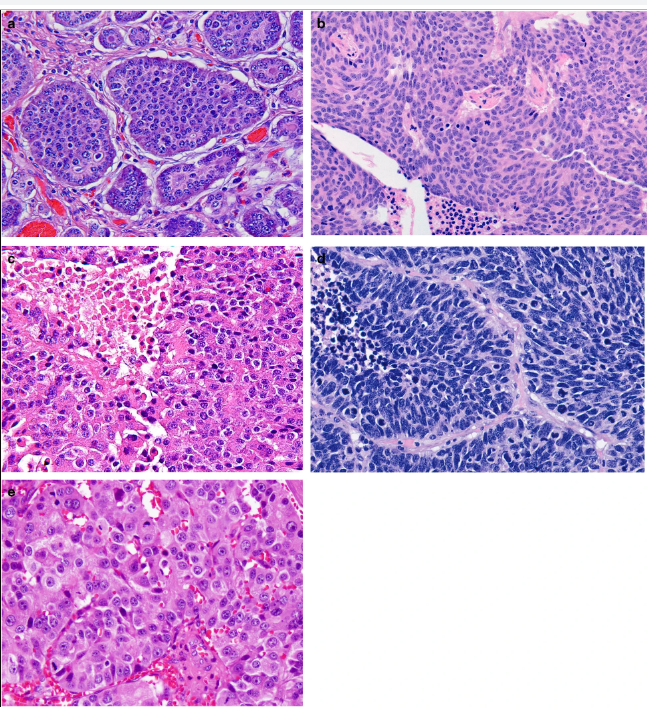
Параметрами морфологической оценки нейроэндокринных новообразований являются: гистологическое строение опухоли, определение сосудистой и периневральной инвазии, митотический индекс. Несмотря на многообразия источников НЭО, морфологическая картина является сходной (рис. 1) [9].
Нейроэндокринное происхождение атипичных клеток доказывает положительная экспрессия так называемых общих нейроэндокринных маркеров. Основные из них это хромогранин А, окрашивающий компоненты нейросекреторных гранул, и пептид синаптофизин, накапливающийся в мелких синаптических везикулах. Также применяется дополнительно установление экспрессии рецепторов соматостатина 2 и 5 типов (SSTR2 и SSTR5). В этом случае возможно определить чувствительность опухолевых клеток к аналогам соматостатина.
Степень злокачественности НЭО определяют на основании двух основных критериев: уровня дифференцированности опухолевых клеток и их пролиферативной активности. Традиционно выделяют три степени злокачественности (grade): G1, G2, G3. Для НЭО ЖКТ и поджелудочной железы введены понятия высокодифференцированных и низкодифференцированных новообразований (или нейроэндокринного рака (карциномы), НЭР). Высокодифференцированные НЭО объединяют G1 (менее 2 митозов на 10 репрезентативных полей зрения (РПЗ) при большом увеличении микроскопа (х400) и индекс Ki-67 ≤ 2%), G2 (2–20 митозов на 10 РПЗ и индекс Ki-67 3–20 %), G3 (> 20 митозов на 10 РПЗ и индекс Ki-67 > 20 %). Grade 3 опухоли разделяют на мелко- и крупноклеточный рак. Опухоли мелкоклеточного типа построены из однотипных клеток округлой, овальной или вытянутой формы, мелкого размера, со скудной цитоплазмой и нечеткими границами. Ядра имеют характерный вид за счет нежного хроматина и невизуализирующихся ядрышек. Определяются массивные некрозы. Крупноклеточные НЭР образованы, соответственно, клетками крупного или среднего размера, с низким ядерно-цитоплазматическим соотношением, выраженной атипией ядер, содержащих гранулярный хроматин и четкие ядрышки. В опухолевой ткани выявляются мультифокальные некрозы, значительное число митозов [8, 9].
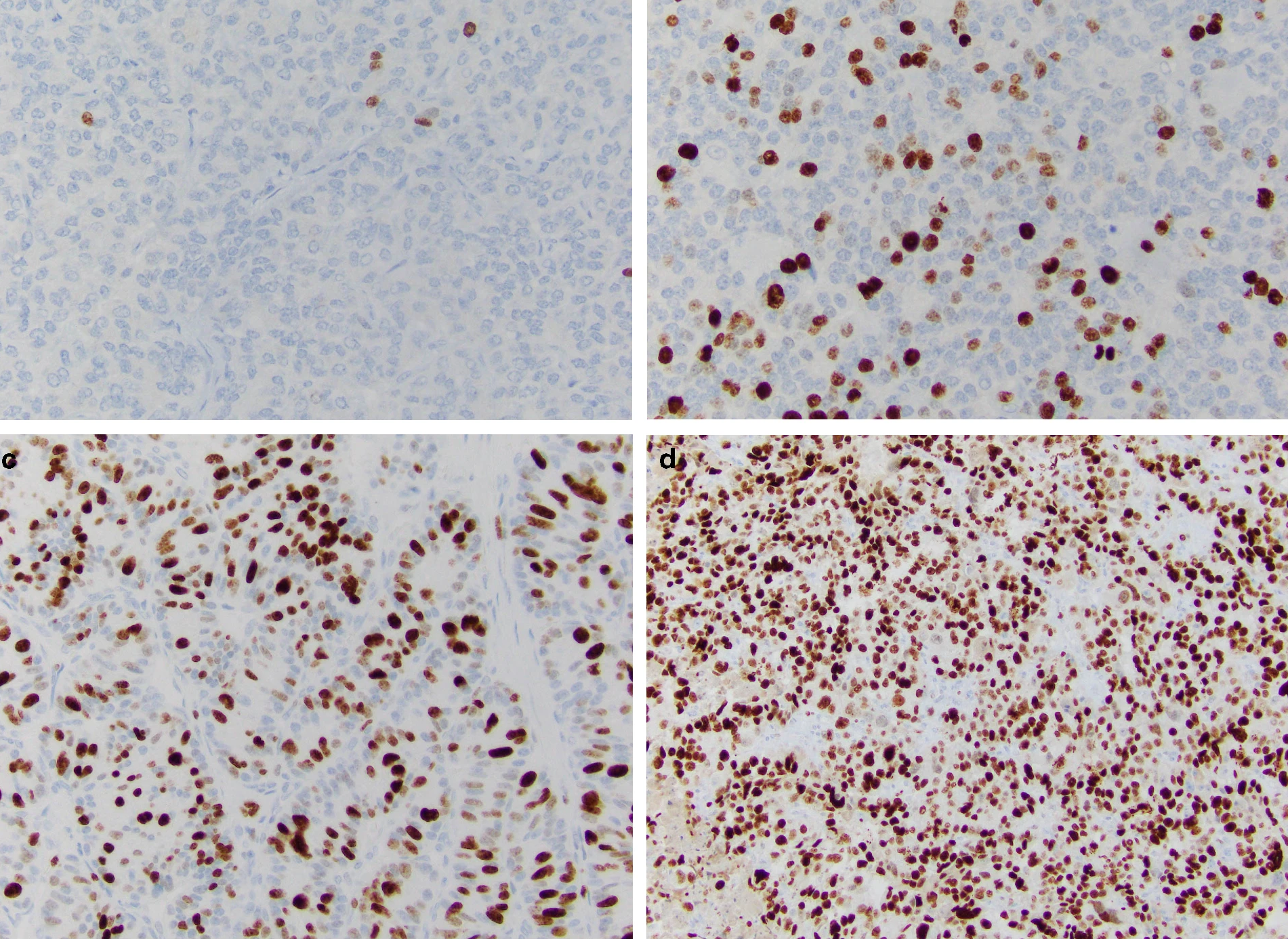
Индекс Ki-67 определяют как средний процент окрашенных ядер при учете 500–2000 злокачественно трансформированных клеток (рис. 2) [9].
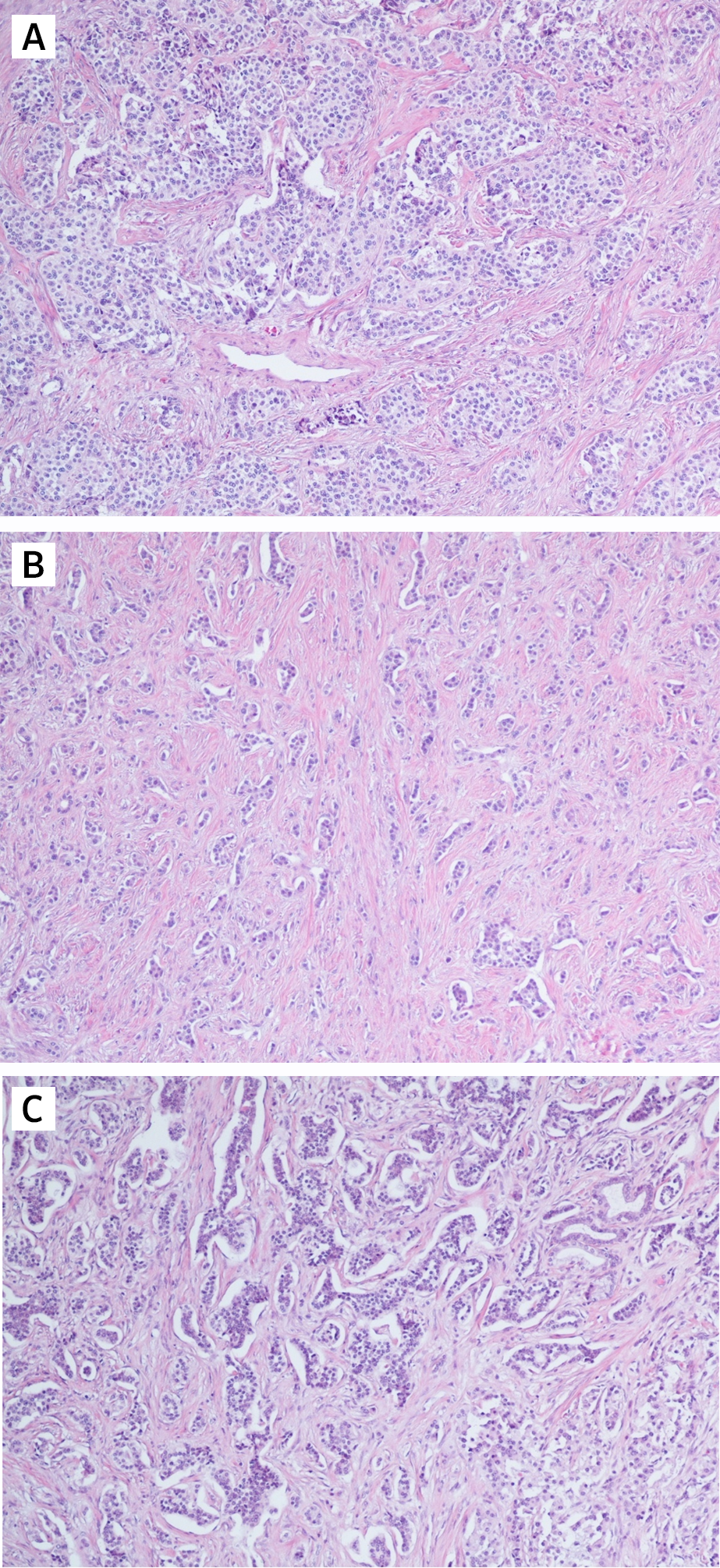
Рассмотрим различия понятий НЭО G3 и НЭР при локализации в поджелудочной железе. Несмотря на высокую степень злокачественности НЭО G3 гистологически имеют органоидную модель строения (рис. 3), отсутствие некрозов [10]. При иммуногистохимическом исследовании опухолевая ткань сохраняет экспрессию общих маркеров нейроэндокринной дифференцировки (диффузно и интенсивно определяется экспрессия синаптофизина, зачастую хромогранина А), а также панкреатические экзокринные или эктопические гормоны. Кроме того, в них отсутствует выраженная экспрессия p53 и утрата экспрессии RB (также определяются иммуногистохимически).
НЭР поджелудочной железы — это опухоли низкой степени дифференцировки и соответственно высокой степени злокачественности. Экспрессия общих маркеров нейроэндокринной дифференцировки атипичными клетками снижается: синаптофизин определяется слабо или диффузно, хромогранин А также слабо или фокально. Экзокринные гормоны отрицательны в таких опухолях [9]. Часто определяется экспрессия р53, белков ремоделирования хроматина DAXX (death-associated protein 6) и ATRX (АТФ-зависимая хеликаза), потеря экспрессии RB (белок ретинобластомы) и ISL1 (энхансер гена инсулина 1) [11].
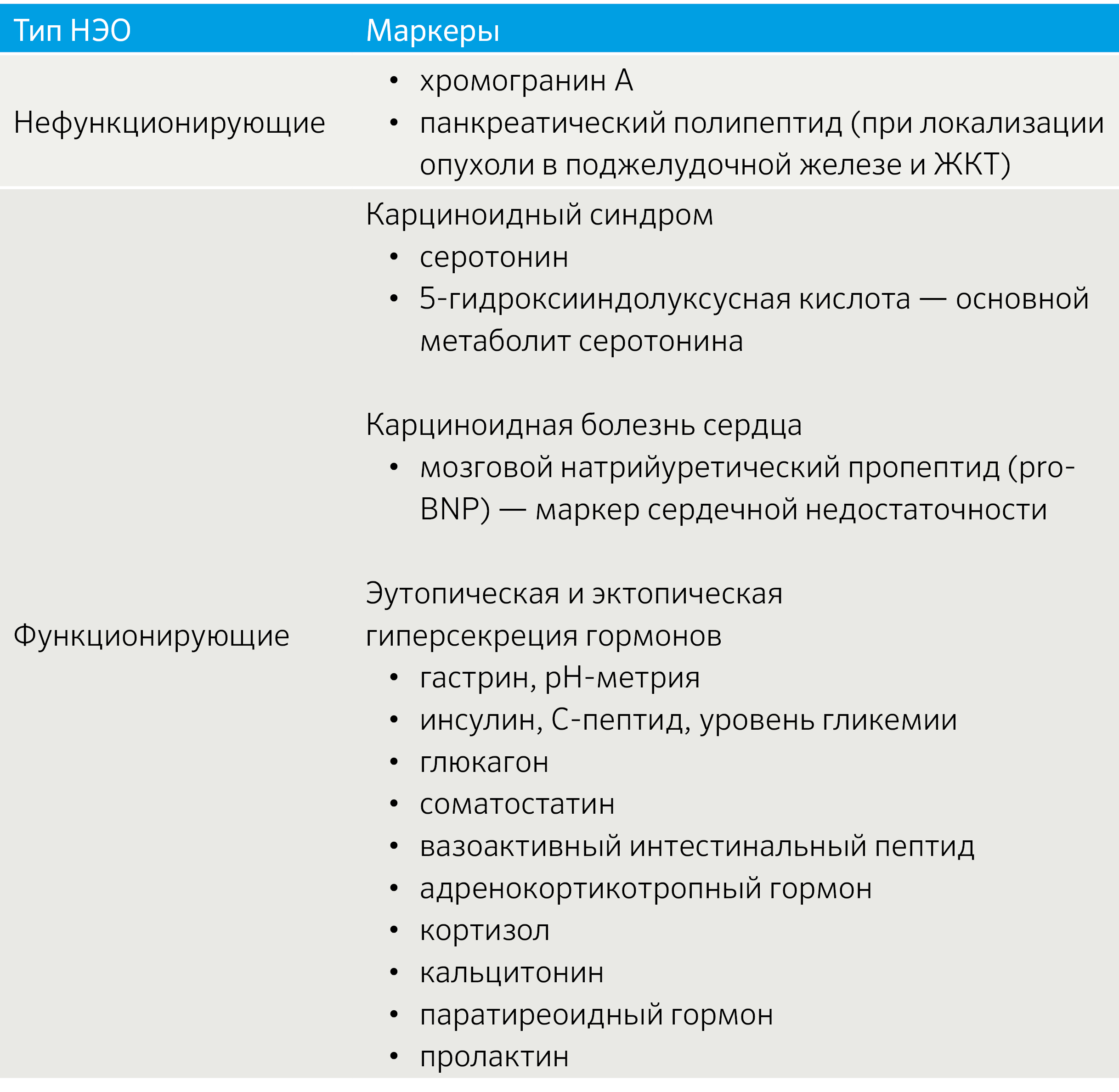
Ввиду многообразия секретирующего профиля НЭО биохимическая диагностика включает различные маркеры, комбинируемые с учетом клинической картины (табл. 4).
Табл. 4 | Спектр биохимических маркеров НЭО [2].
Методы лучевой диагностики включают «классические» КТ и МРТ с контрастированием. Для оценки метастатического поражения печени возможно проведение УЗИ органов брюшной полости.
Радионуклидная диагностика играет важную роль в топической характеристике НЭО. Она включает методы специфической метаболической визуализации ( 123 I-MIBG), рецепторной визуализации ( 111 In-октреотид, 68 Ga-DOTA-TOС/DOTA-NOC/DOTA-TATE) и неспецифической метаболической визуализации ( 18 F-FDG, 18 F-DOPA).
123 I-метайодбензилгуанидин (MIBG) является аналогом норадреналина (норэпинефрина). Он накапливается в адренергических тканях и опухолях, происходящих из них. Сцинтиграфия с 123 I-MIBG используется для диагностики нейробластомы, феохромоцитомы, параганглиомы, карциноидов бронха и тонкой кишки [12].
Для рецепторной визуализации применяют 111 In (индий)-октеотид. Он выявляет высокодифференцированные нейроэндокринные опухоли, опухоли из клеток островкового аппарата поджелудочной железы (гастринома, глюкагонома, инсулинома). Также для верификации НЭО ЖКТ применяется соматостатин-рецепторная сцинтиграфия, так как большинство из них имеют рецепторы к соматостатину (SSTR) на поверхности опухолевых клеток (чаще 2 и 5 типа).
Выбор радионуклидного метода связан со степенью дифференцировки опухолевых клеток. Первичная диагностика НЭО Grade 1 и 2 проводится путем ПЭТ/КТ с радиофармпрепаратами (РФП), мечеными галлием 68 (является ПЭТ-радионуклидом). Сродство (аффинитет) РФП к конкретному подтипу трансмембранных рецепторов соматостатина определяет выбор диагностического индикатора (ПЭТ-лиганда, представленного различными модификациями DOTA). Например, для визуализации НЭО, экспрессирующих рецепторы подтипов SSTR2a и SSTR2b, применяют 68 Ga-DOTA-TATE (DOTA-Tyr3-октреотад). 68 Ga-DOTA-NOC (DOTA-1-Nal3-октреотид) выявляет подтипы SSTR3 и SSTR5, 68 Ga-DOTA-ТOC (DOTA-Tyr3-октреотид) — рецепторы SSTR5 [13].
При отсутствии возможности проведения данного исследования следует выполнить однофотонную эмиссионную компьютерную томографию (ОФЭКТ)/КТ (гибридный метод визуализации) с соматостатин-рецепторным радиофармпрепаратом.
Для недифференцированных НЭО Grade 3 и НЭР при отрицательных результатах соматостатин-рецепторной сцинтиграфии рекомендуется ПЭТ неспецифическая метаболическая визуализация с использованием других РФП. В частности, ПЭТ/КТ c 18F-фтордезоксиглюкозой (18F-ФДГ), которая неэффективна при высокодифференцированных НЭО [14]. Также рассматривают применение 18F-L–DOPA (дигидроксифенил-аланин) — меченого предшественника допамина, который эффективен для обнаружения медуллярного рака щитовидной железы, НЭО, параганглиомы и феохромоцитомы [15].
Современные классификации НЭО в значительной мере основаны на общей морфологии, которую эти новообразования демонстрируют в различных анатомических участках. Закономерно предположить, что такая структурная схожесть является результатом общей «нейроэндокринной» мультигенной программы, стимулирующей дифференцировку нейроэндокринных клеток. Но схожесть не означает идентичность, и несомненно существующая тканеспецифичность нейроэндокринных клеток диктует характерною индивидуальную гормональную продукцию. Профиль экспрессии БАВ атипичными клетками определяет клиническую картину и прогноз заболевания. Поэтому важно иметь возможность точно определяет источник опухоли. С использованием все расширяющихся диагностических возможностей такой подход становится реальным, формируя персонализацию терапевтических стратегий в нейроэндокринной онкологии.
Сложный случай: что такое нейроэндокринные опухоли и канцероматоз брюшины
А Оксана Голубева рассказала, каково это — быть не врачом, а пациентом, где она искала информацию о своем диагнозе, и почему ей повезло.
Что такое НЭО?
Нейроэндокринные опухоли (НЭО) возникают из нейроэндокринных клеток. Последние расположены практически во всех органах и тканях организма. Эти клетки получают сигналы от нервной системы и выделяют в кровь гормоны – процесс называется нейроэндокринной интеграцией, — поясняет Павел Сорокин.
По словам онколога, нейроэндокринные опухоли редкие и разнообразные, поэтому их тяжело изучать.
Нейроэндокринные опухоли яичников составляют 0.5% от всех нейроэндокринных опухолей. Большинство из них растет медленно и выявляется на 1 стадии. Стандарт лечения в таком случае – удаление опухоли и наблюдение. Если появились метастазы НЭО яичника, то по возможности их тоже необходимо удалять. Но требуется ли какое-то дополнительное лечение, чтобы снизить риск рецидива болезни – неизвестно, — уточняет Павел.
Оксана вспоминает, что первые симптомы проявились около 7-8 лет назад. Вернее, симптом был только один, и он женщину не насторожил.
Ночью меня бросало в пот. Я подумала, что это может быть связано с недавней беременностью и лактацией. Тогда я минимально обследовалась: сходила на осмотр к гинекологу, сделала рентгенограмму легких, сдала лабораторные анализы, в том числе гормоны щитовидной железы. Сомнение вызывало незначительное снижение гемоглобина, которое я связала с недосыпом, погрешностями в диете и обильными менструациями, — уточняет Оксана Голубева.
 |
Долгое время опухоль себя не проявляла. Возможно, так продолжалось бы и дальше, если бы не экстренная госпитализация.
4 февраля прошлого года у меня нестерпимо заболел живот. Прямо с рабочего места я попала на операционный стол. В ходе операции врачи обнаружили опухоль яичника и канцероматоз брюшины,— вспоминает Оксана.
Канцероматоз — не самостоятельное заболевание, а вариант распространения опухоли, при котором она метастазирует по брюшине.
Выглядит это как множественные опухолевые узлы на органах брюшной полости, а также на брюшных стенках. Размер очагов может быть от микроскопических, до огромных – 10 см и более. Количество узлов также отличается – от единичных до не поддающихся счету. Чаще всего канцероматоз брюшины развивается при раке яичников, желудка, аппендикса, толстой кишки и поджелудочной железы. При каждой из этих опухолей он отличается по проявлению, лечению и прогнозу. Человека начинают беспокоить симптомы, связанные с накоплением жидкости в животе (асцит) или большой опухолевой массы. Самое частое – увеличение объема живота (в старых учебниках по гинекологии писали «юбка стала мала в поясе»), появление тяжести в животе, запоры, ощущение опухоли в животе, — поясняет Павел.
Поставить такой диагноз можно до операции: по данным УЗИ, МРТ или КТ. Однако, по словам Павла Сорокина, все эти методы позволяют увидеть только крупные очаги – хотя бы 5 мм. Канцероматоз может выглядеть и как сотни мелких, размером с просяное зернышко, очагов, покрывающих брюшину и внутренние органы.
Достоверно оценить распространенность канцероматоза можно только во время операции. Обычно она начинается с лапароскопии: через небольшой прокол вводится специальная камера, позволяющая разглядеть все отделы брюшной полости, — заключает Павел Сорокин.
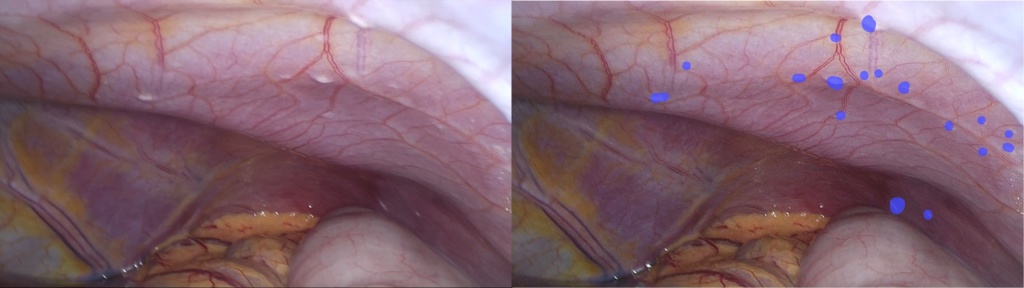 |
Так выглядит канцероматоз брюшины передней брюшной стенки
Сложно исследовать и лечить
С постановкой окончательного диагноза возникли трудности.
Было понятно, что есть нейроэндокринная опухоль яичника и канцероматоз брюшины. Однако НЭО — это очень редкий вид опухолей, который встречается менее, чем в 0.1% случаев от всех новообразований яичников, поэтому их сложно исследовать. У Оксаны опухоль распространилась по брюшине, что встречается еще реже: обычно эти опухоли ограничены яичником.
Опухоль под микроскопом смотрели в четырех ведущих лабораториях Москвы и Санкт-Петербурга, и везде диагноз различался.
А ведь от диагноза зависит план лечения. К тому же, нейроэндокринные опухоли яичника бывают метастатическими. То есть первичная опухоль может быть небольшой и находиться в другом органе, но дать метастаз в яичник, который вырастет в размере и может быть принят за первичную опухоль. Поэтому перед началом лечения требовалось полное обследование, — поясняет Павел Сорокин.
За трудностями в диагностике последовали сложности в назначении лечения.
Для нейроэндокринных опухолей нет стандартного лечения. Весь мировой опыт умещается в нескольких статьях, описывающих пару десятков случаев. Нет однозначного мнения о необходимом объеме обследований, лучшем методе лечения и наблюдении после. Я связался с Вадимом Гущиным – хирургом-онкологом из США, который специализируется на канцероматозе брюшины. И с Марией Дельгранде из Швейцарии, специализирующейся на опухолях яичников. Предложенные ими варианты лечения тоже различались. В итоге мы остановились на циторедуктивной операции, — продолжает Павел.
Операция
Так как я медицинский работник, я не пошла на обследования с первого этапа — с участкового терапевта или онколога. С организацией обследований очень помогали коллеги. И все равно окончательный диагноз мне поставили почти через три месяца! Очень сложно было искать информацию по своему диагнозу. Некоторые сведения я нашла на сайте медицинского общества «МОЛНЭО». Отыскала и пациентскую группу «ВКонтакте», где можно задать вопросы, найти психологическую поддержку и просто поговорить, — делится Оксана.
Оксану ожидала сложная многочасовая операция — циторедуктивная, в ходе которой нужно было полностью освободить брюшную полость от видимой опухоли.
Часто приходится удалять несколько органов, так как их невозможно сохранить, не оставив опухоль. И даже в этом случае нельзя быть уверенным, что не осталось отдельных опухолевых клеток, которые не видны глазу. Чтобы подействовать на них, применяется внутрибрюшная гипертермическая химиоперфузия – HIPEC. В конце операции брюшная полость промывается нагретым раствором химиопрепарата, чтобы подействовать на микроскопические проявления опухоли.
К сожалению, эти операции выполняются в небольшом числе клиник по всему миру, поэтому многие пациенты не могут получить качественное лечение. Это связано со значительной стоимостью самой операции и реабилитации после, необходимости высокой квалификации хирурга и его команды, а также с отбором пациентов, которым эта операция принесет пользу,— объясняет Павел Сорокин.
Оксану прооперировали специалисты из НМИЦ онкологии им. Н.Н. Петрова. В команде врачей был и Павел Сорокин.
 |
По ту сторону
Я чувствовала ужасную слабость, не могла передвигаться без посторонней помощи, нарушилась работа ЖКТ. Две недели я находилась под наблюдением медперсонала в условиях стационара, где получала лекарственную терапию, специальное питание и занималась лечебной физкультурой.
А затем долечивалась амбулаторно. Раз в 10 дней мне нужно было попасть на прием к участковому врачу. Это стоило больших усилий и поддержки со стороны окружающих.
Оказавшись в роли пациента, я в полной мере осознала, как это тяжело — быть больным человеком. Повезло, что я врач. Я представляю, какие вопросы нужно задать, чтобы ускорить решение проблемы. Понимаю, куда нужно обратиться. Если ты не врач, таких знаний у тебя, скорее всего, нет. И тобой никто не занимается. По большому счету ты никому не нужен. Все, что ты можешь организовать, ты делаешь с помощью своих собственных сил и ресурсов,— вспоминает Оксана.
Прогнозы
Прогноз при НЭО яичников обычно хороший – большинство пациенток живут без рецидива многие годы и десятилетия. В случае Оксаны опухоль росла медленно: за несколько месяцев, прошедших от момента установки диагноза до циторедуктивной операции, опухоль не изменилась – это также наталкивает на мысль о ее благоприятном прогнозе, — говорит Павел Сорокин.
Что касается НЭО яичника в сочетании с канцероматозом — тут прогнозы делать сложно из-за недостатка данных.
В литературе встречаются серии и отдельные случаи, когда пациентки жили 10 лет и более после проведенного лечения, — объясняет Павел Сорокин.
С момента операции прошло 7 месяцев. Я работаю, получаю бесплатно один раз в месяц лекарство, уменьшающее проявление симптомов карциноидного синдрома — отлоголоска НЭО, проявляющегося, в частности, в виде сухих приливов и диареи. Выполняю каждые три месяца нейровизуализацию (КТ, МРТ) брюшной полости, контролирую показатели крови.
Жизнь продолжается, после операции она поменялась незначительно. Есть ограничения в питании: сладкое, жирное, кофе, алкоголь, некоторые фрукты исключаются, нельзя много мучного. Не могу поднимать тяжести, пока устаю к концу рабочего дня и недели.
А вообще, я учусь танцевать и считаю себя здоровой,— заключает Оксана Голубева.
Нейроэндокринные опухоли желудка
Нейроэндокринные новообразования желудка, также известные как эндокринные новообразования или карциноиды, составляют относительно небольшую и гетерогенную группу опухолей, значительно различающихся по клинико-патологическому течению, степени дифференцировки, скорости пролиферации и исходу [1].
Хотя по морфологическим и функциональным свойствам в слизистой оболочке желудка человека выделяют до 5 типов эндокринных клеток, большинство желудочных НЭО развиваются из энтерохромаффиноподобных клеток. Эти новообразования могут быть множественными, возникающими на фоне длительной гипергастринемии из-за атрофического гастрита и ахлоргидрии (тип 1), или вследствие сочетанной множественной эндокринной неоплазии — синдрома Золлингера-Эллисона с гипертрофической гастропатией (тип 2), или они могут появляться в слизистой оболочке без предшествующих патологических изменений (тип 3), иногда возникает «атипичный» карциноидный синдром [1].
Нейроэндокринные новообразования желудка значительно различаются по гистологии, клинико-патологическим формам, стадиям и возможным исходам, что подразумевает необходимость большого количества лечебных и диагностических мероприятий. Также стоит отметить необходимость улучшения диагностических и прогностических критериев для выбора соответствующей терапии [1].
Локализация опухоли [2]:
• Кардиальный отдел,
• Дно желудка,
• Тело желудка,
• Преддверие желудка,
• Привратник,
• Малая кривизна желудка,
• Большая кривизна желудка,
• Поражение, выходящее за пределы желудка.
Классификация
Классификация ВОЗ 2010 [2]:
Классификация по степени злокачественности [2,4]
Алгоритм лечения зависит от типа и распространенности опухоли и ориентирован на классификации ВОЗ (2010) и рекомендации Европейского общества по изучению НЭО (ENETS) (2016). В настоящее время ENETS и ВОЗ предложено делить НЭО ЖКТ по степени их злокачественности (Grade) на 3 основные группы — Gl, G2, G3, а также по TNM [2].
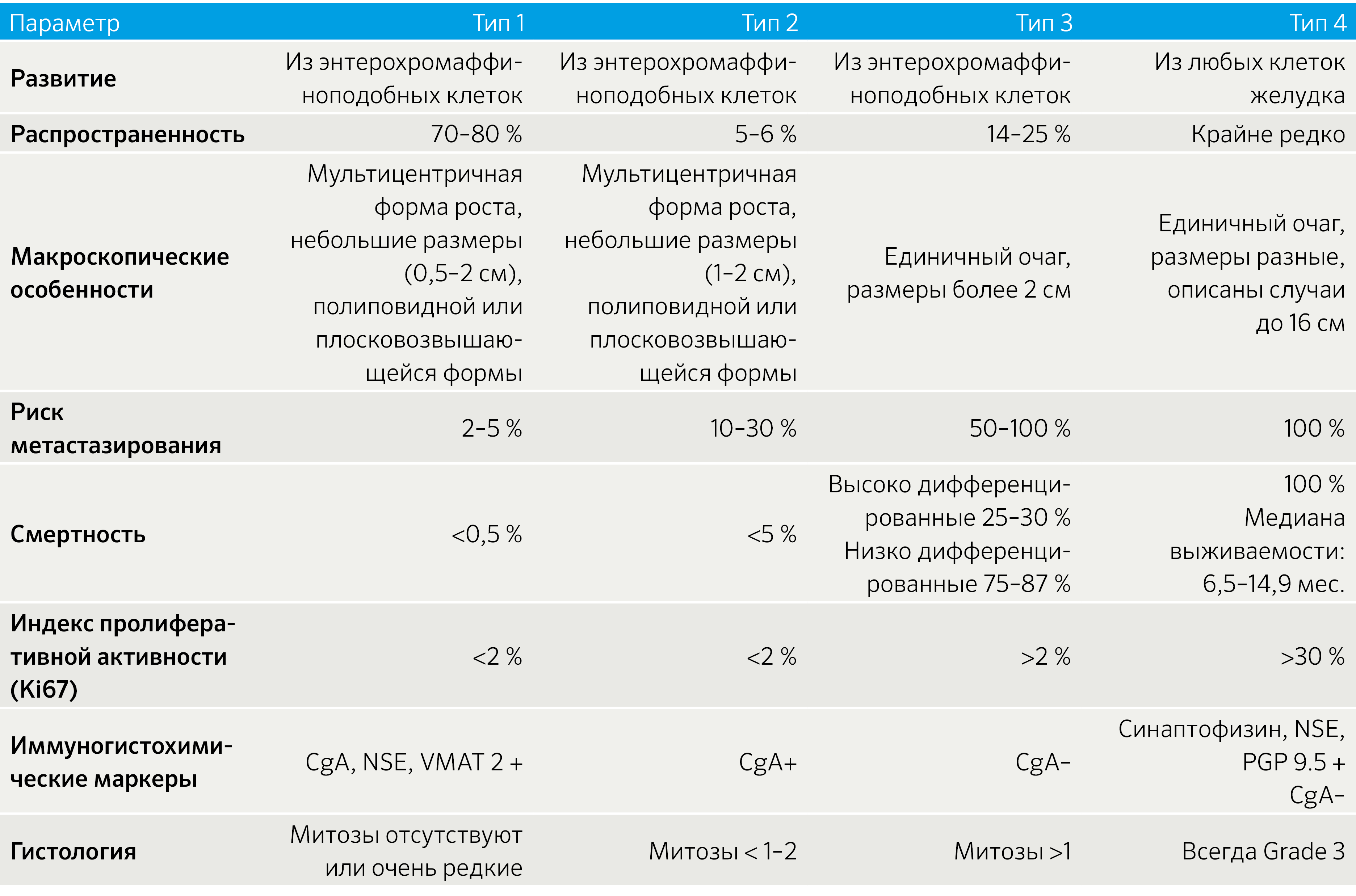
Таблица 1. Характеристика клинико-патологических форм НЭО желудка [3,4]
Клинико-патологические формы НЭО желудка
I тип
70–80 % нейроэндокринных опухолей желудка являются опухолями I типа: диаметр менее 10 мм, опухоли множественные. Часто у пациентов хронический атрофический гастрит в анамнезе. Опухоли локализуются в дне или теле желудка. При микроскопии трабекулярное или плотное расположение клеток. Опухолевые клетки мономорфные, среднего размера, правильной формы, с округлыми ядрами. Митозы либо отсутствуют, либо редкие. Распространение опухоли ограничено слизистой или подслизистым слоем. Гастрин-зависимые НЭО желудка последовательно связаны с генерализованной пролиферацией эндокринных клеток в слизистой оболочке части органа, не пораженной опухолевым процессом. Гистопатологическая классификация была сформулирована для спектра пролиферативных поражений, представленных фундальными эндокринными клетками пациентов с гипергастринемией. Эта классификация распределяет опухоли I типа в последовательности, предположительно отражающей временную эволюцию процесса и увеличивающийся онкологический риск для пациентов. Диагностика НЭО желудка требует эффективного гистопатологического, биохимического и диагностического анализа изображений [3].
Большинство опухолевых клеток первого типа являются позитивными в отношении эндокринных маркеров, таких как хромогранин А (CgA), нейрон-специфическая енолаза (NSE) и транспортер везикулярного моноамина 2, которые характеризуют клетки как гистамин-продуцирующие. Определение экспрессии CgA может быть полезным диагностическим тестом при подозрении на НЭО желудка первого типа. Но концентрация CgA коррелирует с количеством энтерохромаффиноподобных клеток; таким образом, патологически высокая концентрация CgA не является ни патогномоничной, ни необходимой для диагностики НЭО желудка первого типа. Маркер пролиферации MKI67 обычно экспрессируется менее чем в 2 % опухолевых клеток. Опухоли обычно развиваются бессимптомно, диагноз ставят случайно во время гастроскопии. Разрушение париетальных клеток из-за хронического атрофического гастрита в течение длительного времени может привести к снижению секреции внутреннего фактора Касла и, как следствие, к нарушению всасывания витамина B12. Таким образом, дефицит витамина B12 и гиперхромная макроцитарная анемия часто связаны с аутоиммунным атрофическим гастритом и гипергастринемией [3].
НЭО желудка первого типа очень редко метастазируют (5 % для локальных лимфатических узлов, менее 2 % с отдаленными метастазами), без связанных с этим случаев смерти и при стопроцентной длительной выживаемости. Эндоскопическое ультразвуковое исследование может быть полезным для получения картины локализованного заболевания (то есть отсутствия инфильтрации в подслизистом слое), в то время как компьютерная томография (КТ) может выявить метастазы в печени. В зависимости от размера и количества поражений эндоскопическая резекция опухоли является методом выбора [3].
II тип
5–6 % НЭО желудка являются опухолями типа II, которые возникают из гастрин-секретирующей ткани при синдроме Золлингера-Эллисона. Клиническое течение НЭО желудка II типа сходно с опухолями первого типа. Опухоли небольшие (1–2 см), множественные и высоко дифференцированные. Маркер пролиферации MKI67 экспрессируется в 2 см, в среднем 5,1 см), обычно встречаются поодиночке и растут из тела/дна желудка. Находящиеся рядом участки слизистой оболочки желудка без атрофических изменений. НЭО желудка III типа агрессивны и отличаются глубокой инвазией, ранним формированием метастазов. Прогноз неблагоприятный. Как правило, более 2 % опухолевых клеток экспрессируют маркер пролиферации MKI67, но отрицательны на CgA. Гистологически этот тип опухоли характеризуется большими, плохо определяющимися твердыми агрегатами или диффузными массами круглых или веретенообразных клеток. Обнаружены обильные митозы (>1 в поле зрения микроскопа при большом увеличении), часто встречается очаговый некроз. Ультраструктурные исследования подтверждают наличие эндокринных гранул.
Хирургическая резекция и диссекция лимфатического узла являются методом выбора. В зависимости от локальных характеристик роста злокачественных опухолей типа III, лечение может включать расширенную радикальную операцию резекции желудка и регионарную лимфаденэктомию [3].
IV тип
НЭО желудка IV типа — это редкие, крупные, слабо дифференцированные опухоли, которые являются крайне злокачественными. Самая большая из известных НЭО желудка IV типа составляет 16 см. В большинстве случаев во время диагностики НЭО желудка IV типа уже видна инвазия в лимфатические и кровеносные сосуды. Картина при низкодифференцированных НЭО желудка IV характеризуется тяжелой патологией с преобладающей твердой структурой, обильным центральным некрозом и выраженным клеточным атипизмом с частыми атипичными митозами и высоким уровнем MKI67 (>30). CgA обычно отсутствует или экспрессируется только в очаге, что согласуется с небольшим количеством электронно-плотных гранул в ультраструктуре. Выражена экспрессия синаптофизина и цитозольных маркеров NSE и PGP9.5. Несмотря на редкость, низкодифференцированные опухоли IV типа заслуживают особого внимания из-за их агрессивного характера и неблагоприятного прогноза: медиана выживаемости составляет от 6,5 до 14,9 месяцев [3].
НЭО желудка IV типа требует хирургической резекции с последующей химиотерапией и комбинированной адъювантной терапией [3].
Список литературы: