Нефропатия
Для жителей районов Савеловский, Беговой, Аэропорт, Хорошевский
В этом месяце жителям районов Савеловский, Беговой, Аэропорт, Хорошевский» предоставляется скидка 5% на ВСЕ мед.
Скидки для друзей из социальных сетей!
Гуляев Сергей Викторович
Врач-ревматолог, терапевт, нефролог
Кандидат медицинских наук
Нефропатией в медицине обозначается поражение почек, лишающее их основной фильтрационной функции в значительной, а при отсутствии своевременного лечения, и в полной степени. Нефропатия – одна из основных причин почечной недостаточности.
Причины и симптомы нефропатии
Нефропатию может вызывать ряд заболеваний, прежде всего, сахарный диабет, эндокринные расстройства, токсические отравления, онкологические заболевания и т.д.
Возникнув на фоне какого-либо заболевания или вследствие того или иного негативного воздействия на здоровье человека, нефропатия может развиваться довольно медленно, первое время не проявляя себя особыми симптомами.
Затем появляются слабость, одышка и утомляемость, головные боли, боли в поясничной области. Человек начинает чаще испытывать жажду.
При дальнейшем развитии нефропатии начинают появляться отёки, возникают проблемы с давлением. Возникает угроза появления хронической почечной недостаточности.
Кроме того, на фоне нефропатии возрастает риск воспалительных заболеваний почек – пиелонефритов.
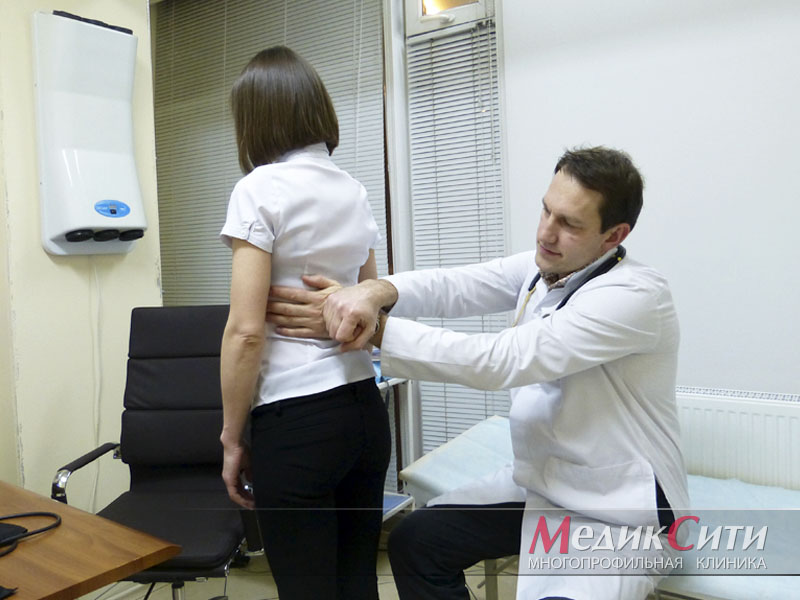
Консультация нефролога в МедикСити
Консультация нефролога в МедикСити
Консультация нефролога в МедикСити
Диагностика и лечение нефропатии
Чтобы избежать негативных последствий развития нефропатии, необходимо своевременно обращаться к врачу. В тех случаях, когда нефропатия возникает на фоне диабетических или онкологических заболеваний, её появление могут выявить при регулярных обследованиях на основании анализов крови и мочи. Признаками нефропатии являются протеинурия (белок в моче), увеличение плотности мочи и др.
Что же касается тех, кто подвергается риску развития нефропатии вследствие токсических отравлений, радиационного облучения и т.д., то им необходимо помнить о риске возникновения подобных проблем и своевременно обследоваться на предмет выявления возможных негативных последствий.
Беременные женщины также должны следить за своим состоянием – нефропатия может развиться вследствие сильного токсикоза.
Лечение нефропатии осуществляется, как правило, медикаментозным путем в условиях стационара.
Основной задачей при этом является купирование развития почечной недостаточности.
При своевременной медицинской помощи нефропатия полностью излечима, и функции почек могут быть восстановлены.
Важно учитывать, что наиболее эффективным противодействием развитию нефропатии является устранение вызвавших её причин, либо их должная профилактика.
Всё это требует внимания высокопрофессиональных опытных специалистов.
В клинике «МедикСити» к вашим услугам опытные врачи-терапевты, врачи-нефрологи, врачи-иммунологи и другие специалисты, в распоряжении которых первоклассная, оснащённая самым современным оборудованием лечебно-диагностическая база, уникальные методики диагностики и лечения заболеваний урологических, нефрологических и других профилей.
Почечная недостаточность: симптомы, стадии, лечение
Почечная недостаточность – острое или хроническое заболевание, при котором нарушаются фильтрационная, выделительная и другие функции почек с развитием многочисленных сбоев в работе всего организма. При этом происходит отравление собственными токсичными продуктами обмена веществ, попавшими в кровь – уремия. Патология, особенно при стремительном развитии, может угрожать жизни больного и требует скорейшего лечения.
Распространенность хронической болезни почек во всем мире в среднем составляет 13,4%. В России почечная недостаточность встречается у 36% лиц старше 60 лет и у 16% граждан трудоспособного возраста.
Причины
Хроническая форма заболевания чаще всего развивается как осложнение других патологий. Ранее основной причиной почечной недостаточности считался гломерулонефрит. В настоящее же время ведущее место занимают гипертоническая болезнь и сахарный диабет, приводящие к поражению мелких сосудов, питающих почки, и стойкому нарушению кровообращения в них.
Острая почечная недостаточность (ОПН) более чем в половине случаев связана с травмой или перенесенными операциями на органах малого таза. Развивается она также при неправильном приеме лекарственных препаратов, нарушении работы сердца, кровотечениях и шоке, генерализованной аллергической реакции, обезвоживании, циррозе, отравлении, аутоиммунных и инфекционных болезнях, онкологии, переливании несовместимой крови.
Симптомы почечной недостаточности
Почки не только очищают кровь от токсинов и выводят их из организма, но также регулируют водно-солевой баланс, контролируют уровень артериального давления, тонус сосудов, концентрацию гемоглобина, помогают в сохранении здоровья опорно-двигательного аппарата и сердца. Учитывая такое многообразие функций органа, почечная недостаточность проявляется многочисленными симптомами, выраженность которых зависит от стадии и формы заболевания.
При остром повреждении почек на начальной стадии имеются лишь проявления основного заболевания. Далее следует самая тяжелая, олигурическая стадия, продолжительностью до 3-х недель, со снижением суточного объема мочи менее 500 мл. Первым признаком болезни становится резкое уменьшение или прекращение мочеиспускания.
Состояние часто обратимо (если обратимо основное заболевание или состояние, приведшее к ОПН) и при правильном лечении переходит в полиурическую стадию почечной недостаточности с восстановлением объема мочи. При этом самочувствие пациента нормализуется, но может развиваться обезвоживание организма и присоединиться инфекция. Стадия полного восстановления продолжается от шести месяцев до года. При выраженных нарушениях состояние переходит в хроническую форму.
Хроническая почечная недостаточность (ХПН) развивается медленно, в течение нескольких месяцев и даже лет, и приводит к стойким изменениям в органе. На начальном этапе специфических симптомов обычно не бывает, но иногда человек может заметить снижение объема выделяемой мочи. Либо единственным проявлением патологии может быть никтурия – частое ночное мочеиспускание.
Осложнения
Болезнь осложняется появлением артериальной гипертензии, анемии, перикардита, аритмии и сердечной недостаточности, остеопороза, подагры, энцефалопатии, язвенной болезни желудка и двенадцатиперстной кишки, атеросклероза сосудов с развитием инфаркта и инсульта, синдрома беспокойных ног.
У детей почечная недостаточность приводит к задержке роста костной ткани.
Развитие почечной недостаточности у женщин во время беременности сопряжено с невынашиванием плода или формированием у него врожденных пороков.
Без лечения ХПН может закончиться смертью пациента от сердечно-сосудистых осложнений или уремической комы.
Диагностика
При первичном обследовании врач собирает анамнез заболевания, уточняя жалобы и давность симптомов. Далее проводятся осмотр кожных покровов, пальпация и поколачивание пальцами поясничной области.
Лечение почечной недостаточности
Обязательно проводятся диагностика и лечение патологии, послужившей причиной почечной недостаточности, а также устранение факторов риска.
При выраженном или длительном нарушении фильтрационной функции почек пациенту показано аппаратное очищение крови – гемодиализ. Процедура проводится регулярно и позволяет убрать из организма токсичные вещества. Альтернативой выступает перитонеальный диализ, при котором в брюшную полость вводится с последующим удалением специальный раствор, забирающий на себя вредные вещества.
В случае тяжелого течения хронической почечной недостаточности выполняется операция по трансплантации почки. После пересадки проводится курс терапии препаратами, подавляющими иммунитет, чтобы не произошло отторжения донорской ткани.
Диабетическая нефропатия: современные принципы классификации, диагностики и особенности сахароснижающей терапии

Статья посвящена современным подходам к терапии сахарного диабета, осложненного поражением почек. Сахарный диабет является важнейшей проблемой современной медицины, что прежде всего обусловлено высокой распространенностью заболевания среди трудоспособного
Abstract. The article is devoted to modern approaches to the treatment of diabetes mellitus complicated by kidney damage. Diabetes mellitus is the most important problem of modern medicine, which is primarily due to the high prevalence of the disease among the working-age population. Diabetic nephropathy is one of the severe chronic complications of diabetes, which increases the disability and mortality of patients. Diabetic nephropathy is the main cause of the development of end-stage renal failure in developed countries and eventually affects about 30% of patients. Kidney damage in patients with diabetes occurs in 6-7% of cases out of the total number of nephropathies in patients receiving treatment in a specialized nephrological department of a multidisciplinary hospital. The first manifestations of diabetic nephropathy develop 3-4 years after the onset of the disease, and reach their peak in 15-20 years. The concept of «chronic kidney disease» includes kidney damage regardless of the primary diagnosis and is characterized by such basic diagnostic criteria as urinary albumin excretion and glomerular filtration rate values, which are markers of kidney damage. Methods for preventing the progression of diabetic nephropathy include general measures to change the lifestyle, control of glycemia and blood pressure, correction of lipid metabolism disorders in combination with nephroprotective therapy. Currently, when choosing therapy in patients with type 2 diabetes mellitus in combination with chronic kidney disease, along with taking metformin, preference is given to sodium-glucose cotransporter type 2 inhibitors and glucagon-like peptide-1 receptor agonists with a nephroprotective effect. For citation: Borisov A. G., Chernavskiy S. V., Smirnova M. A., Stremoukhov A. A. Diabetic nephropathy: modern principles of classification, diagnosis and features of antihyperglycemic therapy // Lechaschy Vrach. 2021; 9 (24): 53-58. DOI: 10.51793/OS.2021.24.9.010
Pезюме. Статья посвящена современным подходам к терапии сахарного диабета, осложненного поражением почек. Сахарный диабет является важнейшей проблемой современной медицины, что прежде всего обусловлено высокой распространенностью заболевания среди трудоспособного населения. Диабетическая нефропатия – одно из тяжелых хронических осложнений диабета, повышающее инвалидизацию и смертность пациентов. Диабетическая нефропатия является основной причиной развития терминальной почечной недостаточности в развитых странах и со временем затрагивает около 30% пациентов. Поражение почек у больных сахарным диабетом встречается в 6-7% случаев из общего числа нефропатий у пациентов, получающих лечение в специализированном нефрологическом отделении многопрофильного стационара. Первые проявления диабетической нефропатии развиваются через 3-4 года от дебюта заболевания и достигают своего пика через 15-20 лет. Понятие «хроническая болезнь почек» включает в себя поражение почек независимо от первичного диагноза, характеризующееся такими основными диагностическими критериями, как экскреция альбумина с мочой и значения скорости клубочковой фильтрации, которые являются маркерами повреждения почек. Методы предупреждения прогрессирования диабетической нефропатии включают в себя общие мероприятия по изменению образа жизни, контроль гликемии и артериального давления, коррекцию нарушений липидного обмена в сочетании с нефропротективной терапией. В настоящее время при выборе терапии у больных сахарным диабетом 2 типа в сочетании с хронической болезнью почек наряду с приемом метформина предпочтение отдается ингибиторам натрий-глюкозного котранспортера 2-го типа и агонистам рецепторов глюкагоноподобного пептида-1, обладающим нефропротективным эффектом.
В настоящее время сахарный диабет (СД) является одной из актуальных проблем современной медицины. Прежде всего это связано с высокой распространенностью заболевания среди трудоспособного населения. Согласно прогнозам, к 2040 г. число людей, страдающих СД в возрасте 20-79 лет, увеличится до 642 миллионов [1, 2].
Немаловажным является и социально-экономическое значение заболевания. Развитие хронических осложнений СД существенно увеличивает раннюю инвалидизацию и смертность больных [3].
Наибольшая опасность, безусловно, связана с развитием сердечно-сосудистых осложнений (ССО) у данных пациентов. Также важное место в этом ряду занимает и диабетическая нефропатия (ДН), которая развивается приблизительно у 20,1% и 6,3% больных СД 1 и 2 типа соответственно [4, 5].
Изучение проблемы поражения почек при СД имеет длительную историю. Еще в 1836 г. британский врач Ричард Брайт отметил наличие у больных СД протеинурии (ПУ), что является признаком почечного повреждения [6]. В дальнейшем в 1936 г. американскими патологоанатомами P. Kimmelstiel и C. Wilson впервые была описана патоморфология почек у пациентов, страдающих СД [7].
У больных СД 2 типа осложнения ДН занимают третье место среди причин смерти после сердечно-сосудистых заболеваний (ССЗ) и злокачественных новообразований [1]. Кроме того, на сегодняшний день нефропатия, ассоции-рованная с СД 2 типа, является главной причиной терминальной почечной недостаточности (ТПН) в Европе, США и Японии [8]. Ранняя диагностика и своевременное обеспечение лечебно-профилактических мероприятий больным СД являются залогом предупреждения развития ДН.
Определение, распространенность и патогенез ДН
Под ДН понимают специфическое поражение всех структур почек (клубочков, канальцев, интерстиция и сосудов), возникающее при СД и сопровождающееся формированием узелкового гломерулосклероза, что может приводить к развитию ТПН, требующей проведения заместительной почечной терапии (диализ, трансплантация). Повреждение клубочков связано с утолщением их базальной мембраны, увеличением объема мезангиального матрикса и последующим развитием узелкового и/или диффузного интеркапиллярного гломерусклероза. Тубулоинтерстициальные изменения заключаются в дистрофии и атрофии эпителия канальцев, фиброзе интерстиция, а сосудистые – в развитии артериогиалиноза и артериосклероза. «Специфическое поражение структур почек» означает, что при отсутствии гипергликемии структурные изменения почек, характерные для СД, не выявляются [9].
Распространенность ДН непрерывно увеличивается, что происходит в результате взаимодействия генетических и средовых факторов у больных как с 1, так и со 2 типом СД. По международным данным максимальный пик развития ДН наблюдается при длительности заболевания от 20 до 30 лет и составляет при СД 1 типа 30-40%, а при СД 2 типа – 35-50%. В России распространенность ДН в среднем составляет при СД 1 типа 19%, при СД 2 типа – 8%. В то же время активный скрининг больных СД 2 типа показывает, что истинная распространенность ДН превышает зарегистрированную от 2 до 8 раз [10, 11].
Частота выявления ДН находится в тесной зависимости от длительности СД. Эта зависимость более изучена при СД 1 типа вследствие более точного определения дебюта заболевания. Частота развития ДН у больных с длительностью СД 1 типа до 10 лет составляет 5–6%, до 20 лет – 20–25%, до 30 лет – 35–40%, до 40 лет – 45%, а максимальный пик развития ДН приходится на сроки от 15 до 20 лет существования СД. Важно отметить, что наряду с классическим диабетическим гломерулосклерозом у больных СД 2 типа часто развивается поражение почек недиабетического генеза (хронический пиелонефрит, мочекаменная болезнь, ишемическая нефропатия и т. д.). Возможность сочетания нескольких форм нефропатии значительно повышает риск необратимого ухудшения функции почек. Установлено, что у пациентов с впервые выявленным СД 2 типа микроальбуминурия (МАУ) уже обнаруживается в 15-40% случаев, ПУ – в 7-10%, а хроническая почечная недостаточность (ХПН) – в 1%. Скорее всего это отражает позднюю диагностику ДН вследствие низкой информированности врачей первичного звена. При относительно точном определении времени дебюта СД 2 типа прослеживается такая же, как и при СД 1 типа, зависимость частоты развития ДН от длительности заболевания: 7-10% при длительности СД 5 лет, 20-35% – при длительности 20-25 лет и 50-57% – при более длительных сроках течения болезни [11].
По данным ГВКГ им. Н. Н. Бурденко доля больных с ДН среди всех пациентов, получающих лечение в нефрологическом отделении, составляет в среднем 6,4% (рис. 1).
В то же время обследование больных эндокринологического отделения ГВКГ им. Н. Н. Бурденко показало, что ДН диагностируется у 35,6% больных с СД 1 типа и 43,1% – СД 2 типа (рис. 2) при сроке заболевания 25 лет. Первые признаки ДН выявляются через 3-4 года от дебюта СД, и частота ее достигает максимума после 20 лет течения болезни.
ДН развивается под действием огромного ряда причин. Но из всего многообразия механизмов ее развития наиболее изученными и доказанными являются метаболические (гипергликемия, гиперлипидемия) и гемодинамические (внутриклубочковая гипертензия, артериальная гипертензия (АГ)).
Безусловно, одним из самых важных метаболических факторов, инициирующих повреждение почек, является гипергликемия. В условиях гипергликемии образуются стабильные продукты гликозилирования, которые приводят к нарушению конфигурации мембраны клубочков, пролиферации гладкомышечных клеток артериол и усилению перекисного окисления липидов. В конечном итоге происходит утолщение гломерулярной базальной мембраны и развитие гломерулосклероза. Кроме того, увеличивается экспрессия в подоцитах сосудистого эндотелиального фактора роста, который аутокринно усиливает свою активность и приводит к повреждению ткани почек [12].
Большую роль в развитии ДН играет гиперлипидемия. Окисленные липопротеиды низкой плотности, ростовые факторы и цитокины увеличивают синтез компонентов мезангиального матрикса, ускоряя склерозирование клубочков. В свою очередь липиды, профильтровавшиеся в первичную мочу, могут приводить к повреждению клеток почечных канальцев [13].
АГ у пациентов с СД является самым мощным фактором прогрессирования хронической болезни почек (ХБП), который во много раз превышает по своему влиянию гипергликемию и гиперлипидемию. Внутриклубочковая гипертензия является основным гемодинамическим фактором развития ДН, которая возникает вследствие токсического действия гипергликемии и активации вазодилатирующих гормонов с развитием дилатации приносящей клубочковой артериолы, с одной стороны, а с другой – за счет активации местного ангиотензина II с констрикцией выносящей почечной артериолы [14].
Классификация и клинические проявления ДН
Впервые детальная классификация стадий ДН была разработана датским исследователем С. Е. Mogensen в 1983 г. Основу ее составляли показатели функциональных и структурных изменений почек (изменения скорости клубочковой фильтрации (СКФ), утолщение базальных мембран клубочков, наличие МАУ или ПУ) [15].
До последнего времени в РФ использовалась классификация ДН от 2000 г., предусматривавшая следующие стадии: микроальбуминурии, ПУ с сохранной азотовыделительной функцией почек и ХПН [16].
Показатель креатинина сыворотки крови использовался долгое время как основной маркер нарушения азотовыделительной функции почек. Благодаря последним исследованиям стало ясно, что из-за компенсаторных возможностей почек его цифры долгие годы могут соответствовать нормальным значениям, в то время как СКФ уже снижена.
Современная классификация ДН основывается на принципах стадирования ХБП, которую возможно диагностировать, если в течение трех и более месяцев имеются отклонения в анатомо-морфологической структуре или функции почек вне зависимости от нозологического диагноза [9]. Уровень СКФ в настоящее время признан лучшим методом оценки функции почек в целом как у здоровых лиц, так и при различных заболеваниях. Именно ее уровень определяет различные стадии ХБП (табл. 1).
Оценка степени поражения почек у больных СД существенно изменилась. Произошел переход от изолированной оценки АУ/ПУ в качестве классического маркера ДН к определению стадии ДН в зависимости от уровня СКФ, дополняя ее индексацией АУ/ПУ. АУ/ПУ рассматриваются как маркеры патологии почек, которые отражают степень повреждения клубочкового аппарата почек (табл. 2).
По данным международных клинико-эпидемиологических исследований, ХБП регистрируется у 40-60% пациентов с СД 2 типа. По данным федерального регистра, в 2016 г. в среднем по РФ ХБП выявлялась у пациентов с СД 1 типа в 23% случаев и при СД 2 типа – в 6,9% случаев. СКФ менее 60 мл/мин у больных СД 1 типа с ДН встречается в 50-60% случаев при наличии стойкой ПУ и в 70–80% случаев – у пациентов с СД 2 типа [2].
По данным ГВКГ им. Н. Н. Бурденко, у 2/3 пациентов, получающих лечение в специализированном нефрологическом отделении с ДН, наиболее часто диагностируются ХБП на стадии 3-5 (табл. 3).
У этих пациентов, кроме типичных осложнений СД, имеется высокий риск развития ССО. Кроме того, наличие ХБП высоких градаций вносит ряд ограничений в возможности сахароснижающей терапии.
У ДН отсутствуют специфические симптомы, клиническую картину определяют собственно проявления СД, его осложнения и проявления ХБП. Основными клиническими проявлениями ХБП являются АУ/ПУ, АГ, анемия, электролитные нарушения, ацидоз, нарушения фосфорно-кальциевого обмена, может присутствовать отечный синдром вследствие формирования нефротического синдрома и/или задержки жидкости в организме.
Диагностика ДН
При появлении ПУ у больного СД с длительным анамнезом заболевания (более 10 лет), с выраженной диабетической ретинопатией и другими признаками микро- и макрососудистых осложнений диагноз ДН не вызывает сомнений. Для ее выявления выполняются обязательные методы лабораторной диагностики: определение соотношения альбумин/креатинин в утренней порции мочи, общеклинический анализ мочи с оценкой содержания белка, суточная ПУ, исследование осадка мочи, определение концентрации в сыворотке крови креатинина, мочевины и калия. При необходимости выполняются ультразвуковое исследование почек и сонографическое исследование почечных артерий.
В настоящее время в клинической практике для расчета СКФ у взрослого населения используют следующие расчетные формулы: Кокрофта–Голта 1976, MDRD 1999, CKD–EPI 2011.
Общепризнанным является тот факт, что наиболее точным расчетным методом определения СКФ является формула CKD–EPI [17].
СКФ = 141 × min(СКР/k, 1)a × max(СКР/k, 1) – 1,209 × 0,993возраст
[× 1,018 для женщин] [× 1,159 для лиц негроидной расы],
где СКР — креатинин сыворотки крови (мг/дл); k – 0,7 (для женщин) или 0,9 (для мужчин); a – коэффициент, равный – 0,329 (для женщин) или – 0,411 (для мужчин).
Поскольку в РФ величина креатинина измеряется в мкмоль/л, необходимо перевести ее в мг/дл, для этого значение нужно разделить на коэффициент 88,4 (т. е. 100 мкмоль/л соответствует 1,13 мг/дл).
Имеется ряд ситуаций, при которых расчетные методы применять не совсем корректно. К ним относятся:
В этих ситуациях СКФ необходимо определять с использованием клиренсовых методов (проба Реберга–Тареева).
Особенности сахароснижающей терапии при ДН
Принципы лечения ДН основаны на коррекции факторов прогрессирования ДН и ХБП с целью предупреждения развития ТПН и снижения риска ССО. Основными направлениями терапии являются компенсация нарушений углеводного, липидного, кальций-фосфорного обмена, анемии и достижение целевых значений АД.
Компенсация углеводного обмена играет ключевую роль в профилактике развития и замедлении прогрессирования ХБП у больных СД. Ряд клинических исследований показал, что строгий контроль гликемии позволяет не только предотвратить развитие ДН у лиц, не страдающих ею, но и затормозить прогрессирование этого осложнения у больных с АУ и ПУ. Это утверждение справедливо как для больных СД 1 типа (исследование DCCT), так и для больных СД 2 типа (исследование UKPDS) [11].
Прогрессирование азотемии, проявляющееся в снижении СКФ, значительно сужает спектр возможного применения пероральных сахароснижающих препаратов (табл. 4).
Клинические практические рекомендациии KDIGO (Kidney Disease Improving Global Outcomes Quality Initiative – Инициатива по улучшению глобальных исходов заболеваний почек) рассматривают гликемический контроль как часть мультифакторной интервенционной стратегии, направленной на контроль АД и кардиоваскулярного риска. В них определены целевые уровни HbA1c у лиц с СД и ХБП с учетом имеющихся рисков. HbA1c
* ФГБУ ГВКГ им. Н. Н. Бурденко МО России, Москва, Россия
** ФГБОУ ДПО РМАНПО Минздрава России, Москва, Россия
Диабетическая нефропатия: современные принципы классификации, диагностики и особенности сахароснижающей терапии/ А. Г. Борисов, С. В. Чернавский, М. А. Смирнова, А. А. Стремоухов
Для цитирования: Борисов А. Г., Чернавский С. В., Смирнова М. А., Стремоухов А. А. Диабетическая нефропатия: современные принципы классификации, диагностики и особенности сахароснижающей терапии // Лечащий Врач. 2021; 9 (24): 53-58. DOI: 10.51793/OS.2021.24.9.010
Теги: сахарный диабет, почки, контроль гликемии, нефропротективная терапия




.png)
.gif)
.gif)
.gif)
.gif)
.gif)



