натальный скрининг что это такое
Для чего нужен неонатальный скрининг?
Врачи-неонатологи роддома больницы Вересаева рассказали, для чего нужен неонатальный скрининг, кому положен и когда проводится.
Неонатальный скрининг – важное обследование, позволяющее уже в первые дни жизни ребенка выявить серьезные врожденные патологии. Неофициально его называют «пяточным» тестом, поскольку кровь берется из пяточки и наносится на специальный тест-бланк.
Скрининг, который проводится в массовом порядке всем новорожденным, позволяет исключить такую пятерку серьезных заболеваний, как муковисцидоз (генетическая мутация, поражающая экзокринные железы органов дыхательной и пищеварительной систем); галактоземию (нарушение углеводного обмена), адреногенитальный синдром (нарушения, связанные с избыточной секрецией гормонов коры надпочечников), врожденный гипотиреоз (заболевание щитовидки) и фенилкетонурию (нарушение метаболизма аминокислот).
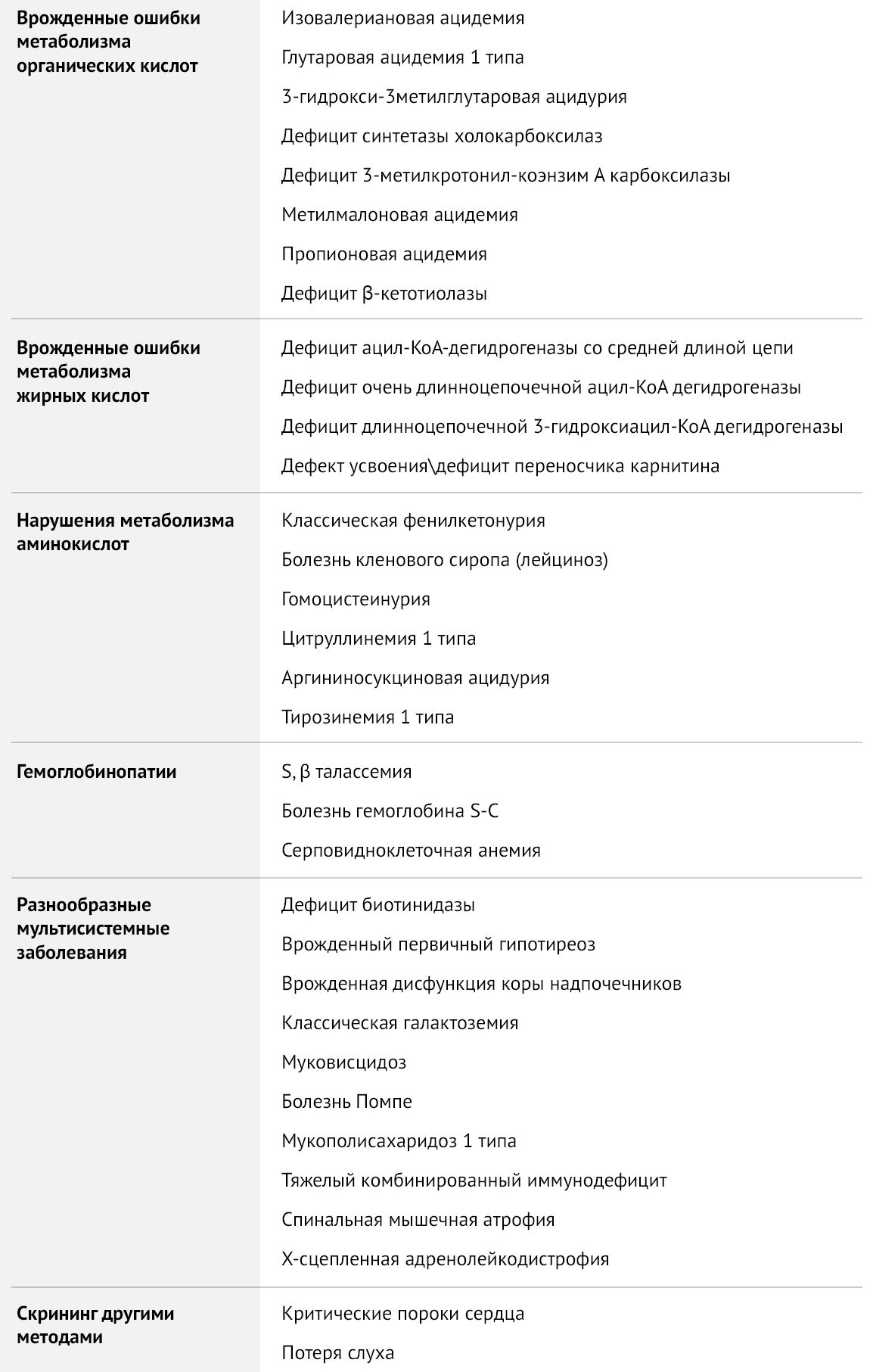
В Москве список расширен до 11 показателей, в него добавлена диагностика еще шести заболеваний из группы органических ацидурий, аминоацидопатий и нарушений обмена жирных кислот.
Все эти наследственно-генетические заболевания встречаются крайне редко, однако «поймать» их важно вовремя, поскольку их своевременное выявление позволяет избежать необратимых последствий и выбрать правильную тактику лечения.
Обычно скрининг делают в роддоме на четвертый день жизни младенца (для недоношенных малышей срок сдвигается), однако в Москве принята ранняя выписка: и мама с малышом (после естественных родов) могут оказаться дома уже на вторые сутки. Если тест не успеют провести в роддоме, то на руки родителям выдадут специальный бланк, где будет указана необходимость проведения скрининга. В таком случае анализ возьмет патронажная медсестра, которая придет навестить малыша в первые дни.
Анализ берут натощак после «голодной» паузы в три часа.
С февраля 2020 года расширенный неонатальный скрининг на 11 заболеваний доступен всем малышам, родившимся в Москве и получившим свидетельство о рождении в роддоме. Исследование проводится бесплатно.
Анализ готовится быстро. На связь с родителями специалисты выйдут только в случае, если какая-либо патология обнаружится. Однако большинство может забыть о тесте сразу после его выполнения, ведь частота встречаемости скринируемых заболеваний крайне мала.
Можно ли отказаться от неонатального скрининга?
Можно, но не стоит. Ведь именно в первые дни жизни малыша можно выстроить максимально эффективную схему лечения, которая в дальнейшем позволит ребенку избежать тяжелых осложнений и инвалидизации.
Натальный скрининг что это такое
Определение сатурации, то есть степени насыщения крови кислородом, также на верхних и нижних конечностях. Для этого используется специальный прибор — детский пульсоксиметр.
Проанализировав полученные данные, врач дает оценку скрининга: он положительный (если что-то внушает подозрение) или отрицательный (когда все показатели в пределах нормы).
Также на третьи сутки малышу выполняется неонатальный аудиологический скрининг, цель которого — выявить потенциальное нарушение слуха. Именно к третьему дню жизнидетское ушко естественным путем освобождается от фрагментов первородной смазки или капелек околоплодных вод, поэтому скрининг становится более информативным.
Аудиоскрининг выполняется при помощи специального прибора (аудиометра), оснащенногодатчиком с высокочувствительным микрофоном. Сверху на него перед исследованием надевают мягкий наконечник (ушной вкладыш) и поочередно вставляют в правый и левый слуховой проход ребенка.
Результат приема детским ушком звукового импульса отображается сразу на мониторе. Если врачу что-то не понравится в нем, ребенок будет записан в группу риска по развитию тугоухости, но уже не в нашей больнице, а по месту жительства. Там, пока малыш не достигнет 3-месячного возраста, ему будут проведены дополнительные обследования, которые либо подтвердят диагноз тугоухости, либо снимут его.
Обращаю внимание, что в группу риска по тугоухости входят дети, перенесшие асфиксию в родах (не сразу закричавшие), родившиеся после переношенной беременности, имеющие дефицит веса или получавшие серьезную лекарственную терапию сразу после родов в связи с каким-то врожденным заболеванием. Такие дети, независимо от результата проведенного аудиологического скрининга в роддоме, также до 3-х месяцев будут обследованы повторно в поликлинике.
«Пяточный тест»: обычный и расширенный неонатальный скрининг
Неонатальный скрининг, известный как «пяточный тест» (или скрининг «пяточка», как называют его мамы) проводят всем новорожденным малышам без исключения. Анализ позволяет выявить наиболее распространенные генетические заболевания, которые представляют угрозу для жизни и здоровья ребенка.
Столь ранняя диагностика просто необходима, ведь дает возможность врачам своевременно начать лечение и избежать тяжелых осложнений. В России длительное время проводился неонатальный скрининг всего 5 наследственных заболеваний. Однако время не стоит на месте. С развитием новых технологий стало возможным расширить перечень болезней. Что сегодня включает «пяточный тест»?
Неонатальный скрининг: как проводится?
Обследование на генетические заболевания проводят детям в первые 10 дней после рождения. Забор капиллярной крови из пяточки выполняют медицинские сотрудники родильного дома или поликлиники доношенным детям на 4 сутки жизни, а недоношенным — на 7 сутки жизни.
Почему скрининг проводят так рано? Такие сроки обследования связаны с тем, что болезни, на которые проверяют малышей, дебютируют в первые месяцы жизни и угрожают развитием тяжелых необратимых осложнений.
Лечение, начатое до появления первых симптомов, увеличивает шансы на успех. Ребенок сможет полноценно расти и развиваться наравне со сверстниками.
Пребывая в хлопотах и заботах, родители порой забывают о том, что их малышу проводили скрининг. Действительно, ведь при отсутствии отклонений от нормы информировать их не принято. Зато при повышении того или иного показателя, у ребенка в кратчайшие сроки возьмут кровь на повторный анализ.
В дальнейшем, если диагноз будет подтвержден, то наблюдение и лечение будет осуществлять специалист в профильном учреждении.
Неонатальный скрининг: прошлое и настоящее
Неонатальный скрининг сейчас — это простой, доступный и перспективный метод обследования новорожденных для выявления тяжелых наследственных заболеваний.
Его история началась в 1960-х годах в США с проведения биохимического теста на выявление фенилкетонурии.
Затем технология распространилась во многих странах мира и стала основой для создания перечня генетических болезней, которые можно диагностировать у детей в первые дни после рождения.
Существуют определенные критерии, по которым заболевание включается в перечень для скрининга в стране:
Пожалуй, последний пункт особенно важен. Ведь основная цель неонатального скрининга — не столько выявить заболевание, сколько начать вовремя лечение, чтобы обеспечить полноценную жизнь ребенку.
На сегодняшний день неонатальный скрининг проводится более чем в 50 странах мира, а перечень насчитывает более 50-60 заболеваний.
При домашних родах или ранней выписке из родильного дома обследование тоже проводят. И пройти его нужно обязательно, это в интересах и родителей, и малыша.
Неонатальный скрининг: 5 основных заболеваний
В большинстве регионов России проводится неонатальный скрининг на 5 основных генетических заболеваний.
Характеризуется поражением центральной нервной системы. Единственный способ избежать тяжелых последствий — соблюдение диеты с низким содержанием фенилаланина уже с первой недели жизни ребенка.
Проявления заболевания разнообразны: от тяжелых нарушений водно-солевого обмена и полиорганной недостаточности до неправильного развития половых органов, маскулинизации и в дальнейшем бесплодия у девочек. В качестве лечения используется заместительная гормонотерапия.
При отсутствии должного лечения происходит задержка психомоторного и речевого развития, наступает отставание в физическом и половом развитии. Показана пожизненная заместительная терапия препаратами тиреоидных гормонов.
Основная роль в лечении отводится диете с пожизненным исключением продуктов, содержащих лактозу и галактозу.
Наиболее ярко болезнь проявляет себя со стороны органов дыхания — респираторная форма. Она дебютирует в раннем возрасте, проявляется частыми ОРВИ, бронхитами и пневмониями, сопровождается постоянным приступообразным кашлем с густой мокротой. В дальнейшем появляются и нарастают явления дыхательной и сердечной недостаточности.
Лечение муковисцидоза симптоматическое (единственное исключение из обязательной «пятерки» скрининга) направлено на снижение вязкости мокроты, восстановление проходимости бронхов и устранение инфекционного воспаления.
Скрининг новорожденных входит в программу ОМС и проводится бесплатно.
Расширенный неонатальный скрининг
Современная технология диагностики — тандемная масс-спектрометрия — позволила на порядок расширить перечень наследственных заболеваний, которые можно включить в программу скрининга новорожденных: болезни обмена веществ, гемоглобинопатии, спинальная мышечная атрофия, тяжелый комбинированный иммунодефицит и другие.
В Москве с 2018 года дополнительно включены 6 заболеваний, отвечающих критериям Всемирной организации здравоохранения:
Все эти заболевания со столь сложными названиями относят к врожденным болезням обмена веществ (ВБО) или врожденным аномалиям метаболизма.
Причина их появления — дефекты единичных генов, которые кодируют ферменты, способствующие превращению одних веществ в другие. В результате таких нарушений метаболизма происходит накопление токсических веществ, воздействующих на различные органы и ткани, и отмечается дефицит важных веществ.
25% всех врожденных болезней обмена веществ дебютирует уже в период новорожденности. При этом они протекают тяжело, часто скрываются под маской других заболеваний и могут привести к смерти ребенка без должного лечения.
Неонатальный скрининг позволяет предупредить дебют опасной болезни и вовремя начать терапию.
Все ВБО контролируются путем соблюдения соответствующей диеты, ограничивающей поступление в организм веществ, обмен которых нарушен. Или, наоборот, путем введения в организм недостающих метаболитов.
До внедрения технологии тандемной масс-спектрометрии в практику неонатального скрининга в Москве было проведено исследование в Свердловской области в 2012-2014 годах. Тестирование прошли более 150 тысяч новорожденных детей на 16 врожденных болезней обмена веществ. Всего было выявлено 9 больных детей, что составляет 1 случай на 1130 детей.
Результат близок к средней по стране распространенности этих заболеваний. Исследование доказало эффективность нового метода диагностики и возможность его внедрения в другие регионы страны.
Тяжелая комбинированная иммунная недостаточность — место в неонатальном скрининге
Первичные врожденные иммунодефициты характеризуются неспособностью организма противостоять микробам и вирусам. Это неизбежно приводит к частым инфекционным заболеваниям, протекающим тяжело, длительно, с осложнениями и необходимостью раз за разом принимать антибиотики.
Наиболее опасной формой первичного иммунодефицита является тяжелая комбинированная иммунная недостаточность (ТКИН), при которой у детей резко снижено число лимфоцитов.
Заподозрить врожденный иммунодефицит в первые месяцы жизни ребенка сложно, ведь какое-то время болезнь может ничем себя не проявлять или имитировать симптомы других более распространенных патологий. Однако именно время установления диагноза во многом определяет успех лечения.
Наиболее эффективный метод лечения детей с тяжелой комбинированной иммунной недостаточностью — это трансплантация гемопоэтических стволовых клеток. В случае ее проведения в возрасте до 3,5 месяцев и при отсутствии инфекционных процессов отмечается хороший результат.
Неонатальный скрининг на ТКИН уже проводится в США, Израиле, некоторых странах Европы, Ближнего Востока и Азии.
Внесение ТКИН в программу неонатального скрининга в нашей стране позволит на ранних сроках диагностировать тяжелый врожденный иммунодефицит, вовремя проводить соответствующее лечение и предупреждать инфекционные осложнения.
Неонатальный скрининг
Неонатальный скрининг, ласково именуемый в нашей стране «пяточка», является одним из первых важных исследований новорожденного. В России скрининг преимущественно направлен на выявление пяти наследственных болезней обмена: фенилкетонурии, врожденного гипотиреоза, врожденной дисфункции коры надпочечников (ВДКН), галактоземии и муковисцидоза. За рубежом этот список расширен до 50 различных заболеваний, в некоторых штатах Америки их свыше 60. Здоровый доношенный новорожденный допускается к скринингу на 4–5 сутки, недоношенный — на седьмой день после рождения. Заболевания, на выявление которых направлен скрининг, никак не проявляют себя в периоде новорожденности, но их ранняя диагностика и своевременно начатое патогенетическое лечение существенно влияют на прогноз и качество жизни ребенка. Помимо исследования крови проводится аудиометрия для оценки слуха и пульсоксиметрия для скрининга пороков сердца, но в данной статье мы преимущественно сосредоточимся на тестировании крови.
Разработка программы скрининга началась в шестидесятых годах прошлого века, когда Роберт Гатри создал технологию тестирования сухих отпечатков крови на фильтровальной бумаге. Первым заболеванием, которое стало кандидатом для массовой диагностики, была фенилкетонурия, так как ее раннее выявление и коррекция питания способны предотвратить развитие тяжелых неврологических нарушений. Затем к скринингу добавилось еще несколько заболеваний: врожденный гипотиреоз, ВДКН, галактоземия и муковисцидоз. Тандемная масс-спектрометрия (ТМС) позволила значительно расширить список заболеваний, добавив к болезням обмена веществ гемоглобинопатии, спинальную мышечную атрофию, тяжелый комбинированный иммунодефицит и др.
Таблица 1 | Рекомендуемая The American College of Obstetricians and Gynecologists (ACOG) скрининг-панель для врожденных заболеваний
В данной статье будут рассмотрены два скрининга, доступные в нашей стране: обязательный, включающий тестирование на пять заболеваний (врожденный гипотиреоз, ВДКН, фенилкетонурия, галактоземия, муковисцидоз) и расширенный скрининг на наследственные нарушения метаболизма.
Обязательный скрининг
На 4–5 сутки после рождения здорового доношенного ребенка или на седьмые сутки жизни недоношенного ребенка проводится тестирование методом «сухого пятна».
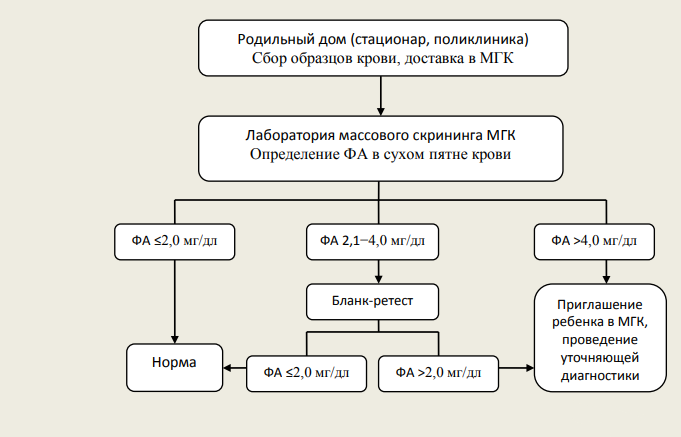
Фенилкетонурия (в современной классификации ― ФАГ-зависимая ФКУ) обусловлена мутацией гена фенилаланингидроксилазы и относится к числу аминокислотных аминоацидопатий. В норме фенилаланин (ФА) путем реакций гидроксилирования превращается в тирозин, однако в случае мутации вышеназванного гена активность превращающего фермента снижается, создается дефицит тирозина одновременно с избытком ФА, образующего токсичные метаболиты (фенилацетат, фенилпируват, фениллактат). Снижение образования тирозина влечет за собой нарушение синтеза гормонов щитовидной железы, нейротрансмиттеров и пигментов меланоцитов, а избыток ФА приводит к дисбалансу аминокислот в тканях мозга, обусловленному торможением их всасывания в желудочно-кишечном тракте или нарушением реабсорбции из почечных канальцев, нарушению образования или стабилизации полирибосом, снижению синтеза миелина, норадреналина и серотонина. Также за счет конкурентного ингибирования создается дефицит тирозиназы, что в совокупности с дефицитом тирозина приводит к снижению образования меланина и гипопигментации.
Основной проблемой пациентов с ФКУ являются нарушения функции ЦНС: от сонливости, вялости, отсутствия аппетита в период манифестации в 2–6 месяцев до тяжелых нарушений психомоторного развития в будущем; нередко развиваются атаксия, гиперкинезы, тремор рук, парезы по центральному типу. Единственный способ предотвратить развитие вышеназванных нарушений — назначение гипофенилаланиновой диеты с момента рождения с поддержанием низкого уровня фенилаланина в течение всей жизни.
Рисунок 1 | Интерпретация результатов исследования на наличие фенилкетонурии
ВДКН обусловлена дефицитом ферментов и транспортных белков, участвующих в биосинтезе кортизола. Наиболее часто встречается дефицит 21-гидроксилазы, что в свою очередь приводит к дефициту кортизола и альдостерона и ответному увеличению секреции АКТГ и гиперплазии коры надпочечников. В условиях дефицита фермента происходит значительное накопление предшественников гормонов, что приводит к увеличению синтеза тестостерона, не зависящего от 21-гидроксилазы. В итоге у пациента формируется надпочечниковая недостаточность и гиперандрогения. Гормональным маркером дефицита 21-гидроксилазы является уровень 17-гидроксипрогестерона (17-ОНП), определяемый в рамках неонатального скрининга. Результат трактуется как положительный, если при двукратном тестировании образца уровень 17-ОНП у доношенных новорожденных составляет ≥ 20 нг/мл. У недоношенных детей при заборе крови на 7–8 сутки после рождения скрининговый результат трактуется как положительный при следующих уровнях 17-ОНП: на сроке 23–32 недели гестации ― ≥ 65 нг/мл; на сроке 33–36 недель гестации ― ≥ 40 нг/мл.
Врожденный гипотиреоз в большинстве случаев вызван дефектами самой щитовидной железы (первичный гипотиреоз). Причины первичного врожденного гипотиреоза можно в широком смысле классифицировать как неспособность щитовидной железы нормально развиваться (дисгенезия) или неспособность структурно нормальной щитовидной железы производить нормальные количества гормона (дисгормоногенез). Дисгенезия щитовидной железы, охватывающая весь спектр агенеза, гипоплазии и эктопии, является наиболее частой причиной врожденного гипотиреоза. В то время как это заболевание остается наиболее частой причиной врожденного гипотиреоза, частота возникновения дисгормоногенеза за последние несколько десятилетий увеличилась. В то время как на дисгормоногенез приходится только 15 % врожденного гипотиреоза, диагностированного в первые дни скрининга новорожденных, у 30–40 % младенцев, прошедших скрининг по современным протоколам, имеется эктопическая щитовидная железа, соответствующая одной из форм дисгормоногенеза. В отличие от дисгенезии щитовидной железы, при которой моногенная причина присутствует только у небольшого количества пациентов, дисгормоногенез часто возникает из-за генетического дефекта на каком-либо этапе синтеза тиреоидных гормонов.
Учитывая разнообразие функций тиреоидных гормонов в организме человека, врожденный гипотиреоз характеризуется разнообразием клинических проявлений с поражением всех органов и систем. При отсутствии своевременного лечения на первый план выходит задержка психомоторного и речевого развития, затем наступают отставание в физическом развитии и задержка полового развития. Основной задачей скрининга является наиболее раннее выявление детей с подозрением на врожденный гипотиреоз.
Рисунок 2 | Интерпретация результатов исследования на наличие врожденного гипотиреоза
Галактоземия — аутосомно-рецессивное наследственное нарушение обмена углеводов, при котором в организме накапливается избыток галактозы и ее метаболитов. В норме галактоза образуется в результате гидролиза лактозы в кишечнике либо в процессе ферментных реакций, обмена гликопротеинов и гликолипидов. Галактоза является материалом для образования клеточных мембран, нервной ткани, нервных окончаний и т. д. В результате ферментных реакций она превращается в глюкозу, и именно дефицит галактозо-1-фосфатуридилтрансферазы лежит в основе патогенеза данного заболевания. Метаболиты галактозы обладают повреждающим действием. Так, галактитол проникает в хрусталик глаза, приводя к повышению осмотического давления, электролитным нарушениям и денатурации белка с формированием катаракты. Другие метаболиты обладают гепато-, нейро- и нефротоксическим действиями, а также вызывают гемолиз эритроцитов. Тормозящее влияние метаболитов галактозы на углеводный обмен приводит к гипогликемии.
Рисунок 3 | Интерпретация результатов исследования на наличие галактоземии
Муковисцидоз — аутосомно-рецессивное заболевание, связанное с мутацией гена МВТР (трансмембранного регулятора муковисцидоза). МВТР является хлорным каналом, мутации гена которого нарушают не только транспорт, но и секрецию ионов хлора. При затруднении их прохождения через клеточную мембрану увеличивается реабсорбция натрия железистыми клетками, нарушается электрический потенциал просвета, что вызывает изменение электролитного состава и дегидратацию секрета желез внешней секреции. В результате выделяемый секрет становится чрезмерно густым и вязким. Поражаются все экзокринные железы организма: печень, поджелудочная железа, мочеполовая система, но наиболее ярко муковисцидоз проявляет себя со стороны органов дыхания, провоцируя бронхообструкцию, дыхательную и сердечную недостаточность, легочную гипертензию.
Рисунок 4 | Интерпретация результатов исследования на наличие муковисцидоза
Расширенный скрининг
Органические ацидемии — группа аутосомно-рецессивных наследственных заболеваний обмена, в основе патогенеза которых лежит дефицит ферментов, участвующих в метаболизме белков, что приводит к повышению уровня кетоновых тел, обладающих токсическим действием на различные органы и ткани, в частности, на ЦНС. Данные заболевания манифестируют уже в стадии декомпенсации, как правило, в период с первой недели до первого года жизни. Триггерами служат стресс, длительное голодание, инфекционные заболевания, иммунизация, реже — чрезмерное употребление белковой пищи. Проявляются преимущественно неврологической симптоматикой: нарушение сознания вплоть до комы, эпилептические приступы, нарушение мышечного тонуса, у детей старшего возраста — нарушения психоречевого развития, атаксия, очаговые неврологические симптомы, синдром Рейе (острая печеночная недостаточность, сочетающаяся с энцефалопатией), психические расстройства.
Нарушения окисления жирных кислот — врожденный дефект метаболизма из-за нарушения либо митохондриального β-окисления, либо транспорта жирных кислот с использованием карнитинового транспортного пути. Проявления зависят от нарушения метаболизма конкретной кислоты, но все они имеют общие черты и требуют схожей тактики лечения. В периоде новорожденности метаболические нарушения проявляются тяжелой кардиомиопатией, гипокетотической гипогликемией, дисфункцией печени в первые несколько дней или недель жизни, часто заканчиваясь летально. В младенческом и детском возрасте характерны эпизоды летаргии и рвоты, развивается дисфункция печени и гипокетотическая гипогликемия, энцефалопатия, что может привести к внезапной младенческой смерти. У подростков и во взрослом возрасте дебютируют эпизодическим рабдомиолизом, мышечной слабостью, миалгией. Лечение включает отказ от голодания, симптоматическую терапию развившихся осложнений и включение в рацион добавок, если это необходимо.
Аминоацидопатии
Болезнь кленового сиропа (она же лейциноз) — наследственное заболевание, обусловленное дефицитом дегидрогеназы кетокислот с разветвленной цепью и нарушением метаболизма лейцина, изолейцина, валина (аминокислоты с разветвленной цепью, АКЦР). Повышение уровня АКЦР и их метаболитов, в частности, кетокислот, приводит к кетоацидозу, атрофии ткани головного мозга, нарушению окислительного фосфорилирования в дыхательной цепи митохондрий. Избыток лейцина обладает нейротоксическим эффектом, вызывая дисфункцию астроцитов, апоптоз нейронов и блокируя транспорт через гематоэнцефалический барьер аминокислот, важных для синтеза нейротрансмиттеров.
Гомоцистеинурия — наследственное заболевание из группы аминоацидопатий, обусловленное нарушением метаболизма серосодержащих аминокислот, в частности, метионина. Дефицит цистатион-b-синтазы нарушает преобразование метионина в цистеин. Высокий уровень гомоцистеина связан с образованием некротически-дегенеративных участков в почках, селезенке, слизистой оболочке желудка и сосудах, активацией XII фактора свертывания, способствующего тромбообразованию.
Тирозинемия 1 типа — заболевание, обусловленное дефицитом фумарилацетоацетатгидролазы, в результате чего происходит накопление высокотоксичных фумарил- и малеилацетоацетата, обладающих гепатотоксическим и канцерогенным действием. Конечные метаболиты — сукцинилацетон и сукцинилацетоацетат — являются митохондриальными токсинами, тормозящими фосфорилирование и блокирующими цикл Кребса. Накопление токсинов приводит к прогрессирующему заболеванию печени с развитием печеночной недостаточности, цирроза, тубулопатии с формированием ренальной тубулопатии, гипофосфатемического рахита, синдрома Фанкони. Острая тирозинемия сопровождается развитием гипертрофической кардиомиопатии. Кроме того, нарушается путь синтеза порфирина, ингибируется синтез порфобилиногена, что приводит к кризам, проявление которых напоминает порфирию. Все пациенты подвержены высокому риску развития гепатоцеллюлярной карциномы, вторичной по отношению к циррозу. Без своевременного лечения дети погибают в возрасте 10 лет.