нарушения левого предсердия на экг что это такое
Что такое трепетание предсердий? Причины возникновения, диагностику и методы лечения разберем в статье доктора Дедова Дмитрия Васильевича, кардиолога со стажем в 28 лет.
Определение болезни. Причины заболевания
У части пациентов трепетание предсердий сочетается с фибрилляцией — другим нарушением ритма, при котором предсердия полностью перестают сокращаться, а желудочки сокращаются неполноценно и нерегулярно.
Такое сочетание патологий раньше называли термином «мерцание-трепетание», но сейчас его называют «фибрилляция-трепетание». По сути, мерцание, или мерцательная аритмия, — это русский перевод английского термина «atrial fibrillation», т. е. фибрилляция предсердий.
По частоте встречаемости трепетание уступает фибрилляции предсердий. Отчасти это связано с недостаточным количеством исследований по распространённости трепетания.
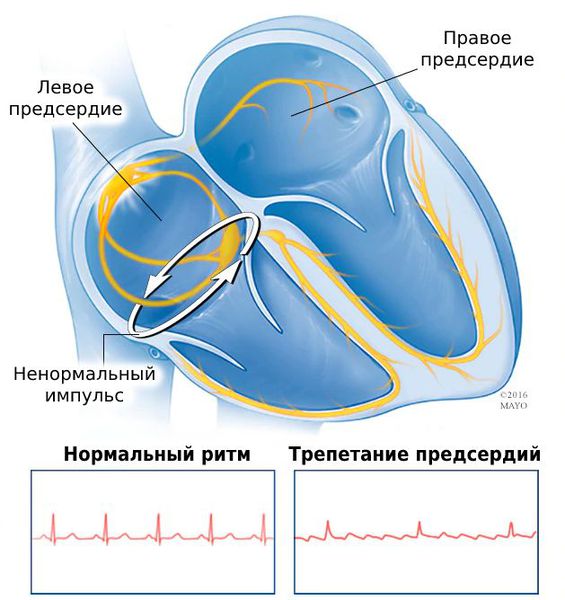
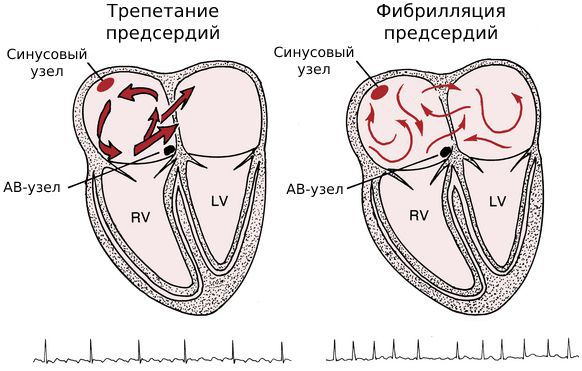
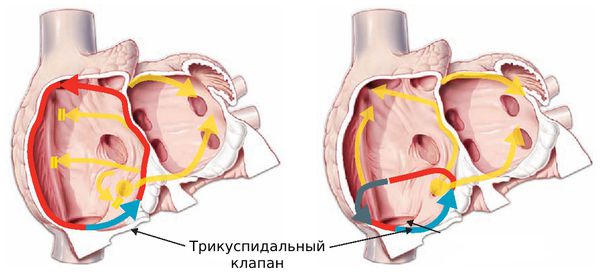
В чём разница между трепетанием и фибрилляцией предсердий?
Т репетание предсердий труднее поддаётся медикаментозному лечению и быстрее приводит к сердечной недостаточности, чем фибрилляция.
Обе патологии связаны с сердечным импульсом. Разница в том, что при трепетании нарушена его проводимость, а при фибрилляции — генерация.
Причины и факторы риска
Причина трепетания — нарушение проведения электрических импульсов по предсердию. Из-за частых сокращений предсердий не все импульсы доходят до желудочков.
Риск развития трепетания на фоне гипертрофии левого желудочка выше, чем на фоне ИБС и гипертонии без такого изменения миокарда.
Трепетание предсердий часто встречается при других состояниях :
Симптомы трепетания предсердий
Наиболее частые симптомы приступа трепетания предсердий:
Патогенез трепетания предсердий
Развитие болезни связано с плохим сокращением предсердий на фоне нарушения сердечного ритма. Учащённое сердцебиение перегружает их: полость предсердий начинает увеличиваться, а объём выталкиваемой крови — уменьшаться. Эти изменения утяжеляют течение сердечной недостаточности. В итоге любая, даже небольшая физическая нагрузка, например уборка по дому, будет вызывать слабость или быстрое утомление.
Из-за п риступов трепетания ухудшается кровоснабжение органов и тканей. Причинами ухудшения становятся:
При трепетании предсердий на фоне ИБС сокращается время расслабления сердечной мышцы, кровь хуже поступает в коронарные артерии, в клетки миокарда поступает меньше кислорода. Эти нарушения сопровождаются чувством «давления за грудиной».
Классификация и стадии развития трепетания предсердий
Первая классификация разделяет все случаи трепетания предсердий на две формы:
Пароксизмальная форма возникает при заболеваниях сердца и органов грудной клетки. Для неё характерны спонтанные приступы трепетания, которые длятся от нескольких секунд до одной недели. В течение этого времени ритм сердца может временно восстанавливаться.
П ароксизмальная форма трепетания может перейти в постоянную, т. е. хроническую. Такая форма отличается своей устойчивостью: её проявления сохраняются больше недели.
Вторая классификация основана на частоте сердечных сокращений — ЧСС. В ней выделяют три формы трепетания предсердий:
Третья классификация выделяет типы трепетания предсердий в зависимости от факторов, которые могли спровоцировать развитие этой аритмии. Всего их пять:
Четвёртая классификация основана на результатах ЭФИ — электрофизиологического исследования сердца. В зависимости от циркуляции импульса трепетание бывает типичным и атипичным:
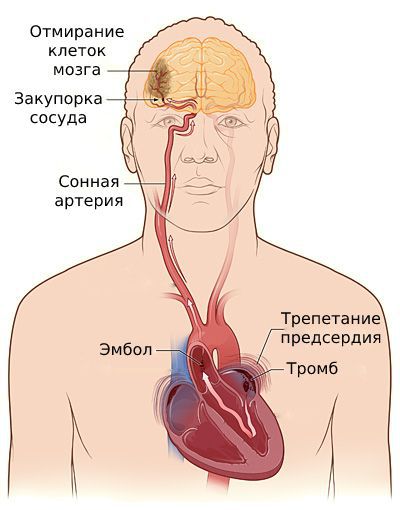
Осложнения трепетания предсердий
Диагностика трепетания предсердий
ЭКГ позволяет определить частоту сердечных сокращений, выявить нарушение сердечного ритма и проводимости импульса. Также она может показать, был ли у пациента инфаркт миокарда, увеличен ли левый желудочек.
Процедура длится 5-10 минут. К груди обследуемого прикрепляют специальные присоски или электроды. Они фиксируют импульсы сердца и передают их на электрокардиограф.
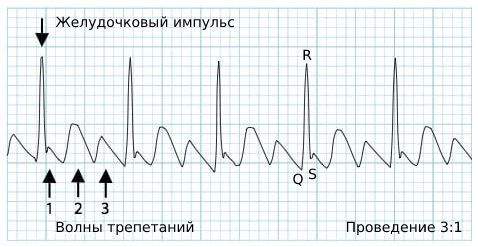
Ритм сокращения самих желудочков правильный. Желудочковый импульс в норме, поэтому комплекс QRS не изменён.
Иногда при трепетании наблюдается проведение 1:1. Эта форма чаще встречается у детей и молодых людей. Такой форме болезни соответствует небольшая частота волн трепетания и не менее 220 сокращений предсердий в минуту. При этом каждый предсердный импульс доходит до желудочков. Но если частота сокращений увеличится до 300 раз в минуту, трепетание с таким проведением может привести к смерти.
Лечение трепетания предсердий
Медикаментозное лечение
Медикаментозная терапия предполагает приём препаратов, восстанавливающих синусовый ритм.
Основными антиаритмическими препаратами являются:
Комбинация этих антиаритмических препаратов увеличивает эффективность лечения.
Амиодарон и соталол — антиаритмические препараты III класса.
Верапамил — антиаритмический препарат IV класса. Его эффективность ниже, чем у амиодарона и соталола, а для профилактики приступов трепетания требуются достаточно высокие дозы. К побочным эффектам относят снижение сердечного ритма до 50 сокращений в минуту, гипотонию и прогрессирование сердечной недостаточности.
Учитывая, что чаще трепетания предсердий возникают на фоне низкого уровня калия в крови, к стандартной медикаментозной терапии добавляют препараты калия:
Электроимпульсная терапия
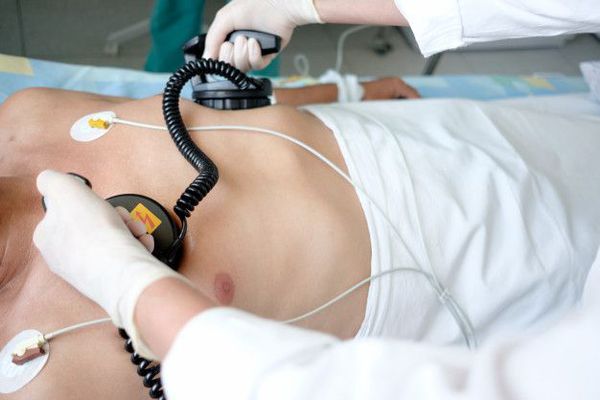
При появлении симптомов сердечной недостаточности предпочтение отдаётся электроимпульсной терапии — ЭИТ. Её проводят с помощью специального прибора — дефибриллятора. Один из его электродов фиксируют немного кнаружи от верхушки сердца, другой — справа от грудины. При трепетании предсердий и стабильном состоянии пациента начинают с разряда в 25 Дж.
После процедуры больной должен соблюдать постельный режим в течение дня. Ему назначают антиаритмическую и антитромботическую терапию. Функция предсердий восстанавливается через несколько дней после купирования приступа трепетания.
Абляция
При типичном трепетании предсердий предпочтение отдаётся абляции — разрушению патологических электрических очагов.
Абляцию, которая проводится с помощью высокочастотных токов, называют радиочастотной. Разрушение патологических очагов с помощью низких температур, до −70 °C, называют криоабляциией.
Прогноз. Профилактика
С увеличением длительности приступа трепетания прогноз ухудшается: восстановить и сохранить нормальный синусовый ритм становится всё сложнее. При появлении симптомов сердечной недостаточности в ближайшие три месяца синусовый ритм сохраняется только у 9,1 % пациентов.
Даже при тщательном подборе антиаритмических препаратов у большинства пациентов с пароксизмальной формой болезни возникает повторный приступ трепетания. В течение месяца рецидивы возможны у пациентов с кардиосклерозом и пороком сердца.
Вероятность ре цидива в первую очередь связана с размерами и массой предсердий. К другим факторам, повышающим риск повторного приступа трепетания, относят:
Заболевания сопровождающиеся нарушением сердечного ритма и проводимости
Нарушения проводимости сердца (блокады) — частая находка при электрокардиографическом (ЭКГ) исследовании. Чаще всего они никак не проявляются клинически, но некоторые блокады требуют имплантации (установки) постоянного электрокардиостимулятора (водителя ритма).
Многие разновидности внутрисердечных блокад (например, неполная блокада правой ножки пучка Гиса) являются вариантом нормы.
Кардиологическое обследование при нарушениях проводимости сердца призвано не только определить вид блокады, но и установить, не служит ли она проявлением органического поражения сердца. Кроме того, далеко не во всех случаях блокады надо лечить. Главные показания к установке электрокардиостимулятора — обмороки и предобморочные состояния, но необходимо быть уверенным, что обмороки вызваны именно нарушениями проводимости сердца.
Проводящая система сердца
В общих чертах проводящая система сердца (система, ответственная за проведение электрических импульсов в сердце) устроена следующим образом. Импульсы генерируются синусовым узлом, расположенным в правом предсердии. По внутрипредсердным путям проведения эти импульсы достигают атриовентрикулярного (АВ) узла, где происходит некоторая задержка импульсов: предсердия и желудочки должны сокращаться неодновременно. Затем импульс идет по ножкам пучка Гиса к клеткам (кардиомиоцитам) желудочков. Пучок Гиса состоит из двух ножек — правой и левой. Левая ножка пучка Гиса состоит из двух ветвей — передней и задней.
Основные методы диагностики нарушений проводимости сердца
1. ЭКГ (электрокардиограмма)
Стандартная ЭКГ в 12 отведениях в покое позволяют выявить все основные виды нарушений проводимости сердца: синоатриальную и атриовентрикулярную блокады, блокады ножек пучка Гиса. Медикаментозные пробы в сочетании с ЭКГ в настоящее время почти не используют.
2. Холтеровский мониторинг (мониторирование) ЭКГ
Этот вид исследования позволяет записать ЭКГ на протяжении суток и более. Он позволяет установить, нет ли у пациента значимых пауз (остановок сердца). Значимыми считают паузы дольше 3 секунд. В случае, если значимых пауз нет, установка электрокардиостимулятора почти никогда не показана.
3. Электрофизиологическое исследование сердца (ЭФИ)
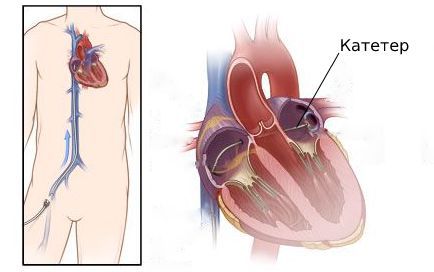
Это самый надежный, но сложный и дорогостоящий метод диагностики аритмий. Выполняется ЭФИ только в стационаре, и требует установки нескольких катетеров в вены рук и ног. Через эти катетеры в сердце проводят электроды и выполняют электрокардиостимуляцию — вызывают и устраняют аритмии, исследуют их параметры.
Для обнаружения самых частых видов нарушений проводимости сердца существует более простая разновидность ЭФИ — чреспищеводное ЭФИ. При этом через рот или через нос в пищевод заводят тонкую проволоку (зонд-электрод) и через него стимулируют левое предсердие. Этот вид исследования выполняют амбулаторно. В частности чреспищеводное ЭФИ позволяет определить, за какое время после прекращения стимуляции, восстанавливается функция синусового узла (то есть собственного водителя ритма) — это нужно для того, чтобы поставить диагноз синдрома слабости синусового узла, одного из самых распространенных видов нарушений проводимости у пожилых.
Отдельные виды блокад
Атриовентрикулярная (АВ-) блокада
Различают АВ-блокады 1-й, 2-й и 3-й степеней. АВ-блокада 1-й степени никак клинически не проявляется, диагноз ставят по ЭКГ (когда интервал PQ на ЭКГ превышает 0,20 секунд). АВ-блокада 1-й степени нередко встречается в норме, например у спортсменов. При ней противопоказаны некоторые препараты, которые могут перевести ее в АВ-блокаду более высоких степеней.
При АВ-блокаде 2-й степени наблюдаются выпадения отдельных сокращений сердца. Различают два типа АВ-блокады 2-й степени, их называют Мобитц I и Мобитц II. Блокада типа Мобитц I носит более доброкачественный характер, имплантация кардиостимулятора при ней почти никогда не показана. АВ-блокада типа Мобитц II указывает на более серьезное поражение проводящей системы сердца, при ней иногда ставят кардиостимулятор из-за риска полной АВ-блокады.
АВ-блокада 3-й степени — это полная АВ-блокада. Импульсы от предсердий к желудочкам не проводятся, желудочки работают за счет того, что АВ-узел генерирует собственные импульсы, частота их, однако, ниже, чем та, которую способен создать синусовый узел, и ритм этот в целом менее надежен. Поэтому полная АВ-блокада, даже бессимптомная, нередко служит показанием для установки кардиостимулятора.
Блокады ножек пучка Гиса
Блокады ножек пучка Гиса тоже диагностируют по ЭКГ. Неполная блокада правой ножки пучка Гиса — вариант нормы. Из всего разнообразия блокад ножек пучка Гиса особого внимания заслуживает только полная блокада левой ножки пучка Гиса. Во-первых, она может указывать на перенесенный передний инфаркт миокарда, во-вторых, она сама по себе приводит к асинхронному (неодновременному) сокращению стенок левого желудочка и может привести к сердечной недостаточности. В последние годы разработан особый вид электрокардиостимуляции, его называют бивентрикулярной (двухжелудочковой) электрокардиостимуляцией (см. ниже).
Синдром слабости синусового узла
Это заболевание проводящей системы сердца обычно встречается у пожилых людей. Оно проявляется обмороками и предобморочными состояниями (нередко во время физической нагрузки), и так называемым синдромом тахи-бради: редкий пульс сменяется частым, когда у пациента возникает мерцательная аритмия. При этом лечить саму мерцательную аритмию (фибрилляцию предсердий) трудно, поскольку большинство антиаритмических препаратов урежают ритм сердца. При синдроме слабости синусового узла показана имплантация электрокардиостимулятора.
Электрокардиостимуляторы
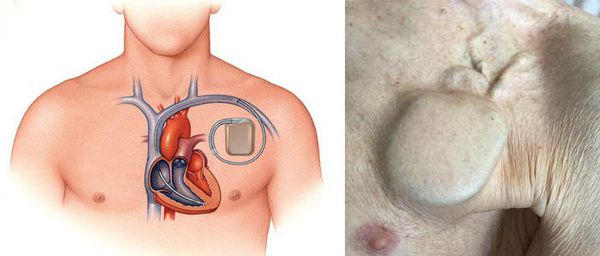
В настоящее время существует множество вариантов постоянной электрокардиостимуляции. Общее у них одно: под кожу передней грудной стенки (обычно возле ключицы) имплантируют электрокардиостимулятор — металлическую коробочку небольших размеров, провода от которой (электроды) — идут через вены к правым отделам сердца. Эти провода улавливают собственную электрическую активность сердца (чтобы синхронизировать свою работу с ней) и передают в сердце импульсы. Современные электрокардиостимуляторы почти всегда стимулируют и предсердия, и желудочки. Кроме того, они настроены таким образом, чтобы частота сердечных сокращений увеличивалась при нагрузке и уменьшалась в покое. Противопоказаний для электрокардиостимуляции в сущности нет: имплантация кардиостимулятора — это несложная и неопасная процедура, которую можно выполнять в любом возрасте.
Отдельный вид электрокардиостимуляции — так называемая бивентрикулярная стимуляция. Ее выполняют не по поводу собственно нарушений проводимости, а чтобы добиться синхронного сокращения всех стенок левого желудочка. Поэтому установку бивентрикулярного стимулятора называют также ресинхронизационной терапией. Электроды от стимулятора идут к правому желудочку и к коронарному синусу (который непосредственно прилежит к левому желудочку). Этот вид лечения сильно помогает некоторым больным с сердечной недостаточностью.
Некоторые электрокардиостимуляторы также обладают функцией дефибриллятора: они распознают угрожающие жизни аритмии и автоматически дают разряд, чтобы их устранить.
Пациенты с электрокардиостимуляторами ведут обычный образ жизни. Им надо лишь избегать действия сильного магнитного поля. Так, больным с имплантированными кардиостимуляторами противопоказана магнитно-резонансная томография (МРТ).
Время от времени пациентам с имплантированными кардиостимуляторами надо показываться специалистам: чтобы проверять исправность стимулятора (в частности, запас его аккумулятора), регулировать параметры стимуляции.
Публикации в СМИ
Кардиомиопатия гипертрофическая
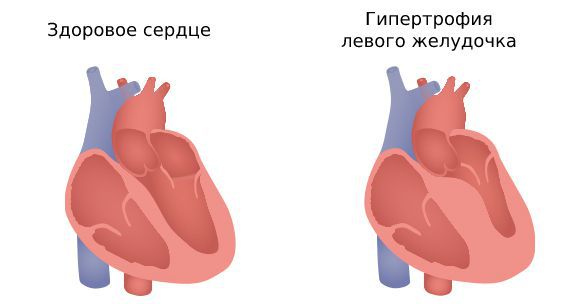
Гипертрофическая кардиомиопатия (ГКМП) — первичное поражение сердца, характеризующееся утолщением стенок левого желудочка и развитием сердечной недостаточности, преимущественно диастолической • Гипертрофия стенки левого желудочка более 15 мм неясного генеза считается диагностическим критерием ГКМП • Различают следующие варианты •• Симметричная ГКМП (увеличение с вовлечением всех стенок левого желудочка) •• Асимметричная ГКМП (гипертрофия с вовлечением одной из стенок): ••• апикальная ГКМП (гипертрофия охватывает изолированно лишь верхушку сердца) ••• обструктивная ГКМП (межжелудочковой перегородки или идиопатический гипертрофический субаортальный стеноз ••• ГКМП свободной стенки ЛЖ.
Статистические данные. ГКМП наблюдают у 0,2% населения, чаще это необструктивные ГКМП (70–80%), реже — обструктивные (20–30%, в виде идиопатического гипертрофического мышечного субаортального стеноза). Мужчины заболевают чаще женщин. Заболеваемость составляет 3 случая на 100 000 человек в год.
Этиология • Многие ГКМП — наследственные заболевания, возникающие в результате мутаций генов, кодирующих сократительные белки миокарда. Кардиомиопатия семейная гипертрофическая: • тип 1: 192600, MYH7, CMH1, 160760 (миозин сердечный, тяжёлая цепь b 7), 14q12; • тип 2: 115195, TNNT2, CMH2, 191045 (тропонин сердечный 2), 1q32; • тип 3: 115196, TPM1, CMH3, 191010 (тропомиозин сердечный 1), 15q22; •; тип 4: 115197, MYBPC, CMH4, 600958 (миозин связывающий белок С), 11p11.2; • тип 7: TNNI3, 191044 (тропонин I сердечный), 19p13.2 q13.2; • с синдромом Вольффа Паркинсона Уайта: CMH6, 600858, 7q3
Патогенез. В результате мутации генов возникает гипертрофия левого желудочка и участки дезорганизации кардиомиоцитов.
• Имеют значение увеличение содержания ионов кальция в кардиомиоцитах, патологическая стимуляция симпатической нервной системы.
• Аномально утолщённые интрамуральные артерии не обладают способностью к адекватной дилатации, что ведёт к ишемии, фиброзу миокарда и его патологической гипертрофии.
• При асимметричной гипертрофии межжелудочковой перегородки, по последним данным, обструкция связана в основном с аномальным движением вперёд в систолу передней створки митрального клапана и в меньшей степени — с гипертрофией перегородки (обструкция выносящего тракта левого желудочка — мышечный субаортальный стеноз: левый желудочек «разделяется» на две части: сравнительно небольшую субаортальную и большую верхушечную; в период изгнания между ними возникает перепад давления).
• Вследствие наличия препятствий для нормального тока крови нарастает градиент давления между левым желудочком и аортой, что приводит к повышению конечного диастолического давления в левом желудочке. У большинства больных отмечают сверхнормальные показатели систолической функции левого желудочка.
• Вне зависимости от градиента давления межу левым желудочком и аортой у больных с ГКМП имеется нарушение диастолической функции левого желудочка, приводящее к увеличению конечного диастолического давления, увеличению давления заклинивания лёгочных капилляров, застою в лёгких, дилатации левого предсердия и фибрилляции предсердий. Развитие диастолической дисфункции связано с уменьшением растяжимости и нарушением расслабления левого желудочка •• Снижение растяжимости возникает вследствие увеличения мышечной массы, уменьшения полости левого желудочка и снижения растяжимости миокарда вследствие его фиброза •• Ухудшение расслабления является результатом систолических (неполное опорожнение левого желудочка вследствие обструкции выходного тракта) и диастолических (уменьшения наполнения желудочков) нарушений.
• ГКМП в ряде случаев сопровождается ишемией миокарда, что связано со следующими причинами •• Снижение вазодилататорного резерва венечных артерий •• Аномальное строение интрамуральных артерий сердца •• Увеличение потребности миокарда в кислороде (увеличенная мышечная масса) •• Сдавление во время систолы артерий, проходящих в толще миокарда •• Увеличения диастолического давления наполнения •• Помимо перечисленных причин, у 15–20% больных наблюдают сопутствующий атеросклероз венечных артерий.
Патоморфология • Макроскопическое исследование •• Основное морфологическое проявление ГКМП — утолщение стенок левого желудочка свыше 30 мм (иногда до 60 мм) в сочетании с нормальными или уменьшенными размерами его полости •• Дилатация левого предсердия (возникает из-за увеличенного конечного диастолического давления в левом желудочке) •• У большинства больных гипертрофированы межжелудочковая перегородка и большая часть боковой стенки левого желудочка, в то время как задняя стенка вовлекается в процесс реже. У других пациентов гипертрофируется только межжелудочковая перегородка. У 30% больных может быть локальная гипертрофия стенки левого желудочка небольших размеров: верхушки левого желудочка (апикальная), только задней стенки, переднебоковой стенки. У 30% больных в гипертрофический процесс вовлекается правый желудочек, сосочковые мышцы или верхушка сердца • Микроскопическое исследование •• Беспорядочное расположение кардиомиоцитов, замещение мышечной ткани на фиброзную, аномальные интрамуральные венечные артерии •• Наличие неупорядоченной гипертрофии, характеризующейся разнонаправленным расположением миофибрилл и необычными связями между соседними клетками миокарда •• Очаги фиброза представлены беспорядочно переплетающимися пучками грубых коллагеновых волокон.
Клинические проявления обусловлены обструкцией выносящего тракта левого желудочка, его диастолической дисфункцией, ишемией миокарда и нарушениями сердечного ритма
• Жалобы •• Заболевание длительное время может протекать бессимптомно, и его случайно выявляют при обследовании по другому поводу •• Одышка в результате увеличения диастолического давления наполнения левого желудочка и пассивного ретроградного увеличения давления в лёгочных венах, что приводит к нарушению газообмена. Увеличение давления наполнения левого желудочка обусловлено ухудшением диастолического расслабления вследствие выраженной гипертрофии •• Головокружение и обмороки при физических нагрузках в результате ухудшения мозгового кровообращения вследствие усугубления обструкции выносящего тракта левого желудочка. Также эпизоды потери сознания могут быть обусловлены аритмиями •• Боли за грудиной вследствие ухудшения диастолического расслабления и увеличения потребности миокарда в кислороде в результате гипертрофии. Могут возникать типичные приступы стенокардии, причинами которых выступают несоответствие между коронарным кровотоком и возросшей потребностью в кислороде гипертрофированного миокарда, сдавление интрамуральных ветвей коронарных артерий субэндокардиальной ишемией в результате нарушения диастолического расслабления •• Сердцебиение может быть проявлением наджелудочковой или желудочковой тахикардии, фибрилляции предсердий.
• При осмотре внешних проявлений заболевания может не быть. При наличии выраженной сердечной недостаточности обнаруживают цианоз. ГКМП может сочетаться с артериальной гипертензией.
• При пальпации можно выявить двойной верхушечный толчок (сокращение левого предсердия и левого желудочка) и систолическое дрожание у левого края грудины.
Инструментальные данные
• Изменения на ЭКГ при ГКМП обнаруживают у 90% больных •• Основные ЭКГ-признаки: гипертрофия левого желудочка, изменения сегмента ST и зубца T, наличие патологических зубцов Q (в отведениях II, III, aVF, грудных отведениях), фибрилляцию и трепетание предсердий, желудочковую экстрасистолию, укорочения интервала P–R (P–Q), неполную блокаду ножек пучка Хиса. Причины появления патологических зубцов Q неизвестны. Их связывают с ишемией миокарда, ненормальной активацией межжелудочковой перегородки, дисбалансом результирующих электрических векторов межжелудочковой перегородки и стенки правого желудочка •• Реже на ЭКГ у с больных ГКМП фиксируются желудочковая тахикардия, фибрилляция предсердий •• При верхушечной кардиомиопатии часто возникают «гигантские» отрицательные зубцы Т (глубиной более 10 мм) в грудных отведениях.
• Суточное мониторирование ЭКГ: наджелудочковые аритмии выявляют у 25–50% больных ГКМП, у 25% больных обнаруживают желудочковую тахикардию.
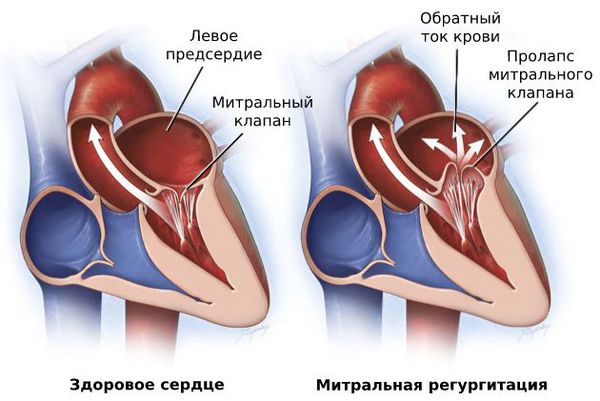
• ЭхоКГ — основной метод диагностики данного заболевания •• Определяют локализацию гипертрофированных участков миокарда, степень выраженности гипертрофии, наличие обструкции выносящего тракта левого желудочка. В 60% выявляют асимметричную гипертрофию, в 30% — симметричную, в 10% — апикальную •• В допплеровском режиме определяют выраженность митральной регургитации, степень градиента давления между левым желудочком и аортой (градиент давления более 50 мм рт.ст. считается выраженным). Кроме того, в допплеровском режиме можно также выявить сопутствующую незначительную или умеренную аортальную регургитацию у 30% больных ГКМП •• У 80% больных можно выявить признаки диастолической дисфункции левого желудочка •• Фракция выброса левого желудочка может быть увеличена •• К признакам ГКМП также относят ••• малый размер полости левого желудочка ••• дилатацию левого предсердия ••• сниженную амплитуду движения межжелудочковой перегородки при нормальном или увеличенном движении задней стенки левого желудочка ••• средне-систолическое призакрытие створок аортального клапана •• Признаки обструктивной ГКМП считают следующие ••• Асимметричная гипертрофия межжелудочковой перегородки с отношением её толщины к толщине задней стенки левого желудочка более 1,3:1 (причём толщина межжелудочковой должна быть на 4–6 мм больше нормы для данной возрастной группы) ••• Систолическое движение передней створки митрального клапана вперёд.
• Рентгенологическое исследование: контуры сердца могут быть нормальными. При значительном повышении давления в лёгочной артерии отмечают выбухание её ствола и расширение ветвей.
Диагностика. Основной метод диагностики — ЭхоКГ, позволяющая выявить утолщение миокарда и оценить наличие обструкции выносящего тракта левого желудочка. Прежде чем диагностировать ГКМП, необходимо исключить причины вторичной гипертрофии, в т.ч. приобретённые и врождённые пороки сердца, артериальную гипертензию, ИБС и т.д.
Дифференциальная диагностика • Другие формы кардиомиопатии • Аортальный стеноз • Недостаточность митрального клапана • ИБС.
ЛЕЧЕНИЕ
Общие рекомендации. При ГКМП (особенно при обструктивной форме) рекомендуют избегать значительных физических нагрузок, поскольку при этом может увеличиваться градиент давления между левым желудочком и аортой, возникать аритмии сердца и обморочные состояния.
Хирургическое лечение. Оперативное лечение проводят при обструктивной форме ГКМП с градиентом давления между левым желудочком и аортой более 50 мм рт.ст. При этом осуществляется септальная миотомия-миэктомия (операция Морроу). При наличии частых пароксизмов желудочковой тахикардии прибегают к имплантации кардиовертера-дефибриллятора.
Течение вариабельно. У большинства больных заболевание протекает относительно стабильно или даже имеет тенденцию к улучшению (у 5–10% в течение 5–20 лет). Женщины с ГКМП обычно хорошо переносят беременность. При длительном течении болезни всё чаще наблюдают развитие сердечной недостаточности.
Прогноз • Без лечения смертность больных с ГКМП составляет 2–4% в год • Пациентов, имеющих более одного фактора риска внезапной сердечной смерти относят к группе высокого риска • У 5–10% больных возможно самостоятельное обратное развитие гипертрофии • В 10% отмечен переход гипертрофической кардиомиопатии в дилатационную • У 5–10% больных развивается осложнение в виде инфекционного эндокардита.
Сопутствующая патология • Аритмии • Системная артериальная гипертензия • Аортальный стеноз • ИБС.
Сокращение. ГКМП — гипертрофическая кардиомиопатия.
МКБ-10 • I42.1 Обструктивная гипертрофическая кардиомиопатия • I42.2 Другая гипертрофическая кардиомиопатия.