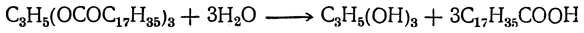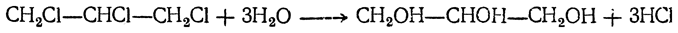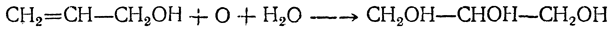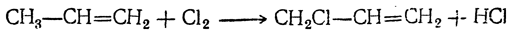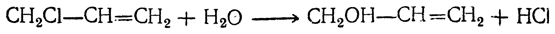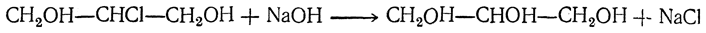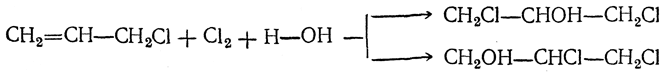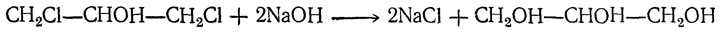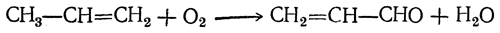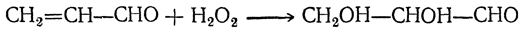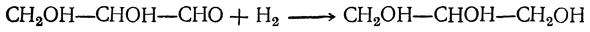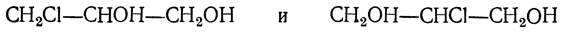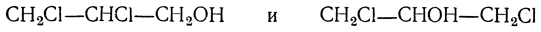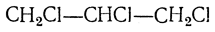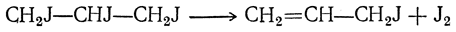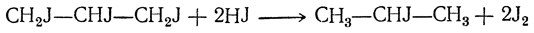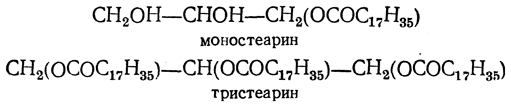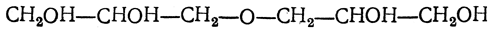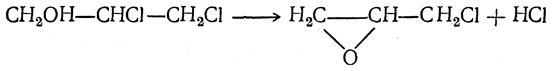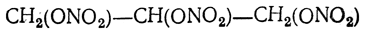на что разлагается глицерин при нагревании
Глицерин
Содержание
[править] История
Глицерин был открыт в 1783 году шведским химиком К.Шееле, который показал, что фрагменты этого соединения составляют основу всех природных жиров и назвал его «сладкое начало масел», поскольку продукт обладал сладким вкусом.
В 1813 году французским химиком М.Шеврелем было установлено, что под действием воды (катализаторы: кислота или щелочь) происходит расщепление жиров с образованием глицерина и высших карбоновых кислот. Им впервые было дано название «глицерин» одному из продуктов, который образуется в данном процессе («глицерос» — сладкий).
Синтез глицерина впервые был проведен в 1873 году французским химиком и минералогом Ш. Фриделем.
[править] Физические свойства
Чистый глицерин представляет собой прозрачную, бесцветную, очень густую, вязкую, сиропообразную, без запаха, тяжелее воды и неядовитую сладковатую на вкус жидкость.
Глицерин обладает способностью поглощать влагу из воздуха и удерживать ее. На воздухе может впитать до 50 % воды. [1] Поэтому глицериновая капля на руке дает впечатление легкого нагрева.
Удельный вес химически чистого глицерина при 15 °С составляет 1,26469.
Молекулярная масса 92,09 г/моль.
При обычном атмосферном давлении глицерин кипит при 290 °C и частично разлагается; под пониженным давлением его можно перегнать, не разложив. [1] Смешивается с водой в любой пропорции. Температура вспышки глицерина составляет 150 °C, температура самовоспламенения — 362 °C. При нагревании глицерин быстро испаряется, а в обычных условиях глицерин не летуч.
Глицерин обладает способностью растворять различные минеральные соли, из-за чего чистый глицерин добывается главным образом путем перегонки. [1]
От сильного и длительного охлаждения глицерин кристаллизуется; температура плавления кристаллов — 20 °C.
Плотность 1,261 г/см 3 при 20 °C. Показатель преломления N D = 1,4735 при 20 °C. диэлектрическая проницаемость ε = 42,5 при 25 °C. дипольный момент молекулы в газовом состоянии μ = 2,56 Дб. [2]
[править] Химические свойства
С водой глицерин смешивается во всех пропорциях, причем объем такого раствора будет немного меньше суммы первоначальных объемов воды и глицерина. Во всех пропорциях смешивается с этанолом. Нерастворим в жирах, масле, бензине, хлороформе. [1]
Наличие гидроксильных групп обусловливает сходство глицерина в одноатомных спиртов, он вступает в те же реакции, но с участием трех гидроксильных групп.
Реакции полного окисления (горения) происходит, как и у других органических веществ, с образованием углекислого газа и воды.
Глицерин вступает в реакцию замещения с металлическим натрием, которая сопровождается выделением водорода.
Реакция с гидроксидами металлов. В отличие от одноатомных спиртов, многоатомные взаимодействуют с гидроксидами щелочных и металлических элементов.
[править] Реакции
Взаимодействие с металлическим натрием:
Взаимодействие с нерастворимыми основаниями:
[править] Получение
Глицерин высокой степени чистоты (не менее 98 %) получают путем алкоголиза растительных жиров с применением вакуум-ректификации.
До разработки синтетических методов глицерин получали щелочным омылением жиров. При этом образуется мыло с водным раствором глицерина. Мыло отделяют путем высаливания с помощью хлорида натрия, а глицерин получают путем повторного сгущения и кристаллизации осажденного хлорида натрия. Полученный 80 % глицерин темного цвета очищается перегонкой и обработкой активированным углем.
Существует ферментативный метод получения глицерина.
Другой метод основан на гидролитическом расщеплении углеводов (крахмала, древесной муки и сахара, особенно тростникового), приводит к образованию смеси глицерина с другими гликолями.
Также глицерин образуется при производстве биотоплива.
[править] Применение в промышленности
В промышленности его получают главным образом при гидролитическом расщеплении жиров. Глицерин выпускают трех видов — сырой, дистиллированный и технически чистый. В косметике разрешено применение двух последних. Глицерин гигроскопичен. Благодаря свойству поглощать из воздуха до 40−50 % воды по отношению к его начальной массе, он получил широкое распространение в косметике как вещество, которое быстро отбирает воду из животной и растительной ткани. Он применяется почти во всех косметических препаратах как смягчающее средство и является одним из основных видов сырья для изготовления зубных паст. Он не засыхает, не горчит, замерзает при очень низких температурах и поэтому применяется как вещество, препятствующее высыханию и замерзанию косметических изделий.
Глицерин используется в парфюмерии и фармации как смягчающим средство или основа мазей, добавка к маслу, в пищевой промышленности — в качестве добавки к напиткам. Спиртовой раствор тринитроглицерина оказывает сосудорасширяющее действие и в виде лекарств используется при сердечных заболеваниях. Глицерин, его олигомеры и полимеры предложены в качестве средств, которые сохраняют свежесть пищевых продуктов.
В кожевенном производстве и текстильной промышленности применяется для обработки пряжи и кожи с целью их смягчения и предоставления эластичности. Глицерин применяется в табачной промышленности, при производстве полиуретанов, резины, фанеры, красителей, чернил и паст, зубной пасты, эмульгаторов, фотографических и других материалов.
Применяется как одно из составных веществ в жидкостях для электронных испарителей.
Из глицерина получают взрывчатое вещество тринитроглицерин, который используется для изготовления динамита.
Глицерин в качестве кормовой добавки повышает надои молока. [3]
Пары глицерина и их влияние на организм человека

За раскрытие вкуса и обильное парообразование отвечают два ингредиента жижи – глицерин и пропиленгликоль. Одно из них, а именно глицерин, довольно широко используется в пищевой промышленности, медицине, косметологии.
Описание вещества
Глицерин – простейший представитель трехатомных спиртов. Вещество представляет собой вязкую, бесцветную, прозрачную жидкость, со сладковатым привкусом, без запаха. Глицерин нетоксичен, его применение разрешено по всему миру в качестве пищевой добавки. Вещество является консервантом и влияет на консистенцию продуктов, делая ее более густой.
Глицерин нашел применение в следующих областях:
Кроме того, глицерин незаменим в производстве жижи для курения. Большинство жидкостей для заправки электронных сигарет состоит из 5 ингредиентов:
Некоторые недобросовестные производители для того, чтобы снизить затраты, заменяют пропиленгликоль более дешевым аналогом – этиленгликолем. Это вещество токсично, поэтому и жижа с его содержанием будет представлять опасность для здоровья.
Какими свойствами обладает глицерин?
Глицерин гигроскопичен, то есть его молекулы поглощают влагу и накапливают ее. Спирт отлично смешивается с водой в любых соотношениях. При растворении в воде объем раствора уменьшается и выделяется тепло. Температура плавления вещества +17,9⁰С, а температура кипения +290⁰С. При нагревании глицерина начинает выделяться акролеин – токсичное вещество, обладающее слезоточивым эффектом.
В различных областях промышленности используют увлажняющее, антисептическое и консервирующее свойства глицерина. Кроме того, спирт является хорошим растворителем, удаляет различные загрязнения, в том числе и жировые.
В составе курительной жижи глицерин отвечает за парообразование. Количество и густота пара напрямую зависят от соотношения глицерина и пропиленгликоля.
Глицерин в составе вейпа
Принцип действия электронной сигареты в том, что в процессе нагревания спирали начинается испарение жидкости, которой пропитан фитиль. Пары, в которых имеет место быть большая концентрация глицерина, и вдыхает вейпер.
Классическое соотношение глицерина и пропиленгликоля в жидкости для вейпа – 3:2, именно такое соотношение обеспечивает средний тротхит, уровень насыщенности и густоты пара. Но если изменить пропорции и увеличить количество глицерина, то пара будет больше, его вкус ярче, а клубы более плотными. Но само парение при этом будет мягче.
Исследования касательно воздействия глицерина на организм человека ведутся не так давно, поэтому подтвержденных данных на сегодняшний день не так много. Но имеющиеся результаты говорят о том, что вдыхание глицерина при парении электронного гаджета в целом не оказывает негативного влияния на здоровье.
Воздействие вещества на организм при курении
За счет гигроскопичности глицерина заправки для вейпа на его основе могут оказывать вредное влияние на организм парильщика. Оно заключается в следующем:
Парить жидкости, имеющие в составе глицерин, нельзя тем, у кого есть предрасположенность к аллергии. Ситуацию усугубляют ароматизаторы, входящие в состав практически любой жижи.
Но наибольшую опасность представляет разложение глицерина, в процессе которого выделяется акролеин – канцероген, оседающий в тканях легких и провоцирующий развитие онкологических заболеваний.
Многие вейперы утверждают, что поскольку глицерин распадается лишь при температуре +3500⁰С, то никакой опасности парения нет. Однако, все больше исследований свидетельствуют о том, что распад глицерина начинается при гораздо более низкой температуре (около +240⁰С), а значит парение может отрицательно влиять на организм человека, оказывая как мгновенный, так и отложенный токсический эффект.
Вдыхание паров глицерина вредно или нет?
Для того, чтобы сделать однозначные выводы о воздействии парения электронных сигарет на здоровье человека, понадобятся десятки лет и множество разнообразных исследований. На сегодняшний день результатов слишком мало и они не позволяют с уверенностью отрицать или подтверждать вред глицерина и других веществ, входящих в состав жижи для электронных сигарет.
Также надо учесть, что влияние на организм оказывает курение состава в целом, а не только глицерина. Имеет значение процентное соотношение и качество входящих в ее состав ингредиентов.
Но кашель, возникающий у большинства активно парящих вейперов, позволяет сделать вывод о том, что глицерин, попадая в легкие вызывает как минимум сухость и дискомфорт, а возможно и более серьезные патологии.
Можно ли парить глицерин из аптеки?
В стремлении изготовить жидкость для парения самостоятельно многие парильщики приобретают глицерин в аптеке. Но заправка, изготовленная на основе этого вещества, чаще всего сильно отличается от жижи, произведенный заводским методом, и не дает ожидаемых ощущений.
Дело в том, что в аптеке обычно продается глицерол – жидкий раствор, в котором содержится не более 70-80% глицерина. Кроме того, аптечный препарат изготовлен на базе природных компонентов, тогда как, по уверениям исследователей, в заправках для электронных сигарет используется вещество, являющееся продуктом переработки нефти и обладающее иными характеристиками.
Токсичность паров
Выявленный вред здоровью от вдыхания паров непосредственно глицерина состоит только в появлении сухости слизистых оболочек, так как вещество забирает влагу у тканей, с которыми контактирует. Но когда речь идет о перегревании нагревательного элемента в вейпе и, как следствие, увеличении температуры глицерина, то воздействие на организм оказывают уже токсины и канцерогены, образующиеся в процессе распада.
Производители утверждают, что правильная эксплуатация электронного гаджета может уберечь от негативных последствий. Так ли это, покажут научные изыскания, которые активно проводятся в настоящее время.
Что будет, если выпить глицерин?
Небольшое количество глицерина содержится в пищевых продуктах и медицинских препаратах, так что вещество в малых дозах не представляет опасности для здоровья. Даже если случайно проглотить пару капель жидкости для электронных сигарет, то скорее всего осложнений ждать не стоит.
Другое дело, если речь идет о большом количестве вещества. В этом случае глицерин спровоцирует не только сильное обезвоживание, но и отравление.
Возможные отрицательные последствия от применения глицерина
Помимо того, что глицерин в составе жижи, провоцирует сухость в горле и кашель, он может стать причиной более серьезных последствий:
Чем еще опасен глицерин, так это вероятностью возникновения аллергической реакции, которая проявляется зудом, высыпаниями на коже. Действие глицерина на организм может вызвать приступ аллергической астмы.
Возможно ли отравление глицерином?
Умеренное употребление глицерина в составе жидкости для парения вряд ли может стать причиной отравления. А вот прием внутрь большого количества вещества, может вызвать интоксикацию, которая проявится такими симптомами, как:
Кроме того, большая доза глицерина может стать причиной поражения центральной нервной системы, что выражается сильной головной болью, мышечными спазмами и судорогами. В тяжелых случаях опасность представляет угнетение дыхательного центра головного мозга, из-за чего возможен летальный исход.
Заключение
При правильном использовании глицерин не представляет опасности для здоровья человека. Но для большей уверенности в безопасности применения надо принимать во внимание индивидуальные особенности организма, а также выбирать только качественный продукт.
Глицерин
Глицерин (пропантриол-1,2,3). Наиболее важным из трехатомных спиртов является простейший, называемый просто глицерином; он имеет строение СН2ОН—СНОН—СН2ОН. Глицерин был открыт в 1779 г. Шееле; его состав был установлен Пелузом в 1836 г., а для уяснения его строения богатые данные дали работы Бертело (1854) и Вюрца (1855—1857). В свободном состоянии глицерин в небольших количествах содержится в крови животных.
Как уже было указано, природные жиры и масла состоят из сложных эфиров глицерина и высших жирных предельных и непредельных кислот, из которых главнейшими являются пальмитиновая C15H31COOH, стеариновая C17H35COOH и олеиновая C17H33COOH. Омыление жиров производится обычно под действием различных катализаторов (кислот, щелочей, энзимов), причем жиры расщепляются на глицерин и жирные кислоты, например:
Полный синтез глицерина был произведен Фриделем (1873) следующим путем. Восстановлением ацетона был получен изопропиловый спирт СН3—СНОН—СН3, при отнятии воды дающий пропилен СН3—СН=СН2, который, присоединяя хлор, превращается в хлористый пропилен СН3—СНСl—СН2Сl; при действии на него хлора получается трихлорпропан (трихлоргидрин глицерина) СН2Сl—СНСl—СН2Сl, при нагревании с водой дающий глицерин:
Глицерин может быть получен также осторожным окислением аллилового спирта перманганатом в щелочной среде (Е. Е. Вагнер):
Глицерин образуется в небольшом количестве при спиртовом брожении; в особых условиях он может быть получен путем брожения и в промышленном масштабе.
В настоящее время осуществлено промышленное производство синтетического глицерина из непищевого сырья (на основе пропилена, выделяемого из газов нефтепереработки).
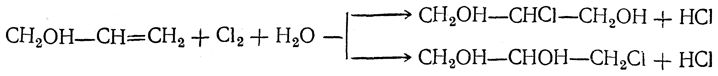
Синтез глицерина из пропилена включает следующие стадии:
Возможен и другой, более короткий путь — присоединение элементов хлорноватистой кислоты к хлористому аллилу
и последующее омыление дихлоргидринов глицерина:
Третий способ, основанный на окислении пропилена, состоит из следующих стадий:
2. Присоединение перекиси водорода к акролеину в присутствии четырехокиси осмия:
Глицерин — сиропообразная бесцветная жидкость сладкого вкуса; смешивается с водой и спиртом, нерастворим в эфире и хлороформе; способен растворять многие органические, а также и неорганические соединения (многие соли, например гипс). Он может быть получен в виде кристаллов, плавящихся при 17° С. Получение глицерина в кристаллическом виде представляет, однако, значительную трудность вследствие его большой склонности к переохлаждению и медленной кристаллизации. Глицерин кипит со слабым разложением при 290° С; относительная плотность d4 20 =1,260.
Химические свойства глицерина определяются наличием в его молекуле трех гидроксильных групп, благодаря чему он может давать три ряда производных, причем моно- и дипроизводные могут существовать в двух структурно-изомерных формах. Монопроизводные глицерина типа СН2Х—СНОН—СН2ОН и дипроизводные СН2Х—СНХ—СН2ОН содержат асимметрический атом углерода, и потому для них возможна оптическая изомерия.
Глицерин дает три ряда металлических производных — глицератов, которые могут получаться даже при действии на глицерин окислов тяжелых металлов, например окиси меди. Это свидетельствует о том, что кислотные свойства у глицерина выражены значительно сильнее, чем у одноатомных спиртов.
Действием галоидоводородных кислот или галоидных соединений фосфора можно получить ряд галоидгидринов глицерина, например монохлоргидрины
и, наконец, трихлорпропан:
При действии иода и фосфора на безводный глицерин получается иодистый аллил, который, вероятно, образуется в результате отщепления иода от непрочного трииодпропана:
Действием иода и фосфора на водный глицерин получается иодистый изопропил. Возможно, что он образуется при неполном восстановлении трииодпропана иодистым водородом:
При недостаточном содержании иодистого водорода в реакционной смеси в качестве побочного продукта получается пропилен СН3—СН=СН2.
Можно предполагать образование также следующих продуктов:
При действии кислот, хлорангидридов или ангидридов на глицерин могут получиться три ряда сложных эфиров.
Сложные эфиры глицерина с органическими одноосновными кислотами получают названия по входящим в их состав кислотам: эфиры пальмитиновой кислоты называются пальмитинами, стеариновой — стеаринами, олеиновой — олеинами и т. д. Три ряда сложных эфиров обозначают, пользуясь приставками моно-, ди- и три-, например:
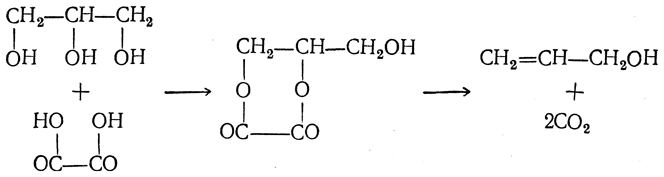
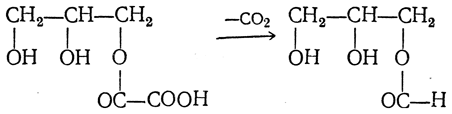
При действии на глицерин безводной щавелевой кислоты НООС—СООН можно получить аллиловый спирт. Если безводную щавелевую кислоту нагревать с избытком глицерина до 150° С, то сначала образуется двузамещенный щавелевоглицериновый эфир, который при дальнейшем нагревании распадается на углекислоту и аллиловый спирт:
Под действием новой порции щавелевой кислоты в результате омыления получается муравьиная кислота, которая при нагревании отгоняется, а глицерин и щавелевая кислота снова вступают в реакцию и т. д. Таким образом с помощью небольшого количества глицерина можно превратить в муравьиную кислоту неограниченное количество щавелевой кислоты.
При действии водоотнимающих средств (KHSO4, H3BO3, безводный MgSO4) из глицерина получается акролеин.
При действии более слабых водоотнимающих средств могут образоваться полиглицериновые алкоголи, например
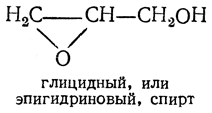
Из производных глицерина, содержащих окисное кольцо, наибольший интерес представляют соединения типа
Глицидный спирт (глицидол) — бесцветная, слабо пахнущая жидкость, смешивающаяся с водой, спиртом и эфиром; т. кип. 180° С. Подобно окиси этилена, он может быть получен действием едкого кали на монохлоргидрин глицерина. Аналогичное ему хлорпроизводное — эпихлоргидрин может быть получено действием едкого кали на дихлоргидрины, например:
Эпихлоргидрин — нерастворимая в воде жидкость с т. кип. 118° С. В настоящее время он приобрел важное значение как исходный полупродукт для получения эпоксидных смол. Эти полимеры получаются поликонденсацией эпихлоргидрина с ароматическими диоксисоединениями, чаще всего с бис-фенолами.
Глицерин находит значительное практическое применение. В больших количествах он расходуется для изготовления полиэфирных, так называемых алкидных смол, в частности глифталевых, широко применяемых в лакокрасочной промышленности. Он употребляется также для подслащивания ликеров и других напитков, для предохранения материалов от высыхания (на этом основано применение его в текстильной промышленности для аппретуры и шлихтования), как средство смягчения кожи и составная часть различных косметических препаратов. Значительные количества глицерина идут на приготовление нитроглицерина.
получающийся при осторожном смешении глицерина с охлажденной смесью концентрированных серной и азотной кислот. Нитроглицерин — маслообразная, тяжелая (относительная плотность 1,601 при 15° С) жидкость, нерастворимая в воде, легкорастворимая в спирте, смешивающаяся с эфиром, хлороформом и бензолом. При охлаждении он кристаллизуется (две полиморфные модификации: неустойчивая с т. пл. 2,2° С и устойчивая с т. пл. 12,2°С). Пары нитроглицерина довольно ядовиты.
Нитроглицерин в смеси с нитратом целлюлозы образует желатинообразную массу («взрывчатый желатин», или «гремучий студень»), которая горит сравнительно медленно и применяется для изготовления бездымных порохов.