Креатинин и клиренс креатинина. Анализ на креатинин и клиренс креатинина.
1. Креатинин, нормальная функция почек и скорость клубочковой фильтрации
Креатинин – это продукт отходов, образующийся в ходе распада мышечной ткани. Креатинин фильтруется почками и удаляется вместе с мочой. Доктора измеряют креатинин в крови, чтобы оценить функционирование почек. Возможность почек удерживать креатинин называется клиренс креатинина. Клиренс креатинина помогает определить скорость клубочковой фильтрации – скорость прохождения крови через почки.
Нормальная функция почек и скорость клубочковой фильтрации (СКФ)
Вся кровь проходит сквозь почки несколько сотен раз за один день. Почки проталкивают жидкость через крошечные фильтры (называемые нефроны). Часть жидкости и отходы остаются в почках и составляют мочу.
Скорость прохождения крови через почки называется скорость клубочковой фильтрации. Непосредственно скорость клубочковой фильтрации невозможно измерить, поэтому используют показатели креатинина и клиренса креатинина.
2. Что такое креатинин и клиренс креатинина?
Креатинин – продукт распада мышечной ткани. Почки фильтруют креатинин и удаляют его из крови почти полностью.
Объём крови, который могут обработать почки за одну минуту, называется клиренсом креатинина. Клиренса креатинина для здорового человека – 125 мл в минуту. Клиренс креатинина может быть разной в зависимости от возраста, пола и параметров тела. Скорость клубочковой фильтрации измеряется с помощью клиренса креатинина.
3. Как измерить клиренс креатинина?
Скорость клубочковой фильтрации отражает функционирования почек. Если почки начинают плохо функционировать, то клиренс креатинина тоже снижается.
Существует два основных способа использования креатинина, с помощью которых доктора могут измерить функционирование почек:
Анализ крови используется гораздо чаще, т.к. более он удобней.
4. Что делать если клиренс креатинина низкий?
Если у вас низкий клиренс креатинина или скорость клубочковой фильтрации, то доктор даст вам необходимые рекомендации.
Главные причины хронических заболеваний почек – высокое артериальное давление и диабет. Если причина низкой скорости клубочковой фильтрации именно в этом, то необходимо начать правильно питаться, заняться спортом и принимать назначенные препараты. Если дело в других причинах, то потребуются дополнительные тесты, для их выяснения.
С возрастом функционирования наших почек снижается, поэтому необходимо проверять их здоровье регулярно.
Клиренс креатинина и скф в чем разница
Определение клиренса эндогенного креатинина – исследование, применяемое для оценки уровня клубочковой фильтрации.
Скорость клубочковой фильтрации, СКФ.
Синонимы английские
Test of renal function, creatinine clearance test, Rehberg test.
Кинетический метод (метод Яффе).
Мкмоль/л (микромоль на литр), ммоль/сут. (миллимоль в сутки), мл (миллилитр), мл/мин. (миллилитр в минуту), % (проценты).
Какой биоматериал можно использовать для исследования?
Венозную кровь, суточную мочу.
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Вся кровь человека сотни раз в день проходит через почки. Они пропускают жидкую часть крови через крохотные фильтры (нефроны), затем большая часть жидкости реабсорбируется обратно в кровь. Жидкие отходы, которые не реабсорбируются почками, удаляются из организма с мочой.
Креатинин (от греческого kreas – «плоть») – продукт распада креатинфосфата в мышечной ткани. Количество его в организме достаточно постоянно и зависит от мышечной массы человека. По химической структуре он является циклическим производным креатина.
Креатинин фильтруется из крови почками, и небольшое его количество активно выделяется с мочой. Канальцевая реабсорбция креатинина минимальна. Если фильтрующая способность почек недостаточна, то уровень креатинина в крови увеличивается. Зная уровни креатинина в моче и крови, можно вычислить клиренс креатинина, который отражает уровень клубочковой фильтрации. Клиренс креатинина (от англ. clearance – «очищение», т. е. очищение от креатинина, его выведение) – количество крови, которое почки могут очистить от креатинина за одну минуту. У здорового молодого человека он составляет около 125 мл в минуту, это значит, что его почки каждую минуту очищают от креатинина 125 мл крови.
Уровень клубочковой фильтрации – сумма уровней фильтрации во всех функционирующих нефронах. Этот показатель позволяет определить количество этих нефронов в почках. Он имеет важное клиническое значение, поскольку является основной характеристикой функции почек.
В случаях тяжелого нарушения функции почек клиренс креатинина повышается, поскольку при активной секреции креатинина выделяется его более крупная фракция.
Кетоновые кислоты, циметидин и триметоприм ограничивают канальцевую секрецию креатинина и снижают точность определения клубочковой фильтрации, особенно при тяжелой почечной недостаточности.
Клиренс креатинина можно определить двумя способами: измерением количества креатинина в крови человека и суточной моче. На практике чаще применяется анализ крови, поскольку это исследование удобнее для пациента.
Если у пациента низкий уровень клубочковой фильтрации, то лечащий врач разработает программу дополнительного обследования для выяснения причины этого патологического состояния. Основными причинами хронических болезней почек являются артериальная гипертония и сахарный диабет. Если они не выявлены, то необходимо дальнейшее обследование для выяснения причины заболевания почек.
Систематическое определение клиренса креатинина позволяет доктору следить за изменением функции почек пациента в динамике и корректировать медикаментозную терапию в зависимости от полученных данных.
Для чего используется исследование?
Когда назначается исследование?
Как оценить работу почек? Что такое СКФ?
Как оценить работу почек? Что такое СКФ?
Здоровая почка состоит из 1-1,2 миллиона единиц почечной ткани — нефронов, функционально связанных с кровеносными сосудами. Каждый нефрон — длиной около 3 см, в свою очередь, состоит из сосудистого клубочка и системы канальцев, длина которых в нефроне 50 — 55 мм, а всех нефронов — около 100 км. В процессе образования мочи нефроны удаляют из крови продукты обмена, регулируют ее состав. За сутки профильтровывается 100–120 литров так называемой первичной мочи. Большая часть жидкости всасывается обратно в кровь – за исключением «вредных» и ненужных организму веществ. В мочевой пузырь попадает лишь 1–2 литра вторичной концентрированной мочи.
Из-за различных заболеваний нефроны один за другим выбывают из строя, по большей части безвозвратно. Функции погибших «собратьев» берут на себя другие нефроны, их же поначалу так много. Однако со временем нагрузка на работоспособные нефроны становится все больше – и они, перетрудившись, погибают все быстрее.
Как оценить работу почек? Если бы можно было точно подсчитывать количество здоровых нефронов, вероятно, это был бы один из наиболее точных показателей. Однако существуют и другие методы. Можно, например, собрать всю мочу больного за сутки и одновременно проанализировать его кровь – рассчитать клиренс креатинина, то есть скорость очищения крови от этого вещества.
Креатинин — конечный продукт обмена белков. Норма содержания креатинина в крови — 50-100 мкмоль/л у женщин и 60-115 мкмоль/л у мужчин, у детей эти показатели ниже в 2-3 раза. Есть и другие показатели нормы (не выше 88 мкмоль/л), такие расхождения частично зависят от используемых в лаборатории реактивов и от развития мышечной массы пациента. При хорошо развитой мускулатуре креатинин может достигать 133 мкмоль/л, при малой мышечной массе — 44 мкмоль/л. Креатинин образуется в мышцах, поэтому его некоторое повышение возможно при тяжелой мышечной работе и обширных травмах мышц. Почками выводится весь креатинин, за сутки примерно 1-2 г.
Впрочем, еще чаще для оценки степени хронической почечной недостаточности используется такой показатель, как СКФ — скорость клубочковой фильтрации (мл/мин).
В НОРМЕ СКФ составляет от 80 до 120 мл/мин, ниже у лиц старшего возраста. СКФ ниже 60 мл/мин считают началом хронической почечной недостаточности.
Приведем несколько формул, позволяющих оценить функцию почек. Они достаточно известны среди специалистов, я привожу их из книги, написанной специалистами отделения диализа С.-Петербургской городской Мариинской больницы (Земченков А.Ю., Герасимчук Р.П., Костылева Т.Г., Виноградова Л.Ю., Земченкова И.Г,. «Жизнь с хронической болезнью почек», 2011).
Это, например, формула расчета клиренса креатинина (формула Кокрофта-Голта, по фамилиям авторов формулы Cockcroft и Gault):
Ccr = (140 – возраст, годы) х вес кг/ (креатинин в ммоль/л) х 814,
Для женщин полученное значение умножается на 0,85
Между тем, справедливости ради надо сказать, что европейские медики не рекомендуют использовать эту формулу для оценки СКФ. Для более точного определения остаточной функции почек нефрологи используют так называемую формулу MDRD:
СКФ = 11,33 х Crк –1,154 х (возраст)–0,203 х 0,742 (для женщин),
где Crк – креатинин сыворотки крови (в ммоль/л). Если в результатах анализа креатинин дан в микромолях (мкмоль/л), эту величину следует разделить на 1000.
У формулы MDRD есть существенный недостаток: она плохо работает при высоких значениях СКФ. Поэтому в 2009 году нефрологи вывели новую формулу для оценки СКФ, формулу CKD-EPI. Результаты оценки СКФ по новой формуле совпадают с результатами MDRD при низких значениях, но дают более точную оценку при высоких значениях СКФ. Иногда бывает так, что человек потерял значительное количество функции почек, а креатинин у него все еще в норме. Формула эта слишком сложна, чтобы приводить ее здесь, но о том, что она существует, стоит знать.
А теперь о стадиях хронической болезни почек:
1 (СКФ больше 90). Нормальная или повышенная СКФ при наличии заболевания, поражающего почки. Требуется наблюдение у нефролога:диагностика и лечение основного заболевания, снижение риска развития сердечнососудистых осложнений
2 СКФ=89-60). Повреждение почек с умеренным снижением СКФ. Требуется оценка скорости прогрессирования ХБП, диагностика и лечение.
3 (СКФ=59-30). Средняя степень снижения СКФ. Необходимы профилактика, выявление и лечение осложнений
4 (СКФ=29-15). Выраженная степень снижения СКФ. Пора готовиться к заместительной терапии (необходим выбор метода).
5 (СКФ меньше 15). Почечная недостаточность. Начало заместительной почечной терапии.
Оценка скорости клубочковой фильтрации по уровню креатинина в крови (сокращенная формула MDRD):
Как оценить почечную функцию в клинической практике?
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Точное измерение экскреторной функции почек крайне важно как в клинической практике, так и в исследовательских работах. Введение рутинного измерения скорости клубочковой фильтрации (СКФ) и новой дефиниции «хронические заболевания почек» возобновили интерес к методам измерения почечной функции. Кроме того, некоторые страны делают попытки скринирования всего населения на выявление заболеваний почек с целью снижения связанного с этими заболеваниями кардиоваскулярного риска. Точное измерение методологически сложно, поэтому более часто в клинической практике используются косвенные показатели, такие как уровень креатинина в плазме крови и специальные формулы (основанные на возрасте пациента, половой принадлежности и уровне сывороточного креатинина). В данной статье описываются рутинные и более специфичые методы оценки почечной функции и обсуждается СКФ.
Почки выполняют несколько связанных между собой функций (табл. 1), которые зависят от СКФ, интегративного показателя функции почек. СКФ определяется, как объем плазмы, очищенный от идеального вещества за единицу времени (обычно выражается в мл/мин.). «Идеальное вещество» – то, которое свободно фильтруется через клубочки и не секретируется, не реабсорбируется почечными канальцами.
Креатинин
Креатинин – эндогенное вещество, максимально близкое к идеальному для измерения СКФ [w1]. Креатинин плазмы крови является продуктом метаболизма креатинина и фосфокреатинина в скелетной мускулатуре (хотя незначительный вклад в его продукцию может вносить и потребление в пищу мяса) [w2,w3].
У пациентов со стабильной почечной функцией содержание креатинина в плазме крови обычно постоянно, варьирует в течение суток не более чем на 8% [w4,w5].
Креатинин свободно фильтруется в клубочках, не реабсорбируется, но (до 15%) активно секретируется почечными канальцами [w6]. При выраженной почечной недостаточности увеличивается экскреция креатинина через гастроинтестинальный тракт [w7].
Клиренс креатинина
Определение клиренса креатинина (КК) с использованием содержания креатинина в плазме крови и анализа собранной за определенный промежуток времени мочи, дает предположение о СКФ:
Клиренс креатинина = (креатинин мочи х объем)/ креатинин плазмы крови
Из–за секреции креатинина почечными канальцами при оценке СКФ по КК зачастую значение СКФ превышает истинное. Это систематичная ошибка при определении стабильных величин, однако до развития выраженной почечной недостаточности (ПН) КК остается адекватным методом оценки почечной функции пациентов. Главная проблема при измерении КК – это необходимость сбора мочи более 24 часов; для пациентов это крайне неудобно, и сбор мочи зачастую производится с погрешностями. Также вариабельность полученного данным методом значения составляет 25% в течение суток [w8]. Поэтому определение КК все реже используется в клинической практике.
Мочевина
Мочевина плазмы крови – менее надежный показатель СКФ, чем креатинин, поскольку ее содержание чаще меняется по причинам, не связанным с СКФ. Диета с высоким содержанием белка, повреждение тканей, обильное кровотечение из гастроинтестинального тракта, лечение кортикостероидами могут привести к увеличению мочевины плазмы крови, в то время как диета с низким содержанием белка и заболевания печени могут привести к ее снижению. Также 40–50% профильтрованной мочевины может реабсорбироваться канальцами, хотя при выраженной почечной недостаточности этот процент меньше [w9].
Содержание мочевины
и клиренс креатинина
При выраженной почечной недостаточности содержание мочевины и КК могут дать более точную информацию о СКФ, чем один КК, поскольку процессы реабсорбции мочевины и секреции креатинина взаимно уравновешивают друг друга [w10]. Этот метод рекомендуется для оценки резидуальной функции почек [w11] у пациентов, находящихся на диализе.
Клиренс инулина
В связи с отсутствием идеальной эндогенной субстанции для измерения СКФ требуется введение экзогенного агента, такого как инулин. Инулин, полимер фруктозы (5200 дальтон), обнаружен в Иерусалимских артишоках, георгинах и цикории и впервые был использован для измерения СКФ в 1951 г. [w12]. Его применение ограничено в связи с дороговизной очищенного инулина и трудностью его измерения, а определени СКФ этим методом требует больших временных затрат как для пациента, так и для врача. Болюсное введение и инфузия инулина выполняются до достижения устойчивой плазменной концентрации, вслед за этим (через несколько часов) выполняются общие анализы крови и мочи для определения содержания инулина. Данный метод (в настоящее время часто используется полифруктозан – Inutest: Fresenius, Австрия) используется только в исследовательских работах, когда необходима очень точная оценка почечной функции.
Радиоизотопные методы
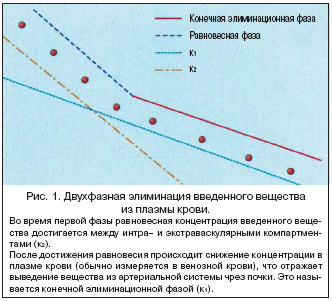
С конца 1960–х гг. стали применяться радионуклеиды и был создан альтернативный метод оценки СКФ, позволяющий исключить некоторые практические недостатки определения КК. Использование радионуклеидов тесно коррелирует с клиренсом инулина [1–4] Обычно прием радионуклеидов производится однократно и СКФ вычисляется по скорости их выведения из плазмы крови, что устраняет необходимость проведения анализов мочи. Выведение вещества происходит в 2 фазы (рис. 1).
Для вычисления СКФ используется компьютерное оборудование на основе данных двух фаз (двойной пул) или терминальной элиминационной фазы (единичный пул). Метод единичного пула имеет то преимущество, что требуется меньшее количество образцов плазмы крови.
Недостаток радиоизотопного метода состоит в необходимости специальных условий хранения, обработки и использования радиоактивного материала. Также он дорог и не может использоваться во время беременности.
Важно отметить, что фаза конечной элиминации значительно удлинена при выраженной почечной недостаточности. У пациентов с почечной недостаточностью средней степени тяжести (СКФ 30–59 мл/мин.) образцы плазмы крови собираются до 5 часов после введения вещества, в то время как у пациентов с выраженной почечной недостаточностью сбор требуется вплоть до 24 часа после введения [5].
Радиоконтрастные агенты
Радиоконтрастные агенты были доступны с 1960–х гг., но трудности химического анализа и неприемлемое количество свободного йода в препарате ограничивало их применение [w13]. Эти проблемы решены, и сегодня радиоконтрастные агенты обладают рядом преимуществ перед радиоизотопами без беспокойства о радиоактивных свойствах. Агенты, используемые в последнее время: йофаламат (Conray; Mallinckrodt, St Louis, MO), сиатризоат меглумина (Hypaque; Amersham Health, NJ) и йохексол (Omnipaque; Amersham Health, NJ). Йохексол – препарат выбора, поскольку он быстр в использовании и результаты сопоставимы с клиренсом инулина [6,7].
Цистатин С
В последнее время возрос интерес к цистатину С, как эндогенному маркеру СКФ. Цистатин С – член цистатинового «суперсемейства» цистеин–протеазных ингибиторов. Он свободно фильтруется через клубочки. Его применение, однако, ограничено более высокой вариабельностью сывороточного уровня, по сравнению с креатинином (75% против 7%) [8]. Также его содержание в плазме крови повышается при опухолях, [w14,w15] ВИЧ–инфекции [w16] и лечении глюкокортикоидами [w17]. В настоящее время у цистатина С нет установленной роли, но он может использоваться для раннего выявления пациентов с почечной недостаточностью в рамках скринирующей программы [w18].
Специальные формулы
Чтобы избежать практических трудностей для измерения КК, существует несколько специальных формул. Наиболее часто используется уравнение Cockcroft и Goult и формулы, основанные на модификации диеты, использованной в исследовании заболеваний почек (рис. 2). В связи с ограниченной возможностью выявления почечной недостаточности по сывороточному креатинину возросла роль формул, в особенности формул MDRD (модификация диеты при заболеваниях почек) [9].
Уравнение Cockcroft и Goult
Уравнение Cockcroft и Goult, которое оценивает КК по уровню сывороточного креатинина, возрасту, полу и весу, было одним из первых [10] и все еще широко используется в клинической практике. Оно основано на экскреции креатинина у мужчины с нормальной функцией почек (с коррекцией для женщин, основанной на данных 3 других исследований [w19,w21]): однако имеется тенденция к оценке почечной функции как более низкой, особенно и ожирении или водной перегрузке (подобно тому, как увеличение веса не свидетельствует об увеличении мышечной массы).
Позже Левей и др. вывели формулу, основанную на данных исследований среди пациентов с выраженной почечной недостаточностью в исследованиях по коррекции диеты при заболеваниях почек [11–14]. Это относится к «6–вариабельной MDRD» или «6–v MDRD» формуле [15]. Эта формула дает оценку СКФ в миллилитрах в минуту по отношению к площади поверхности тела 1,73 м2 и основана на возрасте, поле, расе пациента и уровне мочевины, креатинина и альбумина в плазме крови. Отсутствие веса в формуле позволяет избежать ошибки при водной перегрузке и ожирении.
В 2000 г. формула модификации диеты при заболеваниях почек была упрощена (стали использоваться только возраст пациента, пол, раса и уровень креатинина в плазме крови) [16]. Эта формула получила название «4–вариабельной MDRD» или «4–v MDRD» формула.
Преимущество этих формул состоит в том, что разные лаборатории используют разные методы определения креатинина. Некоторые тесты более чувствительны, чем другие, к некреатининовым хромогенам, которые ложно повышают значения креатинина. Эта ошибка усугубляется при использовании формул, особенно у пациентов с более высоким уровнем почечной функции [17,18]. Для получения результатов, максимально близких к полученным в исследовании по коррекции диеты при заболеваниях почек, все значения сывороточного креатинина в идеале должны быть определены с использованием оригинальных методов клинической лаборатории Cleveland [17,18]. Это создает проблему для поставщиков аналитических систем и практически невыполнимо. Однако некоторые различия методов исследования могут быть скорректированы, и в Содиненном Королевстве (СК) существуют планы по адаптации факторов коррекции. С использованием корректирующих факторов получается немного модифицированная формула 4–v MDRD [19].
Поскольку эти формулы выведены для пациентов с выраженной почечной недостаточностью, правомерен вопрос об их применении для пациентов с нормальной или почти нормальной СКФ. Рекомендовано не использовать данные формулы при уровне СКФ более 60 мл/мин/1,73 м2. Необходимо отметить, что эти формулы не применимы в определенных клинических ситуациях (таких как острая почечная недостаточность, беременность, тяжелое истощение, заболевания скелетной мускулатуры, параплегия и квадриплегия), у детей или при быстром изменении почечной функции.
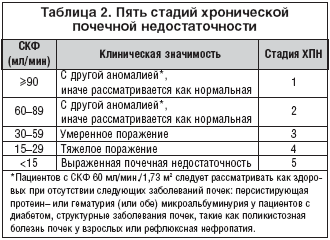
По литературным данным, около 5% взрослой популяции СК имеют хроническое заболевание почек 3 (СКФ 30–59 мл/мин.), 4 (15–29 мл/мин.), или 5 стадии (менее 15 мл/мин.). У этих людей значительно увеличен риск кардиоваскулярной заболеваемости и смертности, и их выявление позволяет по возможности более рано принимать меры для сокращения кардиоваскулярного риска и снижения скорости прогрессирования почечной недостаточности. В таблице 2 перечислены 5 стадий хронической почечной недостаточности.
Нефрологическая Ассоциация СК среди ассоциаций других стран, включая Канаду и Австралию, разработала рекомендации для направленного скринирования населения на выявление сниженной почечной функции на уровне поликлиник, используя CКФ. Эти рекомендации описывают, как лечить большинство пациентов в условиях поликлиники и какие пациенты должны быть направлены к нефрологу.
Заключение
Безусловно, в клинической практике наиболее широко используются специальные формулы, основывающиеся на уровне креатинина плазмы крови. Одна из них, модифицированная 4–v MDRD формула расчета СКФ [19], в настоящее время используется для определения CКФ лабораториями и стала стандартным методом выявления и мониторинга пациентов со сниженной почечной функцией в ОК и в других странах. Выявление и надлежащее лечение пациентов с хроническими заболеваниями почек сокращает кардиоваскулярный риск и замедляет ухудшение функции почек у этих пациентов.
Реферат подготовлен Э.Р. Великовой по материалам статьи Jamie Traynor, Robert Mactier, Colin G Geddes, Jonathan G Fox «How to measure renal function
in clinical practice».
BMJ, No.7571 October 7, 2006, pp733–737.
Список литературы w1–w21 Вы можете найти на сайте bmj.com
Основные положения проекта рекомендаций Всероссийского научного общества кардиологов и научного общества нефрологов России по оценке функционального состояния почек у больных сердечно-сосудистыми заболеваниями или с повышенным риском их развития
1-Российский университет дружбы народов; 2- Московская медицинская академия им. И.М. Сеченова; 3-ФГУ Государственный научно-исследовательский центр профилактической медицины Росмедтехнологии. Москва, Россия
Введение
Нарушения функции почек встречаются часто у пациентов с сердечно-сосудистыми заболеваниями (ССЗ): артериальной гипертонией (АГ), особенно в сочетании с сахарным диабетом (СД), сердечной недостаточностью (СН) и др. Вовлечение почек при многих заболеваниях, в т.ч. исходно не считающихся нефропатиями, делает необходимой разработку унифицированных подходов к ведению пациентов с хронической почечной недостаточностью (ХПН), особенно в плане раннего предупреждения и лечения ее осложнений, например, анемии, нарушений фосфорно-кальциевого обмена, существенно ухудшающих прогноз других заболеваний.
Снижение скорости клубочковой фильтрации (СКФ) рассматривают в качестве маркера неблагоприятного прогноза распространенных в популяции заболеваний, прежде всего ССЗ, что вполне соответствует утвердившейся концепции кардиоре-нальных взаимоотношений [1—3]. Нарушения функции почек являются важным фактором риска (ФР) развития сердечно-сосудистых осложнений (ССО). Сердечно-сосудистая смертность в 10—30 раз выше у пациентов, находящихся на гемодиализе, чем в общей популяции. Результаты эпидемиологических и популяционных исследований свидетельствуют о том, что даже самые ранние субклинические нарушения функции почек являются независимым ФР сердечно-сосудистых событий и смерти, а также повторных событий у пациентов с ССЗ [4].
Частота умеренного, потенциально обратимого или, по крайней мере, стабилизируемого снижения СКФ значительно превосходит частоту терминальной хронической почечной недостаточности (ТХПН).
Назначение медикаментозной терапии способно снизить риск развития ССО и почечных осложнений, замедлить прогрессирование нарушения функции почек. Сохранение субклинических нарушений функции почек на фоне лечения, даже при достижении контроля ФР, например артериального давления (АД), и регрессе других органных поражений, может отрицательно сказываться на прогнозе пациента. Таким образом, оценка функционального состояния почек важна для выбора профилактических и терапевтических мероприятий [National Kidney Foundation. Clinical Practice Guidelines for chronic kidney disease — 2007 kDOQI] [5].
Целями настоящих рекомендаций являются: определение наиболее обоснованных с точки зрения доказательной медицины и применимых в широкой клинической практике методов оценки функции почек; гармонизация национальных рекомендаций с международными руководствами; стандартизация (унифицирование) терминологии для характеристики функционального состояния почек.
Основная область применения рекомендаций — оценка функционального состояния почек у пациентов с ССЗ или повышенным риском их развития с целью стратификации пациентов по риску и выбора медикаментозной терапии.
Основные определения
С целью характеристики функционального состояния почек предлагается использовать следующие термины [6—8]. Хроническая болезнь почек (ХБП) отражает наличие почечного повреждения и/или характеристику СКФ.
— Почечное повреждение > 3 месяцев, со снижением СКФ или без него, определяемое как
• патологические отклонения или
• маркеры повреждения, включая изменения в анализах крови и мочи или при визуализирующих исследованиях;
— СКФ 3 месяцев, с почечным повреждением или без него.
Почечное повреждение — это структурные или функциональные отклонения со стороны почек. Первоначально они могут иметь место при нормальной СКФ, но со временем могут привести к ее снижению. Маркеры почечного повреждения включают в себя изменения в составе крови или мочи и в результатах визуализирующих исследований. Все лица с почечным повреждением независимо от уровня СКФ рассматриваются как имеющие ХБП.
Таким образом, к лицам, имеющим ХБП, относятся:
Основным недостатком является недостаточная точность расчета СКФ по формуле MDRD у пациентов с нормальной или незначительно сниженной функцией почек. При скрининге использование формулы MDRD завышает количество пациентов с ХБП. Не установлена точность формулы у больных ССЗ. Однако у пациентов с дисфункцией левого желудочка (ЛЖ) продемонстрировано, что СКФ 2 положительными количественными тестами с интервалом от одной до двух недель следует рассматривать как имеющих персистирующую патологическую экскрецию белка с мочой; проводить их дальнейшее обследование и лечение. Мониторинг экскреции белка с мочой следует осуществлять количественными методами.
Для количественного определения экскреции Ал с мочой используются радиоиммунные, иммуноферментные и иммунотурбидиметрические методы. Определяется количество экскретируемого Ал за сутки, скорость экскреции, отношение Ал/Кр в произвольном образце мочи. Возможно использование аппаратов для экспресс-диагностики «HemoCue».
Измерение экскреции белка за 24 ч долгое время считалось «золотым стандартом» для количественной оценки протеинурии. По данным некоторых исследований экскрецию белка следует измерять в собранной за ночь порции мочи. Сравнение экскреции белка при ночном и дневном сборе мочи позволяет выявить ортостатическую протеинурию.
Сбор образцов мочи за определенное время неудобен, и может быть сопряжен с ошибками. Концентрация белка в произвольных пробах мочи является грубым показателем скорости экскреции белка; на нее также влияет степень гидратации. Альтернативным методом количественной оценки протеинурии служит измерение отношения содержания белка или Ал к содержанию
Кр в нефиксированном по времени произвольном образце мочи. Соотношения белок/Кр и Ал/Кр в моче дают точную оценку экскреции белков и Ал с мочой и не подвержены влиянию гидратации. Предпочтительна первая утренняя порция мочи, поскольку она лучше коррелирует с 24-часовой экскрецией белка. Если первая утренняя порция мочи недоступна, приемлем произвольный образец мочи.
Диагностические критерии микроальбуминурии (МАУ) и протеинурии. В зависимости от метода определения, диагностическими считают следующие показатели белка (таблица 5). Поскольку экскреция Кр у мужчин выше, чем у женщин, уровни отношения Ал/Кр в моче у мужчин ниже, чем у женщин. Прогностическое значение МАУ в отношении развития ССО позволило предложить термин «альбуминурия низкой степени», диктующий необходимость определения уровня экскреции Ал с мочой
Таблица 5. Определение альбуминурии и протеинурии..
Классификация хронической болезни почек
Классификация ХБП основана на величине СКФ, рассчитанной по формуле MDRD, и наличии почечного повреждения (таблицы 6 и 7) [6,14—16]. Расчет СКФ по формуле MDRD рекомендуется в качестве классифицирующего показателя функционального состояния почек, т.к. формула MDRD наиболее надежно валиди-рована для оценки СКФ у взрослых, для расчета СКФ этим методом используются легко доступные параметры (элементарные демографические данные и Кр сыворотки), показатель может быть рассчитан автоматически и представлен в лабораторном отчет
Таблица 6. Стадии хронической болезни почек.е

Таблица 7. Стадии хронической болезни почек в зависимости от наличия почечного повреждения.
Скрининг пациентов для выявления нарушения функции почек
Рекомендуется следующий алгоритм для выявления нарушения функции почек:
если значения СКФ 30 мг/г сохраняются, по крайней мере, 3 мес.:
Выявление почечного повреждения
У пациентов с ХБП следует оценить наличие почечного повреждения. МАУ/протеинурия являются чувствительными показателями гломеруляр-ной патологии. Для обнаружения других типов ХБП необходимо исследовать осадок мочи (возможно, тест-полосками на эритроциты и лейкоциты) и выполнить визуализирующие исследования: ультразвуковое исследование (УЗИ), внутривенная урография, компьютерная томография, магнито-резонансная томография, радиоизотопная ренография. Общий анализ мочи и УЗИ почек являются полезными неинвазивными методами диагностики почечного повреждения.
Рекомендации по выявлению нарушения функции почек у взрослых пациентов с ССЗ или повышенным риском их развития
Ведение пациентов с ХБП и мониторирование функции почек
Коррекция АД и общие принципы ведения пациентов с ХБП
План ведения пациентов с ХБП учитывает стадию нарушения функции почек (таблицы 9 и 10) [6
Таблица 9. План клинических действий в зависимости от стадии ХБП.]

Таблица 10. Тактика ведения пациентов в зависимости от степени снижения СКФ.
ХБП и ССЗ имеют ряд общих потенциально модифицируемых ФР; наиболее важные среди них — АГ и СД. Для предупреждения/замедления прогрес-сирования ХБП строгий контроль АД и гликемии имеют ключевое значение. Целевым уровнем АД у пациентов с ХБП 3—5 стадии следует считать 5 ммоль/л, уровнем Кр сыворотки
221 мкмоль/л (2,5 мг/дл) следует начинать с осторожностью. Назначение ИАПФ и АРА II пациентам с ХБП требует мониторирования функции почек (таблица 11). Транзиторное снижение СКФ в начале лечения является ожидаемым. Снижение СКФ >30 % от исходного уровня требует коррекции дозы. ИАПФ и АРА II отменить при уровне Кр сыворотки.
Таблица 11. Рекомендованные интервалы мониторирования побочных эффектов ИАПФ и АРАII после начала терапии, увеличения дозы или достижения целевого АД.
265 мкмоль/л (3 мг/дл) или при его повышении > 50 % от исходного, а также при гиперкалиемии (> 6 ммоль/л).
Коррекция анемии [22, 23]
Выявление и оценка степени тяжести анемии.
Уровень гемоглобина (Hb) следует контролировать у всех больных с ХБП не реже 1 раза в год, диагноз анемии устанавливается на основании снижения концентрации Hb согласно критериям ВОЗ:
В настоящее время недостаточно данных, чтобы рекомендовать поддерживать уровень Hb > 130 г/л у больных ХБП, получающих терапию эритропоэз-стимулирующими препаратами (ЭСП).
Не рекомендуется поддерживать уровень Hb > 120 г/л у больных с тяжелой сердечно-сосудистой патологией — III-IV функциональных классов ХСН по классификации Нью-йоркской ассоциации сердца (NYHA).
Не желательно добиваться повышения уровня НЬ > 120 г/л у больных СД 2 типа (СД-2), особенно при сопутствующем поражении периферических сосудов.
Возможно, для больных с хроническими заболеваниями легких допустимы более высокие значения НЬ.
Лечение анемии.
Коррекция дислипидемии (ДЛП) [24]
Выявление ДЛП.
Все больные ХБП должны быть обследованы на наличие ДЛП с определением липидного профиля (ЛП) натощак: общий холестерин (ОХС), липоп-ротеины низкой плотности (ЛНП), липопротеины высокой плотности (ЛВП) и триглицериды (ТГ).
Лечение ДЛП.
Больным > 18 лет ХБП стадии 5 и уровнем ТГ натощак > 5,65 ммоль/л показана коррекция образа жизни и, при необходимости, препараты, снижающие содержание ТГ.
Больным >18 лет ХБП стадии 5 и уровнем ЛНП > 2,59 ммоль/л, показана терапия для снижения ЛНП до 18 лет с ХБП стадии 5 и уровнем ЛНП 2,26 ммоль/л и холестерином-не-ЛВП (ХСЛВП) > 3,36 ммоль/л, показана терапия для снижения ХС-не-ЛВП до 133 мкмоль/л (1,5 мг/дл) у мужчин, > 124 мкмоль/л (1,4 мг/дл) у женщин, снижение СКФ 300 мг/г) свидетельствуют об очень высоком риске развития ССО.
Повышенное нормальное АД (130—139/85— 89 мм рт.ст.) предрасполагает к развитию МАУ: вероятность ее у этой категории пациентов увеличивается в 2,13 раза по сравнению со строго нормотензивными. Рост среднего АД на 10 мм рт.ст. увеличивает риск возникновения МАУ в 1,41 раза, САД в 1,27 раза, диастолического АД (ДАД) — в 1,29 раза. Повышение АД, особенно САД, является одной из наиболее значимых популяционных детерминант МАУ. У пациентов с АГ, не сочетающейся с инсули-норезистентностью (ИР) или СД-2, МАУ отражает гипертоническое поражение почек, конечным этапом которого станет глобальный нефроангиоскле-роз. У больных АГ следует отслеживать динамику МАУ при назначении АГТ. МАУ необходимо оценить после достижения адекватного контроля АД.
АГ при стенозе почечных артерий. Атеросклеротическая реноваскулярная гипертония (РВГ) — атеросклеротический стеноз почечных артерий — ишемическая болезнь почек (ИБП) занимает заметное место в структуре причин необратимого ухудшения почечной функции, особенно у пожилых. Больным атеросклеротической РВГ присуще сочетание сердечно-сосудистых ФР; характерна высокая частота курения. «Почечные» неблагоприятные последствия курения не исчерпываются только атеросклеротическим поражением почечных артерий: у курильщиков наблюдают неблагоприятную перестройку внутрипочечной гемодинамики с генерализованным нарушением микроциркуляции (МЦ), активацию процессов фиброгенеза и тромбогенеза в структурах ткани почки; поэтому курение рассматривают самостоятельным ФР ХБП.
Метаболический синдром
В настоящее время не вызывает сомнения тот факт, что именно сердечно-сосудистые ФР являются ключевыми с точки зрения формирования предрасположенности к стойкому ухудшению функции почек. Скринингу на наличие умеренной ПН подлежат те лица, у которых необходим прицельный поиск ССЗ, особенно у страдающих МС, который увеличивает вероятность развития ХБП не менее чем в 2,6 раза. Изучение взаимосвязей ХБП с МС позволяет утверждать, что высокая распространенность снижения СКФ в общей популяции определяется главным образом нефропатиями обменного генеза — диабетической, уратной, ассоциированной с ожирением, а также гипертоническим нефроангиосклерозом. Факторы, приводящие к их развитию, во многом связаны с особенностями образа жизни; их своевременное и, по возможности, полное устранение
Хроническая сердечная недостаточность
Хорошо известна высокая частота снижения СКФ при ХСН. Само по себе ухудшение фильтрационной функции почек при ХСН увеличивает риск смерти у больных как с умеренным, так и с выраженным снижением фракции выброса (ФВ) ЛЖ. При сниженной систолической функции ЛЖ риск смерти пациентов при наличии ПН возрастает в 3,8 раза, при неизмененной систолической функции — в 2,9 раза. В когорте лиц, включенных в три ветви хорошо известного исследования CHARM (Candesartan in Heart failure: Assessment of Reduction in Mortality and morbidity), снижение СКФ увеличивало частоту смерти и госпитализаций, связанных с ХСН.
У больных с ХСН нередко наблюдают дальнейшее нарастание уровня сывороточного Кр после назначения ИАПФ. Именно нарушение функции почек в наибольшей степени ограничивает возможность применения этого класса препаратов у больных с ХСН, что всегда приводит к значительному снижению эффективности лечения последней, особенно с позиции улучшения долгосрочного прогноза. Следует подчеркнуть высокий риск дальнейшего ухудшения функции почек при ХСН, обусловленной назначением ИАПФ в больших дозах без должного контроля Кр и калия сыворотки, передозировкой петлевых или тиазидных диуретиков, применением некоторых антибактериальных препаратов, рентген-контрастных агентов, а также нестероидных противовоспалительных препаратов, что делает необходимым мониторинг СКФ при ХСН.
При выраженных нарушениях сократимости миокарда ЛЖ снижение СКФ, как правило, совпадает с появлением другого неблагоприятного маркера — роста концентрации натрийуретических пептидов в плазме.
Острый коронарный синдром (ОКС) и инфаркт миокарда (ИМ)
При анализе большой (n=130099) группы пожилых больных острым ИМ (ОИМ) было установлено, что смертность в течение первого года среди больных с сохранной функцией почек составляет 24 %; при умеренном (Кр сыворотки 1,5—2,4 мг/дл) нарушении функции почек — 46 %; при величине сывороточного Кр 2,5—3,9 мг/дл — 66 % (р 0,5 мг/дл в течение суток в период госпитализации, связанной с ОИМ, существенно увеличивает риска смерти в течение последующих 12 мес.
Стойкое снижение СКФ ухудшает прогноз и при остром коронарном синдроме (ОКС). По данным канадского регистра GRACE (Global Registry of Acute Coronary Events) (n=11774) у больных ОИМ с подъемом сегмента ST, не Q-ИМ и нестабильной стенокардией, СКФ в диапазоне 30—60 мл/мин увеличивала риск смерти в 2,09 раза; при СКФ 15 лет) наблюдении за ними.
Заключение
Высокая распространенность стойкого снижения СКФ и неблагоприятный общий прогноз, свойственный этой категории лиц, определяют необходимость раннего выявления и, по возможности, предупреждения ХПН. Очевидна актуальность попыток популяцион-ного подхода к профилактике прогрессирующего необратимого ухудшения функции почек и связанных с ним осложнений, прежде всего, ССО. Констатация снижения СКФ требует активного отношения к предрасполагающим факторам, которые во многом аналогичны известным при ССЗ. Добиться увеличения продолжительности активной жизни этой категории больных возможно лишь при устранении обменных нарушений, курения, АГ, при постоянном приеме лекарственных препаратов, если необходимо — патогенетическом лечении диагностированных хронических нефропатий
Основные клинические исследования у больных с нарушением функции почек