Что такое непредельные углеводороды
Алкены
Номенклатура и изомерия алкенов
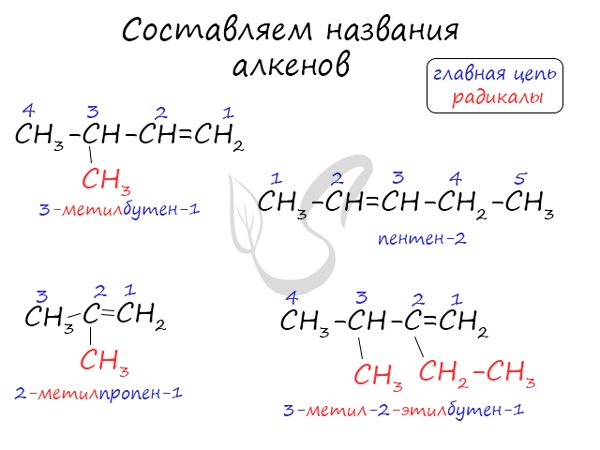
Названия алкенов формируются путем добавления суффикса «ен» к названию алкана с соответствующим числом: этен, пропен, бутен, пентен и т.д.
При составлении названия алкена важно учесть, что главная цепь атомов углерода должна обязательно содержать двойную связь. Принято начинать нумерацию атомов углерода с того края, к которому ближе двойная связь. В конце названия указывают атом углерода, у которого начинается двойная связь.
Атомы углерода, прилежащие к двойной связи находятся в sp 2 гибридизации.
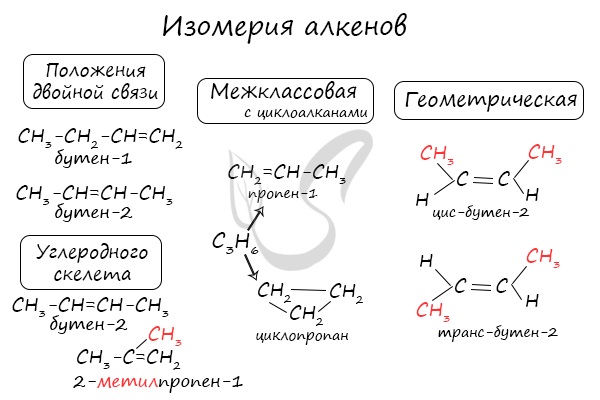
Для алкенов характерна изомерия углеродного скелета, положения двойной связи, межклассовая изомерия с циклоалканами и пространственная геометрическая изомерия в виде существования цис- и транс-изомеров.
Получение алкенов
В результате крекинга нефти образуется один алкан и один алкен.
В реакции галогеналкана со спиртовым(!) раствором щелочи образуется алкен. По правилу Зайцева, водород отщепляется от соседнего наименее гидрированного атома углерода.
Внутримолекулярная дегидратация спиртов происходит при t > 140 °C.
Химические свойства алкенов
Водород присоединяется к атомам углерода, образующим двойную связь. Пи-связь (π-связь) рвется, остается единичная сигма-связь (σ-связь).
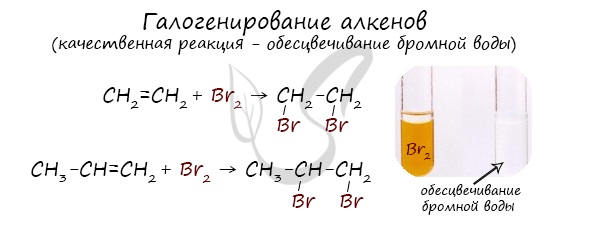
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение его по кратным связям к органическому веществу.
Реакция с хлором на свету протекает по свободнорадикальному механизму, так как на свету молекулы хлора расщепляются, образуя свободные радикалы.
Алкены вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
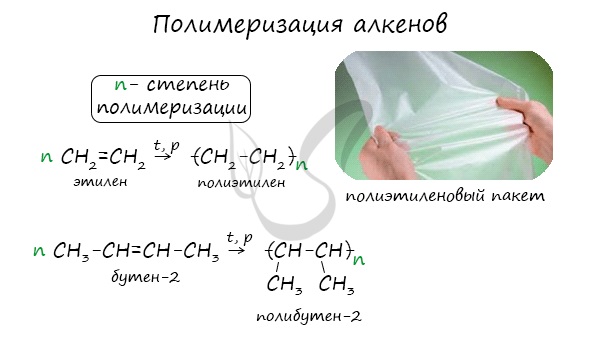
Индекс «n», степень полимеризации, обозначает число мономерных звеньев, которые входят в состав полимера.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Что такое непредельные углеводороды
г) гидрогалогенирование (гидрохлорирование):
Присоединение молекул галогеноводородов протекает по правилу Марковникова (водород присоединяется к наиболее гидрогенизированному атому углерода).
4. Качественные реакции на алкены: обесцвечивание бромной воды (см. уравнение 2 б ) и раствора перманганата калия
Алкины – это непредельные углеводороды, в молекулах которых есть одна тройная связь между атомами углерода
Физические свойства алкинов
Химические свойства алкинов
В этой реакции температура пламени может достигать 3000 o С, поэтому она применяется для сварки металлов.
в) гидрогалогенирование (первая стадия):
CH CH + HCl CH 2 = CHCl
г) гидратация (реакция Кучерова):
ацетальдегид
(уксусный альдегид)
5. Качественные реакции на алкины: обесцвечивание бромной воды (см. реакцию 2 б ) и раствора перманганата калия; образование осадка ацетиленида серебра (см. реакцию 4).
Алкадиены – это непредельные углеводороды, в молекулах которых есть две двойные связи между атомами углерода
Физические свойства алкадиенов
Химические свойства алкадиенов
Такой же состав, как полиизопрен, (C5H8)n – имеет и природный полимер − натуральный каучук.
Алкадиены, как алкены и алкины, обесцвечивают бромную воду (реакция 2 б ) и раствор перманганата калия.
Получение непредельных углеводородов
Алгоритм составления названий непредельных углеводородов
Непредельные углеводороды

Всего получено оценок: 453.
Всего получено оценок: 453.
Органические соединения, содержащие кратные связи (двойные или тройные), называются ненасыщенными или непредельными углеводородами. О том, на какие классы ненасыщенные углеводороды, какими свойствами они обладают, говорим в этой статье.
Классы
К ненасыщенным углеводородам относятся ациклические классы веществ – алкены, алкины, алкадиены. Подробнее о классах ненасыщенных углеводородов рассказано в таблице.
Класс
Определение
Общая формула
Гомологи
Молекулы включают одну двойную связь. Названия формируются аналогично названиям алканов, но с суффиксом «-ен»
Молекулы содержат одну тройную связь. Названия соответствуют алканам с суффиксом «-ин»
Молекулы включают две двойные связи. Название соответствует названиям алканов с суффиксом «-диен»
Для ненасыщенных углеводородов характерна изомерия углеродного скелета, положения кратной связи и межклассовая изомерия (алкины с алкадиенами, алкены с циклоалканами). Пример: бутадиену (СН2=СН-СН=СН2) соответствует бутин-1 (СН≡С-СН2-СН3) и бутин-2 (СН3-С≡С-СН3).
Свойства
В зависимости от количества атомов углерода ненасыщенные углеводороды – это газы (C2-С4), жидкости (C5-С17), твёрдые вещества (C18 и выше). Плотность, температуры плавления и кипения веществ увеличиваются с возрастанием молекулярной массы.
Ненасыщенные углеводороды более активны, чем предельные углеводороды. За счёт разрыва кратных связей в молекулах непредельные углеводороды могут присоединять дополнительные атомы водорода, становясь насыщенными углеводородами. Также присоединяют галогены и галогеноводороды. В таблице описаны основные химические свойства непредельных углеводородов.
Непредельные углеводороды
Непредельные углеводороды — углеводороды с открытой цепью, в молекулах которых между атомами углерода имеются двойные или тройные связи. Непредельные углеводороды способны к реакциям присоединения по двойным и тройным связям в открытой цепи. Они, например, присоединяют бром, легко окисляются раствором перманганата калия. Для многих непредельных углеводородов характерны реакции полимеризации. К непредельным углеводородам принадлежит несколько гомологических рядов: этилена (алкены), ацетилена (алкины), диены.
Полезное
Смотреть что такое «Непредельные углеводороды» в других словарях:
непредельные углеводороды — ненасыщенные углеводороды — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность Синонимы ненасыщенные углеводороды EN unsaturated hydrocarbons … Справочник технического переводчика
непредельные углеводороды — ▲ углеводороды этиленовые, алкены, олефины имеют двойную связь между молекулами углерода и водорода. этилен. пропилен. бутилены. изобутилен. ацетиленовые, алкины имеют тройную связь. ацетилен. диеновые. пропадиен. бутадиен, дивинил. изопрен … Идеографический словарь русского языка
Непредельные углеводороды — см. Нафтены, Нафтилены, Олефины, Полиметиленовые углеводороды, Терпены, Углеводороды ароматические и ацетиленные … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Непредельные углеводороды — то же, что Ненасыщенные углеводороды … Большая советская энциклопедия
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ — то же, что ненасыщенные углеводороды … Химическая энциклопедия
Углеводороды олефиновые — (олефины) – непредельные углеводороды с открытой цепью общей формулы СnН2n; содержат одну двойную связь, обусловливающую их способность к реакциям присоединения и полимеризации … Нефтегазовая микроэнциклопедия
УГЛЕВОДОРОДЫ НЕПРЕДЕЛЬНЫЕ — см. Углеводороды насыщенные (предельные). Геологический словарь: в 2 х томах. М.: Недра. Под редакцией К. Н. Паффенгольца и др.. 1978 … Геологическая энциклопедия
УГЛЕВОДОРОДЫ — обширный класс газообразных, жидких и твёрдых органических соединений, в состав молекул которых входят только атомы углерода и водорода. В зависимости от строения и свойств различают У.: насыщенные, или предельные (простейший представитель метан… … Большая политехническая энциклопедия
Углеводороды — Углеводороды органические соединения, состоящие исключительно из атомов углерода и водорода. Углеводороды считаются базовыми соединениями органической химии, все остальные органические соединения рассматривают как их производные. Поскольку… … Википедия
Углеводороды ацетиленовые — Под этим названием подразумевают непредельные У. формулы CnH2n 2, представителем которых являлся с давних пор ацетилен C2H2 (см. Ацетилен и Углеродистый кальций). В настоящее время У. формулы CnH2n 2 можно подразделить на следующие виды: а)… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Лекция по химии на тему «Непредельные углеводороды. Алкены»
Гибридные орбитали атомов, образующих двойную связь, находятся в одной плоскости, а орбитали, образующие π-связь, располагаются перпендикулярно плоскости молекулы.
Двойная связь является более прочной. Наличие π-связи приводит к тому, что алкены химически более активны, чем алканы, и способны вступать в реакции присоединения.
Гомологический ряд этилена
Неразветвленные алкены составляют гомологический ряд этена (этилена):
Изомерия и номенклатура
Для алкенов, так же как и для алканов, характерна структурная изомерия. Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкен, для которого характерны структурные изомеры, — это бутен.
Особым видом структурной изомерии является изомерия положения двойной связи.
Алкены изомерны циклоалканам (межклассовая изомерия), например:
Номенклатура алкенов, разработанная ИЮПАК, схожа с номенклатурой алканов.
Выбор главной цепи.
Образование названия углеводорода начинается с определения главной цепи — самой длинной цепочки атомов углерода в молекуле. В случае алкенов главная цепь должна содержать двойную связь.
Нумерация атомов главной цепи.
Нумерация атомов главной цепи начинается с того конца, к которому ближе находится двойная связь.
Названия алкенов формируются так же, как и названия алканов. В конце названия указывают номер атома углерода, у которого начинается двойная связь, и суффикс, обозначающий принадлежность соединения к классу алкенов, — ен.
Промышленные способы получения алкенов основаны на превращении алканов в алкены с использованием природных источников УВ (нефть, природный газ).
В процессе термического крекинга предельных углеводородов наряду с образованием алканов происходит образование алкенов, например:
гексадекан октан октен
При пропускании алканов над катализатором (Pt, Ni, Cr 2 О 3 ) при высокой температуре (400—600 °С) происходит отщепление молекулы водорода и образование алкена.
Дегидратация спиртов (отщепление воды).
Эту реакцию называют внутримолекулярной дегидратацией.
При взаимодействии галогеналкана с щелочью в спиртовом растворе образуется двойная связь в результате отщепления молекулы галогеноводорода:
В результате этой реакции образуется преимущественно бутен-2, а не бутен-1, что соответствует правилу Зайцева :
при отщеплении галогеноводорода от вторичных и третичных галогеналканов атом водорода отщепляется от наименее гидрированного атома углерода.
При действии цинка или магния на дибромпроизводное алкана происходит отщепление атомов галогенов, находящихся при соседних атомах углерода, и образование двойной связи:
Первые три представителя гомологического ряда алкенов — газы, вещества состава С 5 Н 10 —С 16 Н 32 — жидкости, высшие алкены — твердые вещества. Температуры кипения и плавления закономерно повышаются при увеличении молекулярной массы соединений.
а) Гидрирование алкенов.
Алкены способны присоединять водород в присутствии катализаторов гидрирования — металлов — платины, палладия, никеля:
Взаимодействие алкена с бромной водой или раствором брома в органическом растворителе приводит к быстрому обесцвечиванию этих растворов в результате присоединения молекулы галогена к алкену и образования дигалогеналканов:
Реакция присоединения галогеноводорода более подробно будет рассмотрена ниже. Эта реакция подчиняется правилу Марковникова: при присоединении галогеноводорода к алкену водород присоединяется к более гидрированному атому углерода, а галоген к менее гидрированному.
г) Гидратация. Гидратация алкенов приводит к образованию спиртов. Например, присоединение воды к этену лежит в основе одного из промышленных способов получения этилового спирта:
Первичный спирт образуется только при гидратации этена. При гидратации пропена или других алкенов образуются вторичные спирты:
Особым случаем реакции присоединения является реакция полимеризации алкенов и их производных. Реакция протекает при повышенной температуре и давлении, а также в присутствии катализатора:
Как и любые органические соединения, алкены горят в кислороде с образованием СО 2 и Н 2 О:
б) Окисление перманганатом калия (реакция Вагнера)
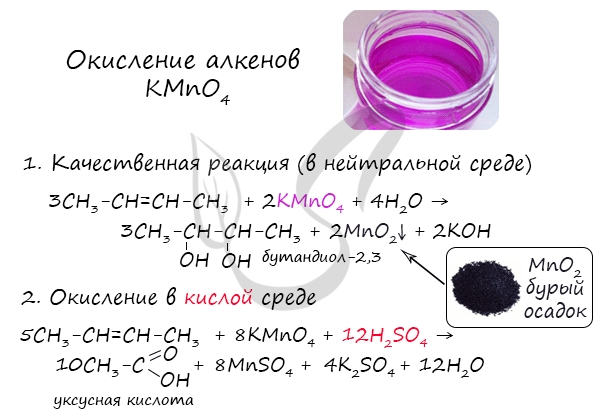
В отличие от алканов, которые устойчивы к окислению в растворах, алкены легко окисляются под действием водных растворов перманганата калия. В нейтральных или слабощелочных растворах на холоду происходит окисление алкенов до диолов (двухатомных спиртов), причем гидроксильные группы присоединяются к тем атомам, между которыми до окисления существовала двойная связь:
В действительности процесс окисления алкенов гораздо сложнее, происходящие при этом превращения можно изобразить уравнением:
Алкены широко используются в химической промышленности как сырье для получения разнообразных органических веществ и материалов. Например, этен — исходное вещество для производства этанола, этиленгликоля, эпоксидов, дихлорэтана.
Большое количество этена перерабатывается в полиэтилен, который используется для изготовления упаковочной пленки, посуды, труб, электроизоляционных материалов.
Из пропена получают глицерин, ацетон, изопропиловый спирт, растворители. Полимеризацией пропена получают полипропилен, который по многим показателям превосходит полиэтилен: имеет более высокую температуру плавления, химическую устойчивость.
В настоящее время из полимеров — аналогов полиэтилена производят волокна, обладающие уникальными свойствами. Так, например, волокно из полипропилена прочнее всех известных синтетических волокон. Материалы, изготовленные из этих волокон, являются перспективными и находят все большее применение в разных областях человеческой деятельности.
Какая структурная особенность отличает непредельные углеводороды от предельных? Приведите примеры подобных соединений.
Как происходит образования σ-связи, а как π-связи? Какие связи являются менее прочными и почему? Укажите качественную реакцию для определения π-связи.
Напишите структурные формулы следующих алкенов: а) пропен, б) бутен-1, в) 3,3-диметилбутен-1, г) 2,3-диметилпентен-1.
Напишите уравнение реакции получения этилена из этанола. Какую роль выполняет концентрированная серная кислота в этой реакции?
Напишите уравнения реакции гидрирования, галогенирования и гидрогалогенирования пентена-2.