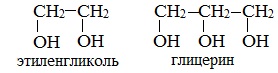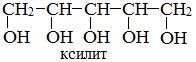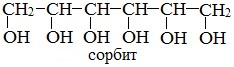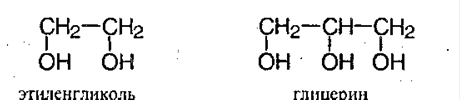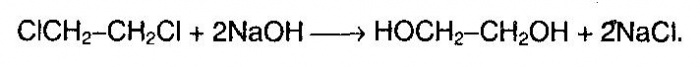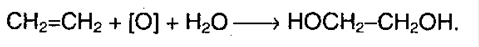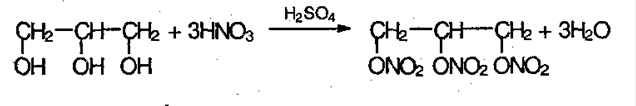Что такое многоатомные спирты
Многоатомные спирты (полиспирты, полиолы) – органические соединения, в молекулах которых содержится несколько гидроксильных групп (-ОН), соединённых с углеводородным радикалом.
Многоатомные спирты — соединения, у которых две или несколько гидроксильных групп расположены у соседних атомов углерода.
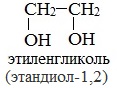
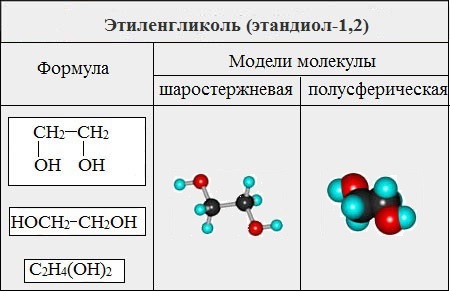
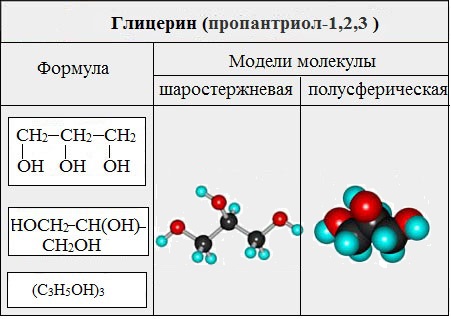
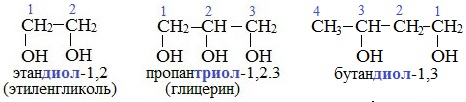
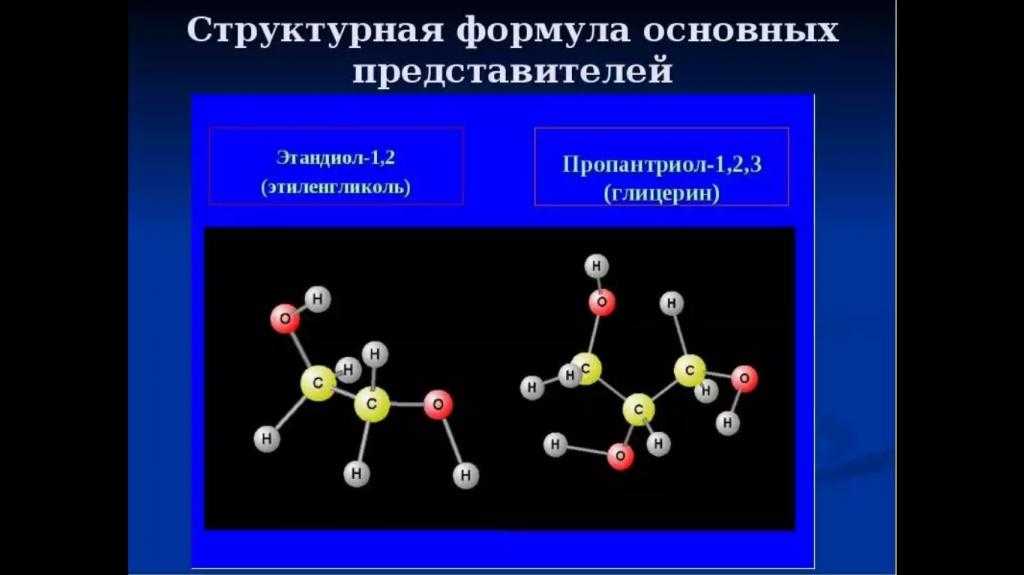
Важнейшими представителями многоатомных спиртов являются двухатомный спирт этандиол-1,2 (этиленгликоль), и трехатомный спирт пропантриол-1,2,3 (глицерин):
или шестиатомный спирт гексанол (сорбит):
I. Гликоли (диолы)
Название гликоли получили вследствие сладкого вкуса многих представителей ряда (греч. «гликос» — сладкий).
II. Глицерины (триолы)
Номенклатура
Физические свойства
Поэтому этиленгликоль широко используется в системах охлаждения двигателей в качестве антифриза (от анг. to freeze — «замерзать») – вещества с низкой температурой замерзания, заменяющего воду в радиаторах автомобильных и авиационных моторов в зимнее время. Антифризы также замедляют ее испарение летом.
Этиленгликоль используется также для производства синтетического волокна полиэфирного волокна – лавсана.
Этиленгликоль очень токсичен! Это сильный яд! Этиленгликоль вызывает длительное угрожающее жизни угнетение центральной нервной системы и поражение почек. Продуктами его превращения в организме являются щавелевая кислота и другие не менее ядовитые соединения. Он имеет спиртовой запах, в связи, с чем может быть принят за этиловый спирт и стать причиной тяжелых отравлений.
Видеоопыт «Изучение физических свойств глицерина»
Глицерин – бесцветная, вязкая, сиропообразная жидкость, сладкая на вкус. Не ядовит. Глицерин не имеет запаха, его tпл = 18 0 С, tкип = 290 0 С. Глицерин гигроскопичен, хорошо смешивается с водой и этанолом. На этом свойстве основано применение глицерина в косметической промышленности, где глицерин используется для увлажнения кожи.
Абсолютно чистый безводный глицерин затвердевает при +18 0 С, но получить его в твердом виде чрезвычайно сложно.
Глицерин широко распространен в живой природе. Он играет важную роль в процессах обмена в организмах животных, входит в состав большинства липидов – жиров и других веществ, содержащихся в животных и растительных тканях и выполняющих в живых организмах важнейшие функции. Благодаря этим свойствам глицерин является важным компонентов многих пищевых продуктов, кремов, косметических средств.
Этиленгликоль и глицерин, благодаря наличию гидроксильных групп, могут образовывать водородные связи с молекулами воды, этим объясняется их не ограниченная растворимость в воде.
Многоатомные спирты.
Важнейшими представителями многоатомных спиртов являются этиленгликоль и глицерин:
Они представляют собой вязкие жидкости, сладкие на вкус, хорошо растворимы в воде и плохо растворимы в органических растворителях.
Получение многоатомных спиртов.
1. Гидролиз алкилгалогенидов (одноатомных спиртов):
2. Этиленгликоль образуется при окислении этилена водным раствором KMnO4:
Химические свойства многоатомных спиртов.
Для двухатомных спиртов характерны основные реакции одноатомных спиртов. Взаимное влияние гидроксильных групп проявляются в том, что многоатомные спирты являются более сильными кислотами. Соли двухатомных спиртов называются гликолятами, трехатомных – глицератами.
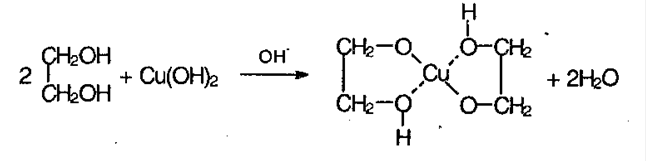
Качественная реакция на спирты – ярко-синее окрашивание при действии свежеосажденного гидроксида меди (II). Цвет возникает от возникновения комплекса меди:
Для многоатомных спиртов характерно образование тринитрата глицерина, известного как нитроглицерин:
Применение многоатомных спиртов.
Этиленгликоль нашел широкое применение в косметике, фармацевтике, производстве взрывчатых веществ, пищевой промышленности.
Динамит – взрывчатое вещество, в основе которого лежит тринитроглицерин.
Свойства и получение многоатомных спиртов
Напомним, что многоатомные спирты – это органические соединения, в молекулах которых содержится несколько гидроксильных групп. Общая формула многоатомных спиртов — CnH2n+1(OH)k, где n и k – целые числа более 2. Классификация, строение, изомерия и номенклатура спиртов рассмотрены раннее в соответствующем разделе. В настоящем разделе рассмотрим свойства и получение многоатомных спиртов.
Важнейшие представители многоатомных спиртов содержат от двух до шести гидроксильных групп. Двухатомные спирты (гликоли) или алкандиолы, содержащие две гидроксильные группы в своей молекуле, трехатомные спирты (алкантриолы) – три гидроксильные группы. Четырех-, пяти- и шестиатомные спирты (эритриты, пентиты и гекситы) содержат 4, 5 и 6 ОН-групп соответственно.
Физические свойства многоатомных спиртов
Многоатомные спирты хорошо растворяются в воде и спиртах, хуже в других органических растворителях. Спирты с небольшим числом углеродных атомов представляют собой вязкие сладковатые на вкус жидкости. Высшие члены ряда — твердые вещества. По сравнению с одноатомными спиртами они имеют более высокие плотности и температуры кипения. Тривиальные названия, названия по систематической номенклатуре и физические свойства некоторых спиртов представлены в таблице:

Получение многоатомных спиртов
Получение гликолей
Гликоли могут быть получены практически всеми способами получения одноатомных спиртов. Выделим основные:
Получение глицерина
За счет разрыва С2-С3 связи образуется небольшое количество этиленгликоля и треита (стереоизомер эритрита).
Помимо глюкозы каталитическому гидрированию можно подвергнуть и другие полисахариды, содержащие глюкозные звенья, например, целлюлозу.
4. Гидролиз жиров щелочью проводят с целью получения мыла (калиевые или натриевые соли сложных карбоновых кислот): Такой процесс называется омылением.
Получение четырехатомных спиртов (эритритов)
В природе эритрит (бутантетраол-1,2,3,4) содержится как в свободном виде, так и виде сложных эфиров в водорослях и некоторых плесневых грибах.
Искусственно его получают из бутадиена-1,4 в несколько стадий:
Пентаэритрит (тетраоксинеопентан) в природе не встречаются. Синтетически можно получить при взаимодействии формальдегида с водным раствором ацетальдегида в щелочной среде:
Химические свойства многоатомных спиртов
Химические свойства многоатомных спиртов сходны со свойствами одноатомных спиртов. Однако наличие в молекулах многоатомных спиртов нескольких гидроксильных групп увеличивает их кислотность. Поэтому они могут вступать в реакции с щелочами и с гидроксидами тяжелых металлов, образуя соли.
Замещение второй гидроксогруппы этиленгликоля происходит труднее (под действием РСl5 или SOCl2 – замещение происходит легче).
Взаимодействие с азотной кислотой
Данные соединения являются взрывчатыми веществами. Тринитроглицерин, кроме этого, используют в медицине в качестве лечебного препарата.
Взаимодействие с уксусной кислотой
Если в реакции этерификации этиленгликоля участвует двухосновная кислота, то возможно получение полиэфира (реакция поликонденсации):
Обычно в качестве R выступает терефталевая кислота. Продуктом такой реакции является терилен, лавсан:
При дегидратации этиленгликоля получается соединение, имеющее 2 таутомерные формы (кето-енольная таутомерия):
Дегидратация этиленгликоля может происходить с одновременной его димеризацией:
При дегидратации 1,4-бутандиола можно получить тетрагидрофуран (оксолан):
Дегидратация других гликолей сопровождается процессом пинаколиновой перегруппировки:
При окислении этиленгликоля вначале получается гликолевый альдегид, далее глиоксаль, который при дальнейшем окислении переходит в дикарбоновую кислоту:
При окислении глицерина образуется смесь соответствующего альдегида и кетона:
Спирты
Классификация спиртов
Одноатомные спирты также подразделяются в зависимости от положения OH-группы: первичные (OH-группа у первичного атома углерода), вторичные (OH-группа у вторичного атома углерода) и третичные (OH-группа у третичного атома углерода).
Номенклатура и изомерия спиртов
Названия спиртов формируются путем добавления суффикса «ол» к названию алкана с соответствующим числом атомов углерода: метанол, этанол, пропанол, бутанол, пентанол и т.д.
Для спиртов характерна изомерия углеродного скелета (начиная с бутанола), положения функциональной группы и межклассовая изомерия с простыми эфирами, которых мы также коснемся в данной статье.
Получение спиртов
Присоединения молекулы воды (HOH) протекает по правилу Марковникова. Атом водорода направляется к наиболее гидрированному атому углерода, а гидроксогруппа идет к соседнему, наименее гидрированному, атому углерода.
В результате восстановления альдегидов и кетонов получаются соответственно первичные и вторичные спирты.
Синтез газом в промышленности называют смесь угарного газа и водорода, которая используется для синтеза различных химических соединений, в том числе и метанола.
В ходе брожения глюкозы выделяется углекислый газ и образуется этанол.
Химические свойства спиртов
Щелочные металлы (Li, Na, K) способны вытеснять водород из спиртов с образованием солей: метилатов, этилатов, пропилатов и т.д.
Необходимо особо заметить, что реакция с щелочами (NaOH, KOH, LiOH) для предельных одноатомных спиртов невозможна, так как образующиеся алкоголяты (соли спиртов) сразу же подвергаются гидролизу.
Реакция с галогеноводородами протекают как реакции обмена: атом галогена замещает гидроксогруппу, образуется молекула воды.
В результате реакций спиртов с кислотами образуются различные эфиры.
Дегидратация спиртов (отщепление воды) идет при повышенной температуре в присутствии серной кислоты (водоотнимающего) компонента.
Качественной реакцией на спирты является взаимодействие с оксидом меди II. В ходе такой реакции раствор приобретает характерное фиолетовое окрашивание.
Замечу, что в обычных условиях третичные спирты окислению не подвергаются. Для них необходимы очень жесткие условия, при которых углеродный скелет подвергается деструкции.
Вторичные и третичные спирты определяются другой качественной реакцией с хлоридом цинка II и соляной кислотой. В результате такой реакции выпадает маслянистый осадок.
Такой реакцией является взаимодействие многоатомного спирта со свежеприготовленным гидроксидом меди II. В результате реакции раствор окрашивается в характерный синий цвет.
Важным отличием многоатомных спиртов от одноатомных является их способность реагировать со щелочами (что невозможно для одноатомных спиртов). Это говорит об их более выраженных кислотных свойствах.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
В современной промышленности широко используются полиолы. Это вещества органического происхождения, обладающие рядом полезных свойств. Полиолы используют для производства полимеров, антифризов, взрывчатых веществ, в косметической и пищевой продукции.
Определение и общие свойства полиспиртов
Основным способом получения спиртов является синтез природного сырья. В природе полиолы можно встретить в составе воска, кашалотового жира и других сходных по составу веществ. Это сложные эфиры органических кислот, из которых многоатомные спирты легко выделяются.
Физические и химические свойства высших спиртов

Высшие спирты окисляются быстрее низкомолекулярных соединений. Свет и соприкосновение с воздухом ускоряют процесс окисления.
Промышленное применение
Полиспирты используют практически во всех промышленных сферах. Удивительно применение одних и тех же веществ в очень далеких друг от друга отраслях. Так, глицерин используют в косметологии и в изготовлении взрывчатых веществ. Без полиолов невозможно производство пластмасс, лакокрасочных материалов, полиуретанов, термоактивных полимерных смол, антифризов.
В производстве пластмасс полиспирты позволяют повысить упругость, устойчивость к деформации, увеличить долговечность изделий.
Использование в пищу спиртов не требует для усвоения выделения инсулина, поэтому особенно важным является возможность их применения в изготовлении диабетической продукции. Так, с использованием полиспиртов выпускают жевательную резинку, шоколад, газированные напитки, диабетические сладости.
Часть сахарозаменителей имеют полезные свойства, не относящиеся к способности придавать сладость продуктам. Так, глюцит (второе название сорбита) используется в фармакологии в качестве ароматизатора и загустителя для жидких лекарственных форм. Ксилит включают в состав раствора для внутривенного питания.
Также сорбит используют как гигроскопичное вещество при изготовлении мясных полуфабрикатов для увеличения срока годности продукта. Это же свойство удерживать влагу позволяет использовать сорбит в косметологии при производстве кремов, лосьонов и зубной пасты.
Сахарозаменители. Полиолы в пищевой индустрии
Сорбит и ксилит синтезируют из кукурузного крахмала, отходов переработанного хлопка, древесины некоторых лиственных деревьев.
По сладости сахарозаменители уступают обычному сахару более чем на 50 %. Зато другие достоинства полиолов перевешивают важность интенсивности вкусовых ощущений:
Кроме сладости ко вкусовым ощущениям добавляется холодящий эффект, что делает применение сорбита и ксилита непригодным для добавления в некоторые продукты. Однако эти же эффекты являются ценными качествами для производства жевательной резинки.
Шоколад с полиолами
Присущие сорбиту и ксилиту холодок и остаточный привкус способны исказить вкус какаосодержащих продуктов. Именно поэтому чаще всего диабетический шоколад имеет такой специфический вкус и остаточное холодящее ощущение на языке.
Этот факт не означает, что полиолов в шоколаде нужно обязательно избегать. Используя в качестве сырья для производства полиолов свеклу, синтезируют такой продукт, как изомальт. Это вещество неотличимо от обычного сахара, но менее калорийно и подходит для диабетиков. Видя среди ингредиентов шоколада Е953, покупатель может быть уверен, что получит продукт с чистым и насыщенным вкусом какао.
Влияние полиспиртов на человека. Польза и вред
С увеличением интереса к правильному питанию появляется интерес потребителя к информации о полиолах. Что это такое, вредно или нет, хотят знать многие. Говоря о пользе и вреде многоатомных спиртов, в первую очередь нужно рассматривать вещества, используемые в качестве пищевых добавок.
Как уже было сказано выше, сорбит, ксилит и изомальт являются средствами, заменяющими сахар в продуктах. При этом очевидна их польза в качестве антибактериальных, диабетических, диетических и профилактических добавок. Сорбит и ксилит при этом оказывают положительное влияние на перистальтику кишечника и используются в качестве щадящего слабительного средства.
Отрицательное воздействие на организм человека зависит от количества и периодичности употребления. Постоянный прием в больших дозах сахарозаменителей на основе полиолов способен спровоцировать дисбаланс в ЖКТ, обострить холецистит, вызвать тошноту, головные боли. Применять сахарозаменители людям, страдающим печеночной или почечной недостаточностью, болезнями ЖКТ и хроническим гепатитом, не рекомендуется.
Ксилит представляет собой смертельную опасность для собак. Организм животного принимает даже минимальную дозу вещества за сахар и запускает мощный выброс инсулина. Результатом становится гликемия с печальным прогнозом.
Мировой и российский рынок полиолов
Полиспирты для нужд промышленности синтезируют во всех развитых странах мира. Существующих объемов мощности производства высших спиртов в нашей стране недостаточно для насыщения всего рынка. Поэтому большая часть сырья импортируется из других стран. Соотношение внутреннего производства к импорту полиолов выглядит как 1:3. В первую очередь это относится к нефтехемическим продуктам.
Оценка спроса на многоатомные спирты однозначно прогнозирует рост потребностей всех отраслей во всех странах. Значит, производство полиолов будет развиваться и увеличивать объемы во всем мире.