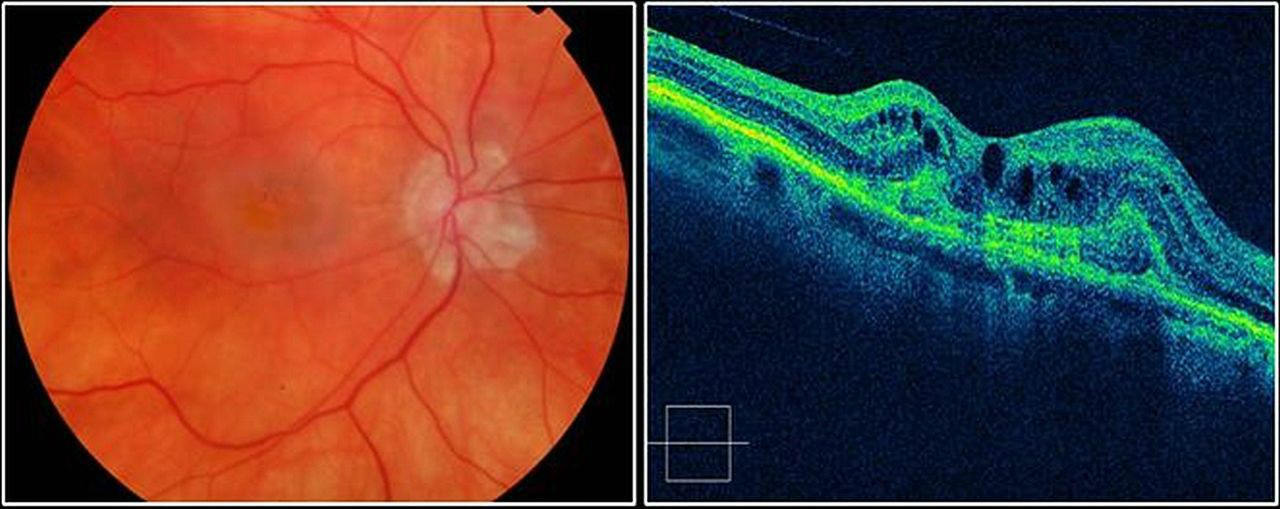
Что такое миопическая снм
Субретинальная неоваскулярная мембрана
Проявления СНМ
На глазном дне, клинические проявления СНМ выглядят округлым или овальным фокусом сероватого и серовато-зеленоватого цвета. Нередко, он окаймлён пигментом, перифокальной геморрагией либо местной отслойкой пигментного эпителия.
Картина флюоресцеинангиографии на ранних фазах СНМ имеет вид колеса велосипеда или даже кружева. На поздних фазах, это уже сплошная сливающаяся гиперфлюоресценция, обусловленная экстравазальным выходом флюоресцеина сквозь стенку новообразованных сосудов. Если субретинальнуюнеоваскулярную мембрану покрывает плотный экссудат, детали ее не проявляются на ранних фазах ФАГД.
Вызванный СНМ разрыв новообразованных сосудов, часто приводит к суб-, интра- или преретинальным кровоизлияниям, а также, к экссудативно-геморрагическим отслойкам нейроэпителия, который после замещается фибриноваскулярным рубцом.
Диагностика
Основными диагностическими методами выявления СНМ являются: офтальмоскопия, флюоресцентная ангиография глазного дна, которую выполняют с применением различных красителей (флюоресцеин натрия, индоцианин зелёный), а также оптическая когерентная томография. Но несмотря на серьезные исследования в этой области, критерии степени активности данного заболевания пока не определены.
Лечение
Изредка при СНМ наблюдается спонтанное рубцевание. С целью ускорения процессов рубцевания, рекомендуется назначать актовегин или солкосерил. При этом, актовегин применяют местно и в инъекциях (субконъюнктивально, а также внутримышечно). Наиболее эффективным методом лечения субретинальнойнеоваскулярной мембраны признана лазерная коагуляция.
В медицинском центре «Московская Глазная Клиника» все желающие могут пройти обследование на самой современной диагностической аппаратуре, а по результатам – получить консультацию высококлассного специалиста. Мы открыты семь дней в неделю и работаем ежедневно с 9 ч до 21 ч. Наши специалисты помогут выявить причину снижения зрения, и проведут верное лечение выявленных патологий. Опытные рефракционные хирурги, детальная диагностика и обследование, а также большой профессиональный опыт наших специалистов гарантирует максимально благоприятный результат для пациента.
Уточнить расценки на ту или иную процедуру, записаться на прием в «Московскую Глазную Клинику» Вы можете по многоканальному телефону 8 (800) 777-38-81 (ежедневно с 9:00 до 21:00, бесплатно для мобильных и регионов РФ) или воспользоваться формой онлайн-записи.
Субретинальная неоваскулярная мембрана (СНМ)
Субретинальная неоваскулярная мембрана (СНМ) – патология, которая при длительном существовании вызывает слепоту. Она развивается на фоне различных поражениях макулы (центральной хорио-ретинальной дистрофии, осложненной миопии и пр.). СНМ проявляется прорастанием в сетчатку патологических новообразованных сосудов, которые имеют хориоидальное происхождение.
Диагностика
Наиболее информативным методом установки диагноза является ангио-ОКТ (оптическая когерентная томография сетчатки в режиме ангиографии), т.к. ФАГ (флуоресцентная ангиография сетчатки глаза) не доступна из-за отсутствия контрастного вещества в России.
Лечение
Субретинальная неоваскулярная мембрана в начальных стадиях в основном лечится методом лазеркоагуляции. Однако, подобное лазерное воздействие на патологические сосуды сетчатки повреждает и окружающие ткани, что становится причиной ухудшения зрения. Поэтому, лазеркоагуляция проводится в основном, не для улучшения остроты зрения, а чтобы сохранить оставшуюся зрительную функцию.
К сожалению, в ранних стадиях заболевания пациент редко обращается к врачу, поэтому, в основном, офтальмологи имеют дело с развитыми формами.
Видео операции удаления СНМ
В нашей клинике собрано лучшее диагностическое оборудование, что позволяет выявить заболевание уже на самой ранней стадии и начать необходимую терапию. Работающие здесь специалисты имеют большой опыт лечения субретинальной неоваскулярной мембраны с помощью интравитреального введения препарата Луцентис или витреоретинальной хирургии. Благодаря накопленному опыту, врачи добиваются максимально возможных результатов без серьезных осложнений, способных негативным образом отразиться на зрительной функции.
Цены на лечение субретинальной неоваскулярной мембраны сетчатки
ВНИМАНИЕ! Точную стоимость лечения можно будет сказать только после очной коснультации, когда будет определено состояние сетчатки глаз пациента и составлен план лечения. Узнать стоимость основных процедур и операций вы можете в разделе ЦЕНЫ.
Субретинальная неоваскулярная мембрана
Формирование субретинальной неоваскулярной мембраны (СНВ) нередко происходит при заболеваниях глазного дна. Чаще всего встречаются инволюционные центральные хориоретинальные дистрофии, токсоплазмоидный хориоретинит, ангиоидные полосы сетчатки, вторичные поствоспалительные дистрофии сетчатки и осложненная миопия. В ряде случаев установить причину формирования субретинальной неоваскулярной мембраны не удается, то есть она носить идиопатический характер.
Патогенез
В результате формирования субретинальной неоваскулярной мембраны сквозь дефекты (трещины или разрывы) в мембране Бруха хориоретинальные капилляры врастают в субпигментное и субретинальное пространство.
Диагностика
Чтобы выявить наличие субретинальной неоваскулярной мембраны, назначают флуоресцентную ангиографию и офтальмоскопию.
Клиника
Внешне субретинальная неоваскулярная мембрана выглядит как округлое или овальное образование серого или зеленоватого цвета. Обычно она имеет перифокальную геморрагию и пигментное окаймление, а также сопровождается локальной отслойкой пигментного эпителия.
При проведении ангиографии после введения флуоресеина на ранних стадиях заболевания имеется картина кружева или колеса велосипеда. В более поздних стадиях она трансформируется в сплошную и сливающуюся область гиперфлуоресценции. Это обусловлено выходом флуоресцеина сквозь поврежденную стенку за пределы сосудов. Если субретинальную неоваскулярную мембрану прикрывает плотный экссудат, то на ранних фазах флуоресцентной ангиографии ее можно не заметить.
При разрыве вновь образованных сосудов возникают суб-, пре- или интраретинальные кровоизлияния. Также высока вероятность экссудативно-геморрагической отслойки нейроэпителия, который в дальнейшем замещается фибриноваскулярным рубцом.
Лечение
Крайне редко происходит спонтанное рубцевание. Чтобы ускорить этот процесс можно использовать актовегин и солкосерил для местного (субконъюнктивального) или внутримышечного введения. Методом выбора при развитии субретинальной неоваскулярной мембраны является лазерная коагуляция.
В ряде случаев может быть показано трансретинальное удаление мембраны, однако нужно учитывать все возможные риски от этого сложного хирургического вмешательства.
И будет ли после операции пациент видеть нормально?
Микрохирургия глаза имени академика С.Н. Федорова
Министерства здравоохранения Российской Федерации
Хирургическое лечение
Анти-VEGF терапия (Препаратами Луцентис и Эйлеа):
Возрастная макулярная дегенерация:
По данным Всемирной Организации Здравоохранения, возрастная макулярная дегенерация (ВМД) является одной из наиболее частых причин слепоты и слабовидения у лиц старшей возрастной группы. ВМД — хроническое дегенеративное нарушение, которым чаще всего страдают люди после 50 лет. В России заболеваемость ВМД составляет 15 на 1000 населения. Это социально значимое заболевание, занимает второе место среди причин инвалидности по зрению во всем мире.
ВМД проявляется прогрессирующим ухудшением центрального зрения и необратимым поражением макулярной зоны. Макулодистрофия — двустороннее заболевание (до 60% случаев поражаются оба глаза), однако, как правило, поражение более выражено и развивается быстрее на одном глазу, на втором глазу ВМД может начать развиваться через 2-5 лет. Очень часто пациент не сразу замечает проблемы со зрением, поскольку на начальном этапе заболевания всю зрительную нагрузку на себя берёт лучше видящий глаз.
ВАЖНО! При снижении остроты зрения как вдаль, так и на близком расстоянии; затруднениях, возникающих при чтении и письме; появлении перед глазом полупрозрачного фиксированного пятна, а также искажении контуров предметов, их цвета и контрастности — следует немедленно обратиться к врачу офтальмологу для диагностики, постановки точного диагноза и выбора метода лечения.
Высокоинформативным является самоконтроль зрительных функций каждого глаза в отдельности при помощи теста Амслера.
Факторы риска развития ВМД:
Симптомы «влажной» формы ВМД:
Основная цель лечения влажной формы ВМД
Воздействовать на хориоидальную неоваскуляризацию, т.е. препятствовать росту новообразованных сосудов и повышенной проницаемости сосудистой стенки.
В настоящее время так называемая анти-VEGF терапия полностью изменила подходы к лечению ВМД, позволяя сохранить зрение и поддержать качество жизни миллионов людей во всем мире. Анти-VEGF терапия может не только уменьшить прогрессирование ВМД, но в некоторых случаях даже позволяет улучшить зрение. Лечение эффективно, но только в тех случаях, когда оно проведено до образования рубцовой ткани и до необратимой потери зрения.
Препараты для лечения возрастной макулярной дегенерации – ЛУЦЕНТИС (Lucentis) и ЭЙЛЕА (Eylea)
Первым препаратом для анти-VEGF терапии в виде интравитреальных инъекций, сертифицированным в России в 2008 для применения в офтальмологии, был ЛУЦЕНТИС, совершивший настоящую революцию в лечении ВМД и ставший «золотым стандартом». В Хабаровском филиале ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России Луцентис применяется с 2009г.
Ученые продолжали исследования, чтобы создать препарат более пролонгированного действия, не уступающий по качественным результатам ЛУЦЕНТИСу и в марте 2016 года в РФ зарегистрирован новый препарат — ЭЙЛЕА для лечения влажной формы ВМД. В Хабаровском филиале ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н.Федорова» Минздрава России Эйлеа применяется с 2017 г.
Частота приема и дозировка
Анти-VEGF терапия выполняется в условиях стерильной операционной врачом-офтальмологом.
Луцентис (ранибизумаб) вводится интравитреально 0,5 мг (0,05 мл) в режиме, включающем 3 следующих друг за другом «загрузочных» интравитреальных введения данного препарата с последующим ежеквартальным мониторингом состояния глазного дна и возобновлением поддерживающей терапии в виде дополнительных интравитреальных инъекций при неполном регрессе, либо рецидивах экссудативно-геморрагической активности.
Интравитреальное введение Луцентиса позволяет остановить прогрессирование этого заболевания, а в ряде случаев улучшить функциональные и анатомические показатели. Современное оборудование в ХФ МНТК позволяет выявить это заболевание на самых ранних стадиях и предложить пациентам соответствующее лечение.
Эйлеа (афлиберцепт) вводится интравитреально 2мг (0,05 мл).
Терапию начинают с введения трех последовательных инъекций 1 раз в месяц, затем выполняют по потребности, в зависимости от активности процесса.
Сама процедура интравитреальных инъекций проводится в условиях операционной МНТК под местной капельной анестезией. Продолжительность процедуры 3-5 минут.
В ряде крупных международных испытаний и в реальной клинической практике были доказаны активность и безопасность препаратов Луцентис и Эйлеа. Результаты поистине впечатляют – у большинства пациентов не только остановилось прогрессирование заболевания, и сохранилась острота зрения, но этот показатель значительно улучшился.
Клинический случай: Пациент К., 76 лет
Как и любое другое оперативное вмешательство интравитреальное введение Луцентиса и Эйлеа может вызвать ряд осложнений, но процент их очень низок, что позволяет говорить об относительной безопасности этого метода лечения. Эффективность и безопасность – вот основные составляющие успеха этого метода во всем мире.
Миопическая хориоидальная неоваскуляризация (ХНВ)
Миопия — самое распространенное нарушение рефракции у людей трудоспособного возраста во всем мире. В России в структуре инвалидности патологическая миопия (ПМ) занимает 2 место. Частота инвалидности — 4,5 случая на 10000 населения.
Хориоидальная неоваскуляризация (ХНВ) — одно из самых серьезных осложнений ПМ. При миопической ХНВ 36% инвалидов имеют 1и 2 группу.
Жалобы предъявляемые пациентами с миопической ХНВ:
Современные возможности лечения ХНВ при дегенеративной миопии – применение Анти-VEGF терапии – Луцентис и Эйлеа.
Кратность и длительность применения определяет лечащий врач.
Тромбоз (окклюзия) вен сетчатки
Тромбоз вен сетчатки – острое нарушение кровообращения в сосудах сетчатки. Заболевание это достаточно часто встречается (2,14 случая на 1000 человек) и может привести к стойкому и значительному снижению зрения, вплоть до слепоты. Окклюзии вен сетчатки нередко называют сосудистыми катастрофами. Основным клиническим симптомом тромбоза вен сетчатки является резкое безболезненное снижение зрения или выпадения полей зрения одного глаза. Чаще всего окклюзия вен сетчатки развивается на фоне артериальной гипертензии, атеросклероза, сахарного диабета, а также состояний, сопровождающихся нарушением вязкости крови (наследственные и приобретенные тромбофилии, лейкемия, прием диуретиков, противозачаточных препаратов и многое другое).
Наиболее типичной локализацией тромбоза является место выхода центральной вены сетчатки в толще зрительного нерва (окклюзия центральной вены сетчатки) и артериовенозный перекрест 1-го или 2-го порядка (окклюзия ветви центральной вены сетчатки). В результате предрасполагающих факторов, в месте пересечения вены сетчатки с артерией, происходит компрессия вены, локальное замедление кровотока в ней и формирование тромба, частично или полностью закрывающего просвет сосуда. Происходит резкое нарушение или прекращение венозного оттока по пораженной вене. Это приводит к резкому нарушению перфузии тканей сетчатки, гипоксии (кислородному голоданию), ишемии (появлению участков микроинфарктов сетчатки), повышению сосудистой проницаемости, появлению кровоизлияний и развитию отека сетчатки.
Макулярный отек – главное осложнение, приводящее к снижению зрения.
Диагностика тромбоза вен сетчатки.
Постановка диагноза не составляет большого труда. Для этого необходим осмотр глазного дна врачом-офтальмологом при помощи специальных диагностических линз на широком зрачке. Для выявления тяжести поражения и определения наиболее подходящей лечебной тактики, возможно проведение дополнительных диагностических методов, таких как оптическая когерентная томография (ОКТ) и ангио-ОКТ.
Лечение:
Лечение должно быть начато сразу после постановки диагноза.
Учитывая тот факт, что в подавляющем большинстве случаев заболевание возникает на фоне скачка артериального давления, необходима нормализация его уровня. Стабилизация соматического состояния является залогом успешного лечения. Необходимо определить параметры свертывающей системы крови.
Согласно современным мировым стандартам, в максимально ранние сроки после свершившегося тромбоза, необходимо провести интравитреальное введение специального препарата, направленного на подавление макулярного отека сетчатки. В настоящее время существует 3 основных препарата, обладающих высокой эффективностью в отношении макулярного отека на фоне окклюзии вен сетчатки: анти-VEGF препараты: Луцентис и Эйлеа, а также внутриглазной имплантат с дексаметазоном Озурдекс. При легкой степени нарушений сетчатки для восстановления или улучшения зрения может быть достаточно одной инъекции анти-VEGF препарата или внутриглазного имплантата. В тяжелых случаях могут потребоваться неоднократные инъекции препаратов, которые необходимо комбинировать или сочетать с лазерной коагуляцией сетчатки. Интравитреальное введение вышеперечисленных препаратов проводится в условиях стерильной операционной МНТК, под местной капельной анестезией.
Необходимо помнить, что своевременная диагностика и вовремя начатое адекватное лечение значительно повышает шансы на восстановление зрения при тромбозе вен сетчатки.
При запоздалом и неправильном лечении возможно развитие атрофии зрительного нерва, неоваскулярной глаукомы и рубцовых изменений сетчатки.
Диабетическая ретинопатия
Сахарный диабет (СД) входит в тройку заболеваний, приводящих к инвалидности и смерти. Общая численность пациентов с СД в РФ на конец 2020 г составила 4,819 млн чел., это 3,3% населения РФ, из них 92% пациентов страдают СД2 типа. Более, чем 10 млн. пациентов, страдающих СД в России. С увеличением длительности течения СД возрастает риск возникновения диабетической ретинопатии (ДР), которую вызывает высокий сахар крови, приводящий к повреждению сосудов сетчатки. Так через 20 лет после начала заболевания у всех пациентов с СД1 диагностируется ДР, в 50% случаев имеет место ее пролиферативная стадия с полной потерей зрения у каждого 30-го больного. При СД2 ДР выявляется в 15-30% случаев уже при установлении диагноза СД, а через 30 лет – имеет место более чем у 90% пациентов. В РФ зарегистрированы более 630 000 пациентов с различными стадиями ДР. Распространенность ДР среди взрослых с СД1 — 41,74%, с СД2 – 17,41%. В целом, каждый пятый пациент с СД имеет те или иные проблемы со зрением.
Диабетический макулярный отек (ДМО) выявляется у 27% пациентов с не менее чем 9 летним стажем СД1 типа, и у 28% с не менее чем 20 летним стажем СД2 типа. При отсутствии лечения 32% больных с «клинически значимым ДМО» имеют 3-летний риск серьезной потери центрального зрения.
Основными направлениями лечения ДМО в настоящее время являются:
Субретинальная неоваскулярная мембрана при центральной серозной хориоретинопатии.
Центральная серозная хориоретинопатия (ЦСХР) — заболевание заднего полюса глаз широко распространенное во всем мире. Оно занимает четвертое место среди заболеваний сетчатки после возрастной макулярной дегенерации, диабетической и посттромботической ретинопатии и чаще встречается у молодых пациентов.
Жалобами таких пациентов является наличие «пятна», размытости перед пораженным глазом, снижение зрения.
Так же в ряде случаев, это заболевание может вызвать рост новообразованных сосудов – субретинальную неоваскулярную мембрану (СНМ), при котором значительно снижается острота зрения.
Для лечением развившейся СНМ используется интравитреальное введение препарата Ранибизумаб (Луцентис). Режим лечения подбирают индивидуально для каждого пациента, основываясь на активности заболевания. Некоторым пациентам может потребоваться только одна инъекция в течение первого года лечения, другим же могут потребоваться более частые инъекции, включая ежемесячные.
Кросслинкинг роговичного коллагена:
В 2014г. в отделении был внедрен способ лечения пациентов с кератоконусом и тяжелыми эпителиально-эндотелиальными дистрофиями роговицы — кросслинкинг роговичного коллагена. Методика перекрестного связывания коллагена, разработанная G. Wollensak, T. Seiler, в 2003 г., основана на эффекте фотополимеризации стромальных волокон под воздействием фоточувствительной субстанции (раствор рибофлавина) и низких доз ультрафиолетового излучения. Перекрестное связывание коллагена приводит к биомеханической стабилизации роговицы, в основе которой лежит увеличение числа интра – и интерфибриллярных ковалентных связей.
Кросслинкинг роговичного коллагена эффективный метод, позволяющий добиться биомеханической стабилизации и остановки прогрессирования заболевания.
Традиционным способом проводим лечение пациентов на 1-2 стадиях кератоконуса.
Методом трансэпителиального кросслинкинга (модифицированный трансэпителиальный метод ионофореза, разработанный в Уфимском НИИ глазных болезней, способствующий проникновению рибофлавина в роговицу без удаления эпителия, и последующему проведению кросслинкинга роговичного коллагена) – с тяжелыми эпителиально-эндотелиальными дистрофиями (ЭЭД) различного генеза.
Реваскуляризирующие операции
С 1995 г. в ХФ МНТК внедрены и успешно применяются по настоящее время при заболеваниях сетчатки и зрительного нерва операции с использованием биоматериала серии «Аллоплант», разработанные во Всероссийском центре глазной и пластической хирургии профессором Э.Р. Мулдашевым (г. Уфа).
Аллоплант — уникальный биоматериал, который стимулирует поражённые ткани и органы самостоятельно восстанавливаться. Происходит процесс самооздоровления за счёт регенерации тканей, усиленного роста новых здоровых клеток.
Полученные коллективом Всероссийского Центра глазной и пластической хирургии научные результаты и их практическая реализация позволили на основе трансплантационной технологии Аллоплант развить концепцию регенеративной хирургии. Аллоплант одобрен Министерством Здравоохранения Российской Федерации.
При использовании различных видов биоматериалов Аллоплант можно стимулировать регенерацию кровеносных и лимфатических сосудов, роговицы, склеры, кожных покровов, конъюнктивы, нервов, паренхимы печени, слизистой оболочки ЖКТ и т.д.
За последние три десятилетия Аллоплант был успешно использован при лечении диабетической ретинопатии, ретинопатии недоношенных, пигментного ретинита, атрофии и невритов зрительного нерва, увеитов, тромбозов вен сетчатки, бельм, травм, кератитов, миопии, ожогов и врожденных дефектов. Аллоплант широко применяется в офтальмологии, пластической хирургии, стоматологии, грудной хирургии, нейрохирургии, проктологии, ортопедии, травматологии, хирургии печени, гинекологии и т.д.
Биоматериалы Аллоплант – изготавливаются из кадаверных тканей человека.
Механизм лечебного действия Аллопланта:
Виды АЛЛОПЛАНТОВ, применяемых при лечении заболеваний заднего отрезка глаза:
Применение Аллопланта при различной офтальмологической патологии:
Аллоплант дает возможность лечить болезни, считающиеся «безнадежными». Он провоцирует организм на усиленное производство собственных здоровых клеток, гасит воспаление, стимулирует иммунитет.
Для ЛЕЧЕНИЯ в отделении комплексно-реабилитационного лечения Пациенту необходимо иметь при себе:
— Общий анализ крови + тромбоциты (действителен 10 дней)
— Свертываемость и длительность кровотечения, ПТИ (действителен 1 месяц). Для пациентов, получающих варфарин — МНО
— Анализ крови на сахар (действителен 10 дней)
— ЭКГ с описанием (при патологии — заключение кардиолога) (действительна 1 месяц)
— Результат флюорографии органов грудной клетки (действителен 1 год)
Консультации специалистов (иметь при себе бланки анализов, оригиналы или ксерокопии):
— Заключение терапевта, эндокринолога (если получает препараты, указать название и дозировку — действительно 1 месяц)
После прохождения комплексного обследования в диагностическом отделе ХФ МНТК “Микрохирургия глаза” и консультации врача определяются показания к оперативному лечению.
При наличии показаний операция будет выполнена на следующий рабочий день. Иногородним пациентам необходимо заранее позаботится о проживании в гостиницах г. Хабаровска
ВНИМАНИЕ. Точную стоимость платного лечения можно будет сказать только после очной консультации, когда будет определено состояние глаз пациента и составлен план лечения.
Субретинальная неоваскулярная мембрана (СНМ) и ее лечение
Ведущей причиной слабовидения и полной слепоты у лиц старшего и пожилого возраста, по данным эпидемиологических исследований, является возрастная макулярная дегенерация (ВМД). Заболевание имеет наследственную предрасположенность и, в первую очередь, поражает пигментный эпителий, а также хориокапилляры в центральной (макулярной) зоне сетчатой оболочки.
Подавляющее большинство (почти 90%) случаев утери зрения от ВМД обусловлено развитием экссудативной формы этого заболевания, по-другому называемой «влажной». Данная форма ВМД сопровождается чрезмерным ростом аномальных, новообразованных сосудов, прорастающих из хориокапиллярного слоя сосудистой оболочки сквозь дефекты в мембране Бруха под нейроэпителий и/или пигментный эпителий сетчатки. В офтальмологии подобное состояние получило название субретинальной (локализованной под сетчаткой) неоваскулярной мембраны (СНМ).
Новообразованные сосуды при СНМ имеют аномально слабую стенку, из-за чего под сетчатку начинает просачиваться жидкая часть крови, с отложением там липидов и холестерина. Зачастую эти сосуды рвутся, и возникают кровоизлияния, как правило, небольшие по объему и локальные, а в некоторых случаях и довольно значительные. Все это нарушает питание сетчатки и приводит к возникновению фиброза, когда прозрачная ткань сетчатки замещается соединительной. В исходе влажной формы ВМД формируется субретинальный рубец, из-за чего сетчатка перестает выполнять свои функции
К абсолютной слепоте центральная хориоретинальная дистрофия (ЦХРД) не приводит никогда. Но из-за появления в центральной части поля зрения темного пятна (абсолютной скотомы) у человека постепенно пропадает центральное зрение. Так как патологический процесс затрагивает лишь центральную часть (макулу), периферическое поле зрения остается сохранным. В исходе процесса остаточное зрение, как правило, составляет 0,1 (первая строчка таблицы) и пациент видит лишь «боковым зрением.
Патологический процесс всегда протекает индивидуально, но развитие СНМ «включает» временной фактор, который приобретает первостепенное значение. При этом, избежать полной потери зрения поможет только ранняя диагностика заболевания и своевременно начатое адекватное лечение, приводящее к длительной ремиссии или обратному развитию патологического процесса.
Методы лечения неоваскулярной мембраны
Среди методов лечения субретинальной неоваскулярной мембраны при влажной форме ВМД выделяют лазеркоагуляцию сетчатки, транспупиллярную термотерапию (ТТТ), фотодинамическую терапию (ФДТ) и удаление СНМ хирургическим способом.
Однако за последние несколько лет терапия данного заболевания вышла на новый уровень, благодаря появлению эффективных лекарственных препаратов. Это препараты-ингибиторы выработки фактора эндотелиального роста сосудов (VEGF).
Ведь хотя причины возникновения СНМ до конца не изучены, из данных исследований последних лет ученые сделали вывод, что роль VEGF в ее развитии очень важна. Таким образом, фармакологические ингибиторы VEGF возможно являются новым и наиболее перспективным направлением в терапии данных патологий.
В современной клинической практике, сегодня уже широко применяют следующие препараты:
Мacugen® (Макуджен)
Это один из первых фармакологических ингибиторов VEGF, применяющийся в офтальмологии. Мacugen® или Макуджен (основное вещество пегаптаниб) позиционируется, как так называемый анти-VEGF аптамер. Лечение им помогает замедлить снижение остроты зрения пациентов с СНМ при влажной форме ВМД. Эффективность препарата сравнима с действием фотодинамической терапии. Он стал первым из препаратов данной группы, разрешенным FDA для интравитреального введения в полость стекловидного тела при лечении любых форм субретинальной неоваскулярной мембраны при возрастной макулодистрофии (2004 г.). Особенно хороший эффект от применения препарата Макуджен наблюдается на ранних стадиях ВМД.
Lucentis® (Луцентис)
Препарат Lucentis® или Луцентис (основное вещество ранибизумаб) действует как антиген-связующий фрагмент к VEGF антител мышей. Препарат является рекомбинантным, полученным одним из методов генной инженерии. Молекула ранибизумаба — высокоспецифичная часть антитела мыши к VEGF с низким молекулярным весом (48 кДа). Она может проникать сквозь все слои сетчатой оболочки к патологическому объекту блокируя рецепторы VEGF входящих в СНМ новообразованных сосудов. Lucentis — первый препаратом данной группы, терапия которым ведет к частичному восстановлению зрения, а не только к торможению его прогрессирующего снижения (стабилизация зрения в 95% случаев, повышение остроты зрения в 25-40% случаев). Положительные результаты клинических исследований позволили FDA утвердить Lucentis, как средство лечения субретинальной неоваскулярной мембраны при ВДМ (2006 г.).
Avastin™ (Авастин)
Бевацизумаб — действующее вещество препарата Avastin™ (Авастин), является полноразмерным антителом против любых изоформ (разновидностей) VEGF. Еще в 2004 году его стали активно использовать в онкологии при лечения рака прямой кишки и толстого кишечника.
Первый опыт применения Авастина у пациентов с влажной формой ВМД принадлежит американским исследователям Rosenfeld и Puliafito. Это произошло в 2005 году, когда положительные результаты от его применения были получены у пациентов с СНМ и прогрессирующим падением остроты зрения после поведения фотодинамической терапии и лечения Макудженом. Пациентам выполнялось 2-3 кратное введение Авастина внутривенно по 5 мг/кг с перерывом в две недели. При этом было достоверно зафиксировано проведением ОКТ повышение остроты зрения, а также уменьшение толщины сетчатки в зоне макулы.
Какое-то время целесообразность интравитреального введения препарата оставалась под сомнение. Ведь его молекулярная масса в несколько раз выше, чем у Макуджена и Луцентиса, и были сомнения насчет его способности проникать сквозь сетчатку. Но опубликованные в последующем результаты исследований убедительно доказали, что введенный в полость стекловидного тела бевацизумаб, легко проникать сквозь все слои сетчатой оболочки.
При внутривенном введении Авастина существует риск потенциально возможных побочных эффектов, уже описанных при применении его в онкологии. Среди них: повышение АД, носовые кровотечения, риск тромбоэмболии, протеинурия. Однако интравитреальные инъекции данного препарата буквально сводят на нет возможность возникновения указанных побочных эффектов, ведь применяемая доза в 400-500 раз меньше. В тоже время этот путь введения обеспечивает высокую концентрацию действующего вещества именно в месте поражения.
Введение Авастина в полость стекловидного тела осуществляют раз в 3-4 недели в дозировке 1,25 мг. По результатам многочисленных исследований такие инъекции повышают остроту зрения в 30-43% случаев и стабилизируют ее в 53-56% случаев. Положительный эффект от инъекций Авастина сводится к уменьшению толщины сетчатки в зоне макулы, что подтверждается данными ОКТ, а также к стабилизации объема СНМ и к уменьшению пропотевания флюоресцеина сквозь сосудистую стенку по данным ФАГ. Максимальная эффективность препарата бнаруживается с первых инъекций. При этом, степень выраженности ее не зависит проводимых ранее фотодинамической терапии и/или лечения Макудженом. По имеющимся данным, повторное ухудшение зрения, а также скопление в субретинальном пространстве жидкости после однократной инъекции Авастина возникает в 30% случаев примерно через 70-80 дней, что делает особенно актуальной своевременность следующей инъекции.
Наиболее частыми неприятными последствиями интравитреального введения Авастина бывают: транзиторная (преходящая) инъекция конъюнктивальных сосудов и кровоизлияние в зоне введения препарата. Возникновения системных побочных эффектов подобного способа введения до настоящего времени не отмечалось.
В странах Европы, как и в США показания к применению Авастина в офтальмологической практике до сих пор отсутствуют в официальном перечне и препарат применяется по т.н. системе «off-label». И все же, Авастин с каждым годом становится все более популярным в группе препаратов-ингибиторов VEGF. Не последнюю роль в этом играет и экономический фактор, ведь инъекции Авестина имеют самую низкую стоимость в сравнении со средствами аналогичного действия – Макудженом и Луцентисом, а также процедурами фотодинамической терапии.
За последние два года появилось немало публикаций с результатами исследований терапии препаратом Avastin у пациентов с субретинальной неоваскулярной мембраной при влажной форме ВМД. Однако, отдаленных результатов подобного лечения пока нет и ожидается не ранее, чем через 3-5 лет. Но все же, имеющийся уже сегодня высокий процент положительных результатов интравитреального введении группы ингибиторов VEGF говорит о том, что достаточно эффективный метод лечения экссудативной формы возрастной макулярной дегенерации наконец появился. Применение Авастина или какого-либо из иных препаратов–ингибиторов VEGF является сегодня методом выбора при лечении пациентов с ВМД, как альтернатива дорогостоящей процедуре фотодинамической терапии.