Что такое малигнизированная киста
С.П. Даренков, А.А. Проскоков, А.А. Агабекян, И.А. Трофимов
Кафедра урологии Центральной государственной медицинской академии Управления делами Президента РФ; ФГБУ «Клиническая больница» Управления делами Президента РФ, Москва, Россия
Литература
1. Bas O., Nalbant I., Sener C., Firat H., Yeşil S., Zengin K., Yalcınkaya F., Imamoglu A. Management of Renal Cysts. JSLS. 2015;19(1): e2014.00097. Doi: 10.4293/JSLS.2014.00097.
2. Skolarikos A., Laguna M.P., de la Rosette J.J. Conservative and radiological management of simple renal cysts: a comprehensive review. BJU Int. 2012;110(2):170–8. Doi: 10.1111/j.1464-410X.2011.
3. Hemal A.K. Laparoscopic management of renal cystic disease. Urol Clin North Am. 2001;28:115–126.
4. Bosniak M.A. The current radiological approach to renal cysts. Radiology. 1986;158:1–10. Doi: 10.1148/radiology.158.1.3510019.
5. Bosniak MA. Problems in the radiologic diagnosis of renal parenchymal tumors. Urol Clin North Am. 1993;20:217–230.
6. Bosniak M.A. Diagnosis and management of patients with complicated cystic lesions of the kidney. AJR Am J Roentgenol. 1997;169:819–21. Doi: 10.2214/ajr.169.3.9275903.
7. Bosniak M.A. The use of the Bosniak classification system for renal cysts and cystic tumors. J Urol. 1997;157:1852–53. Doi: 10.1016/S0022-5347(01)64883-3.
8. Muglia V.F., Carlos A. Bosniak classification for complex renal cysts: history and critical analysis. Westphalen Radiologia Brasileira. 2014;47(6):368–373.
9. Eknoyan G. A clinical view of simple and complex renal cysts. J Am Soc Nephrol. 2009;20:1874–1876.
10. Smith A.D., Remer E.M., Cox K.L., Lieber M.L., Allen B.C., Shah S.N., Herts B.R. Bosniak category IIF and III cystic renal lesions: outcomes and associations. Radiology. 2012;262:152–160. Doi: 10.1148/radiol.11110888.
11. O’Malley R.L., Godoy G., Hecht E.M., Stifelman M.D., Taneja S.S. Bosniak category IIF designation and surgery for complex renal cysts. J Urol. 2009;182:1091–1095. Doi: 10.1016/j.juro.2009.05.046.
12. Song C., Min G.E., Song K., Kim J.K., Hong B., Kim C.S., Ahn H. Differential diagnosis of complex cystic renal mass using multiphase computerized tomography. J Urol. 2009;181:2446–50. Doi: 10.1016/j.juro.2009.01.111.
13. Malkhasyan V.A., Semenyakin I.V., Andreev R.Yu., Ivanov V.Yu., Makhmudov T.B., Pushkar D.Yu. Laparoscopic excision of the kidney cyst (Deroofing). Voprosy urologii i andrologii. 2017;5(2):45–50. Russian (Малхасян В.А., Семенякин И.В., Андреев Р.Ю., Иванов В.Ю., Махмудов Т.Б., Пушкарь Д.Ю. Лапароскопическое иссечение кисты почки (Deroofing). Вопросы урологии и андрологии. 2017;5(2):45–50).
14. Hinev A., Anakievski D. Acta Chir Iugosl. Laparoscopic transperitoneal renal cyst decortication. 2014;61(1):35–40.
15. Gadelmoula M., KurKar A., Shalaby M.M. The laparoscopic management of symptomatic renal cysts: A single-centre experience. Arab J Urol. 2014;12(2):173–177. Doi: 10.1016/j.aju.2013.12.001.
16. Alekseev B.Ya., Shevchuk I.M., Efremov G.D., Samoilova S.I. Multilocular cystic renal neoplasia of low malignant potential: the experience of the O.N. Lopatkin Research Institute of Urology and Interventional Radiology. OU. 2017;3:34–38. Doi: 10.17650/1726-9776-2017-13-3-34-38. Russian (Алексеев Б.Я., Шевчук И.М., Ефремов Г.Д., Самойлова С.И. Мультилокулярная кистозная почечная неоплазия низкого злокачественного потенциала: опыт НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина. ОУ. 2017;3:34–38. Doi: 10.17650/1726-9776-2017-13-3-34-38).
17. Srigley J.R., Delahunt B., Eble J.N., Egevad L., Epstein J.I., Grignon D., Hes O., Moch H., Montironi R., Tickoo S.K., Zhou M., Argani P. The International Society of Urological Pathology (ISUP) Vancouver classification of renal neoplasia. Am J Surg Pathol. 2013;37(10):1469–1489. Doi: 10.1097/PAS.0b013e318299f2d1.
18. Mousessian P.N., Yamauchi F.I., Mussi T.C., Baroni R.H. Malignancy Rate, Histologic Grade, and Progression of Bosniak Category III and IV Complex Renal Cystic Lesions. AJR Am J Roentgenol. 2017;209(6):1285–1290. Doi: 10.2214/AJR.17.18142.
19. Schoots I.G., Zaccai K., Hunink M.G., Verhagen P.C.M.S. Classification for complex renal cysts reevaluated: a systematic review J Urol. 2017;198(1):12–21. Doi: 10.1016/j.juro.2016.09.160.
20. Whelan T.F. Guidelines on the management of renal cyst disease. Can Urol Assoc J. 2010;4:98–99.
21. Jhaveri K., Gupta P., Elmi A., Flor L., Moshonov H., Evans A., Jewett M. Cystic renal carcinomas: do they grow, metastasize, or recur? AJR Am J Roentgenol. 2013;201(2):292–296. Doi: 10.2214/AJR.12.9414.
Малигнизация
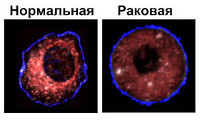
Малигнизация – процесс трансформации доброкачественных клеток в злокачественные. Может происходить в любых нормальных тканях или тканях доброкачественных опухолей. Сопровождается снижением уровня дифференцировки, изменением морфологических свойств, нарушением функции и бурным размножением клеток, прогрессирующим ростом новообразования и развитием отдаленных метастазов. Малигнизацию подтверждают на основании клинических данных, результатов лабораторных и инструментальных исследований. В процессе лечения опухоли обычно применяют хирургические вмешательства, химиотерапию и радиотерапию. Возможно использование гормонов, иммуностимуляторов и других препаратов.
Общие сведения
Малигнизация (озлокачествление, злокачественное перерождение) – сложный патоморфологический процесс, в ходе которого доброкачественные клетки приобретают свойства злокачественных. Малигнизации могут подвергаться как нормальные клетки, так и уже измененные, но не проявляющие признаков злокачественности. Чаще всего очаги озлокачествления возникают в области язв, полипов и различных доброкачественных опухолей. Причиной малигнизации могут стать генетическая предрасположенность и вредные факторы окружающей среды.
На начальных стадиях малигнизация протекает бессимптомно, поэтому ранняя диагностика злокачественных новообразований сопряжена со значительными затруднениями, однако регулярные профилактические осмотры, использование современных лабораторных и инструментальных методов исследования позволяют частично решить проблему раннего выявления малигнизации. Диагностику и лечение осуществляют специалисты в области онкологии, гастроэнтерологии, пульмонологии, неврологии, дерматологии, отоларингологии, гинекологии, ортопедии и врачи других специальностей (в зависимости от локализации опухоли).
В настоящее время злокачественные опухоли являются второй по распространенности причиной смертности после сердечно-сосудистых заболеваний. В 2012 году от рака умерло более 8 миллионов человек. Вероятность малигнизации увеличивается с возрастом, однако, наряду с людьми преклонных лет, злокачественные опухоли нередко поражают детей и пациентов трудоспособного возраста. Самыми распространенными видами рака являются рак легких, рак желудка, рак молочной железы, рак печени и рак толстого кишечника.
Причины малигнизации
Причиной малигнизации клеток является сочетание нескольких факторов, в числе которых специалисты указывают химические канцерогены, особенности окружающей среды, некоторые вирусы, состояния гормонального дисбаланса, возраст, вредные привычки и неблагоприятную наследственность. При проведении исследований было установлено, что малигнизацию могут провоцировать более 2000 различных химических веществ, однако степень их влияния на процессы злокачественного перерождения клеток может сильно различаться.
В перечень химических соединений, безусловно, вызывающих малигнизацию клеток, входят полициклические ароматические углеводороды (источниками являются транспорт, промышленные предприятия и отопительные системы), нитрозамины (содержатся в сигаретах, некоторых сортах пива и амидопирине), производные гидразина (входят в состав гербицидов и некоторых лекарственных средств), асбест и другие минеральные волокна (источником являются промышленные производства), а также некоторые соединения металлов.
Самым значимым физическим фактором малигнизации является солнечное излучение, от уровня которого напрямую зависит вероятность развития рака кожи. Чем светлее кожа и волосы и чем дольше человек подвергается воздействию солнечных лучей – тем выше риск развития меланомы, базалиомы и плоскоклеточного рака кожи. Кроме того, малигнизацию может стимулировать ионизирующее излучение, провоцирующее возникновение лейкозов, костных опухолей (радиоактивный стронций) и рака щитовидной железы (радиоактивный цезий и йод).
Доказано, что вероятность малигнизации повышается при воздействии на клетки определенных вирусов, в частности – вируса ATLV (вызывает лейкоз), вируса Эпштейна-Барр (провоцирует развитие лимфомы Беркитта), вируса папилломы человека (играет определенную роль в возникновении рака шейки матки) и вируса герпеса II типа. Малигнизации также способствуют нарушения гормонального баланса. Гормоны могут напрямую провоцировать озлокачествление, действовать на клетки опосредованно, стимулируя их пролиферацию, оказывать негативное влияние на иммунитет и изменять метаболизм некоторых канцерогенов.
Существенную роль в процессе малигнизации играет генетическая предрасположенность. Описано множество наследственных заболеваний с высокой вероятностью малигнизации, например, системный полипоз кишечника, при котором у большинства пациентов к 40-50 годам развивается рак толстой кишки, или болезнь Дауна, при которой риск развития лейкоза в 11 раз выше, чем в среднем по популяции. Прослеживается связь между малигнизацией и врожденными пороками развития.
Выявляется зависимость между вероятностью малигнизации тканей определенных органов и полом пациента. Мужчины в 2,4 раза чаще страдают опухолями глаз, в 2,1 раза чаще – новообразованиями желудка, в 2 раза чаще – злокачественными поражениями носоглотки, в 1,7 раза – опухолями костей. У женщин вдвое чаще выявляется малигнизация тканей щитовидной железы. Первое место по распространенности у мужчин занимают опухоли дыхательных путей, у женщин – опухоли половых органов и молочной железы. В большинстве случаев вероятность малигнизации у пациентов обоих полов увеличивается с возрастом, однако некоторые виды новообразований чаще выявляются у детей или молодых людей.
В число привычек, оказывающих наиболее сильное влияние на малигнизацию клеток, входят курение, неправильное питание и прием алкоголя. У курящих рак легких развивается в 11 раз чаще; опухоли полости рта, гортани и глотки – в 7 раз чаще; новообразования мочевого пузыря – в 2,2 раза чаще; опухоли поджелудочной железы – 1,7 раз чаще, чем у некурящих. Основными пищевыми привычками, увеличивающими вероятность малигнизации, являются прием большого количества мясной, жирной, острой и пряной пищи, склонность к пересаливанию и употребление недостаточного количества растительной клетчатки. Алкоголь сам по себе не вызывает малигнизацию, но выступает в роли активатора, усиливая воздействие других факторов.
Стадии и этапы малигнизации
Начальной стадией малигнизации является инициация – мутация клеток под воздействием внутренних или внешних вредных факторов. В геноме клетки появляются клеточные или вирусные онкогены – измененные гены, вызывающие рост и размножение дефектных клеток. В организме человека постоянно образуются дефектные клетки, но в норме процесс малигнизации прерывается на этапе инициации, поскольку такие клетки подвергаются апоптозу – регулируемому процессу клеточной гибели. При одновременном выключении генов, вызывающих апоптоз, и активации генов, препятствующих апоптозу, дефектные клетки не погибают, а продолжают развиваться.
При повторном воздействии на клетки того же или другого вредного фактора наступает вторая стадия малигнизации – промоция. Онкогены активизируются, стимулируя пролиферацию дефектных клеток. Однако, даже этого недостаточно для развития злокачественной опухоли. Рост новообразования становится возможным только после прохождения третьей стадии малигнизации – уклонения дефектных клеток от процесса дифференцировки. Уклонение обычно происходит под влиянием определенных микроРНК.
Кроме того, переход на третью стадию малигнизации может быть обусловлен недостатком цитокининов, способствующих переходу клетки на более высокий уровень дифференцировки. Со временем количество низкодифференцированных клеток увеличивается, возникает микроскопический участок измененной ткани. Клетки с преобладающим набором хромосом формируют так называемую стволовую линию – основу опухоли. Одной из особенностей малигнизации является генетическая нестабильность клеток, из-за которой клеточный состав новообразования постоянно меняется, вместо одной стволовой линии появляются другие.
Измененные клетки, утратившие способность реагировать на внешние воздействия (влияние микросреды, иммунный надзор), продолжают активно делиться. Наступает четвертая стадия развития злокачественного новообразования – опухолевая прогрессия. Ткань, изменившаяся в процессе малигнизации, прорастает соседние органы, разрушает стенки кровеносных и лимфатических сосудов. Клетки новообразования попадают в кровь и лимфу, а затем разносятся по организму, «оседая» в лимфатических узлах и отдаленных органах. Из «осевших» клеток формируются новые очаги опухолевого роста – вторичные новообразования (метастазы).
С точки зрения свойств ткани можно выделить следующие этапы малигнизации: гиперплазия ткани, появление участков очаговой пролиферации, возникновение доброкачественной опухоли, образование участков дисплазии, рак in situ (злокачественная опухоль, не прорастающая окружающие ткани), инвазивное злокачественное новообразование. В ряде случаев этап доброкачественной опухоли может отсутствовать. Этапы очаговой пролиферации, доброкачественной опухоли и дисплазии рассматриваются, как предраковые состояния.
Свойства опухоли после малигнизации
Злокачественные новообразования обладают рядом свойств, отсутствующих у любых нормальных клеток и тканей организма:
Не пропустить рак. 10 вопросов о кистах и опухолях яичников
Рак яичников находится на 8 месте в мире в структуре всех онкологических заболеваний женщин. Ежегодно регистрируется около 295 000 новых случаев! К сожалению, часто проблема обнаруживается на поздних стадиях, что значительно снижает эффективность лечения и ухудшает прогнозы. На вопросы об опухолях и опухолевидных заболеваниях яичников отвечают врачи-специалисты медицинского центра «Аква-Минск Клиника».