Что такое изолированный мочевой синдром
Клинико-морфологическая характеристика и оценка эффективности лечения хронических гломерулонефритов, дебютировавших изолированным мочевым синдромом
Ульяновский государственный университет
Ульяновская областная клиническая больница
Введение. Литературные данные свидетельствуют о том, что в настоящее время значительно увеличилось число больных, у которых заболевания почек протекают клинически стерто и проявляются только изменениями в моче. Это приводит к поздней обращаемости больных к врачу и к поздней диагностике заболеваний почек [10].
Изолированный мочевой синдром (ИМС) выявляется при диспансеризации или случайном осмотре по поводу какого-либо другого заболевания или направлении на санаторно-курортное лечение. Под ИМС могут скрываться случаи детского и подросткового нефрита [12]. Гломерулонефрит (ГН) – группа заболеваний, характеризующаяся воспалительными изменениями преимущественно в клубочках почек [13], которая сочетается с поражением тубулоинтерстициального аппарата, определяющего скорость прогрессирования заболевания [1,15]. Особое место среди актуальных вопросов нефрологии принадлежит проблеме изучения факторов прогрессирования хронических заболеваний почек [7].
Не исключается, что конституциональные факторы могут влиять на возможность развития заболевания, особенности лечения и прогноз при хроническом гломерулонефрите [9]. Очень часто трудно найти причину развития гломерулопатии [6].
В настоящее время классификация ГН базируется на особенностях морфологической картины нефробиоптата после проведения световой, электронной, иммунофлюоресцентной микроскопий, что позволяет определить характер распределения в почечной ткани иммуноглобулинов и компонентов системы комплемента [1]. Морфологическая диагностика, основанная лишь на результатах светооптического исследования, недостаточно информативна, так как морфологические светооптические феномены так же неспецифичны, как и клинические, особенно в дебюте заболевания [2].
Установлено, что один и тот же гистологический вариант ГН может иметь различную этиологию, патогенез, клиническую симптоматику [11].
В свете современных данных, полученных при морфологическом исследовании почечной ткани, выделяют 2 группы ГН. Первую группу составляют пролиферативные ГН: мезангиопролиферативный (МезПГН), диффузный пролиферативный, экстракапиллярный ГН. Для этих вариантов ГН в первую очередь характерен нефритический синдром («богатый» мочевой осадок, эритроциты, эритроцитарные цилиндры, лейкоциты), протеинурия обычно не более 3 г/сутки, почечная недостаточность. Морфологическими вариантами пролиферирующих ГН, являются: острый диффузный пролиферативный ГН, экстракапиллярный (ГН с полулуниями), МезПГН, мезангиокапиллярный ( МезКГН) ГН.
В группу непролиферирующих ГН относятся варианты заболевания, при которых поражаются преимущественно слои клубочкового фильтра (базальная мембрана, подоциты). В эту группу входят следующие гистологические варианты ГН: мембранозная нефропатия, болезнь минимальных изменений, фокальный сегментарный гломерулосклероз (ФСГС).
Эти варианты ГН проявляются преимущественно нефротическим синдромом (протеинурия больше 3,5 г/сутки, гипоальбуминемия, гиперлипидемия, «богатый» мочевой осадок, отеки).
Поскольку гистологическое исследование нефробиоптата доступно только специализированным лечебным учреждениям, в клинической практике бытует классификация, основанная на ведущих клинических синдромах, к числу которых относится ИМС, характеризующийся отсутствием клинической симптоматики, скудной протеинурией, микрогематурией, цилиндрурией.
По мнению ряда нефрологов [8], подобные случаи проявления ГН следует расценивать как латентное течение заболевания, большая часть которого приходится на вторичный, скрытый период болезни, а при нефробиопсии при ИМС выявляются изменения аналогичные тем, которые обнаруживаются в развернутой стадии болезни. Следует признать, что ИМС может быть не только проявлением ГН, но и дебютом других заболеваний почек (амилоидоз, опухоли, вторичные нефропатии и т.д.).
Поэтому выявление ИМС случайно или при целенаправленном обследовании больного требует проведения нефробиопсии с последующим морфологическим исследованием биоптата почечной ткани в специализированном лечебно-профилактическом учреждении.
Цель исследования. В условиях проспективного наблюдения за больными с впервые выявленным ИМС, установить нозологический диагноз нефропатий и оценить эффективность патогенетического лечения.
Материалы и методы. Под наблюдением в течение достаточно длительного времени (от 1 года до 15 лет) находилось 108 больных, которые поступали на клиническое обследование и лечение в нефрологическое отделение Ульяновской областной клинической больницы (ГУЗ УОКБ) с первоначальным диагнозом ИМС.
Из этого числа больных в окончательную разработку было включено 55 больных, которым для постановки диагноза потребовалось использование современных методов исследования, включая электронную микроскопию, гистохимические исследования нефробиоптата. 53 больным, поступавшим на клиническое обследование и лечение, нефробиопсию провести по разным причинам не удалось. Однако на основании комплексного обследования и пролонгированного диспансерного наблюдения у нефролога диагноз заболевания почек был установлен, и больным проводится соответствующее лечение. Из 55 больных с установленным морфологическим диагнозом женщин было 24 (43,6%), мужчин 31 (56,4%), средний возраст больных 42,2±16,2 лет. Продолжительность заболевания с момента выявления ИМС в среднем составила 6,3±4,2 года. Предшествующим заболеванием у 46 (83,6%) больных была острая респираторная инфекция (ОРВИ), по поводу которой они обращались к врачу. У оставшейся части больных (16,4%) ИМС был выявлен случайно при обследовании по какому-либо другому заболеванию, либо при заполнении санаторно-курортной карты. При ГН случайное выявление ИМС встречалось в 74,8% случаев.
В 20% случаев наследственность была отягощена артериальной гипертензией, а в 7,3% заболеваниями почек. В подавляющем большинстве случаев больные жалоб нефрологического характера не предъявляли. Объективный осмотр также не позволял заподозрить какое-либо заболевание почек.
Латентное течение ГН, проявляющегося ИМС, по результатам наблюдений Е.М. Тареева, может длиться 25-31 год [8].
Диагноз основного заболевания, дебютирующего ИМС, ставился на основании комплексного обследования больных, включая оценку и интерпретацию общего анализа крови, мочи, проб Зимницкого, Нечипоренко, Реберга-Тареева, определения суточной протеинурии, скорости клубочковой фильтрации по CKD- EPI, 2011, биохимических констант крови.
Из инструментальных методов исследования использовались: УЗИ органов брюшной полости и почек с акцентом внимания на состояние почек, УЗДГ сосудов почек, обзорная рентгенография органов грудной клетки (облигатно) и брюшной полости (факультативно), компьютерная томография органов брюшной полости (по необходимости), радионуклидная ренография с I 131. 55 больным с ИМС была проведена прицельная чрезкожная нефробиопсия.
Морфологическое исследование нефробиоптата проводилось в лаборатории электронной микроскопии и иммуногистохимии Первого Московского государственного университета им. И. М. Сеченова, патологоанатомическом отделении Городской клинической больницы №52 г. Москвы и патологоанатомическом отделении ГУЗ УОКБ. Всем больным была проведена световая микроскопия, а также иммуногистохимическое исследование и электронная микроскопия нефробиоптата на аппарате Tecnai-12. Увеличение определялось индивидуальными характеристиками нефробиоптата (от 2550 до 87000 раз).
Больные, находившиеся в нефрологическом отделении ГУЗ УОКБ, получали комплексную терапию: глюкокортикостероиды ( преднизолон 0,5-1,0 мг/кг массы тела перорально, пульс-терапия солумедролом, метилпреднизолоном из расчета 15-20 мг/кг массы тела в/в на протяжении 3 дней подряд), цитостатики ( пульс-терапия циклофосфамидом 15-20 мг/кг массы тела ежемесячно, либо 10-15 мг/кг массы тела дважды в месяц до 12-18 месяцев под контролем гемограммы), циклоспорин А перорально (3-5 мг/кг массы тела) ежедневно в два приема на протяжении длительного времени под контролем концентрации в крови, микоменолата мофетил до 1000 мг два раза в день длительно под контролем нейтрофилов крови, нефропротекторы (ингибиторы АПФ, статины, антиагреганты) и др. К важным условия успеха терапии ХГН относятся: уточнение этиологии и нозологической формы нефрита, оценка его активности, а также выбор надежных критериев контроля эффективности лечения [14].
Статистическая обработка материала проводилась с помощью лицензированного пакета программ Statistica 6.0. Данные представлены в виде М ± m, где М – среднее значение показателя, m – ошибка средней, р- уровень статистической значимости. Критический уровень значимости принимался равным 0,05.
Мочевой синдром у исследованных больных характеризовался протеинурией 0,6±0,3 г/л, гематурией 9,0±4,2 в поле зрения, лейкоцитурией 2,7±1,1 в поле зрения, цилиндрурией (зернистые) 1,3±0,8 в поле зрения.
Проводилось биохимическое исследование крови: общий белок составил 61,2±1,2 г/л, альбумин 32,8±3,2 г/л, креатинин 89,7±9,6 мкмоль/л, мочевина 7,1±1,1 ммоль/л, мочевая кислота 409,9±20,5 ммоль/л, общий билирубин 7,8±3,3 мкмоль/л, АЛТ 26,4±15,6 U/l, АСТ 26,0±13,0 U/l, холестерин 8,7±2,8 ммоль/л, кальций 2,1±0,1 ммоль/л, калий 4,7±0,4 ммоль/л, фосфор 1,4±0,2 ммоль/л, натрий 140,3±4,2 ммоль/л, фибриноген 6350,7±1202,7 г/л, протромбиновый индекс 90,1±7,0%. Проведенные иммунологические пробы сыворотки крови не выявили отклонений от нормы: Ig G 7,9±3,1 г/л, Ig A 2,3±0,8 г/л, Ig M 1,2±0,4г/л, ЦИК 24,9±10,2 Ед, СРБ 2,8±2,0 г/л, антитела к гломерулярной базальной мембране 10,0±4,0 Ед/мл, ANCA 0,33±0,1 Ед, антитела к ДНК 14,4±9,4 МЕ/мл, комплемент 58,7±11,6 Ед, С3 1,4±0,37 г/л, С4 0,2±0,08 г/л. Функциональные почечные пробы представлены в табл. 1.
Таблица 1. Результаты исследования функциональных почечных проб
Результаты. Исследования показали, что у 53 (96,4%) больных ИМС был проявлением ГН и только у 2 (3,6%) диагностировались вторичные нефропатии.
Среди обследованных больных с ХГН мезангиопролиферативный вариант отмечался (МезПГН) у 21 (38,2%) больного, мезангиокапиллярный (МезкГн) у 13 (23,6%), ГН с минимальными изменениями у 8 (14,5%), мембранозная нефропатия у 5 (9,0%), ФСГС у 2 (3,6%), амилоидоз почек, нефросклероз, ANCA—ассоциированная нефропатия, экстракапиллярный гломерулонефрит, IgA-нефропатия, острый гломерулонефрит по 1 (1,8%) случаю.
В структуре поражений почек ведущее положение занимает МезПГН, который встречался у 21 (38,2%) больных.
Мезангиопролиферативный гломерулонефрит является самой распространенной формой ХГН [21] и наиболее благоприятным вариантом заболевания [19]. Частота выявления МезПГН составляет до 67-68% [8]. По данным Б.И. Шулутко с соавторами, 10-ти летняя почечная выживаемость при МезПГН составляет 64% [17], по данным других авторов до 90% [15]. Этот вариант ГН с самого начала проявлялся ИМС, чаще всего у мужчин в 14 (66,6%) случаях в возрасте от 20 до 55 лет.
Клинически МезПГН у наблюдаемых больных проявлялся в дальнейшем нефротическим, гипертоническим, гематурическим синдромами, что совпадает с результатами исследований других авторов [2].
Обращает внимание на себя вот этот факт, что у мужчин трансформация ИМС в нефротический вариант произошла в среднем через 19 лет после его выявления, тогда как у женщин для этого понадобилось только 3 года.
В настоящее время, по данным светооптических, иммунногистохимических, электронномикроскопических и морфометрических исследований, различают 3 морфологических варианта МезПГН в зависимости от класса иммуноглобулинов в сочетании с С3 фракцией комплемента, преобладающих в клубочковых депозитах [3]. У исследованных нами пациентов наиболее часто в клубочковых депозитах одновременно выявлялись все три класса иммуноглобулинов в сочетании с С3 фракцией комплемента или без него.
Находясь в стационаре, больные с МезПГН с трансформацией ИМС в нефротический синдром (НС) получали лечение глюкокортикостероидами (преднизолон), цитостатиками (циклофосфан, циклоспорин А, микофенолата мофетил) по принятым в современной нефрологии дозировкам [16,18]. Наряду с этим им проводилось нефропротективное и симптоматическое лечение.
После проведенного комплексного лечения у исследованных больных с МезПрГн существенно уменьшилась протеинурия с 6,8±4,2 до 0,9±0,4 г/сутки (р˂0,001), СКФ по CKD-EPI, 2011 г. возросла (статистически недостоверно, р>0,05 ) с 64,3±28,6 до 68,8±32,1 мл/мин, значимо повысились уровни альбумина и общего белка крови соответственно с 25,0±6,3 до 35,3±4,2 г/л (р˂0,05), с 55,6±7,53 до 70,7±3,7 (р˂0,001).
Вторым по частоте встречаемости среди наблюдаемых больных был мезангиокапиллярный гломерунефрит. В последнее время этот вариант гломерулонефрита встречается по данным литературы в 5-6% случаев [13].
Данная патология была отмечена у мужчин в 8 (61,5%) случаях, у женщин в 5 (38,5%) случаях. Возраст преимущественно до 60 лет. У всех больных МезКГН дебютировал ИМС без каких бы то ни было клинических проявлений.
В анамнезе больных не удалось выявить каких-либо факторов риска развития заболевания. Поэтому с достаточным основанием этот вариант ГН расценивался как идиопатическая форма.
По классификации Е.М. Тареева [8], выделяется несколько морфологических вариантов МезКГН, которые могут протекать клинически по нефротическому, гипертоническому или смешанному вариантам.
По данным некоторых авторов [20], МезКГН – одна из неблагоприятных форм заболевания, и через какое-то время при отсутствии лечения развивается почечная недостаточность.
За время наблюдения МезКГН трансформировался в нефротический синдром у 12 из 13 больных, преимущественно у мужчин.
Результаты комплексного лечения, включавшие глюкокортикостероиды, цитостатики, нефропротекторы и симптоматические средства показали, что из 12 больных полная клинико-лабораторная ремиссия отмечалась у 3 больных, неполная клинико-лабораторная ремиссия у 4, которые продолжают получать лечение. У 5 больных, не смотря на проводимую терапию, ремиссии достичь не удалось.
После проведенного комплексного лечения у исследованных больных с МезКГН суточная протеинурия статистически достоверно уменьшилась протеинурия с 2,8±1,4 до 0,8±0,2 г/сутки (р˂ 0,001), СКФ по CKD-EPI, 2011 г. возросла (статистически достоверно, р˂0,05 ) с 64,2±11,3 до 80,5±13,7 мл/мин, значимо повысились уровни альбумина и общего белка крови с 23,3±2,8 до 38,0±2,3 г/л (р˂0,001), с 39,2±0,2 до 65,6±3,8 (р˂0,001) соответственно.
Гломерулонефрит с минимальными изменениями диагностировался у 5 мужчин и у 3 женщин. Во всех случаях ИМС трансформировался в НС после перенесенного ОРВИ.
На фоне проводимой терапии полная клинико-лабораторная ремиссия достигнута у 7 больных, неполная клинико-лабораторная ремиссия у 1. Суточная протеинурия статистически достоверно уменьшилась протеинурия с 4,7±3,1 до 0,4±0,2 г/сутки (р˂ 0,001), СКФ по CKD-EPI, 2011 г. возросла (статистически достоверно, р˂0,05 ) с 62,0±4,1 до 96,0±22,1 мл/мин, значимо повысились уровни альбумина и общего белка крови с 21,3±5,6 до 33,8±4,3 г/л (р˂0,001), с 43,7±7,6 до 66,9±3,8 (р˂0,05) соответственно.
Мембранозный вариант гломерулонефрита диагностирован у 5 больных. У мужчин в 2 случаях, у женщин в 3. Возраст больных до 50 лет. У всех больных ИМС трансформировался в НС после перенесенного ОРВИ или ангины.
На фоне проводимой терапии у всех была достигнута неполная клинико-лабораторная ремиссии. 4 больных продолжают получать лечение. У одного больного отмечалось снижение азотвыделительной функции почек, соответствующее III b стадии хронической болезни почек.
Как отмечалось выше, отдельные варианты ХГН (ФСГС (по данным большинства авторов не более 10% от всех первичных гломерулопатий [4], IgA-нефропатия, экстракапиллярный гломерулонефрит) встречались сравнительно редко, поэтому более детальный анализ клинического течения и лечения будет представлен в дальнейших публикациях.
У части наблюдаемых больных по разным причинам (чаще всего отказа больных), нефробиопсию провести не удалось, и поставить морфологический диагноз заболевания почек было невозможно.
Тем не менее с учетом результатов комплексного обследования и пролонгированного наблюдения за больными в условиях нефрологического стационара из 53 больных диагноз хронического гломерулонефрита с гипертоническим синдромом был поставлен 19 (35,8%), тубулоинтерстициальный нефрит 6 (11,3%) латентное течение хронического гломерулонефрита с ИМС 14 (26,4%), нефритический синдром 4 (7,5%), хронический гломерулонефрит с нефротическим синдромом – 10 (18,9%).
Всем больным проводилось комплексное лечение, включавшее в себя нефропротективные, симптоматические лекарственные средства, а при наличии показаний цитостатические препараты. Результаты лечения таковы. Полная клинико-лабораторная ремиссия была достигнута у 4 (7,5%) больных, неполная – у 4 (7,5%), развитие терминальной почечной недостаточности наступило у 8 (15%) больных. Тенденция к снижению клубочковой фильтрации наблюдалась у 7 (13,2%) больных, у остальных пациентов азотовыделительная функция почек осталась без изменений.
Таким образом, результаты проведенных исследований свидетельствуют о том, что ИМС могут проявляться самые разнообразные заболевания почек первичного или синдромального генеза. Однако наиболее часто ИМС встречается у больных гломерулонефритами и, в частности, при мезангиопролиферативном и мезангиокапиллярном вариантах заболевания.
Углубленное морфологическое исследование нефробиоптата показывает на то, что ИМС отражает латентное течение заболевание почек, а не его клинический дебют. В том отношении результаты наших исследований совпадают с выводами других авторов.
ИМС, по нашим наблюдениям, может длительное время быть единственным проявлением ГН. Максимальный срок латентного течения заболевания среди исследованных больных составляет около 15 лет и в конце концов манифестируется нефротическим синдромом и терминальной почечной недостаточностью.
Выводы
2. Среди исследованных больных с ХГН, дебютировавшими ИМС, наиболее часто диагностировались мезангиопролиферативный и мезангиокапиллярный варианты заболевания.
3. Комплексное лечение больных с мезангиопролиферативным и мезангиокапиллярным вариантами гломерулонефритов, включавшее в себя глюкокортикостероиды, цитостатики, нефропротективные и симптоматические средства, сопровождалось у 22 больных положительной клинико-лабораторной динамикой показателей течения заболеваний.
Список использованных источников:
2. Соотношение между клиническими и морфологическими формами первичных гломерулопатий/ В.М. Беспалова, Т.Н. Цвирко// Нефрология и диализ. – 2005. – Т.7, №2. – С.181-185.
3. Об уточнении клинико-морфологической классификации хронического гломерулонефрита/ В.А. Варшавский, Е.П. Проскурнева, А.Б. Гасанов, Л. О. Севергина, Л.А. Шестакова// Нефрология и диализ. – 1999. – Т.1, № 2-3. – С.99-102.
5. Частота, динамика и клинические проявления морфологических форм первичной гломерулопатии/ Б.Р. Джаналиев, В.А. Варшавский// Нефрология и диализ. – 2001. – Т.3, №1. – С. 75-78.
8. Клиническая нефрология. Т.2/ под ред. Е.М. Тареева. – М.: Медицина, 1983. – 416 с.
9. Куликова Е.В., Кухтевич А.В., Зиновьев В.Г. Конституциональная характеристика и течение хронического гломерулонефрита// Нефрология и диализ. – 2003. – Т5, № 2. – С 148-152.
11. Диагностика и лечение болезней почек/ Н.Я. Мухин, И.Е. Тареева, Е.М. Шилов. – М.: ГЭОТАР-МЕД, 2002. – 384 с.
12. Нефрология: Руководство для врачей/ под редакцией И.Е. Тареевой. – М.: Медицина, 2000. – 688 с.
13. Нефрология: учебное пособие для послевузовского образования/ под ред. Е.М. Шилова. – М.: ГЭОТАР-Медиа, 2007. – 688 с.
15. Прогностические факторы ускоренного прогрессирования хронического гломерулонефрита и хронических невоспалительных гломерулопатий/ М.Я. Ратнер, В.В. Серов, В.А. Варшавский, Н.Д. Федорова// Терапевтический архив. – 1998. – Т.70, №6. – С. 7-11.
16. Рациональная фармакотерапия в нефрологии: Руководство для практикующих врачей/ под ред. Н.А. Мухина, Л.В. Козловской, Е.М. Шилова. – М.: Литтерра, 2006. – 896 с.
17. Гломерулонефриты/ Б.И. Шулутко, С.В. Макаренко, В.Р. Шумилкин. – СПб., 2001. – 214 с.
Журнал «Здоровье ребенка» 1 (36) 2012
Вернуться к номеру
Изолированный мочевой синдром у детей и тактика врача в условиях поликлиники
Авторы: Кафедра педиатрии факультета интернатуры и последипломного образования совместно с профессором кафедры педиатрии № 1 Т.П. Борисовой Донецкого национального медицинского университета им. М. Горького и зав. отделом детской нефрологии ГУ «Институт нефрологии НАМН Украины» (г. Киев) профессором И.В. Багдасаровой.
Версия для печати
Актуальность проблемы. Анализ мочи является одним из самых распространенных клинических методов исследования. Изменения в анализе мочи являются наиболее постоянными, а на определенном этапе — и единственными проявлениями поражения мочевой системы, кроме этого, они встречаются и при многих других соматических заболеваниях. Поэтому умение правильно трактовать отклонения в анализе мочи и объяснить их причину является актуальным для врача-педиатра.
Общая цель: уметь диагностировать мочевой синдром, определить диагностическую тактику ведения больного, поставить наиболее вероятный клинический диагноз.
Конкретные цели: выделить основные признаки мочевого синдрома, составить план обследования больного с мочевым синдромом, провести дифференциальную диагностику мочевого синдрома для уточнения этиологического фактора и поставить наиболее вероятный клинический диагноз.
Содержание обучения
Теоретические вопросы
1. Методика сбора мочи, показатели общего анализа мочи в норме, определение понятия «изолированный мочевой синдром».
2. Гематурия, критерии диагностики, причины развития, дифференциальная диагностика.
3. Протеинурия, критерии диагностики, причины и механизмы развития.
4. Лейкоцитурия, критерии диагностики, причины развития.
5. План обследования ребенка с изолированным мочевым синдромом.
Ориентировочная основа деятельности
Во время подготовки к занятию необходимо ознакомиться с основными теоретическими вопросами с помощью источников литературы.
Правила сбора мочи. Общему анализу подвергают среднюю порцию утренней мочи, выделенной при свободном мочеиспускании, при тщательном соблюдении гигиенических условий. С целью предотвращения размножения бактериальной флоры и разрушения форменных элементов мочи, неизбежных при ее хранении, микроскопию мочевого осадка проводят не позднее 1–2 часов после сбора мочи. Если свежевыпущенную мочу нельзя быстро исследовать, ее следует держать в холодиль- нике.
Проба по Нечипоренко — определение количества эритроцитов и лейкоцитов в 1 мл мочи из средней порции, проба по Аддису — Каковскому — количественные исследования мочевого осадка всей мочи, выделенной за 12 часов (далее полученный показатель удваивают), суточная протеинурия — определение белка в моче, выделенной за сутки.
Мочевой синдром — это патологические изменения в анализе мочи в виде гематурии, протеинурии, лейкоцитурии, цилиндрурии.
Гематурия
До настоящего времени в литературе существуют значительные расхождения и противоречия в отношении диагностики патологически значимого уровня гематурии. Одним из объяснений этому может быть использование разных методов для сбора, хранения анализов мочи. Большинство авторов понимают под гематурией присутствие в моче патологического числа эритроцитов (более 3–5 в поле зрения), определяемого при исследовании осадка центрифугированной порции мочи, в трех последовательно проведенных исследованиях с промежутком в 1 неделю.
Количественная характеристика гематурии — наличие в 1 мл мочи более 2 ґ 103/мл эритроцитов в пробе по Нечипоренко или более 2 ґ 106/сут в пробе по Аддису — Каковскому.
С клинико-лабораторной точки зрения выделяют 4 типа гематурии: макрогематурию, изолированную микрогематурию, микрогематурию с протеинурией, микрогематурию с клиническими симптомами (дизурия, геморрагический синдром, лихорадка, болевой синдром и др.).
Макрогематурия определяется невооруженным глазом. Моча при этом имеет ярко-красную, бурую, ржавую окраску или цвет мясных помоев.
В зависимости от окрашивания порций мочи и наличия эритроцитов в трехстаканной пробе гематурию разделяют:
— на инициальную (появление крови в первой порции мочи, в начале мочеиспускания, свидетельствует о поражении уретры);
— терминальную (окрашенной является последняя порция мочи, при изгнании которой за счет сокращения мускулатуры мочевого пузыря травмируется измененная слизистая оболочка и вызывается кровотечение, характерна для заболеваний шейки мочевого пузыря, предстательной железы);
— тотальную (равномерное распределение эритроцитов во время всего акта мочеиспускания, свидетельствует о почечном происхождении гематурии).
Истинную гематурию следует отличать от ложной, при которой окрашивание мочи происходит вследствие примеси гемоглобина, появляющейся при гемолизе эритроцитов. Ложная гематурия также связана с употреблением в пищу свеклы, красной смородины, продуктов питания, содержащих красители, медикаментов (нитрофурантоин, рифампицин).
Микрогематурия обнаруживается при микроскопическом исследовании мочи. Микрогематурия подразделяется на незначительную (до 10–15 эритроцитов в поле зрения), умеренную (20–40 эритроцитов в поле зрения), значительную (40–100 эритроцитов в поле зрения).
Причины гематурии целесообразно разделить на почечные, заболевания мочевыводящего тракта, патологию почечных сосудов, системные нарушения коагуляции, прочие (табл. 1).
Спектр заболеваний, проявляющихся гематурией, различен в зависимости от возраста ребенка (табл. 2).
При проведении дифференциальной диагностики гематурии необходимо обратить внимание на ряд клинических особенностей заболеваний, при которых она наблюдается.
Наиболее частой причиной ренальной гематурии является гломерулонефрит (ГН). Появление одновременно с гематурией артериальной гипертензии и отеков характерно для острого ГН. Данное заболевание может протекать также с изолированной гематурией. Признаком, позволившим поставить диагноз острого ГН в данном случае, будет указание в анамнезе на перенесенную 1–2 недели назад острую инфекцию (чаще стрептококковую — острый тонзиллит, стрептодермия, скарлатина и др.). Диагностика хронического ГН, протекающего с гематурией, базируется на персистировании эритроцитурии в течение более 1 года при исключении других ее причин. В случае появления на фоне фарингита, острой респираторной вирусной инфекции эпизодов макрогематурии, сопровождающихся болями в пояснице, диагноз хронического гломерулонефрита сомнения не вызывает, поскольку данные проявления характерны для IgA-нефропатии. Подтвердить этот диагноз возможно прижизненным морфологическим исследованием почек, позволяющим выявить депозицию IgA в мезангиуме.
Поражение почек (вторичный ГН) при системных болезнях соединительной ткани и системных васкулитах (системная красная волчанка, узелковый полиартериит, геморрагический васкулит) проявляется изолированной гематурией либо гематурией в сочетании с протеинурией, лейкоцитурией. Постановка диагноза затруднена, если развитие почечного синдрома предшествует появлению других симптомов, типичных для каждой болезни. При системной красной волчанке наблюдаются лихорадка, похудание, кожный («бабочка», дискоидные высыпания, фотосенсибилизация), суставной синдромы, гематологические (гемолитическая анемия, лейкопения, тромбоцитопения), иммунологические нарушения (положительный LE-клеточный тест, повышение титра антител к нативной ДНК, антинуклеарных антител). При узелковом полиартериите гематурия сочетается с кожным (сетчатое ливедо, локальные отеки, некрозы), абдоминальным синдромами, поражением нервной системы, развитием злокачественной артериальной гипертензии. Для геморрагического васкулита характерна симметричная папулезно-геморрагическая сыпь на коже голеней, стоп, ягодиц, разгибательной поверхности локтевых суставов, у части больных отмечаются абдоминальный и суставной синдромы.
Наследственный нефрит и болезнь тонких базальных мембран — наиболее распространенные неиммунные генетически детерминированные гломерулопатии, сопровождающиеся на протяжении всей жизни пациента гематурией. При наследственном нефрите (синдроме Альпорта) гематурия и/или протеинурия нередко сочетаются с нейросенсорной тугоухостью и патологией зрения, наблюдается склонность к прогрессированию заболевания и развитию хронической почечной недостаточности (ХПН). Чаще выявляется у мальчиков. В редких случаях тугоухость и поражение глаз предшествуют гематурии, что вызывает затруднения в правильной постановке диагноза. Болезнь тонких базальных мембран в большинстве случаев не имеет тенденции к прогрессированию, поэтому называется семейной доброкачественной гематурией. Для уточнения диагноза генетически детерминированных гломерулопатий целесообразно изучение семейного анамнеза, исследование анализов мочи членов семьи, динамическое нефрологическое обследование пациента для решения вопроса о проведении прижизненного морфологического исследования почек.
Гематурия может наблюдаться при гемолитико-уремическом синдроме. Наличие эпизода диареи с примесью крови и таких проявлений, как гемолитическая анемия, тромбоцитопения, острая почечная недостаточность, помогает установлению диагноза.
Наиболее частая причина почечной экстрагломерулярной гематурии — тубулоинтерстициальный нефрит, который возникает вследствие воздействия многообразных причин: инфекции, интоксикации лекарственными средствами и др. При этом в анализах мочи определяются гематурия, небольшая лейкоцитурия, возможна протеинурия при снижении относительной плотности мочи.
Гематурия является одним из важных признаков мочевого синдрома при дисметаболической нефропатии. У этих пациентов часто отмечается лейкоцитурия, носящая абактериальный характер, обязательно наличие в моче кристаллов тех или иных солей в виде крупных и/или мелких агрегированных частиц, гиперстенурии (до 1030 и выше), в жаркий летний период — олигурии. Для подтверждения диагноза «дисметаболическая нефропатия» при выявлении кристаллов солей в общем анализе мочи проводится биохимическое исследование мочи.
Гематурия при пиелонефрите не является постоянным симптомом заболевания в отличие от лейкоцитурии и бактериурии. Считается, что появление макрогематурии при пиелонефрите связано с поражением венозных сплетений форникальных отделов почек. Диагностика форникального кровотечения основана на выявлении форникального рефлюкса при урографии.
Поликистоз почек клинически проявляется увеличением почек, их бугристой поверхностью. При аутосомно-рецессивном типе заболевания кроме поражения почек с исходом в ХПН происходят пролиферация и расширение желчных протоков с развитием перипортального фиброза, портальной гипертензии. Аутосомно-доминантный поликистоз почек проявляется гематурией и протеинурией, рецидивирующей инфекцией мочевой системы, болями в поясничной области, артериальной гипертензией. В диагностике помогают характерные данные ультразвукового исследования почек.
Травма почки сопровождается гематурией при разрыве почечной паренхимы и надрыве почечной лоханки. Основными симптомами являются боль, припухлость и отечность в поясничной области, появление перитонеальных симптомов, олигурии.
Нефробластома определяется при пальпации в виде гладкого образования в брюшной полости и сопровождается болью в животе, микро- или макрогематурией, анемией, артериальной гипертензией. С целью уточнения диагноза показано проведение компьютерной томографии почек.
Поражение мочевой системы при туберкулезе обычно вторично, первичный очаг локализуется в легких. Туберкулез мочевой системы проявляется после многих лет скрытого течения. Первыми и постоянными признаками являются микрогематурия (в 80–90 % случаев), лейкоцитурия и минимальная протеинурия. Диагностика туберкулеза мочевой системы основана на исследованиях мочи и мокроты на бактерии Коха, данных рентгенологического исследования, туберкулиновых проб.
Для ряда урологических заболеваний характерна гематурия. В этих случаях в моче обнаруживаются негломерулярные эритроциты, а при ультразвуковом, рентгенологическом исследованиях почек выявляется урологическая патология. Нефролитиаз клинически проявляется приступами болевого синдрома (почечная колика), дизурическими явлениями, наличием в анализах мочи большого количества негломерулярных эритроцитов, лейкоцитов, кристаллов солей. Нефроптоз имеет бессимптомное течение, однако чаще наблюдаются боли в поясничной области, особенно при движении и прыжках. Боли сопровождаются микро- или макрогематурией в связи со сдавлением почечных сосудов и перегибами мочеточника, венозным застоем. Основной метод диагностики нефроптоза — экскреторная урография в вертикальном положении больного.
При патологии мочевыводящего тракта одновременно с гематурией, как правило, имеются лейкоцитурия и дизурические проявления, что требует проведения исследований рентгенурологической направленности. Для установления диагноза постренальной гематурии очень важны результаты цистоскопии. Цистоскопия, проведенная во время кровотечения, позволяет точно установить его источник или по меньшей мере определить, из какого мочеточника поступает кровь. Трудности иногда возникают при установлении источника кровотечения у девочек (мочевые пути или половые органы). Если при обычном осмотре определить его не удается, то прибегают к катетеризации мочевого пузыря.
Травмы мочевыводящих органов — ушибы, размозжения, разрывы — сопровождаются развитием болевого шока, нарушением мочеиспускания, образованием мочевых затеков, урогематом, мочевых свищей, гематурией.
Заболевания почечных сосудов как причина гематурии встречаются у детей редко. Наличие артериальной гипертензии требует исключения стеноза почечной артерии. Тромбоз почечной артерии клинически проявляется внезапным выраженным болевым синдромом в поясничной области, гипертензией, протеинурией и гематурией. Тромбоз почечных вен чаще наблюдается у детей первых месяцев жизни при коагулопатии потребления (ДВС-синдроме) как следствии асфиксии, дегидратации, шока, сепсиса. Состояние сопровождается беспокойством в связи с острыми болями в животе, олигурией, гематурией, протеинурией, увеличением размеров почек, лихорадкой.
Коагуло- и тромбопатии, проявляющиеся гематурией, имеют, как правило, и кожную манифестацию в виде геморрагического синдрома петехиально-пятнистого или гематомного типа. Это помогает при проведении дифференциальной диагностики гематурии.
Гематурия может быть функциональной, когда появляется небольшое количество эритроцитов в моче после тяжелой физической нагрузки (например, у спортсменов).
Протеинурия
Протеинурия — это появление в моче белка, количество которого превышает нормальные значения. При определении концентрации белка в моче с использованием 3% раствора сульфосалициловой кислоты допустимым значением является 0,033 г/л. С учетом суточных колебаний выделения белка с мочой (максимальное количество в дневное время), различий в количестве теряемого белка в разных порциях для оценки потери белка с мочой изучается суточная протеинурия. В моче здорового ребенка определяется до 100 мг белка в сутки. По степени выраженности различают минимальную (до 1,0 г/сут), умеренную, не превышающую 3 г/сут, и высокую протеинурию (более 3 г/сут). Минимальная протеинурия характерна для тубулопатий, обструктивной уропатии, тубулоинтерстициального нефрита, нефролитиаза, поликистоза, опухоли почки. Умеренная протеинурия наблюдается при остром пиелонефрите, ГН, амилоидозе. Высокая протеинурия, как правило, сопровождается развитием нефротического синдрома, который характеризуется выраженными отеками, гипопротеинемией (гипоальбуминемией), диспротеинемией, гиперхолестеринемией, гиперлипидемией.
Выделяют интермиттирующую и персистирующую протеинурию.
Интермиттирующая протеинурия может быть функциональной и ортостатической. Развитие функциональной протеинурии связано с лихорадкой, чрезмерной физической нагрузкой, переохлаждением, психоэмоциональным стрессом. Возможно появление преходящей протеинурии после употребления обильной белковой пищи — алиментарной протеинурии; после приступа эпилепсии и сотрясения мозга — центрогенной протеинурии; при сердечной недостаточности, опухолях брюшной полости — застойной протеинурии. Функциональная протеинурия обычно прекращается по мере разрешения индуцировавшего ее фактора.
Ортостатическая протеинурия наблюдается преимущественно у подростков и подразумевает появление белка в моче после пребывания исследуемого в течение нескольких часов в вертикальном положении. У таких лиц в горизонтальном положении суточная протеинурия не превышает 150 мг, но при свободном двигательном режиме достигает 1,0– 1,5 г/сут. Для подтверждения диагноза проводится ортостатическая проба. Утром, не вставая с постели, больной мочится в отдельную чистую посуду (первая порция мочи). Затем в течение 1/2–1 часа он должен ходить с заложенными за голову руками (в таком положении увеличивается лордоз), после чего повторно мочится (вторая порция мочи). В обеих порциях мочи определяют содержание белка. Если в первой порции белок отсутствует, а во второй обнаруживается, то это говорит в пользу ортостатической протеинурии.
Под персистирующей протеинурией подразумевается экскреция с мочой патологического количества белка независимо от физической активности больного, его положения и функционального состояния различных систем организма. По механизму развития она может быть ренальной (гломерулярная, тубулярная, смешанная), преренальной (переполнения) и секреторной.
Гломерулярная протеинурия возникает при нарушении проницаемости гломерулярного барьера для плазменных белков. В зависимости от соотношения в моче белковых фракций различают селективную и неселективную протеинурию. Селективная протеинурия — это проникновение в мочу белков только с низкой молекулярной массой — альбумина и близких ему фракций (например, при нефротическом синдроме — ГН с минимальными изменениями). Неселективная протеинурия характеризуется появлением в моче наряду с альбумином в значительном количестве высокомолекулярных глобулинов (свидетельствует о прогрессировании гломерулопатии, при этом нередко определяются фибропластические изменения в клубочках). Гломерулярная протеинурия характерна для первичных и вторичных ГН, включая ГН с минимальными изменениями, амилоидоза почек, диабетической нефропатии, тромбоза почечных вен.
Тубулярная протеинурия является результатом нарушения процессов реабсорбции белков ультрафильтрата и характеризуется высоким содержанием низкомолекулярных протеинов так называемой преальбуминовой фракции (b2-микроглобулин, лизоцим и др). Изолированная тубулярная протеинурия обычно не превышает 1–2 г/сут и наблюдается при тубулопатиях, пиелонефрите, тубулоинтерстициальном нефрите, токсическом действии солей тяжелых металлов (свинец, ртуть, кадмий, висмут) и лекарственных средств (салицилаты и др.).
Смешанная протеинурия обусловлена вовлечением гломерулярных и тубулярных механизмов, наблюдается при гломерулонефрите, диабетической нефропатии, пиелонефрите и амилоидозе почек.
Преренальная протеинурия (переполнения) развивается вследствие накопления в плазме крови низкомолекулярных парапротеинов, легко фильтрующихся через неповрежденный клубочковый барьер. Перегрузка канальцевого эпителия профильтрованным белком, а также повреждающее действие молекул парапротеинов на клетки эпителия приводят к блокированию реабсорбции. Суточная экскреция белка при этом составляет 0,5–2,0 г и более. Эта разновидность протеинурии наблюдается при лейкозах, злокачественных лимфомах, миеломной болезни, а также при массивных некрозах тканей (миоглобинурия) и внутрисосудистом гемолизе (гемоглобинурия), вызванном переливанием несовместимой крови, воздействием гемолитических ядов, лекарственным и иммунологически опосредованным воздействием.
Секреторная протеинурия обычно не превышает 1–2 г/сут, она обусловлена повышенной секрецией различных белков клетками тубулярного эпителия, а также слизистой оболочки и желез мочеполовых органов, что наблюдается при пиелонефрите, тубулоинтерстициальном нефрите и простатите. Некоторые авторы выделяют постренальную протеинурию, обусловленную патологией мочевыводящих путей и попаданием воспалительного экссудата, богатого белком, в мочу. У детей встречается относительно редко, незначительна по величине, обычно сопровождается лейкоцитурией и бактериурией.
Протеинурия может быть изолированной или сопровождаться изменениями в мочевом осадке. Изолированная протеинурия характерна для ГН с минимальными изменениями в клубочках, нефроптоза, амилоидоза почек (в последнем случае иногда одновременно с микрогематурией). Протеинурия в сочетании с гематурией встречается при первичных и вторичных ГН, диабетической нефропатии. Протеинурия в сочетании с лейкоцитурией нейтрофильного характера возникает при пиелонефрите, обструктивных уропатиях. Протеинурия с гематурией и лейкоцитурией мононуклеарного характера наблюдается при тубулоинтерстициальном нефрите, дисметаболических нефропатиях, туберкулезе почек.
Лейкоцитурия
Признаком лейкоцитурии считается наличие в анализе мочи более 6 лейкоцитов в поле зрения у мальчиков и более 10 лейкоцитов у девочек. При очень большом количестве лейкоцитов (пиурия) при внешнем осмотре мочи определяется ее помутнение и наличие комочков и хлопьев.
Однако при обычных анализах мочи не всегда можно выявить лейкоцитурию, поэтому в сомнительных случаях исследование проводится специальными методами, из которых наибольшее распространение получили пробы по Аддису — Каковскому и Нечипоренко. Наличие в 1 мл мочи более 2 ґ 103/мл лейкоцитов в пробе по Нечипоренко или более 4 ґ 106/сут в пробе по Аддису — Каковскому рассматривается как лейкоцитурия.
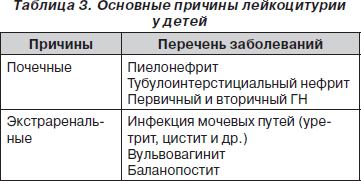
Основные причины лейкоцитурии представлены в табл. 3. Лейкоцитурия может быть истинной и ложной, когда появление лейкоцитов в моче обусловлено примесью к моче выделений из наружных половых органов при вульвовагините, баланопостите, недостаточно тщательном туалете наружных половых органов при сборе мочи для анализа. В этом случае чаще всего в анализе мочи будет указано, что лейкоциты выявляются в скоплениях.
Истинная лейкоцитурия — проявление воспалительного процесса в почках бактериальной либо абактериальной природы. Массивная лейкоцитурия практически всегда является инфекционной, умеренная лейкоцитурия (до 30–50 ґ 103/мл лейкоцитов в пробе по Нечипоренко) может быть и абактериальной.
Для разграничения двух видов почечной лейкоцитурии имеют значение бактериологическое исследование мочи, изучение качественных особенностей лейкоцитов. Так, преобладание в осадке мочи нейтрофилов характерно для бактериального воспаления, лимфоцитов — для ГН, тубулоинтерстициального нефрита. Важным критерием для уточнения генеза лейкоцитурии как проявления инфекции мочевой системы является наличие у пациента таких симптомов, как дизурия (цистит, уретрит), фебрильная лихорадка (пиелонефрит).
Цилиндрурия
Цилиндрурия — это экскреция с мочой цилиндров, которые представляют собой «слепок», образующийся в просвете канальцев из белка или клеточных элементов. Цилиндры имеют исключительно почечный генез, т.е. они образуются только в почечных канальцах и всегда свидетельствуют о поражении почек. Все виды цилиндров хорошо выявляются и длительно сохраняются лишь в кислой моче, тогда как при щелочной реакции мочи они вообще не образуются или быстро разрушаются и в таких случаях отсутствуют либо обнаруживаются в незначительном количестве.
В зависимости от того, какие частицы и в каком количестве покрывают белковый слепок цилиндра, различают гиалиновые, зернистые, восковидные, эритроцитарные и лейкоцитарные цилиндры. Гиалиновые цилиндры обнаруживаются в моче при всех заболеваниях почек, сопровождающихся протеинурией. Единичные гиалиновые цилиндры иногда могут встречаться и в моче здоровых людей, особенно после большой физической нагрузки.
Свернувшийся в просвете проксимальных отделов канальцев белок покрывается остатками (в виде зерен) погибших и распавшихся клеток эпителия, в результате образуются зернистые цилиндры.
Восковидные цилиндры образуются в просвете дистальных отделов канальцев в результате дистрофии и атрофии эпителия последних, поэтому наличие в моче восковидных цилиндров в прогностическом отношении является неблагоприятным симптомом. Эритроцитарные цилиндры могут наблюдаться в моче при выраженной гематурии различного происхождения, лейкоцитарные — при пиурии у больных с пиелонефритом.
Для диагностики мочевого синдрома показано исследование общего анализа мочи. Исследовать мочу в практике педиатра необходимо перед проведением профилактических прививок, в возрасте 1 года, при оформлении в детское дошкольное учреждение, школу, ежегодно у школьников в начале учебного года, у неорганизованных детей 1–2 раза в год, после перенесенных заболеваний (острый тонзиллит, стрептодермия, скарлатина, осложненные острые респираторные заболевания), у спортсменов 1–2 раза в год, у часто болеющих детей, при наличии хронических очагов инфекции, у детей с отягощенным семейным анамнезом по нефропатии. Широкое распространение в последние годы получила экспресс-диагностика мочи при помощи тест-полосок для определения рН, белка, глюкозы, кетонов, эритроцитов, лейкоцитов, нитритов (бактерий) в моче.
При выявлении мочевого синдрома объективное обследование ребенка должно включать пальпацию почек, перкуссию, аускультацию сердца, осмотр наружных гениталий, поясничной и надлобковой области.
При гематурии важным для планирования диагностической тактики является уточнение анамнестических данных, тщательный клинический осмотр ребенка. Уточняется связь гематурии с травмой, приемом лекарственных препаратов, чрезмерной физической нагрузкой, перенесенными накануне заболеваниями. Семейный анамнез должен включать вопросы о наличии у членов семьи гематурии, мочекаменной болезни, глухоты, хронической почечной недостаточности, кровотечений, артериальной гипертензии, поликистоза почек.
При объективном обследовании пациента особое внимание уделяют выявлению таких клинических симптомов, как отеки, артериальная гипертензия, геморрагический синдром, лихорадка, болевой синдром, дизурия и др. При наличии макрогематурии определяется ее продолжительность — в течение всего акта мочеиспускания, в начале или в конце его. Осмотр наружных половых органов может выявить связанные с гематурией признаки инфекции, травмы или инородное тело. У девочек пубертатного возраста поводом для ошибочного заключения о гематурии может стать первая скудная менструация.
Дальнейшая диагностика генеза гематурии основывается на результатах лабораторных и инструментальных методов. Наличие у ребенка макрогематурии, гематурии с протеинурией, гематурии с клиническими симптомами (дизурия, геморрагический синдром, лихорадка, болевой синдром и др.) является показанием для госпитализации в стационар.
Обследованию на уровне первичного звена медицинской помощи подлежат пациенты с изолированной микрогематурией. На первом этапе необходимо исключить менструацию, усиленные физические нагрузки, сексуальную активность, вирусные заболевания, травму. Далее проводится топическая диагностика гематурии — выяснение уровня ее возникновения в органах мочевой системы. Для разграничения гематурии из нижних мочевых путей и почечной гематурии применяют трехстаканную пробу, изучают структуру эритроцитов. Для гломерулярной гематурии характерно наличие более 80 % дисморфных (измененных) эритроцитов в мочевом осадке. Наличие эритроцитарных или гемоглобиновых цилиндров при микроскопии мочевого осадка является маркером гломерулярного источника гематурии.
У всех больных с изолированной гематурией в качестве первого метода визуализации рекомендуется УЗИ почек и мочевого пузыря. Определение уровня креатинина крови необходимо для уточнения функционального состояния почек. Если в семейном анамнезе имеются указания на нефролитиаз или в анализе мочи выявлены кристаллы кальциевых оксалатов, необходимо проведение пробы Сулковича (качественная реакция на гиперкальциурию).
При сочетании гематурии с дизурией, пиурией, бактериурией необходимо провести лечение инфекции мочевой системы. При успешных результатах лечения делают повторный анализ мочи, который должен подтвердить исчезновение гематурии.
Таким образом, прежде чем решать вопрос о необходимости применения инвазивных методов обследования у детей с изолированным мочевым синдромом, проявляющимся в виде гематурии, необходимо провести изложенное выше базисное обследование в амбулаторных условиях. Это позволит, с одной стороны, предотвратить ненужную госпитализацию, а с другой — сократить пребывание детей на специализированной койке, если потребуется более углубленное обследование.
Следует подчеркнуть, что причина изолированной гематурии остается неразгаданной в ряде случаев. В этом случае ребенок наблюдается с диагнозом «гематурия неуточненного генеза». Таким пациентам целесообразно проводить нефрологическое обследование минимум 2 раза в год, даже при отсутствии или исчезновении данного симптома. Это может способствовать уточнению генеза гематурии.
При обнаружении минимальной протеинурии на поликлиническом этапе исключается функциональная протеинурия, показана консультация детского нефролога. При наличии умеренной и высокой протеинурии необходимо углубленное нефрологическое обследование больного в специализированном отделении.
Изолированная незначительная лейкоцитурия в первую очередь нуждается в исключении вульвовагинита, баланопостита, нарушения правил сбора мочи. Сочетание лейкоцитурии с интоксикацией, дизурией не вызывает сомнений в диагностике инфекции мочевой системы. Для выявления дизурических расстройств необходим учет ритма спонтанных мочеиспусканий (время мочеиспускания и количество выделенной мочи). При изолированной стойкой лейкоцитурии показано изучение типа лейкоцитурии, бактериологического посева мочи с определением микробного числа, проведение УЗИ почек и мочевого пузыря.
Таким образом, тактика педиатра, семейного врача на амбулаторно-поликлиническом этапе при выявлении изолированного мочевого синдрома заключается в первичной диагностике наиболее часто встречающихся причин его развития и отборе пациентов для дальнейшего углубленного нефрологического обследования.
Основная
1. Мазурин А.В., Воронцов И.М. Пропедевтика детских болезней. — М.: Медицина,1985. — С. 221-237.
2. Вибрані питання дитячої нефрології / Іванов Д.Д. — К.: Ходак, 2003. — 134 с.
3. Игнатова М.С., Вельтищев Ю.Е. Детская нефрология: Руководство для врачей. — Л.: Медицина, 1989. — С. 128-134.
4. Нефрология детского возраста / Под общ. ред. Е.В. Прохорова, Т.П. Борисовой. — Донецк, 2008. — С. 7-21.
5. Папаян А.В., Савенкова Н.Д. Клиническая нефрология детского возраста. — СПб., 2008. — С. 66-76.
Дополнительная
1. Руководство по нефрологии: Пер. с англ. / Под ред. Дж.А. Витворт, Дж.Р. Лоренса. — М.: Медицина, 2000. — С. 114-119.
2. Нефрология: Руководство для врачей / Под ред. И.Е. Тареевой. — М.: Медицина, 2000. — С. 76-88.
3. Ривкин А.М. Общий анализ мочи и его трактовка // Рос. педиатрич. журнал. — 2008. — № 3. — С. 48-50.