Что такое инсульт поджелудочной железы
Университет
Фото носит иллюстративный характер. Из открытых источников
Татьяна Мохорт, заведующая кафедрой эндокринологии БГМУ, доктор мед. наук, профессор
Инсулиномы, являющиеся опухолями поджелудочной железы, — наиболее распространенная причина гипогликемических состояний, развивающихся вследствие эндогенного гиперинсулинизма. При наличии клинической симптоматики гипогликемии, лабораторным маркером инсулиномы традиционно являются уровни инсулина, значимо превышающие нормальные значения. В то же время нормальные уровни инсулина и C-пептида при подтвержденном гипогликемическом синдроме необязательно исключают диагноз.
Пациентка Д., 28 лет, переведена в отделение эндокринологии 1-й ГКБ Минска из инфекционного стационара, куда госпитализирована с нарушением сознания и подозрением на менингоэнцефалит. При обследовании выявлены уровень глюкозы крови 1,2 ммоль/л (ниже 2,5 ммоль/л — неоднократно), нарушение сознания, потливость, тремор, судороги, что позволило установить диагноз гипогликемической болезни. С учетом общепринятых причин заболевания (см. табл.) проведено обследование для уточнения причины состояния пациентки.
На этапе сбора анамнеза и клинического наблюдения за пациенткой исключены постпрандиальные гипогликемии, так как снижение уровня глюкозы крови отмечалось в ночное время и спустя 2–5-часового перерыва после приема пищи.
Гипогликемии повторялись и были зарегистрированы многократно при нормальном питании, поэтому проведение пробы с голоданием признано необоснованным. Исключены экзогенно-индуцированные причины, обусловленные приемом антигипергликемических препаратов. Неоднократно исследовались уровни инсулина и С-пептида, которые не выходили на пределы референсных значений натощак и после пищевой нагрузки. Уровни тиреотропного, соматотропного, кортикотропного, лютеотропного и фолликулостимулирующего гормонов, профиль кортизола в течение суток, инсулиновый фактор роста-1 также не выходили за пределы нормальных показателей.
Наиболее вероятными причинами развития гипогликемии при нормальном уровне инсулина являются внепанкреатические опухоли мезенхимального происхождения (мезотелиома, фибросаркома, рабдомиосаркома, лейомиосаркома, липосаркома и гемангиоперицитома), органоспецифические карциномы (печеночная, адренокортикальная, мочеполовой системы и молочной железы), феохромоцитомы, карционидные опухоли, злокачественные заболевания крови (лейкемия, лимфома и миелома).
Механизм развития таких гипогликемий во многих случаях объясняется нарушением питания, обусловленным опухолью и потерей веса вследствие жирового, мышечного и тканевого истощения, которое нарушает глюконеогенез в печени, повышением утилизации глюкозы опухолевыми тканями или секрецией аномальных гипогликемических факторов, отличных по своей природе от инсулина, но оказывающих инсулиноподобное действие. При обследовании проведен онкопоиск, опухолевой патологии не выявлено.
Повторяющиеся гипогликемии могут развиться у пациентов с системной карнитиновой недостаточностью, которая проявляется тошнотой, рвотой, гипераммониемией и печеночной энцефалопатией (одна из форм синдрома Рейе) или при недостаточности карнитин-пальмитоилтрансферазы, проявляющейся миопатией при физической нагрузке с миоглобинурией. Ферментопатии проявляются, как правило, в детском возрасте. Клинические признаки заболевания у наблюдаемой не соответствовали.
С учетом отсутствия набора массы тела высказано предположение о патологии желудочно-кишечного тракта или ферментопатии. После обследования у гастроэнтерологов и консультации генетиков, а также пробного лечения крахмалом для исключения ферментопатий проведена визуализация головного мозга, по результатам МРТ патологии не выявлено.
Длительное обследование только подтверждало наличие у пациентки гипогликемической болезни с нормальными уровнями инсулина.
Поскольку частые гипогликемические эпизоды приводили к повторяющимся нарушениям сознания, а причина патологии, способная определить этиопатогенетически обоснованное лечение, не была установлена, назначена терапия ex juvantibus диазоксидом (Diazoxide), который снижает инсулиновую секрецию и выраженность гипогликемий, в дозе 100 мг 4 раза в день. Состояние пациентки улучшилось, гипогликемические эпизоды не повторялись.
Через 3 месяца при осмотре отмечен выраженный гипертрихоз — избыточный рост волос на теле, который расценен как побочный эффект приема диазоксида, что привело к необходимости изменения терапии. В качестве препаратов выбора обсуждались глюкокортикостероиды, обладающие контринсулярным эффектом и способные снизить потенциальное антителообразование при аутоиммунном инсулиновом синдроме (синдром Хирата). Из анамнеза известно, что кратковременные потери сознания с подтвержденной однократно гипогликемией (во время отпуска за рубежом) у женщины регистрировались за 1–2 месяца до обращения к врачам, но после стрессовой ситуации их повторяемость уменьшилась и за 2 недели не было отмечено ни одного эпизода гипогликемии. В результате принято решение об инициации терапии глюкокортикостероидами (метилпреднизолон 12 мг со снижением до 8 мг в сутки) в дозе, которая обеспечивала бы предупреждение гипогликемических эпизодов.
За время наблюдения (в течение 2 лет) пациентке неоднократно проводились исследования уровней инсулина и С-пептида, проинсулина, подтверждающие нормоинсулинемию, визуализация поджелудочной железы с контрастированием (компьютерная томография) также не позволяла принять решение о хирургическом лечении. Прием метилпреднизолона привел к перераспределению жировой клетчатки, проявлению полос растяжения, уменьшению мышечной массы конечностей, нарушению менструального цикла, однако гипогликемические эпизоды стали редкими (менее 1 в месяц).
Через 2 года наблюдения контрольная компьютерная томография брюшной полости показала васкуляризированное узловое образование 1,1 см в диаметре на границе головки и тела поджелудочной железы, которое расценено как потенциальная нейроэндокринная опухоль (инсулинома), что позволило обосновать проведение хирургического лечения.
Выявленное образование удалено лапароскопически в Минском городском онкологическом диспансере. Резецирована головка поджелудочной железы с гомогенной опухолью 1,7х1,5 см и проведена одномоментная холецистэктомия.
Морфологические и иммуногистохимические исследования подтвердили нейроэндокринную природу опухоли c низким пролиферативным индексом (без некрозов и признаков инвазии с митотическим индексом до 1 митоза в 10 полях зрения СК(+), Syn(+++), ChrA(+++), Ki-67(3%)) и позволили подтвердить инсулиному как окончательный диагноз.
В послеоперационном периоде после отмены метилпреднизолона при контроле уровня гликемии гипогликемические эпизоды не зарегистрированы. Амбулаторный контроль не выявил нарушений уровня глюкозы. В настоящее время контроль гликемии пациентке не проводят в связи с отсутствием жалоб.
Классические инсулиномы клинически характеризуются триадой Уиппла: эпизодическими гипогликемиями с появлением гипогликемической симптоматики (нейрогликопенической и адренергической); снижением уровня глюкозы в крови (ниже 2,5 ммоль/л) и купированием приступа внутривенным введением глюкозы. У данной пациентки при наличии классической триады Уиппла не удавалось выявить причину гипогликемической болезни для выбора и проведения обоснованного лечения.
В течение 75 лет тест с 72-часовым голоданием рассматривался как «золотой стандарт» для верификации диагноза инсулиномы. Однако проведенные исследования подвергли сомнению необходимость соблюдать столь длительное голодание.
При наблюдении 170 пациентов, оперированных по поводу инсулиномы, 33% завершили голодание в связи с развитием гипогликемии в течение 12 ч, 65% через 24 ч, 84% спустя 36 ч, 93% — 48 ч. Аналогичные результаты получены Hirshberg с соавт., которые предложили использовать 48-часовое голодание. В данном клиническом случае у пациентки были проявления гипогликемии при голодании менее 12 часов. Низкие уровни инсулина у наблюдаемой могут быть, предположительно, следствием супрессии инсулиновой секреции повторяющимися гипогликемическими эпизодами, сопровождающимися нейроглюкопенической и адренергической симптоматикой.
Критерии диагноза инсулиномы (Endocrine Society Clinical Practice Guidelines (ESCPG)):
Пациентка не соответствовала указанным критериям, но у нее диагностирована инсулинома.
Медицинский вестник, 17 марта 2017
Неотложные состояния. Острый панкреатит
Как поставить диагноз? Какие осложнения несут угрозу для жизни пациента? Можно ли остановить рост заболеваемости? Острый панкреатит — одно из самых сложно диагностируемых и вместе с тем широко распространенных заболеваний пищеварительной системы.
Как поставить диагноз?
Какие осложнения несут угрозу для жизни пациента?
Можно ли остановить рост заболеваемости?
Острый панкреатит — одно из самых сложно диагностируемых и вместе с тем широко распространенных заболеваний пищеварительной системы. Специфическая терапия практически отсутствует; проявления чрезвычайно разнообразны и поставить диагноз трудно даже с помощью лабораторных тестов. Ему сопутствует целый ряд осложнений, угрожающих жизни, а клиническое течение и исход непредсказуемы.
В основу данной статьи легли новые рекомендации Британского гастроэнтерологического общества, касающиеся ведения больных острым панкреатитом. Больным, незнакомым с симптомами и возможными серьезными последствиями этого заболевания, полезно обратиться к буклету, выпущенному группой поддержки больных панкреатитом [1].
На Международном симпозиуме, проходившем в Атланте в 1972 году [2], предложено такое определение острого панкреатита: «острое воспаление поджелудочной железы, обыкновенно с острым началом, выраженным болевым синдромом, напряжением мышц живота, рвотой, и последующим вовлечением в процесс различных органов и систем». Объективно заболевание подтверждается «повышенным содержанием панкреатических ферментов в крови или моче». Более точной является классификация осложнений, на которой строится сравнительный анализ и научные исследования (табл. 1).
Таблица 1. Клиническая классификация, предложенная Международным симпозиумом в Атланте [1]
Различные диагностические критерии делают недостоверными показатели заболеваемости. Однако установлено, что частота его в молодом возрасте среди городского населения существенно коррелирует со злоупотреблением алкоголя, а у пожилых сельских жителей — с желчнокаменной болезнью.
По статистике в Великобритании ежегодно острым панкреатитом заболевают 200 из миллиона человек, около 1500 умирают. В среднем врач общей практики сталкивается с вновь заболевшим один раз в три-четыре года. За последние полвека заболеваемость росла синхронно с увеличением потребления алкоголя. В это время госпитальная смертность оставалась в пределах 10%, общая достигала 20%, учитывая случаи посмертной диагностики.
Большинство приступов ограничивается поражением только поджелудочной железы, тогда как в остальных развиваются осложнения, угрожающие жизни или приводящие к смертельному исходу. Обычно это рано развивающаяся органная недостаточность, сопровождающаяся поражением поджелудочной железы в виде некроза, абсцесса или формирования псевдокисты (табл. 1). По последним сообщениям из Йоркшира и западной Шотландии, из 730 случаев острого панкреатита 73% пациентов полностью поправились после легкого приступа, 18% выжили, несмотря на осложнения, и 9% погибли.
Внезапная острейшая боль, иррадиирующая в спину, тошнота или рвота — вот типичное начало приступа. Нередко ему предшествует прием пищи или алкоголя
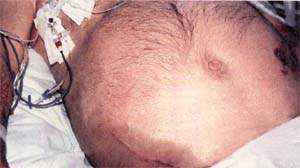 |
| Рисунок 1. Распространение воспалительного экссудата по заднебрюшинной клетчатке вызывает кровоподтеки на боках и в околопупочной области Нарушение пигментации обусловлены разрушением гемоглобина; эти пятна изчезают за несколько дней |
или недавний подобный приступ. При обследовании выявляется бледность, похолодание конечностей, тахикардия, гипотензия, указывающие на гиповолемию.
Иногда присутствует умеренная лихорадка, желтушность кожи и слизистых; абдоминальные симптомы варьируют от легкого напряжения мышц в эпигастрии до генерализованных симптомов раздражения брюшины, развивающегося также и при перфорации внутренних органов. В некоторых случаях обнаруживаются признаки шока и метаболических нарушений при отсутствии объективных абдоминальных симптомов.
Кровоподтеки (рис. 1) патогномоничны только в том случае, если захватывают и пупочную область (как при прерывании эктопической беременности) и боковые стенки живота (как при разрыве аневризмы аорты). Подобный признак указывает на тяжесть приступа, и вероятность смертельного исхода увеличивается в четыре раза.
Диагностически значимым является и четырех-шестикратное увеличение содержания в крови амилазы. Определение амилазы в моче с помощью тест-полоски используется как метод быстрого скрининга. Возможные ошибочные диагнозы, при которых требуется скорее срочная лапаратомия, чем консервативное лечение, приведены в табл. 2.
Таблица 2. Возможные ошибки при определении гиперамилаземии
По данным йоркширской/шотландской статистики, большинство приступов в мире провоцируется желчнокаменной болезнью и алкоголем — 41% и 25% соответственно. Но причина многих из них так и остается неизвестной, хотя и предложено множество этиологических сочетаний (табл. 3) [3].
Начиная с тиазидов в 1959 году предложено более тысячи лекарственных препаратов, способных провоцировать приступ, но в каждом конкретном случае для доказательства лекарственной этиологии необходимо исключить множество других причин, что практически весьма трудно.
Повышенный риск нарушения функции почек и желудочно-кишечных кровотечений исключает применение нестероидных противовоспалительных препаратов.
Стандартный набор больничных исследований включает общий клинический и биохимический анализ крови, определение газов крови и общий анализ мочи. В первые сутки течение заболевания непредсказуемо, и пациент требует постоянного наблюдения и ухода, предпочтительно в специализированном отделении.
К системным осложнениям относятся: дыхательная недостаточность (развивается в 20% приступов), почечная недостаточность (5%), сердечно-сосудистый коллапс, такой же, как при септическом шоке (5% пациентов).
Срочную ретроградную холангиопанкреатографию и эндоскопическую папиллотомию рекомендуется проводить при тяжелых приступах. Хотя данные о результатах таких процедур различны, их эффективность подтверждают британские исследования [5]. При тяжелых приступах повышается интенсивность катаболических процессов, и при продолжительном голодании (более трех-четырех дней) возникает необходимость в парентеральном питании наряду с дополнительным энтеральным введением пищи для сохранения барьерной функции слизистой оболочки кишечника. Диеты придерживаются до тех пор, пока у пациента не восстанавливается переносимость жидкостей и не ослабевают боль и мышечная защита.
Абсцесс поджелудочной железы проявляется симптомами общей интоксикации у 2 — 3% пациентов, обычно через несколько недель после приступа. Инкапсулированный жидкий гной либо аспирируется, либо удаляется через чрезкожный дренаж. Острая псевдокиста осложняет 2 — 3% приступов, содержит панкреатический сок, отграниченный зрелой фиброзной или грануляционной тканью в отличие от эпителия истинных кист.
Псевдокисты развиваются вследствие повреждения панкреатического протока. Диагноз ставится при обычном рентгенологическом исследовании, но иногда кисты определяются даже пальпаторно. Лучшие методы для их исследования — компьютерная томография и магнитно-резонансная томография. Ультразвуковой метод применяется для контроля за их развитием.
При разрывах может возникать панкреатический асцит, эрозии в сосуды приводят к развитию воспалительных псевдоаневризм или серьезных кровотечений. Увеличение абсцесса вызывает боль, билиарную или пилорическую обструкцию.
Таблица 3. Этиологические факторы, точно установленные и возможные
В йоркширском/глазговском исследовании 90% смертей были связаны с системной органной недостаточностью, что частично перекрывается 50% смертей, вызванных накоплением жидкости в поджелудочной железе. Интенсивное лечение ранних осложнений, казалось, должно было бы увеличить выживаемость, но из-за поздних, с трудом поддающихся лечению осложнений общая смертность остается на прежнем уровне. Ей также способствуют истощенные биологические резервы организма и отягощенный преморбидный фон.
За жизнь тысяч пациентов приходится бороться, и выжившие, как правило, выздоравливают полностью. Молодым пациентам, возвращающимся к трудовой деятельности, рекомендуется проводить более интенсивное лечение.
Потеря веса длится около месяца после окончания приступа. В это время у многих пациентов подавленное состояние, и их важно убеждать в том, что оно нормализуется. Стимуляция поджелудочной железы сводится к минимуму посредством диеты, бедной жирами и с высоким содержанием крахмалистых веществ. Короткий курс панкреатина способствует восстанавлению веса, эндо- и экзокринной функций. Вне зависимости от этиологии заболевания необходимо воздерживаться от алкоголя в течение трех месяцев. При подозрении на наличие алкоголизма необходимо тщательно собрать не только анамнез жизни пациента, но и семейный анамнез.
Профилактика предполагает установление и устранение причины развития приступа. Национальная программа борьбы с алкоголизмом в Скандинавии позволила остановить рост заболеваемости, но в остальном профилактика является, по существу, вторичной. Уровень трансаминаз, превышающий 60 МЕ/л, дает возможность подозревать наличие желчных камней; если они не обнаруживаются при ультразвуковом исследовании, то РХПГ способна выявить их или установить иную, поддающуюся коррекции причину.
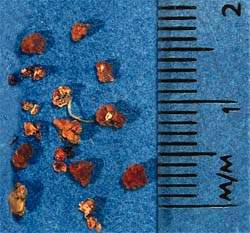 |
| Рисунок 2. Во всем мире большая часть панкреатитов вызывается камнями желчного пузыря или алкоголем |
Несмотря на диету с низким содержанием жира, распространенным остается рецидивирующий панкреатит, обусловленный камнями в желчном пузыре. Наилучшие результаты в данном случае дает холецистэктомия, но при условии хорошей подготовленности пациента и нормализации функции печени.
К холецистэктомии прибегают и в случае повторных идиопатических приступов, если, по данным РХПГ, желчь содержит кристаллы холестерола. Определять содержание алкоголя в крови бессмысленно, поскольку приступ может развиться через несколько дней после приема алкоголя. Совет воздерживаться от приема спиртных напитков, как правило, игнорируется.
Гиперкальциемия и гиперлипопротеидемия, обнаруженные после выздоровления, требуют специальной коррекции. Несмотря на все прилагаемые усилия по установлению этиологии, около четверти приступов остаются идиопатическими.
Многочисленные, в основном британские исследования так и не выявили какого-либо роста выживаемости. Причина тому — отсутствие возможности четкой демонстрации «отрицательных» результатов в контрольных группах (ошибка II типа).
Пациенты, находящиеся в тяжелом состоянии, нуждаются в постоянном уходе со стороны опытного персонала, состоящего из различных специалистов. При отсутствии такой возможности пациента с тяжелым приступом необходимо перевести в специализированный центр. Опыт показывает, что увеличение процента выживаемости происходит в том случае, если туда поступают еще не умирающие пациенты.
1. Neoptolemos J. P. What’s wrong with my pancreas? Produced by the Pancreatitis Supporters Network. (Information leaflet available from Duphar Laboratories, Southampton).
2. Braganza J. M, ed. The Pathogenesis of Pancreatitis. Manchester: Manchester University Press, 1991.
3. Bradley E. L. A clinically based classification for acute pancreatitis. Arch. Surg, 1993; 128:586-90.
4. Kingsnorth A. N. Role of cytokines and their inhibitors in acute pancreatitis. Gut 1997; 40:1-4.
5. Neoptolemus J. P., Carr-Locke D. L, London N. J., Bailey I. A., James D. F., Ossard D. P. Controlled trial of urgent endoscopic cholangio-pancreatography and endoscopic sphincterotomy versus conservative treatment for acute pancreatitis due to gallstones. Lancet ii:979-983.
6. Larvin M., Chalmers A. G., McMahon M. J. Dynamic contrast enchanced computed tomography: a precise technique for identifying and localising pancreatic necrosis. Br. Med. J., 1990; 300:1425-1428.
7. Saiffudin A., Ward J., Rigway L., Chalmers A. G. Comparison of MR and CT scanning un severe acute pancreatitis: initial experiences. Clin. Radiol, 1993;48:111-16.
8. Larvin M., Chalmers A. G., Robinson P. J., Mc Mahon M. J. Debridement and closed cavity irrigation for the treatment of pancreatic necrosis. Br. J. Surg, 1989; 76:465-471.
Панкреатит
Панкреатит – это воспаление поджелудочной железы (органа, ответственного за выработку пищеварительного сока).
Поджелудочная железа в организме человека выполняет очень важную функцию: вырабатывает ферменты, которые, попадая в тонкий кишечник, активируются и участвуют в переваривании белков, жиров и углеводов. Орган вырабатывает гормон инсулин, который регулирует уровень глюкозы в крови.
Формы панкреатита
Острая – характеризуется острой опоясывающей болью в верхней части живота. Часто боль появляется после употребления жирной пищи или алкоголя. Неприятные ощущения могут быть как едва заметными, так и нестерпимыми с иррадиацией в лопатку или грудину. Наблюдается тошнота, рвота, нарушение стула. Из-за затрудненного оттока желчи кожа принимает желтоватую окраску.
Хроническая – основная локализация боли находится на верхней части брюшной стенки с иррадиацией в спину, грудную клетку (левую часть), нижнюю часть живота. Неприятные ощущения возникают после приема жирной тяжелой пищи, алкогольных напитков, постоянных стрессов.
Развитие хронического панкреатита характеризуется тошнотой, потерей аппетита, вздутием живота, нарушением стула, иногда рвотой.
Хроническая форма патологии отличается от острой периодами ремиссии и обострения. С течением заболевания периоды обострения становятся все чаще, возможно развитие кишечных расстройств, нарушения нормального пищеварения, снижение массы тела.
Хронический панкреатит часто дает осложнения (желудочные кровотечения, рак, кисты и абсцессы, поражение печени, сахарный диабет, энтероколит). Вот почему к заболеванию нужно относиться серьезно и при малейшем подозрении на развитие воспаления, обратиться к врачу.
Причины развития панкреатита
Болезнь развивается из-за поражения тканей поджелудочной железы. Это происходит по следующим причинам:
злоупотребление алкоголем и табаком
травмы живота, хирургические вмешательства
неконтролируемый и долговременный прием медикаментов: антибиотиков, гормональных препаратов, кортикостероидов, некоторых диуретиков
интоксикация пищевыми продуктами, химическими веществами
неправильный рацион питания с преобладанием острой и жирной еды и с большими перерывами между приемами пищи
Симптомы панкреатита

Боль – интенсивная, постоянная, характер болевых ощущений описывается больными как режущий, тупой.
Высокая температура тела, высокое или низкое давление – самочувствие пациента быстро ухудшается из-за стремительного развития воспалительного процесса.
Бледный или желтоватый цвет лица.
Тошнота и рвота – появляется сухость во рту и белый налёт, приступы рвоты не приносят облегчения. Самый правильный шаг в этот момент – голодать, любой приём пищи может только ухудшить ситуацию.
Диарея или запор – стул при остром панкреатите чаще всего пенистый, частый со зловонным запахом, с частицами не переваренной пищи. Бывают и наоборот запоры, вздутие, затвердение мышц живота, что может быть самым первым сигналом начинающегося острого приступа панкреатита.
Вздутие живота – желудок и кишечник во время приступа не сокращаются.
Одышка – появляется из-за потери электролитов при рвоте.
Хронический панкреатит характеризуется следующими признаками:
Боль в животе – может быть опоясывающей или иметь чёткую локализацию с иррадиацией в спину. Появляется после принятия пищи.
Интоксикация организма – появляются общая слабость, снижение аппетита, тахикардия, повышение температуры тела, снижение артериального давления.
Эндокринные нарушения – кетоацидоз, сахарный диабет, склонность к гипогликемии. Также могут появиться ярко-красные пятна в области живота, спины, груди, которые не исчезают при надавливании.
При длительном течении заболевания у больного постепенно возникает анемия, потеря массы тела, сухость кожи, ломкость волос и ногтей, симптомы авитаминоза, повышенная утомляемость.
Первая помощь при приступе панкреатита
Чтобы снизить болевые ощущения, можно использовать грелку, наполненную холодной водой. Её нужно приложить на область живота, а именно на эпигастральную область (область под мечевидным отростком, соответствующая проекции желудка на переднюю брюшную стенку). Это позволяет снизить интенсивность болей, немного убрать отек и воспаление.
Больному необходимо соблюдать больничный режим. Это позволит уменьшить приток крови к органу, а значит уменьшит воспаление.
Запрещено принимать пищу. Процесс переваривания может вызвать более сильные боли, появиться тошнота и рвота. А диета уменьшит выработку ферментов, усиливающих воспалительную реакцию и боли. Придерживаться голодания нужно 3 суток. Можно пить чистую воду без газов.
Нужно обязательно вызвать врача для осмотра, даже если больной точно не уверен, что это приступ острого панкреатита. Как мы уже знаем, эта патология может затихнуть, а затем стремительно рецидивировать. В это время можно выпить обезболивающий препарат, чтобы снизить неприятные ощущения.
Диагностика заболевания к частной медицинской клинике «Медюнион»
Диагностировать это заболевание не составляет труда, так как первые признаки говорят сами за себя. Однако, чтобы назначить адекватное лечение, нужно обязательно определить форму заболевания. Для этого врач проводит лапароскопию – метод, позволяющий осмотреть с помощью специального инструмента брюшную полость изнутри.
При подозрении на острый панкреатит проводятся лабораторные анализы:
Общий анализ крови
Биохимический анализ крови
УЗИ, МРТ или рентгенография органов брюшной полости
Компьютерная томография по показаниям
При хронической форме проводятся те же исследования, однако анализы лучше брать в период обострения заболевания.
Лечение острого панкреатита
При обнаружении острого панкреатита пациента нужно немедленно госпитализировать. Лечение должно проходить в условиях стационара, так как это состояние является весьма опасным.
Для снятия боли принимают спазмолитики, в сложных случаях проводят откачивание содержимого желудка для снятия нагрузки на железу.
При обострении панкреатита больные нуждаются в госпитализации с ежедневным в течение первой недели контролем параметров крови, водного баланса, числа лейкоцитов, уровня ферментов в сыворотке крови. В первые 1–3 дня рекомендуются голод, прием щелочных растворов каждые 2 часа.
Во время обострения хронического панкреатита пациенту показана терапия, аналогичная острому процессу. Пациент должен на протяжении всей жизни соблюдать диету и принимать препараты из группы спазмолитиков и препараты, нормализирующие секреторную функцию органа.
Самое главное при хронической форме заболевания поддерживать диету, которая предполагает исключение из рациона жирной и жареной пищи. При малейшем нарушении режима у больного могут начаться неприятные ощущения и тошнота. При интенсивных болях врач назначает спазмолитики. Коротким курсом может применяться антисекреторная терапия.
Диета при панкреатите

Также необходимо ограничить потребление соли, питаться небольшими порциями по 6 раз в день. Блюда всегда должны подаваться в тёплом виде. Необходимо исключить все продукты с высоким содержанием экстрактивных веществ или эфирных масел (рыбные, мясные бульоны, какао, кофе и др.), свежих ягод, овощей, зелени, фруктов, плодов, кислых соков, газированных напитков, маринадов.
Где пройти лечение панкреатита в Красноярске?
Если вы или ваши близкие страдаете от воспаления поджелудочной железы, обратитесь за помощью в медицинский центр «Медюнион». Мы занимаемся диагностикой и лечением любых заболеваний в Красноярске. Мощное оборудование для проведения КТ, МРТ и рентгена, опытные врачи, которые при необходимости проведут первичный осмотр на дому, ждут вас в «Медюнион». Чтобы узнать подробности или записаться на прием, позвоните по телефону 201-03-03.


