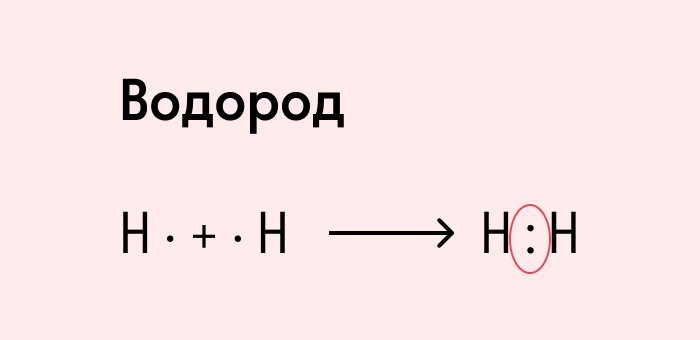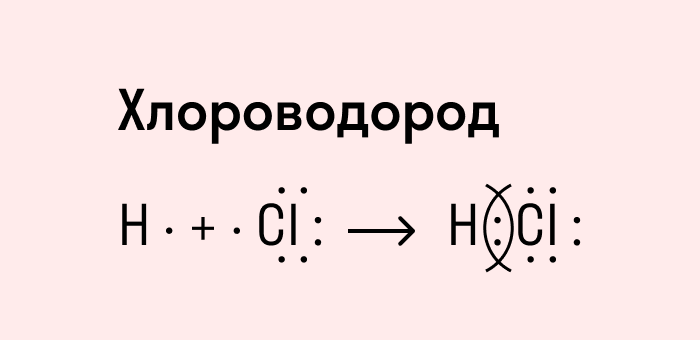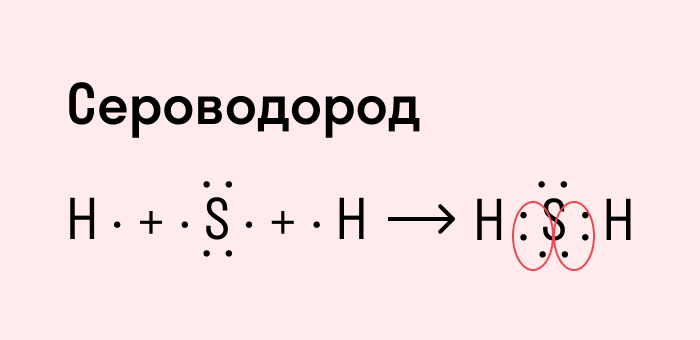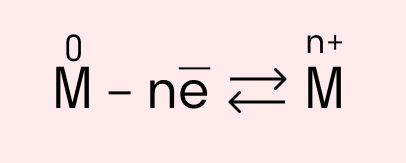Что такое двойная связь
Двойная связь
Полезное
Смотреть что такое «Двойная связь» в других словарях:
Двойная связь — Двойная связь: Двойная связь химическая связь между двумя атомами, образованная двумя парами электронов; частный случай кратной связи. Двойная связь (или двойное послание) психологическая концепция в теории шизофрении Грегори Бейтсона … Википедия
ДВОЙНАЯ СВЯЗЬ — En.: Double bind Согласно Эриксону и Росси, двойная связь это предложение достаточно упрощенного и иллюзорного выбора (Erickson & Rossi, 1976, стр.62.): «Желаете ли вы испытать транс глубокий или средний?» Предлагается альтернатива, но результэт… … Новый гипноз: глоссарий, принципы и метод. Введение в эриксоновскую гипнотерапию
двойная связь — dvigubasis ryšys statusas T sritis chemija apibrėžtis Du kovalentiniai ryšiai tarp dviejų atomų. atitikmenys: angl. double bond; ethylene bond rus. двойная связь; этиленовая связь ryšiai: sinonimas – dvilypis ryšys sinonimas – etileninis ryšys … Chemijos terminų aiškinamasis žodynas
двойная связь — dvilypis ryšys statusas T sritis fizika atitikmenys: angl. double bond vok. Doppelbindung, f rus. двойная связь, f pranc. liaison double, f … Fizikos terminų žodynas
ДВОЙНАЯ СВЯЗЬ — хим. связь между соседними атомами в молекуле, осуществляемая двумя парами электронов. Характерна гл. обр. для органич. соединений. Графически изображается двумя валентными штрихами, например Соединения с Д. с. (см., напр., Этилен, Бутены,… … Большой энциклопедический политехнический словарь
ДВОЙНАЯ СВЯЗЬ — см. Кратные связи … Химическая энциклопедия
ДВОЙНАЯ СВЯЗЬ — см. Кратные связи … Естествознание. Энциклопедический словарь
Двойная связь — Нарушения общения, наблюдающиеся в семьях больных шизофренией. Общение больных с родителями приобретает как бы разноплановый характер, протекает в двух плоскостях, несовместимых в аффективном отношении. Например, больной шизофренией, радуясь… … Толковый словарь психиатрических терминов
Двойная связь — нарушение в сфере коммуникации ребёнка и родителя, когда ребёнок получает от последнего противоречивые послания. Например, мать, не принимая своего нежного чувства к ребёнку, отталкивает ребёнка своей холодностью, а затем выражает показную любовь … Энциклопедический словарь по психологии и педагогике
Двойная связь (химия) — У этого термина существуют и другие значения, см. Двойная связь. Рис.1.Сигма связь … Википедия
Двойная связь (химия)
Двойная связь — ковалентная связь двух атомов в молекуле посредством двух общих электронных пар. Строение двойной связи отражено в теории валентных связей. В этой теории считалось, что двойная связь образуется комбинацией сигма- (рис.1) и пи- (рис.2) связей.
На симпозиуме по теоретической органической химии (Лондон, сентябрь 1958 г.) был представлен докла Л.Полинга, дважды лауреата Нобелевских премий. Доклад Полинга был посвящён природе двойной связи. Был предложен новый путь описания двойной связи как комбинации двух одинаковых изогнутых связей. [1]
Полинг особое внимание уделил на кулоновскую электронную корреляцию: «Взаимодействие электронов (отталкивание) может играть весьма сущестенную роль в повышении устойчивости изогнутых связей…»
Описание двойной и тройной связи с помощью представления об изогнутых связях поразительным образом объясняет некоторые из их свойств. Так, если кратные связи имеют вид дуг длиной 1,54 Å (длина простой связи углерод-углерод) и начальное направление их совпадает с тетраэдрическим, то их вычисленная длина оказывается равной 1,32 Å для двойной связи и 1,18 Å для тройной, что хорошо соответствует экспериментальным значениям 1,33 и 1,20 Å.»
Дальнейшее развитие представлений об электростатическом отталкивании электронов предпринято в теории отталкивания электронных пар Р.Гиллеспи. [2]
Примечания
См. также
Полезное
Смотреть что такое «Двойная связь (химия)» в других словарях:
ХИМИЯ ОРГАНИЧЕСКАЯ. КЛАССЫ СОЕДИНЕНИЙ — Органические соединения (углеводороды и их производные) можно разделить на два типа: ациклические (или алифатические, т.е. с открытой углеродной цепью) и циклические; последние в свою очередь подразделяются на алициклические, в молекулах которых… … Энциклопедия Кольера
Тройная связь — Рис.1.Тройная связь в рамках теории валентных связей Тройная связь ковалентная связь двух атомов в молекуле посредством трёх общих связывающих электронных пар. Первая картина наглядного строения тройной связи была дана в … Википедия
Химическая связь — взаимное притяжение атомов, приводящее к образованию молекул и кристаллов. Принято говорить, что в молекуле или в кристалле между соседними атомами существуют Х. с. Валентность атома (о чём подробнее сказано ниже) показывает число связей … Большая советская энциклопедия
Ковалентная связь — Рис.1. Модель одинарной ковалентной связи (электронная плотность выделена красным цветом) Ковалентная связь (атомная связь, гомеополярная связь) химическая связь, образованная перекрытием (обобществлением) пары … Википедия
Пи-связь — Рис.1.Пи связь в молекуле этилена … Википедия
ОРГАНИЧЕСНАЯ ХИМИЯ — первоначально составляла часть химии вообще и не имела особого названия; позже под О. х. стали разуметь химию веществ, встречающихся только в животном и растительном организме. Берцелиус (Berzelius) определил в 1827 г. О. х. как химию… … Большая медицинская энциклопедия
Сигма-связь — Рис.1.Сигма связь … Википедия
Ионная связь — В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете … Википедия
Гибридизация (химия) — У этого термина существуют и другие значения, см. Гибридизация. Модель молекулы метана, образованной sp3 гибридными орбиталями … Википедия
Металлическая связь — Металлическая связь это одновременное существование положительно заряженных атомов и свободного электронного газа. Содержание 1 Механизм металлической связи 2 Характерные кристаллические решётки … Википедия
Двойная связь
 | Список значений слова или словосочетания со ссылками на соответствующие статьи. Если вы попали сюда из другой статьи Википедии, пожалуйста, вернитесь и уточните ссылку так, чтобы она указывала на статью. |
Полезное
Смотреть что такое «Двойная связь» в других словарях:
ДВОЙНАЯ СВЯЗЬ — En.: Double bind Согласно Эриксону и Росси, двойная связь это предложение достаточно упрощенного и иллюзорного выбора (Erickson & Rossi, 1976, стр.62.): «Желаете ли вы испытать транс глубокий или средний?» Предлагается альтернатива, но результэт… … Новый гипноз: глоссарий, принципы и метод. Введение в эриксоновскую гипнотерапию
двойная связь — dvigubasis ryšys statusas T sritis chemija apibrėžtis Du kovalentiniai ryšiai tarp dviejų atomų. atitikmenys: angl. double bond; ethylene bond rus. двойная связь; этиленовая связь ryšiai: sinonimas – dvilypis ryšys sinonimas – etileninis ryšys … Chemijos terminų aiškinamasis žodynas
двойная связь — dvilypis ryšys statusas T sritis fizika atitikmenys: angl. double bond vok. Doppelbindung, f rus. двойная связь, f pranc. liaison double, f … Fizikos terminų žodynas
ДВОЙНАЯ СВЯЗЬ — хим. связь между соседними атомами в молекуле, осуществляемая двумя парами электронов. Характерна гл. обр. для органич. соединений. Графически изображается двумя валентными штрихами, например Соединения с Д. с. (см., напр., Этилен, Бутены,… … Большой энциклопедический политехнический словарь
ДВОЙНАЯ СВЯЗЬ — см. Кратные связи … Химическая энциклопедия
ДВОЙНАЯ СВЯЗЬ — см. Кратные связи … Естествознание. Энциклопедический словарь
Двойная связь — Нарушения общения, наблюдающиеся в семьях больных шизофренией. Общение больных с родителями приобретает как бы разноплановый характер, протекает в двух плоскостях, несовместимых в аффективном отношении. Например, больной шизофренией, радуясь… … Толковый словарь психиатрических терминов
Двойная связь — нарушение в сфере коммуникации ребёнка и родителя, когда ребёнок получает от последнего противоречивые послания. Например, мать, не принимая своего нежного чувства к ребёнку, отталкивает ребёнка своей холодностью, а затем выражает показную любовь … Энциклопедический словарь по психологии и педагогике
Двойная связь (химия) — У этого термина существуют и другие значения, см. Двойная связь. Рис.1.Сигма связь … Википедия
Химическая связь
Химическая связь и строение вещества
Все системы стремятся к равновесию и к уменьшению свободной энергии — так гласит один из постулатов химической термодинамики. Атомы, взаимодействующие в молекуле вещества, тоже подчиняются этому закону. Они стремятся образовать устойчивую конфигурацию — 8-электронную или 2-электронную внешнюю оболочку. Этот процесс взаимодействия называется химической связью, благодаря ему получаются молекулы и молекулярные соединения.
| Химическая связь — это взаимодействие между атомами в молекуле вещества, в ходе которого два электрона (по одному от каждого атома) образуют общую электронную пару либо электрон переходит от одного атома к другому. |
Как понятно из определения химической связи, при взаимодействии двух атомов один из них может притянуть к себе внешние электроны другого. Эта способность называется электроотрицательностью (ЭО). Атом с более высокой электроотрицательностью (ЭО) при образовании химической связи с другим атомом может вызвать смещение к себе общей электронной пары.
Механизм образования химической связи
Существует два механизма взаимодействия атомов:
обменный — предполагает выделение по одному внешнему электрону от каждого атома и соединение их в общую пару;
донорно-акцепторный — происходит, когда один атом (донор) выделяет два электрона, а второй атом (акцептор) принимает их на свою свободную орбиталь.
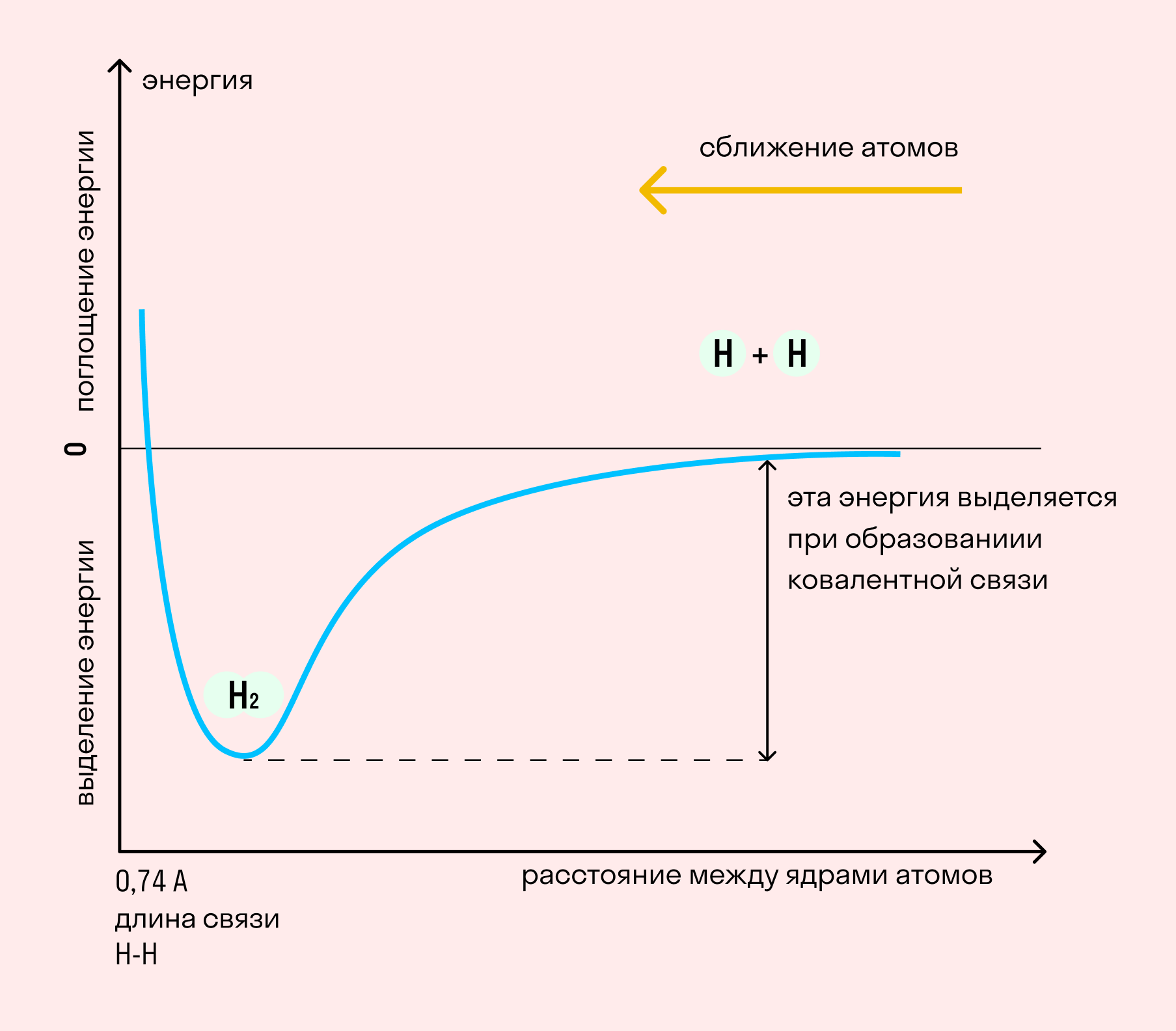
Независимо от механизма химическая связь между атомами сопровождается выделением энергии. Чем выше ЭО атомов, т. е. их способность притягивать электроны, тем сильнее и этот энергетический всплеск.
| Энергией связи называют ту энергию, которая выделяется при взаимодействии атомов. Она определяет прочность химической связи и по величине равна усилию, необходимому для ее разрыва. |
Также на прочность влияют следующие показатели:
Длина связи — расстояние между ядрами атомов. С уменьшением этого расстояния растет энергия связи и увеличивается ее прочность.
Кратность связи — количество электронных пар, появившихся при взаимодействии атомов. Чем больше это число, тем выше энергия и, соответственно, прочность связи.
На примере химической связи в молекуле водорода посмотрим, как меняется энергия системы при сокращении расстояния между ядрами атомов. По мере сближения ядер электронные орбитали этих атомов начинают перекрывать друг друга, в итоге появляется общая молекулярная орбиталь. Неспаренные электроны через области перекрывания смещаются от одного атома в сторону другого, возникают общие электронные пары. Все это сопровождается нарастающим выделением энергии. Сближение происходит до тех пор, пока силу притяжения не компенсирует сила отталкивания одноименных зарядов.
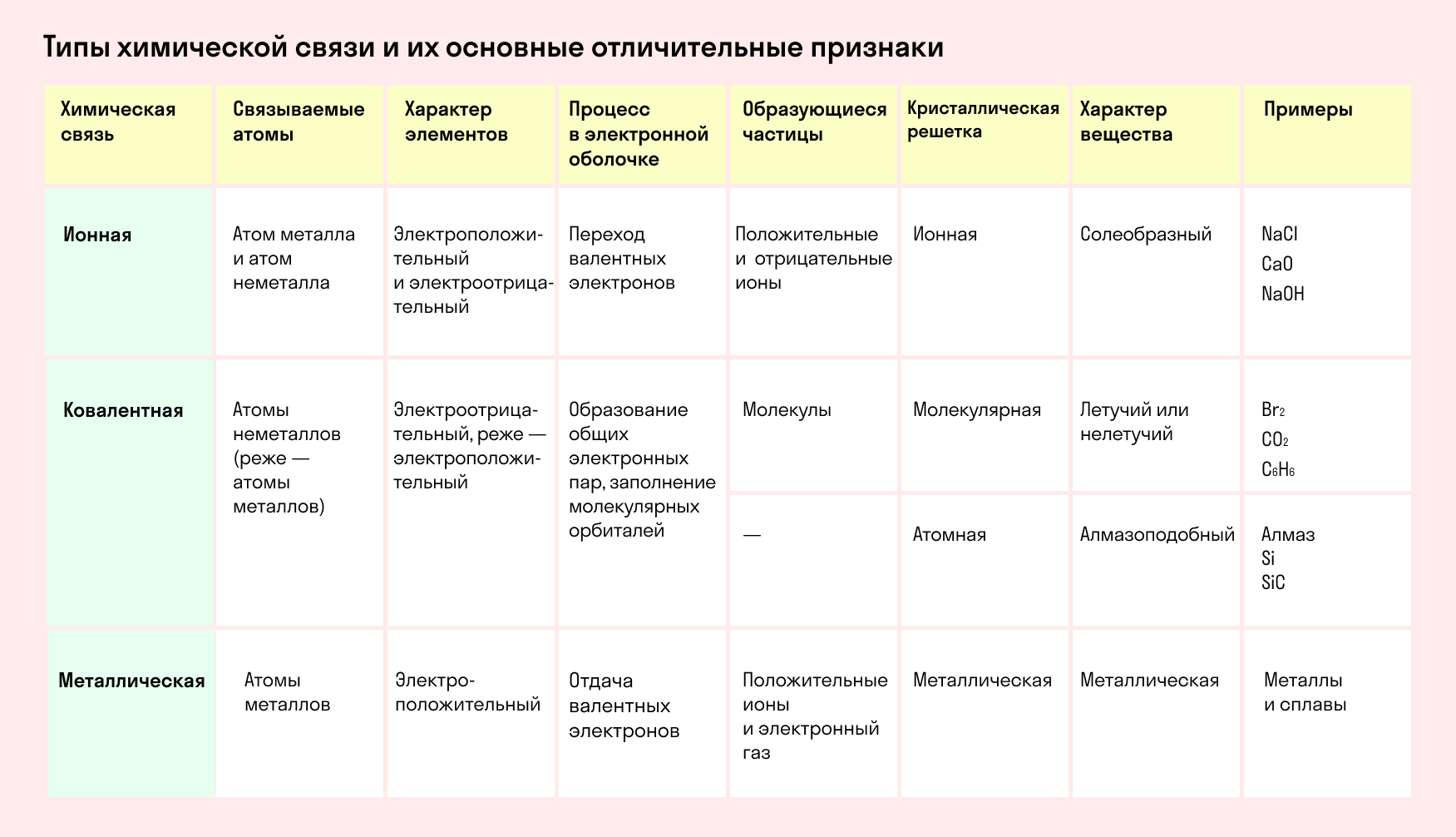
Основные типы химических связей
Различают четыре вида связей в химии: ковалентную, ионную, металлическую и водородную. Но в чистом виде они встречаются редко, обычно имеет место наложение нескольких типов химических связей. Например, в молекуле фосфата аммония (NH4)3PO4присутствует одновременно ионная связь между ионами и ковалентная связь внутри ионов.
Также отметим, что при образовании кристалла от типа связи между частицами зависит, какой будет кристаллическая решетка. Если это ковалентная связь — образуется атомная решетка, если водородная — молекулярная решетка, а если ионная или металлическая — соответственно, будет ионная или металлическая решетка. Таком образом, влияя на тип кристаллической решетки, химическая связь определяет и физические свойства вещества: твердость, летучесть, температуру плавления и т. д.
Основные характеристики химической связи:
насыщенность — ограничение по количеству образуемых связей из-за конечного числа неспаренных электронов;
полярность — неравномерная электронная плотность между атомами и смещение общей пары электронов к одному из них;
направленность — ориентация связи в пространстве, расположение орбиталей атомов под определенным углом друг к другу.
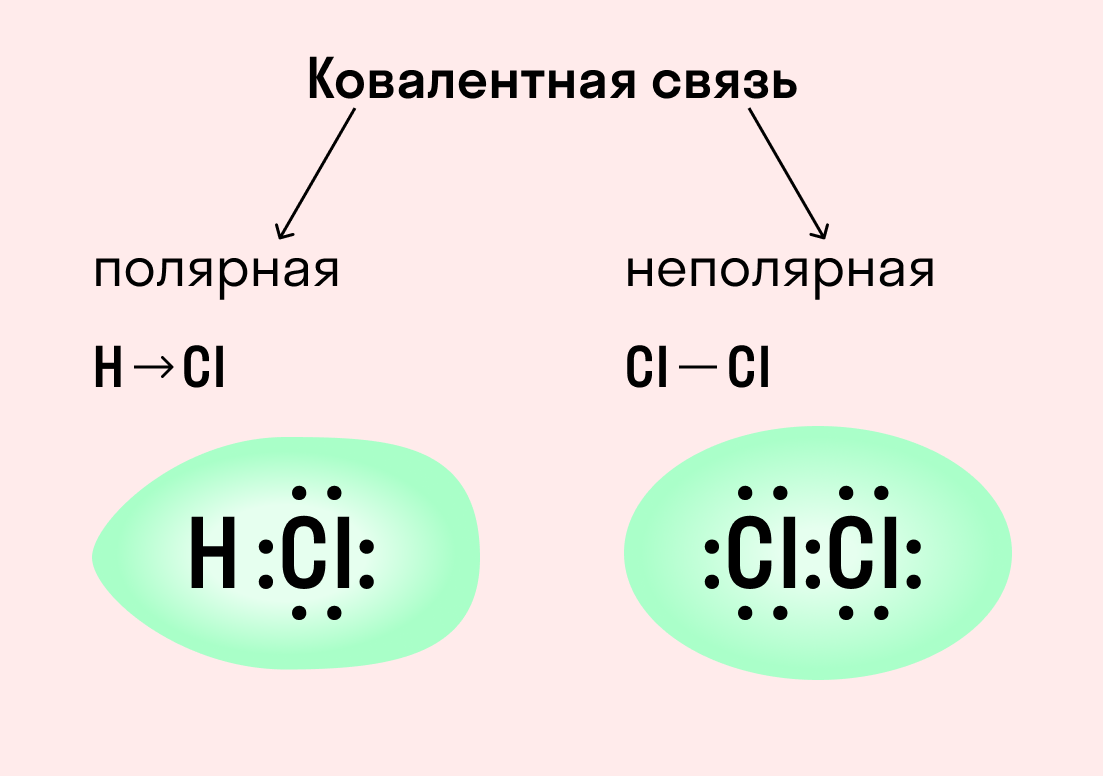
Ковалентная связь
Как уже говорилось выше, этот тип связи имеет два механизма образования: обменный и донорно-акцепторный. При обменном механизме объединяются в пару свободные электроны двух атомов, а при донорно-акцепторном — пара электронов одного из атомов смещается к другому на его свободную орбиталь.
| Ковалентная связь — это процесс взаимодействия между атомами с одинаковыми или близкими радиусами, при котором возникает общая электронная пара. Если эта пара принадлежит в равной мере обоим взаимодействующим атомам — это неполярная связь, а если она смещается к одному из них — это полярная связь. |
Как вы помните, сила притяжения электронов определяется электроотрицательностью атома. Если у двух атомов она одинакова, между ними будет неполярная связь, а если один из атомов имеет большую ЭО — к нему сместится общая электронная пара и получится полярная химическая связь.
Ковалентная неполярная связь образуется в молекулах простых веществ, неметаллов с одинаковой ЭО: Cl2, O2, N2, F2 и других.
Посмотрим на схему образования этой химической связи. У атомов водорода есть по одному внешнему электрону, которые и образуют общую пару.
Ковалентная полярная связь характерна для неметаллов с разным уровнем ЭО: HCl, NH3,HBr, H2O, H2S и других.
Посмотрим схему такой связи в молекуле хлороводорода. У водорода имеется один свободный электрон, а у хлора — семь. Таким образом, всего есть два неспаренных электрона, которые соединяются в общую пару. Поскольку в данном случае ЭО выше у хлора, эта пара смещается к нему.
Другой пример — молекула сероводорода H2S. В данном случае мы видим, что каждый атом водорода имеет по одной химической связи, в то время как атом серы — две. Количество связей определяет валентность атома в конкретном соединении, поэтому валентность серы в сероводороде — II.
Число связей, которые могут быть у атома в молекуле вещества, называется валентностью.
Характеристики ковалентной связи:
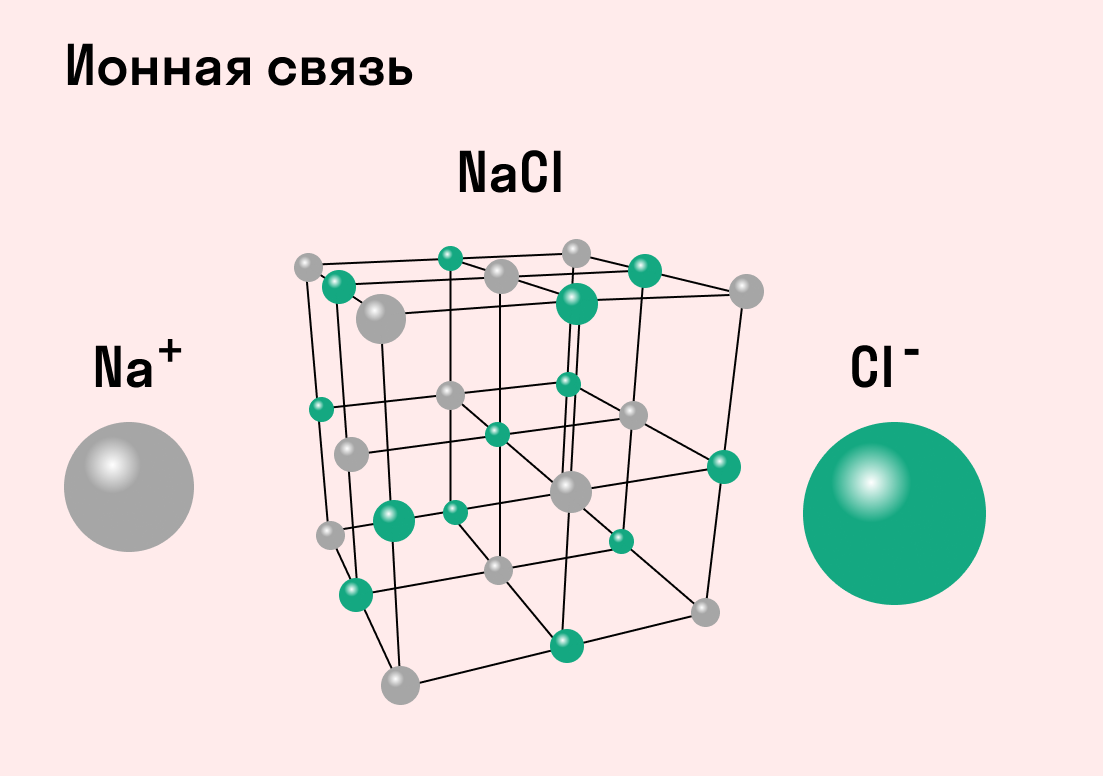
Ионная связь
Как понятно из названия, данный тип связи основан на взаимном притяжении ионов с противоположными зарядами. Он возможен между веществами с большой разницей ЭО — металлом и неметаллом. Механизм таков: один из атомов отдает свои электроны другому атому и заряжается положительно. Второй атом принимает электроны на свободную орбиталь и получает отрицательный заряд. В результате этого процесса образуются ионы.
| Ионная связь — это такое взаимодействие между атомами в молекуле вещества, итогом которого становится образование и взаимное притяжение ионов. |
Разноименно заряженные ионы стремятся друг к другу за счет кулоновского притяжения, которое одинаково направлено во все стороны. Благодаря этому притяжению образуются ионные кристаллы, в решетке которых заряды ионов чередуются. У каждого иона есть определенное количество ближайших соседей — оно называется координационным числом.
Обычно ионная связь появляется между атомами металла и неметалла в таких соединениях, как NaF, CaCl2, BaO, NaCl, MgF2, RbI и других. Ниже схема ионной связи в молекуле хлорида натрия.
Характеристики ионной связи:
не имеет направленности.
Ковалентная и ионная связь в целом похожи, и одну из них можно рассматривать, как крайнее выражение другой. Но все же между ними есть существенная разница. Сравним эти виды химических связей в таблице.
Характеризуется появлением электронных пар, принадлежащих обоим атомам.
Характеризуется появлением и взаимным притяжением ионов.
Общая пара электронов испытывает притяжение со стороны обоих ядер атомов.
Ионы с противоположными зарядами подвержены кулоновскому притяжению.
Имеет направленность и насыщенность.
Ненасыщенна и не имеет направленности.
Количество связей, образуемых атомом, называется валентностью.
Количество ближайших соседей атома называется координационным числом.
Образуется между неметаллами с одинаковой или не сильно отличающейся ЭО.
Образуется между металлами и неметаллами — веществами со значимо разной ЭО.
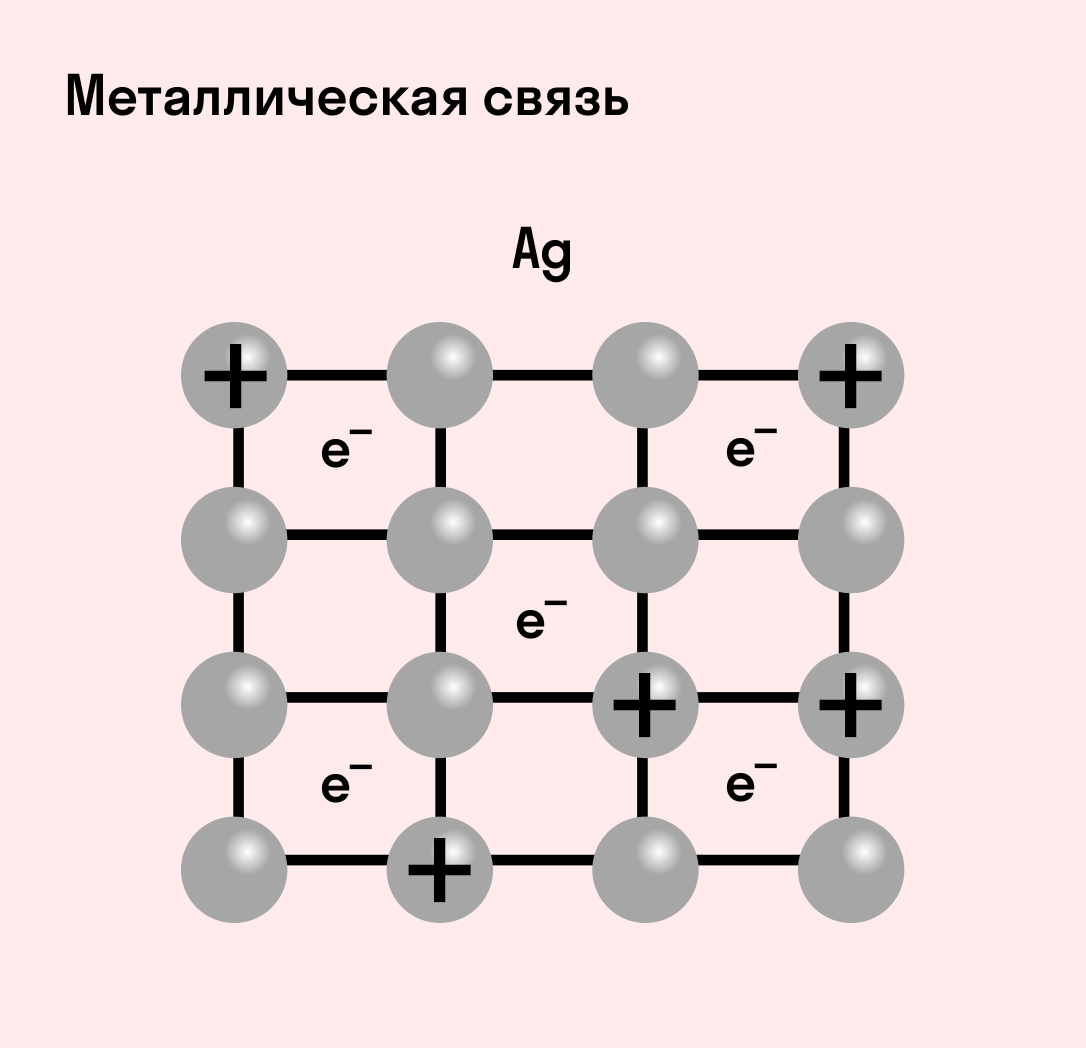
Металлическая связь
Отличительная особенность металлов в том, что их атомы имеют достаточно большие радиусы и легко отдают свои внешние электроны, превращаясь в положительно заряженные ионы (катионы). В итоге получается кристаллическая решетка, в узлах которой находятся ионы, а вокруг беспорядочно перемещаются электроны проводимости, образуя «электронное облако» или «электронный газ».
Свободные электроны мигрируют от одного иона к другому, временно соединяясь с ними и снова отрываясь в свободное плавание. Этот механизм по своей природе имеет сходство с ковалентной связью, но взаимодействие происходит не между отдельными атомами, а в веществе.
| Металлическая связь — это взаимодействие положительных ионов металлов и отрицательно заряженных электронов, которые являются частью «электронного облака», рассеянного по всему объему вещества. |
Наличие такого «электронного облака», которое может прийти в направленное движение, обусловливает электропроводность металлов. Другие их качества — пластичность и ковкость, объясняются тем, что ионы в кристаллической решетке легко смещаются. Поэтому металл при ударном воздействии способен растягиваться, но не разрушаться.
Характеристики металлической связи:
Металлическая связь присуща как простым веществам — таким как Na, Ba, Ag, Cu, так и сложным сплавам — например, AlCr2, CuAl11Fe4, Ca2Cu и другим.
Схема металлической связи:
M — металл,
n — число свободных внешних электронов.
К примеру, у железа в чистом виде на внешнем уровне есть два электрона, поэтому его схема металлической связи выглядит так:
Обобщим все полученные знания. Таблица ниже описывает кратко химические связи и строение вещества.
Типы химической связи и их основные отличительные признаки
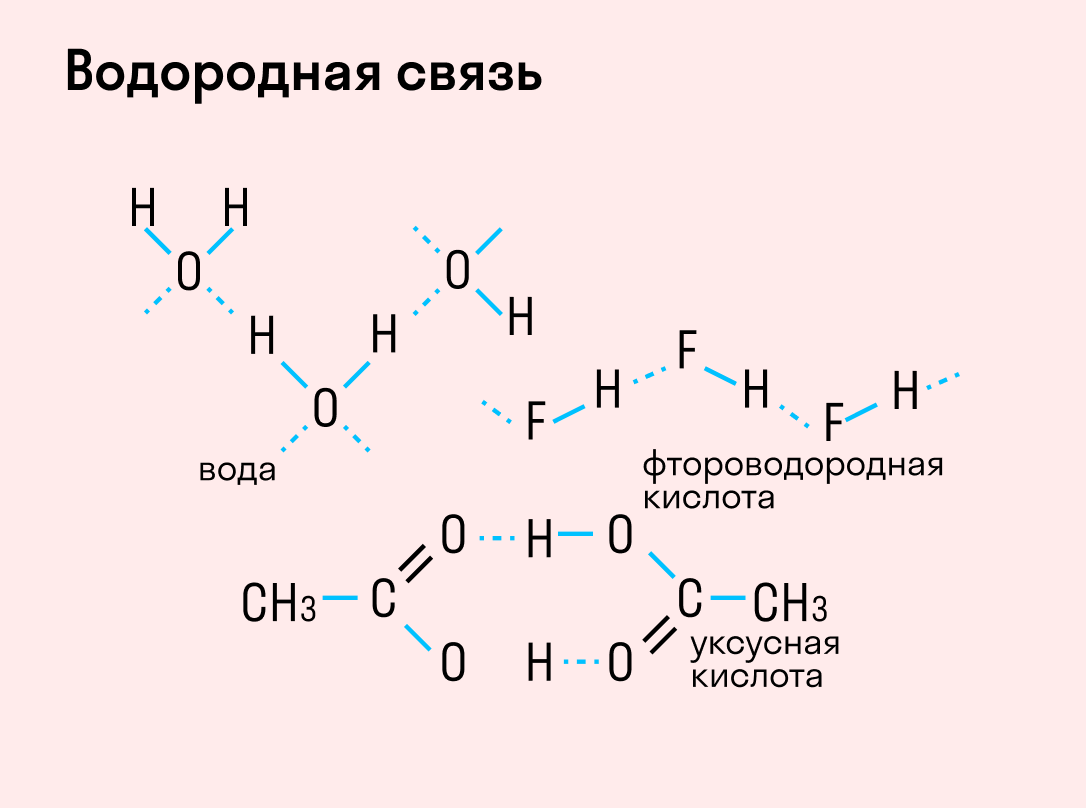
Водородная связь
Данный тип связи в химии стоит отдельно, поскольку он может быть как внутри молекулы, так и между молекулами. Как правило, у неорганических веществ эта связь происходит между молекулами.
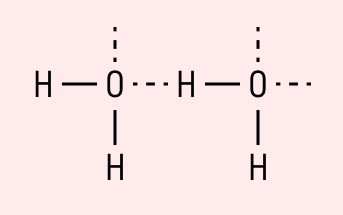
| Водородная связь образуется между молекулами, содержащими водород. Точнее, между атомами водорода в этих молекулах и атомами с большей ЭО в других молекулах вещества. |
Объясним подробнее механизм этого вида химической связи. Есть молекулы А и В, содержащие водород. При этом в молекуле А есть электроотрицательные атомы, а в молекуле В водород имеет ковалентную полярную связь с другими электроотрицательными атомами. В этом случае между атомом водорода в молекуле В и электроотрицательным атомом в молекуле А образуется водородная связь.
Такое взаимодействие носит донорно-акцепторный характер. Донором электронов в данном случае выступают электроотрицательные элементы, а акцептором — водород.
Графически водородная связь обозначается тремя точками. Ниже приведена схема такого взаимодействия на примере молекул воды.
Характеристики водородной связи:
Кратко о химических связях
Итак, самое главное. Химической связью называют взаимодействие атомов, причиной которого является стремление системы приобрести устойчивое состояние. Во время взаимодействия свободные внешние электроны атомов объединяются в пары либо внешний электрон одного атома переходит к другому.
Образование химической связи сопровождается выделением энергии. Эта энергия растет с увеличением количества образованных электронных пар и с сокращением расстояния между ядрами атомов.
Основные виды химических связей: ковалентная (полярная и неполярная), ионная, металлическая и водородная. В отличие от всех остальных водородная ближе к молекулярным связям, поскольку может быть как внутри молекулы, так и между разными молекулами.
Как определить тип химической связи:
Ковалентная полярная связь образуется в молекулах неметаллов между атомами со сходной ЭО.
Ковалентная неполярная связь имеет место между атомами с разной ЭО.
Ионная связь ведет к образованию и взаимному притяжению ионов. Она происходит между атомами металла и неметалла.
Металлическая связь бывает только между атомами металлов. Это взаимодействие положительных ионов в кристаллической решетке и свободных отрицательных электронов. Масса рассеянных по всему объему свободных электронов представляет собой «электронное облако».
Водородная связь появляется при условии, что есть атом с высокой ЭО и атом водорода, связанный с другой электроотрицательной частицей ковалентной связью.
Химическая связь и строение молекулы: типом химической связи определяется кристаллическая решетка вещества: ионная, металлическая, атомная или молекулярная.
Определить тип химической связи в 8 классе поможет таблица.
3.2. Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа.
Большинство органических соединений имеют молекулярное строение. Атомы в веществах с молекулярным типом строения всегда образуют только ковалентные связи друг с другом, что наблюдается и в случае органических соединений. Напомним, что ковалентным называется такой вид связи между атомами, который реализуется за счет того, что атомы обобществляют часть своих внешних электронов с целью приобретения электронной конфигурации благородного газа.
По количеству обобществлённых электронных пар ковалентные связи в органических веществах можно разделить на одинарные, двойные и тройные. Обозначаются данные типы связей в графической формуле соответственно одной, двумя или тремя чертами:
Кратность связи приводит к уменьшении ее длины, так одинарная С-С связь имеет длину 0,154 нм, двойная С=С связь – 0,134 нм, тройная С≡С связь – 0,120 нм.
Типы связей по способу перекрывания орбиталей
Как известно, орбитали могут иметь различную форму, так, например, s-орбитали имеют сферическую, а p-гантелеобразную форму. По этой причине связи также могут отличаться по способу перекрывания электронных орбиталей:
• ϭ-связи – образуются при перекрывании орбиталей таким образом, что область их перекрывания пересекается линией, соединяющей ядра. Примеры ϭ-связей:
• π-связи – образуются при перекрывании орбиталей, в двух областях – над и под линией соединяющей ядра атомов. Примеры π-связей:
Как узнать, когда в молекуле есть π- и ϭ-связи?
При ковалентном типе связи ϭ-связь между любыми двумя атомами есть всегда, а π-связь имеет только в случае кратных (двойных, тройных) связей. При этом:
Укажем данные типы связей в молекуле бутин-3-овой кислоты:
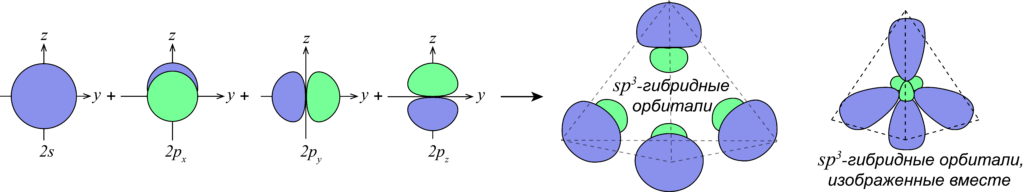
Гибридизация орбиталей атома углерода
Гибридизацией орбиталей называют процесс, при котором орбитали, изначально имеющие разные формы и энергии смешиваются, образуя взамен такое же количество гибридных орбиталей, равных по форме и энергии.
В случае атомов углерода в гибридизации всегда принимает участие s-орбиталь, а количество p-орбиталей, которые могут принимать участие в гибридизации варьируется от одной до трех p-орбиталей.
Как определить тип гибридизации атома углерода в органической молекуле?
| Количество атомов, с которыми связан атом углерода | Тип гибридизации атома углерода | Примеры веществ |
| 4 атома | sp 3 | CH4 – метан |
| 3 атома | sp 2 | H2C=CH2 – этилен |
| 2 атома | sp | HC≡CH — ацетилен |
Потренируемся определять тип гибридизации атомов углерода на примере следующей органической молекулы:
Радикал. Функциональная группа
Под термином радикал, чаще всего подразумевают углеводородный радикал, являющийся остатком молекулы какого-либо углеводорода без одного атома водорода.
Название углеводородного радикала формируется, исходя из названия соответствующего ему углеводорода заменой суффикса –ан на суффикс –ил.
| Формула углеводорода | Название углеводорода | Формула радикала | Название радикала |
| CH4 | метан | -CH3 | метил |
| C2H6 | этан | -С2Н5 | этил |
| C3H8 | пропан | -С3Н7 | пропил |
| СnН2n+2 | …ан | -СnН2n+1 | … ил |
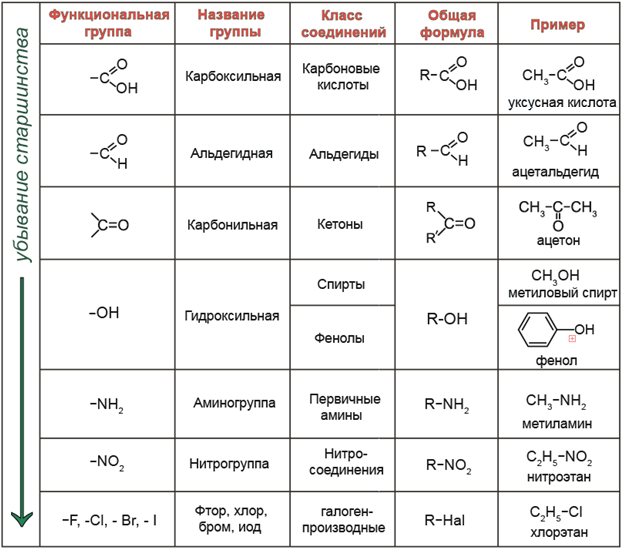
Функциональная группа — структурный фрагмент органической молекулы (некоторая группа атомов), который отвечает за её конкретные химические свойства.
В зависимости того, какая из функциональных групп в молекуле вещества является старшей, соединение относят к тому или иному классу.
R – обозначение углеводородного заместителя (радикала).
Радикалы могут содержать кратные связи, которые тоже можно рассматривать как функциональные группы, поскольку кратные связи вносят вклад в химические свойства вещества.
Если в молекуле органического вещества содержится две или более функциональных группы, такие соединения называют полифункциональными.