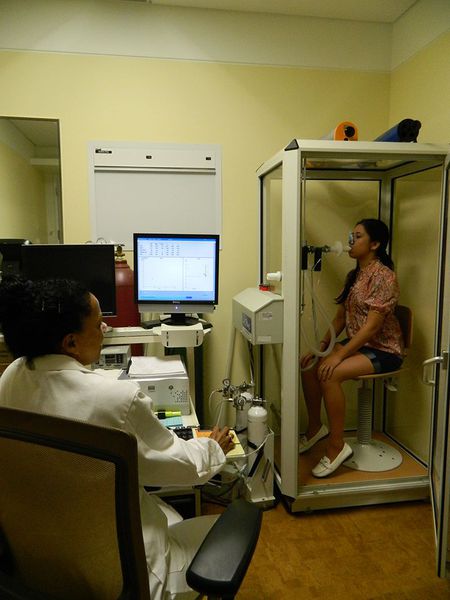
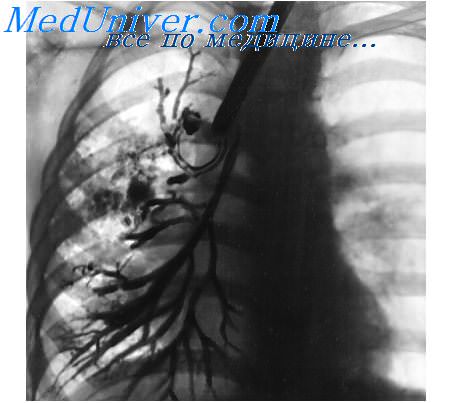
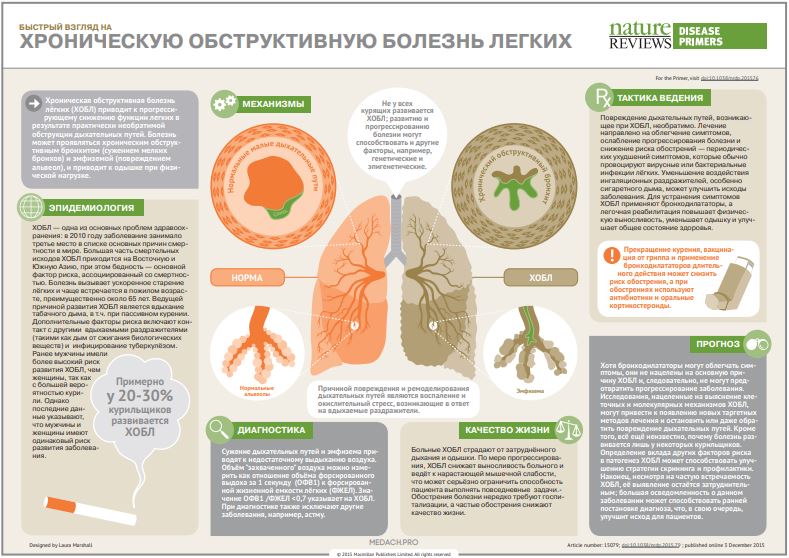
Что такое хроническая обструктивная болезнь легких (ХОБЛ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Никитина И. Л., врача УЗИ со стажем в 26 лет.
Определение болезни. Причины заболевания
Данная болезнь коварна тем, что основные симптомы болезни, в частности, при табакокурении проявляются лишь через 20 лет после начала курения. Оно долгое время не даёт клинических проявлений и может протекать бессимптомно, однако, в отсутствии лечения незаметно прогрессирует обструкция дыхательных путей, которая становится необратимой и ведёт к ранней нетрудоспособности и сокращению продолжительности жизни в целом. Поэтому тема ХОБЛ представляется в наши дни особенно актуальной.
Важно знать, что ХОБЛ — это первично хроническое заболевание, при котором важна ранняя диагностика на начальных стадиях, так как болезнь имеет тенденцию к прогрессированию.
Если врач поставил диагноз «Хроническая обструктивная болезнь лёгких (ХОБЛ)», у пациента возникает ряд вопросов: что это значит, насколько это опасно, что изменить в образе жизни, какой прогноз течения болезни?
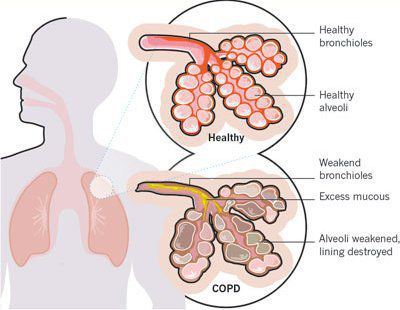
Итак, хроническая обструктивная болезнь лёгких или ХОБЛ – это хроническое воспалительное заболевание с поражением мелких бронхов (воздухоносных путей), которое приводит к нарушению дыхания за счёт сужения просвета бронхов. [1] С течением времени в лёгких развивается эмфизема. Так называется состояние, при котором снижается эластичность лёгких, то есть их способность сжиматься и расширяться в процессе дыхания. Лёгкие при этом находятся постоянно как будто в состоянии вдоха, в них всегда, даже во время выдоха, остается много воздуха, что нарушает нормальный газообмен и приводит к развитию дыхательной недостаточности.
Основными причинами заболевания ХОБЛ являются:
К другим причинам относятся:
Симптомы хронической обструктивной болезни легких
ХОБЛ — болезнь второй половины жизни, чаще развивается после 40 лет. Развитие болезни — постепенный длительный процесс, чаще незаметный для пациента.
Обратиться к врачу заставляют появившиеся одышка и кашель — самые распространённые симптомы заболевания (одышка почти постоянная; кашель частый и ежедневный, с выделениями мокроты по утрам). [2]
Типичный пациент с ХОБЛ — курящий человек 45-50 лет, жалующийся на частую одышку при физической нагрузке.
Кашель — один из самых ранних симптомов болезни. Он часто недооценивается пациентами. На начальных стадиях болезни кашель носит эпизодический характер, но позже становится ежедневным.
Мокрота также относительно ранний симптом заболевания. На первых стадиях она выделяется в небольших количествах, в основном по утрам. Характер слизистый. Гнойная обильная мокрота появляется во время обострения заболевания.
Одышка возникает на более поздних стадиях заболевания и отмечается вначале только при значительной и интенсивной физической нагрузке, усиливается при респираторных заболеваниях. В дальнейшем одышка модифицируется: ощущение недостатка кислорода во время обычных физических нагрузкок сменяется тяжёлой дыхательной недостаточностью и через время усиливается. Именно одышка становится частой причиной для того, чтобы обратиться к врачу.
Когда можно заподозрить наличие ХОБЛ?
Вот несколько вопросов алгоритма ранней диагностики ХОБЛ: [1]
При положительно ответе более чем на 2 вопроса необходимо проведение спирометрии с бронходилятационным тестом. При показателе теста ОФВ1/ФЖЕЛ ≤ 70 определяется подозрение на ХОБЛ.
Патогенез хронической обструктивной болезни легких
При ХОБЛ страдают как дыхательные пути, так и ткань самого лёгкого — лёгочная паренхима.
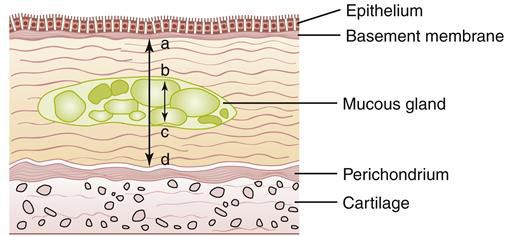
Начинается заболевание в мелких дыхательных путях с закупорки их слизью, сопровождающейся воспалением с формированием перибронхиального фиброза (уплотнение соединительной ткани) и облитерации (зарастание полости).
При сформировавшейся патологии бронхитический компонент включает:
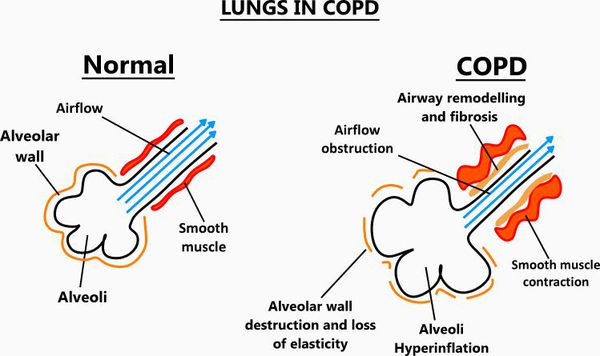
Эмфизематозный компонент приводит к разрушению конечных отделов дыхательных путей — альвеолярных стенок и поддерживающих структур с образованием значительно расширенных воздушных пространств. Отсутствие тканевого каркаса дыхательных путей приводит к их сужению вследствие тенденции к динамическому спадению во время выдоха, что становится причиной экспираторного коллапса бронхов. [4]
Ко всему прочему, разрушение альвеолярно-капиллярной мембраны влияет на газообменные процессы в лёгких, снижая их диффузную способность. В результате этого возникают уменьшение оксигенации (кислородное насыщения крови) и альвеолярной вентиляции. Происходит избыточная вентиляция недостаточно перфузируемых зон, приводящая к росту вентиляции мёртвого пространства и нарушению выведения углекислого газа СО2. Площадь альвеолярно-капиллярной поверхности уменьшена, но может быть достаточной для газообмена в состоянии покоя, когда эти аномалии могут не проявляться. Однако при физической нагрузке, когда потребность в кислороде возрастает, если дополнительных резервов газообменивающихся единиц нет, то возникает гипоксемия — недостаток содержания кислорода в крови.
Появившаяся гипоксемия при длительном существовании у пациентов с ХОБЛ включает ряд адаптивных реакций. Повреждение альвеолярно-капиллярных единиц вызывает подъём давления в лёгочной артерии. Поскольку правый желудочек сердца в таких условиях должен развивать большее давление для преодоления возросшего давления в лёгочной артерии, он гипертрофируется и расширяется (с развитием сердечной недостаточности правого желудочка). Кроме того, хроническая гипоксемия способна вызывать увеличение эритропоэза, который впоследствии увеличивает вязкость крови и усиливает правожелудочковую недостаточность.
Классификация и стадии развития хронической обструктивной болезни легких
| Стадия течения ХОБЛ | Характеристика | Наименование и частота надлежащих исследований |
|---|---|---|
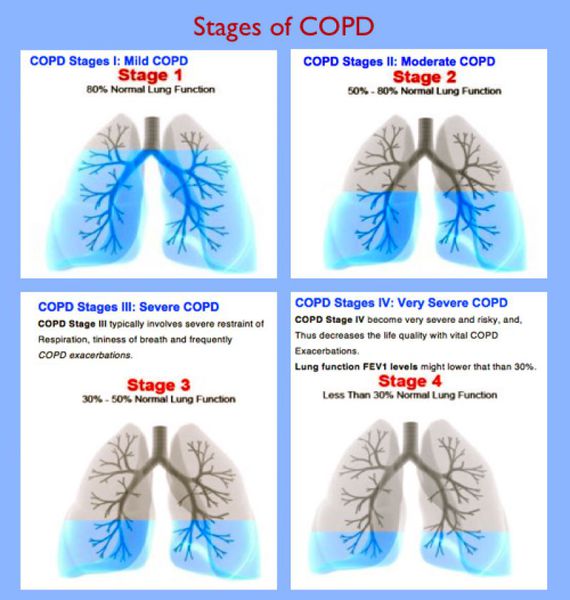
| I. легкая | Хронический кашель и продукция мокроты обычно, но не всегда. ОФВ1/ФЖЕЛ ≤ 70% ОФВ1 ≥ 80% должных величин | Клинический осмотр, спирометрия с бронходилятационным тестом 1 раз в год. В период ХОБЛ — общий анализ крови и рентгенография органов грудной клетки. |
| II. среднетяжёлая | Хронический кашель и продукция мокроты обычно, но не всегда. ОФВ1/ФЖЕЛ ≤ 50% ОФВ1 Дыхательная недостаточность — состояние аппарата внешнего дыхания, при котором либо не обеспечивается поддержание напряжения О2 и СО2 в артериальной крови на нормальном уровне, либо оно достигается за счёт повышенной работы системы внешнего дыхания. Проявляется, главным образом, одышкой. Хроническое лёгочное сердце — увеличение и расширение правых отделов сердца, которое происходит при повышении артериального давления в малом круге кровообращения, развившееся, в свою очередь, в результате лёгочных заболеваний. Основной жалобой пациентов также является одышка. Диагностика хронической обструктивной болезни легкихЕсли у пациентов кашель, выделение мокроты, одышки, а также были выявлены факторы риска развития хронической обструктивной болезни лёгких, то у них у всех должен предполагаться диагноз ХОБЛ. Для того, чтобы установить диагноз, учитываются данные клинического обследования (жалобы, анамнез, физикальное обследование). При физикальном обследовании могут выявляться симптомы, характерные для длительно протекающего бронхита: «часовых стекол» и/или «барабанных палочек» (деформация пальцев), тахипноэ (учащённое дыхание) и одышка, изменение формы грудной клетки (для эмфиземы характерна бочкообразная форма), малая подвижность её во время дыхания, западение межреберных промежутков при развитии дыхательной недостаточности, опущение границ лёгких, изменение перкуторного звука на коробочный, ослабленное везикулярное дыхание или сухие свистящие хрипы, которые усиливаются при форсированном выдохе (то есть быстром выдохе после глубокого вдоха). Тоны сердца могут прослушиваться с трудом. На поздних стадиях может иметь место диффузный цианоз, выраженная одышка, появляются периферические отёки. Для удобства заболевание подразделяют на две клинические формы: эмфизематозную и бронхитическую. Хотя в практической медицине чаще встречаются случаи смешанной формы заболевания. Самый важный этап диагностики ХОБЛ — анализ функции внешнего дыхания (ФВД). Он необходим не только для определения диагноза, но и для установления степени тяжести заболевания, составления индивидуального плана лечения, определения эффективности терапии, уточнения прогноза протекания болезни и оценки трудоспособности. Установление процентного соотношения ОФВ1/ФЖЕЛ чаще всего применяется в лечебной практике. Уменьшение объема форсированного выдоха в первую секунду к форсированной жизненной ёмкости лёгких ОФВ1/ФЖЕЛ до 70 % — начальный признак ограничения воздушного потока даже при сохранённой ОФВ1>80% должной величины. Низкая пиковая скорость потока воздуха на выдохе, незначительно меняющаяся при применении бронходилятаторов также говорит в пользу ХОБЛ. При впервые диагностируемых жалобах и изменениях показателей ФВД спирометрия повторяется на протяжении года. Обструкция определяется как хроническая, если она фиксируется не менее 3-х раз за год (невзирая на проводимое лечение), и диагностируется ХОБЛ. Мониторирование ОФВ1 — важный метод подтверждения диагноза. Спиреометрическое измерение показателя ОФВ1 осуществляется многократно на протяжении нескольких лет. Норма ежегодного падения ОФВ1 для людей зрелого возраста находится в пределах 30 мл в год. Для пациентов с ХОБЛ характерным показателем такого падения является 50 мл в год и более. Бронхолитический тест — первичное обследование, при котором определяется максимальный показатель ОФВ1, устанавливаются стадия и степень тяжести ХОБЛ, а также исключается бронхиальная астма (при положительном результате), избирается тактика и объём лечения, оценивается эффективность терапии и прогнозируется течение заболевания. Очень важно от личить ХОБЛ от бронхиальной астмы, так как у этих часто встречаемых заболеваний одинаковое клиническое проявление — бронхообструктивный синдром. Однако подход к лечению одного заболевания отличается от другого. Главный отличительный признак при диагностике — обратимость бронхиальной обструкции, которая является характерной особенностью бронхиальной астмы. Установлено, что у людей с диагнозом ХО БЛ после приёма бронхолитика процент увеличения ОФВ 1 — менее 12% от исходного (или ≤200 мл), а у пациентов с бронхиальной астмой он, как правило, превышает 15%. Рентгенография грудной клетки имеет вспомогательное зн ачение, так как изменения появляются лишь на поздних стадиях заболевания. ЭКГ может выявлять изменения, которые характерны для лёгочного сердца. ЭхоКГ необходима для выявления симптомов лёгочной гипертензии и изменений правых отделов сердца. Общий анализ крови — с его помощью можно оценить показатели гемоглобина и гематокрита (могут быть повышены из-за эритроцитоза). Определение уровня кислорода в крови (SpO2) – пульсоксиметрия, неинвазивное исследование для уточнения выраженности дыхательной недостаточности, как правило, у больных с тяжёлой бронхиальной обструкцией. Кислородная насыщенность крови менее 88%, определяемая в покое, указывает на выраженную гипоксемию и необходимость назначения оксигенотерапии. Лечение хронической обструктивной болезни легкихЛечение ХОБЛ способствует: К основным направлениям лечения относятся: Ослабление степени влияния факторов риска Производственные вредности также следует контролировать и снижать их влияние, применяя адекватную вентиляцию и воздухоочистители. Образовательные программы Образовательные программы при ХОБЛ включают в себя: Обучение пациентов занимает значимое место в лечении пациентов и влияет на последующий прогноз (уровень доказательности А). Метод пикфлоуметрии даёт возможность пациенту ежедневно самостоятельно контролировать пиковый объём форсированного выдоха — показатель, тесно коррелирующий с величиной ОФВ1. Пациентам с ХОБЛ на каждой стадии показаны физические тренирующие программы с целью увеличения переносимости физических нагрузок. Медикаментозное лечение Фармакотерапия при ХОБЛ зависит от стадии заболевания, тяжести симптомов, выраженности бронхиальной обструкции, наличия дыхательной или правожелудочковой недостаточности, сопутствующих заболеваний. Препараты, которые борются с ХОБЛ, делятся на средства для снятия приступа и для профилактики развития приступа. Предпочтение отдают ингаляционным формам препаратов. Для купирования редких приступов бронхоспазма назначают ингаляции β-адреностимуляторов короткого действия: сальбутамол, фенотерол. Препараты для профилактики приступов: Если применение ингаляции невозможно или их эффективность недостаточна, то возможно необходимо применение теофиллина. При бактериальном обострении ХОБЛ требуется подключение антибиотиков. Могут быть применены: амоксициллин 0,5-1 г 3 раза в сутки, азитромицин по 500 мг трое суток, кларитромицин СР 1000 мг 1 раз сутки, кларитромицин 500 мг 2 раза в сутки, амоксициллин + клавулановая кислота 625 мг 2 раза в сутки, цефуроксим 750 мг 2 раза в сутки. Снятию симптомов ХОБЛ также помогают глюкокортикостероиды, которые также вводят ингаляционно (беклометазона дипропионат, флутиказона пропионат). Если ХОБЛ протекает стабильно, то назначение системных глюкокортикостероидов не показано. Традиционные отхаркивающие и муколитические средства дают слабый положительный эффект у пациентов с ХОБЛ. У тяжёлых пациентов с парциальным давлением кислорода (рО2) 55 мм рт. ст. и менее в покое показана кислородотерапия. Прогноз. ПрофилактикаНа прогноз заболевания влияет стадия ХОБЛ и число повторных обострений. При этом любое обострение негативно сказывается на общем течении процесса, поэтому крайне желательна как можно более ранняя диагностика ХОБЛ. Лечение любого обострения ХОБЛ следует начинать максимально рано. Важно также полноценная терапия обострения, ни в коем случае не допустимо переносить его «на ногах». Зачастую люди решаются обратиться к врачу за медицинской помощью, начиная со II среднетяжелой стадии. При III стадии болезнь начинает оказывать довольно сильное влияние на пациента, симптомы становятся более выраженным (нарастание одышки и частые обострения). На IV стадии происходит заметное ухудшение качества жизни, каждое обострение становится угрозой для жизни. Течение болезни становится инвалидизирующим. Эта стадия сопровождается дыхательной недостаточностью, не исключено развитие лёгочного сердца. На прогноз заболевания влияет соблюдение больным медицинских рекомендаций, приверженность лечению и здоровому образу жизни. Продолжение курения способствует прогрессированию заболевания. Отказ от курения приводит к замедлению прогрессирования заболевания и замедлению снижения ОФВ1. В связи с тем, что заболевание имеет прогрессирующее течение, многие пациенты вынуждены принимать лекарственные средства пожизненно, многим требуются постепенно возрастающие дозы и дополнительные средства в период обострений. Наилучшими средствами профилактики ХОБЛ являются: здоровый образ жизни, включающий полноценное питание, закаливание организма, разумную физическую активность, и исключение воздействия вредных факторов. Отказ от курения – абсолютное условие профилактики обострения ХОБЛ. Имеющиеся производственные вредности, при постановке диагноза ХОБЛ — достаточный повод для смены места работы. Профилактическими мерами также являются избегание переохлаждений и ограничение контактов с заболевшими ОРВИ. С целью профилактики обострений пациентам с ХОБЛ показана ежегодная противогриппозная вакцинация. Людям с ХОБЛ в возрасте 65 лет и старше и пациентам при ОФВ1 Бронходилятация что это такоеНарушения бронхиальной проходимости обычно сочетаются с изменением ОЕЛ и ее структуры. Это проявляется смещением уровня функциональной остаточной емкости (ФОЕ) в инспираторную область, незначительным ростом ОЕЛ и закономерным увеличением ООЛ, который при обострении БА достигает иногда 300-400% должной величины. На ранних этапах заболевания ЖЕЛ не изменяется, но при развитии выраженных изменений она отчетливо снижается, и тогда ООЛ/ОЕЛ может достигать 75% и более. При использовании бронходилататоров наблюдалась отчетливая динамика изучаемых показателей с их почти полной нормализацией в фазу ремиссии, что говорит о снижении бронхомоторного тонуса. У больных БА чаще, чем при другой патологии легких как в межприступный период, так и в фазу ремиссии, наблюдается общая альвеолярная гипервентиляция с отчетливыми признаками ее неравномерности распределения и неадекватности легочному кровотоку. Эта гипервентиляция связана с избыточной стимуляцией дыхательного центра со стороны коры и подкорковых структур, ирритантных и механорецепторов легких и дыхательных мышц, вследствие нарушений контроля бронхиального тонуса и механики дыхания у больных БА. Прежде всего происходит увеличение вентиляции функционального мертвого пространства. Альвеолярная гиповентиляция чаще наблюдается при тяжелых приступах удушья, к ней обычно присоединяется выраженная гипоксемия и гиперкапния. Последняя может достигать 92,1 + 7,5 мм рт.ст. при III стадии астматического статуса. При отсутствии признаков развития пневмофиброза и эмфиземы легких у больных БА не отмечается снижения диффузионной способности легких и ее компонентов (по методу с задержкой дыхания по СО) ни во время приступа удушья, ни в межприступный период. После применения бронхолитиков на фоне существенного улучшения состояния бронхиальной проходимости и структуры ОЕЛ часто наблюдается снижение диффузионной способности легких, увеличение вентиляционно-перфузионной неравномерности и гипоксемии из-за включения в вентиляцию большего числа гиповентилируемых альвеол. ФВД имеет свои особенности и у больных хроническими нагноительными заболеваниями легких, исходом которых являются в той или иной мере выраженные деструктивные изменения легких. К хроническим нагноительным заболеваниям легких относят бронхоэктазии, хронические абсцессы, кистозную гипоплазию легких. Развитию бронхоэктазов, как правило, способствуют нарушение бронхиальной проходимости и воспаление бронхов. Наличие очага инфекции неизбежно приводит к развитию бронхита, в связи с чем в значительной степени связаны нарушения ФВД. Причем, степень выраженности нарушений вентиляции прямо зависит от объема поражения бронхов. Наиболее характерными функциональными изменениями при бронхоэктазах являются смешанные или обструктивные. Рестриктивные нарушения встречаются всего в 15-20% случаев. В патогенезе нарушений бронхиальной проходимости основную роль играют отечно-воспалительные изменения бронхиального дерева: отек, гипертрофия слизистой, скопление в бронхах патологического содержимого. Примерно у половины больных играет роль и бронхоспазм. При сочетании бронхоэктазов с пневмосклерозом, эмфиземой легких, плевральными сращениями изменения механики дыхания становятся еще более неоднородными. Растяжимость легких часто бывает снижена. Отмечается увеличение ООЛ и отношения ООЛ/ОЕЛ. Возрастает неравномерность вентиляции. Более чем у половины больных отмечаются нарушения диффузии легких, а выраженность гипоксемии в начале заболевания невелика. Кислотно-основное состояние соответствует обычно метаболическому ацидозу. При хроническом абсцессе нарушения ФВД практически не отличаются от нарушений дыхания при бронхоэктазах. При кистозном недоразвитии бронхов выявляются более выраженные нарушения бронхиальной проходимости и меньшая выраженность диффузионных нарушений, чем при приобретенных бронхоэктазах, что свидетельствует о хорошей компенсации этого дефекта и ограниченном характере воспалительного процесса. Хроническая обструктивная болезнь легких (перевод статьи из Nature)Хроническая обструктивная болезнь легких (ХОБЛ) является одной из самых актуальных проблем мирового здравоохранения, характеризующейся неуклонно растущими показателями заболеваемости и смертности. Вследствие этого, в целях поддержания здоровья населения, необходимо повышать уровень осведомлённости о заболевании, а также внедрять эффективную систему терапии ХОБЛ. Лечение стабильной ХОБЛ должно основываться на степени тяжести болезни, оцениваемой по степени ограничения воздушного потока, выраженности симптомов и наличия факторов риска обострения. Ведущее место в терапии ХОБЛ занимают бронходилатирующие препараты. Последние достижения в разработке М-холиноблокаторов и β2-адреномиметиков длительного действия позволяют не только улучшить функционирование дыхательной системы в целом и уменьшить выраженность симптомов, но и снизить как частоту обострений, так и темп прогрессирования бронхообструкции. С учетом частой этиологической связи ХОБЛ с воспалительными изменениями дыхательных путей, пациентам, подверженным частым обострениям, а так же при сочетании ХОБЛ с бронхиальной астмой, рекомендовано применение ингаляционных глюкокортикостероидов наряду с индивидуально подобранным режимом терапии ингаляционными бронходилататорами длительного действия. В настоящее время ведется поиск новых терапевтических мишеней в патофизиологическом каскаде развития ХОБЛ в целях формирования новых подходов к лечению, которые бы позволили уменьшить скорость прогрессирования заболевания, развитие сопутствующих заболеваний и снизить величину показателя смертности. Введение Текущие рекомендованные подходы к терапии ХОБЛ Бронходилататоры β2- адреномиметики активируют β 2-адренорецепторы в составе гладкой мускулатуры стенок дыхательных путей. Эти рецепторы сопряжены с активирующим аденилатциклазу G-белком, поэтому связь агонистов с ними приводит к повышению внутриклеточного уровня цАМФ и активации протеинкиназы A. Подобные клеточные изменения способствуют инактивации киназы легких цепей миозина и усилению работы соответствующей фосфатазы. Более того, β2- адреномиметики способствуют открытию кальций-зависимых калиевых каналов, последующему развитию гиперполяризации в гладкомышечных клетках (ГМК), а следовательно, мышечному расслаблению и бронходилатации. Метилксантин является конкурентным неселективным ингибитором фосфодиэстеразы, действие которого проявляется в повышении концентрации внутриклеточного цАМФ с последующей миорелаксацией и бронходилатацией. Бронходилататоры короткого действия Антихолинергические препараты и β2- адреномиметики короткого действия рекомендуются к использованию у пациентов с умеренной непостоянной клинической симптоматикой. Действие β 2- адреномиметиков развивается быстрее, нежели м-холиноблокаторов, в то время как максимальная эффективность в отношении бронходилатации у последних выше. Возможно использование монотерапевтического подхода, однако более предпочтительно сочетанное применение двух групп препаратов короткого действия, так как суммарное их действие, направленное на расширение бронхов, в комбинации проявляется сильнее. Бронходилататоры длительного действия Антихолинергические препараты длительного действия Примерами препаратов данной группы являются тиотропий, гликопирроний, аклидиний и умеклидиний. Эти вещества имеют больший аффинитет в отношении рецепторов М3, нежели М2 и диссоциируют из связи с рецептором типа М3 медленне, что способствует длительному расширению просвета бронхов. Тиотропий – наиболее изученное к настоящему времени антихолинергическое средство длительного действия для ежедневного применения, избирательно связывающееся с М1 и М3-типами рецепторов. В литературе имеются данные о том, что при систематическом применении тиотропия отмечается достоверное улучшение легочной функции (увеличение ОФВ1 и ФЖЕЛ) и качества жизни, а так же повышение переносимости физической нагрузки, уменьшение выраженности одышки и снижение частоты обострений ХОБЛ. Кроме того, многими авторами предполагается, что прием тиотропия способствует замедлению темпа снижения ОФВ1 у пациентов с ХОБЛ умеренно тяжелого течения –. Существуют противоречивые данные о неблагоприятном влиянии тиотропия на сердечно-сосудистую систему. В одном из последних проведенных мета-анализов показано, что применение мелкодисперсного аэрозольного ингалятора, содержащего тиотропий, — «Респимат» (Respimat®)- ассоциировано со значительным повышением риска летального исхода. Особенно часто описанная зависимость отмечается у пациентов с ХОБЛ тяжелого течения, вынуждающего использовать высокие суточные дозы препарата в процессе терапии. В то же время, данные продолжительного рандомизированного исследования показали, что препараты тиотропия снижают риск смерти от любых причин на 11 % по сравнению с плацебо. Сходные результаты были получены в ходе одного из последних рандомизированных двойных слепых исследований, которое подтвердило безопасность применения мелкодисперсного аэрозольного ингалятора с тиотропием. Гликопирроний – антихолинергическое средство для ежедневного приема, так же селективно взаимодействующее с M1 и M3 типами холинорецепторов. Гликопирроний эффективно улучшает показатели функции легких (в частности, ОФВ1) и снижает выраженность одышки и частоту обострений. β2- адреномиметики длительного действия К β 2- адреномиметикам длительного действия относятся такие препараты, как сальметерол, формотерол, индакатерол, олодатерол и вилантерол. До настоящего времени антихолинергические средства длительного действия имели преимущества в назначении перед β2- адреномиметиками длительного действия, в связи с эффективностью первых на протяжении 24 часов, а так же удобством приема (1 раз в сутки) и дозирования. β2- адреномиметики, в свою очередь, для достижения адекватного эффекта требуют двухкратного приема в течение суток. В настоящее время, с появлением адреномиметиков, которые можно применять раз в сутки, назначение того или иного средства определяется характером сопутствующей патологии у пациента и развитием побочных эффектов. Сальметерол и формотерол используются для поддержания стабильности течения ХОБЛ. Особенностью формотерола по сравнению с сальметеролом является более быстрое развитие и большая сила действия. Оба препарата значительно улучшают легочную функцию, уменьшают тяжесть одышки, улучшают прогноз и качество жизни пациента, что было продемонстрировано в плацебо-контролируемых исследованиях. Сравнение β 2- адреномиметиков и антихолинергических препаратов длительного действия Как м-холиноблокаторы, так и β2-адреномиметики длительного действия могут применяться раз в день, поэтому с клинической точки зрения важен вопрос: какая группа препаратов предпочтительна в терапии ХОБЛ? В одном из рандомизированных контролируемых исследований было проведено сравнение препаратов длительного действия с однократным режимом приема: индакатерола (группа β 2- адреномиметиков) и тиотропия (группа антихолинергических средств). По результатам проводимых в течение 26 недель наблюдений за пациентами с ХОБЛ умеренно тяжелого и тяжелого течения, к 12 неделе преимущество индакатерола в улучшении легочной функции и ОФВ1 в сравнении с тиотропием не оставляло сомнений, однако к 26 неделе оба препарата сравнялись по эффективности, которая была значительно выше плацебо. Данное исследование показало более значительно снижение выраженности одышки (транзиторный индекс одышки) и улучшение показателей качества жизни, определяемого состоянием здоровья (опросник St. George) на фоне приема индакатерола, чем при приеме тиотропия. По степени снижения частоты осложнений и по переносимости терапии оба препарата показали примерно одинаковые результаты. Другое недавно проведенное рандомизированное контролируемое исследование, в котором в течение 12 недель принимали участие пациенты с умеренно тяжелым и тяжелым течением ХОБЛ, выявило большую эффективность индакатерола по сравнению с тиотропием в уменьшении выраженности одышки, улучшении показателей качества жизни и снижении потребности в приеме препаратов короткого действия. В то же время влияние на величину ОФВ1 у обоих ЛС было примерно одинаковым. Комбинированная терапия Метилксантин Метилксантин является препаратом, дополняющим основную терапию бронходилататорами и ингаляционными глюкокортикостероидами. У пациентов с ХОБЛ чаще используется пролонгированная таблетированная форма теофиллина. Для него характерен более умеренный бронходилатирующий эффект по сравнению с ингаляционными бронходилататорами. Для достижения эффективного расширения просвета бронхов рекомендовано поддержание плазменного уровня теофиллина в диапазоне от 10 до 20 мг/мл. Вследствие доказанной токсичности метилксантиновых препаратов необходимо проведение строго мониторинга их концентрации в крови. В последние годы появились сообщения о противовоспалительном эффекте низких доз теофиллина (приблизительно, 5 мг/мл), который, вероятно, реализуется за счет усиления экспрессии НDAC2 b и активации альвеолярных макрофагов. Ингаляционные кортикостероиды Ингибиторы ФДЭ-4 Новые терапевтические мишени будущей фармакотерапии ХОБЛ Терапевтические мишени будущей фармакотерапии ХОБЛ. Последние достижения в рамках исследований хронического воспаления, лежащего в основе заболевания, позволили определить новые терапевтические мишени у пациентов с ХОБЛ. Среди возможных терапевтических подходов можно назвать новые антиоксиданты, ингибиторы инфламмасом, антагонисты цитокинов и хемокинов, ингибиторы провоспалительных киназ, антипротеазы, эпигенетическая модуляция. IKK: ингибитор NF κB-киназы (киназы ядерного фактора «Каппа-Би»); ИЛ: интерлейкин; JAK: янус-киназа; MAPK: митоген-активируемая киназа; NRF-2: NF-E2-ассоциированный фактор (фактор, ассоциированный с ядерным фактором NF-E2); NLRP3: Семейство NOD (нуклеотидсвязывающий олигомерный домен)-подобных рецепторов, содержащих пириновый домен-3; PI3K: фосфоинозитид-3-киназа Заключение Последние достижения в области разработок длительно действующих бронхолитиков обеспечили значимое улучшение симптоматики и легочной функции у пациентов с ХОБД. Эти препараты также в некоторой степени снижают риск обострений и скорость прогрессирования ограничения воздушного потока. Для создания новейших стратегий терапии ХОБЛ, которые смогут значительно замедлить прогрессирование заболевания, уменьшить смертность и частоту сопутствующей патологии, требуются новые терапевтические подходы для воздействия на лежащее в основе ХОБЛ хроническое воспаление и патофизиологические изменения в легких; в настоящий момент такие подходы проходят клинические испытания. Список сокращений цАМФ: циклический аденозинмонофосфат ХОБЛ: Хроническая обструктивная болезнь легких ОФВ1: Форсированный объем выдоха за 1 секунду ФЖЕЛ: Форсированная жизненная емкость легких ДПИ: дозированный порошковый ингалятор ДАИ: дозированный аэрозольный ингалятор ЛС: лекарственное средство ГМК: гладкомышечные клетки ПИ: порошковый ингалятор; ОФВ1: Объем форсированного выдоха за первую секунду; ФЖЕЛ: Форсированная жизненная емкость легких; ИКС: Ингаляционный кортикостероид; ДДБА: длительно действующий β2-агонист; ДДМХБ: длительно действующие м-холиноблокаторы; ДИ: дозирующий ингалятор; КЖ: качество жизни; КДБА: короткодействующий β2-агонист; SGRQ: Анкета госпиталя Святого Георгия для оценки дыхательной функции (St. George’s respiratory questionnaire); ИМА: Ингалятор с «мягким» аэрозолем (Soft mist inhaler); ДИО: динамический индекс одышки. Источники Halbert RJ, Natoli JL, Gano A, Badamgarav E, Buist AS, Mannino DM: Global burden of COPD: systematic review and meta-analysis.Eur Respir J 2006, 28:523-532. Ford ES, Croft JB, Mannino DM, Wheaton AG, Zhang X, Giles WH: COPD surveillance—United States, 1999–2011.Chest 2013, 144:284-305. Menezes AM, Perez-Padilla R, Jardim JR, Muino A, Lopez MV, Valdivia G, et al. Chronic obstructive pulmonary disease in five Latin American cities (the PLATINO study): a prevalence study. Lancet. 2005;366:1875–81. Buist AS, McBurnie MA, Vollmer WM, Gillespie S, Burney P, Mannino DM, et al. International variation in the prevalence of COPD (the BOLD Study): a population-based prevalence study. Lancet. 2007;370:741–50. Fukuchi Y, Nishimura M, Ichinose M, Adachi M, Nagai A, Kuriyama T, et al. COPD in Japan: the Nippon COPD Epidemiology study. Respirology. 2004;9:458–65. Lopez AD, Shibuya K, Rao C, Mathers CD, Hansell AL, Held LS, et al. Chronic obstructive pulmonary disease: current burden and future projections. Eur Respir J. 2006;27:397–412. Hogg JC: Pathophysiology of airflow limitation in chronic obstructive pulmonary disease.Lancet 2004, 364:709-721. Hogg JC, Chu F, Utokaparch S, Woods R, Elliott WM, Buzatu L, et al. The nature of small-airway obstruction in chronic obstructive pulmonary disease. N Engl J Med. 2004;350:2645–53. O’Donnell DE, Webb KA: Exertional breathlessness in patients with chronic airflow limitation. The role of lung hyperinflation.Am Rev Respir Dis 1993, 148:1351-1357. O’Donnell DE, Revill SM, Webb KA: Dynamic hyperinflation and exercise intolerance in chronic obstructive pulmonary disease.Am J Respir Crit Care Med 2001, 164:770-777. Hogg JC, Macklem PT, Thurlbeck WM: Site and nature of airway obstruction in chronic obstructive lung disease.N Engl J Med 1968, 278:1355-1360. McDonough JE, Yuan R, Suzuki M, Seyednejad N, Elliott WM, Sanchez PG, et al. Small-airway obstruction and emphysema in chronic obstructive pulmonary disease. New Engl J Med. 2011;365:1567–75. Lai H, Rogers DF: New pharmacotherapy for airway mucus hypersecretion in asthma and COPD: targeting intracellular signaling pathways.J Aerosol Med Pulm Drug Deliv 2010, 23:219-231. Barnes PJ, Celli BR: Systemic manifestations and comorbidities of COPD.Eur Respir J 2009, 33:1165-1185. Agusti AG, Noguera A, Sauleda J, Sala E, Pons J, Busquets X: Systemic effects of chronic obstructive pulmonary disease.Eur Respir J 2003, 21:347-360. Soriano JB, Visick GT, Muellerova H, Payvandi N, Hansell AL: Patterns of comorbidities in newly diagnosed COPD and asthma in primary care.Chest 2005, 128:2099-2107. Belman MJ, Botnick WC, Shin JW: Inhaled bronchodilators reduce dynamic hyperinflation during exercise in patients with chronic obstructive pulmonary disease.Am J Respir Crit Care Med 1996, 153:967-975. Santus P, Radovanovic D, Henchi S, Di Marco F, Centanni S, D’Angelo E, et al. Assessment of acute bronchodilator effects from specific airway resistance changes in stable COPD patients. Respir Physiol Neurobiol. 2014;197:36–45. Scichilone N, Benfante A, Bocchino M, Braido F, Paggiaro P, Papi A, et al. Which factors affect the choice of the inhaler in chronic obstructive respiratory diseases? Pulm Pharmacol Ther. 2015;31:63–7. Johnson M: The beta-adrenoceptor.Am J Respir Crit Care Med 1998, 158:S146-153. Roux E, Molimard M, Savineau JP, Marthan R: Muscarinic stimulation of airway smooth muscle cells.Gen Pharmacol 1998, 31:349-356. Essayan DM: Cyclic nucleotide phosphodiesterases.The Journal of allergy and clinical immunology 2001, 108:671-680. Ofir D, Laveneziana P, Webb KA, Lam YM, O’Donnell DE: Mechanisms of dyspnea during cycle exercise in symptomatic patients with GOLD stage I chronic obstructive pulmonary disease.Am J Respir Crit Care Med 2008, 177:622-629. O’Donnell DE, Laveneziana P, Ora J, Webb KA, Lam YM, Ofir D: Evaluation of acute bronchodilator reversibility in patients with symptoms of GOLD stage I COPD.Thorax 2009, 64:216-223. Bone R, Boyars M, Braun SR, Buist S, Campbell S, Chick T, et al. In chronic obstructive pulmonary disease, a combination of ipratropium and albuterol is more effective than either agent alone. An 85-day multicenter trial. COMBIVENT Inhalation Aerosol Study Group. Chest 1994, 105:1411–1419. Vogelmeier C, Banerji D: NVA237, a long-acting muscarinic antagonist, as an emerging therapy for chronic obstructive pulmonary disease.Ther adv Respir Dis 2011, 5:163-173. Gavalda A, Miralpeix M, Ramos I, Otal R, Carreno C, Vinals M, et al. Characterization of aclidinium bromide, a novel inhaled muscarinic antagonist, with long duration of action and a favorable pharmacological profile. J Pharmacol Exp Ther. 2009;331:740–51. Gross NJ: Tiotropium bromide.Chest 2004, 126:1946-1953. Casaburi R, Mahler DA, Jones PW, Wanner A, San PG, ZuWallack RL, et al. A long-term evaluation of once-daily inhaled tiotropium in chronic obstructive pulmonary disease. Eur Respir J. 2002;19:217–24. Donohue JF, van Noord JA, Bateman ED, Langley SJ, Lee A, Witek Jr TJ, et al. A 6-month, placebo-controlled study comparing lung function and health status changes in COPD patients treated with tiotropium or salmeterol. Chest. 2002;122:47–55. Dusser D, Bravo ML, Iacono P: The effect of tiotropium on exacerbations and airflow in patients with COPD.Eur Respir J 2006, 27:547-555. Niewoehner DE, Rice K, Cote C, Paulson D, Cooper Jr JA, Korducki L, et al. Prevention of exacerbations of chronic obstructive pulmonary disease with tiotropium, a once-daily inhaled anticholinergic bronchodilator: a randomized trial. Ann Intern Med. 2005;143:317–26. van Noord JA, Bantje TA, Eland ME, Korducki L, Cornelissen PJ: A randomised controlled comparison of tiotropium nd ipratropium in the treatment of chronic obstructive pulmonary disease.The Dutch Tiotropium Study Group. Thorax 2000, 55:289-294 Vincken W, van Noord JA, Greefhorst AP, Bantje TA, Kesten S, Korducki L, et al. Improved health outcomes in patients with COPD during 1 yr’s treatment with tiotropium. Eur Respir J. 2002;19:209–16. Vogelmeier C, Hederer B, Glaab T, Schmidt H, Rutten-van Molken MP, Beeh KM, et al. Tiotropium versus salmeterol for the prevention of exacerbations of COPD. N Engl J Med. 2011;364:1093–103. Decramer M, Celli B, Kesten S, Lystig T, Mehra S, Tashkin DP: Effect of tiotropium on outcomes in patients with moderate chronic obstructive pulmonary disease (UPLIFT): a prespecified subgroup analysis of a randomised controlled trial.Lancet 2009, 374:1171-1178. Troosters T, Celli B, Lystig T, Kesten S, Mehra S, Tashkin DP, et al. Tiotropium as a first maintenance drug in COPD: secondary analysis of the UPLIFT trial. Eur Respir J. 2010;36:65–73. Tashkin DP, Celli BR, Decramer M, Lystig T, Liu D, Kesten S: Efficacy of tiotropium in COPD patients with FEV1 >/= 60 % participating in the UPLIFT(R) trial.COPD 2012, 9:289-296. Singh S, Loke YK, Enright PL, Furberg CD: Mortality associated with tiotropium mist inhaler in patients with chronic obstructive pulmonary disease: systematic review and meta-analysis of randomised controlled trials.BMJ 2011, 342:d3215. Dong YH, Lin HH, Shau WY, Wu YC, Chang CH, Lai MS: Comparative safety of inhaled medications in patients with chronic obstructive pulmonary disease: systematic review and mixed treatment comparison meta-analysis of randomised controlled trials.Thorax 2013, 68:48-56. Tashkin DP, Celli B, Senn S, Burkhart D, Kesten S, Menjoge S, et al. A 4-year trial of tiotropium in chronic obstructive pulmonary disease. N Engl J Med. 2008;359:1543–54. Wise RA, Anzueto A, Cotton D, Dahl R, Devins T, Disse B, et al. Tiotropium Respimat inhaler and the risk of death in COPD. N Engl J Med. 2013;369:1491–501. D’Urzo A, Ferguson GT, van Noord JA, Hirata K, Martin C, Horton R, et al. Efficacy and safety of once-daily NVA237 in patients with moderate-to-severe COPD: the GLOW1 trial. Respir Res. 2011;12:156. Kerwin E, Hebert J, Gallagher N, Martin C, Overend T, Alagappan VK, et al. Efficacy and safety of NVA237 versus placebo and tiotropium in patients with COPD: the GLOW2 study. Eur Respir J. 2012;40:1106–14. Jones PW, Singh D, Bateman ED, Agusti A, Lamarca R, de Miquel G, et al. Efficacy and safety of twice-daily aclidinium bromide in COPD patients: the ATTAIN study. Eur Respir J. 2012;40:830–6. Kerwin EM, D’Urzo AD, Gelb AF, Lakkis H, Garcia Gil E, Caracta CF: Efficacy and safety of a 12-week treatment with twice-daily aclidinium bromide in COPD patients (ACCORD COPD I).COPD 2012, 9:90-101. Decramer M, Maltais F, Feldman G, Brooks J, Harris S, Mehta R, et al. Bronchodilation of umeclidinium, a new long-acting muscarinic antagonist, in COPD patients. Respir Physiol Neurobiol. 2013;185:393–9. Mahler DA, Donohue JF, Barbee RA, Goldman MD, Gross NJ, Wisniewski ME, et al. Efficacy of salmeterol xinafoate in the treatment of COPD. Chest. 1999;115:957–65. Rennard SI, Anderson W, ZuWallack R, Broughton J, Bailey W, Friedman M, et al. Use of a long-acting inhaled beta2-adrenergic agonist, salmeterol xinafoate, in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2001;163:1087–92. Calverley PM, Anderson JA, Celli B, Ferguson GT, Jenkins C, Jones PW, et al. Salmeterol and fluticasone propionate and survival in chronic obstructive pulmonary disease. N Engl J Med. 2007;356:775–89. Dahl R, Greefhorst LA, Nowak D, Nonikov V, Byrne AM, Thomson MH, et al. Inhaled formoterol dry powder versus ipratropium bromide in chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2001;164:778–84. Lombardi D, Cuenoud B, Kramer SD: Lipid membrane interactions of indacaterol and salmeterol: do they influence their pharmacological properties?Eur J Pharm Sci 2009, 38:533-547. Dahl R, Chung KF, Buhl R, Magnussen H, Nonikov V, Jack D, et al. Efficacy of a new once-daily long-acting inhaled beta2-agonist indacaterol versus twice-daily formoterol in COPD. Thorax. 2010;65:473–9. Donohue JF, Fogarty C, Lotvall J, Mahler DA, Worth H, Yorgancioglu A, et al. Once-daily bronchodilators for chronic obstructive pulmonary disease: indacaterol versus tiotropium. Am J Respir Crit Care Med. 2010;182:155–62. Kornmann O, Dahl R, Centanni S, Dogra A, Owen R, Lassen C, et al. Once-daily indacaterol versus twice-daily salmeterol for COPD: a placebo-controlled comparison. Eur Respir J. 2011;37:273–9. Koch A, Pizzichini E, Hamilton A, Hart L, Korducki L, De Salvo MC, et al. Lung function efficacy and symptomatic benefit of olodaterol once daily delivered via Respimat(R) versus placebo and formoterol twice daily in patients with GOLD 2–4 COPD: results from two replicate 48-week studies. Int J Chron Obstruct Pulmon Dis. 2014;9:697–714. ZuWallack R, Allen L, Hernandez G, Ting N, Abrahams R: Efficacy and safety of combining olodaterol Respimat((R)) and tiotropium HandiHaler((R)) in patients with COPD: results of two randomized, double-blind, active-controlled studies.Int J Chron Obstruct Pulmon Dis 2014, 9:1133-1144. Ferguson GT, Feldman GJ, Hofbauer P, Hamilton A, Allen L, Korducki L, et al. Efficacy and safety of olodaterol once daily delivered via Respimat(R) in patients with GOLD 2–4 COPD: results from two replicate 48-week studies. Int J Chron Obstruct Pulmon Dis. 2014;9:629–45. Buhl R, Dunn LJ, Disdier C, Lassen C, Amos C, Henley M, et al. Blinded 12-week comparison of once-daily indacaterol and tiotropium in COPD. Eur Respir J. 2011;38:797–803. Decramer ML, Chapman KR, Dahl R, Frith P, Devouassoux G, Fritscher C, et al. Once-daily indacaterol versus tiotropium for patients with severe chronic obstructive pulmonary disease (INVIGORATE): a randomised, blinded, parallel-group study. The Lancet Respiratory medicine. 2013;1:524–33. Karner C, Cates CJ: Long-acting beta(2)-agonist in addition to tiotropium versus either tiotropium or long-acting beta(2)-agonist alone for chronic obstructive pulmonary disease.Cochrane Database Syst Rev 2012., 4Article ID CD008989 Celli B, Crater G, Kilbride S, Mehta R, Tabberer M, Kalberg CJ, et al. Once-daily umeclidinium/vilanterol 125/25 mcg in COPD: a randomized, controlled study. Chest. 2014. Donohue JF, Maleki-Yazdi MR, Kilbride S, Mehta R, Kalberg C, Church A: Efficacy and safety of once-daily umeclidinium/vilanterol 62.5/25 mcg in COPD.Respir Med 2013, 107:1538-1546. Donohue JF, Niewoehner D, Brooks J, O’Dell D, Church A. Safety and tolerability of once-daily umeclidinium/vilanterol 125/25 mcg and umeclidinium 125 mcg in patients with chronic obstructive pulmonary disease: results from a 52-week, randomized, double-blind, placebo-controlled study. Respir Res. 2014;15:78. Maleki-Yazdi MR, Kaelin T, Richard N, Zvarich M, Church A: Efficacy and safety of umeclidinium/vilanterol 62.5/25 mcg and tiotropium 18 mcg in chronic obstructive pulmonary disease: results of a 24-week, randomized, controlled trial.Respir Med 2014, 108:1752-1760. Rodrigo GJ, Plaza V: Efficacy and safety of indacaterol and Glycopyrronium in COPD: an update.Chest 2014., 146Article ID e75 Rodrigo GJ, Plaza V: Efficacy and safety of a fixed-dose combination of indacaterol and Glycopyrronium for the treatment of COPD: a systematic review.Chest 2014, 146:309-317. Vincken W, Aumann J, Chen H, Henley M, McBryan D, Goyal P: Efficacy and safety of coadministration of once-daily indacaterol and glycopyrronium versus indacaterol alone in COPD patients: the GLOW6 study.Int J Chron Obstruct Pulmon Dis 2014, 9:215-228. Barnes PJ: Theophylline for COPD.Thorax 2006, 61:742-744. Culpitt SV, de Matos C, Russell RE, Donnelly LE, Rogers DF, Barnes PJ: Effect of theophylline on induced sputum inflammatory indices and neutrophil chemotaxis in chronic obstructive pulmonary disease.Am J Respir Crit Care Med 2002, 165:1371-1376. Hirano T, Yamagata T, Gohda M, Yamagata Y, Ichikawa T, Yanagisawa S, et al. Inhibition of reactive nitrogen species production in COPD airways: comparison of inhaled corticosteroid and oral theophylline. Thorax. 2006;61:761–6. Kobayashi M, Nasuhara Y, Betsuyaku T, Shibuya E, Tanino Y, Tanino M, et al. Effect of low-dose theophylline on airway inflammation in COPD. Respirology. 2004;9:249–54. Ito K, Lim S, Caramori G, Cosio B, Chung KF, Adcock IM, et al. A molecular mechanism of action of theophylline: Induction of histone deacetylase activity to decrease inflammatory gene expression. Proc Nat Acad Sci U S A. 2002;99:8921–6. Ito K, Ito M, Elliott WM, Cosio B, Caramori G, Kon OM, et al. Decreased histone deacetylase activity in chronic obstructive pulmonary disease. N Engl J Med. 2005;352:1967–76. Cosio BG, Tsaprouni L, Ito K, Jazrawi E, Adcock IM, Barnes PJ: Theophylline restores histone deacetylase activity and steroid responses in COPD macrophages.J Exp Med 2004, 200:689-695. Ito K, Yamamura S, Essilfie-Quaye S, Cosio B, Ito M, Barnes PJ, et al. Histone deacetylase 2-mediated deacetylation of the glucocorticoid receptor enables NF-kappaB suppression. J Exp Med. 2006;203:7–13. Celli BR, Thomas NE, Anderson JA, Ferguson GT, Jenkins CR, Jones PW, et al. Effect of pharmacotherapy on rate of decline of lung function in chronic obstructive pulmonary disease: results from the TORCH study. Am J Respir Crit Care Med. 2008;178:332–8. Miravitlles M, Soler-Cataluna JJ, Calle M, Soriano JB: Treatment of COPD by clinical phenotypes: putting old evidence into clinical practice.Eur Respir J 2013, 41:1252-1256. Bettoncelli G, Blasi F, Brusasco V, Centanni S, Corrado A, De Benedetto F, De Michele F, Di Maria GU, Donner CF, Falcone F, et al.: The clinical and integrated management of COPD. An official document of AIMAR (Interdisciplinary Association for Research in Lung Disease), AIPO (Italian Association of Hospital Pulmonologists), SIMER (Italian Society of Respiratory Medicine), SIMG (Italian Society of General Medicine). Multidisciplinary respiratory medicine 2014, 9:25. Wedzicha JA, Calverley PM, Seemungal TA, Hagan G, Ansari Z, Stockley RA: The prevention of chronic obstructive pulmonary disease exacerbations by salmeterol/fluticasone propionate or tiotropium bromide.Am J Respir Crit Care Med. 2008, 177:19-26. Calverley PM, Stockley RA, Seemungal TA, Hagan G, Willits LR, Riley JH, et al. Reported pneumonia in patients with COPD: findings from the INSPIRE study. Chest. 2011;139:505–12. Fukuchi Y, Samoro R, Fassakhov R, Taniguchi H, Ekelund J, Carlsson LG, et al. Budesonide/formoterol via Turbuhaler(R) versus formoterol via Turbuhaler(R) in patients with moderate to severe chronic obstructive pulmonary disease: phase III multinational study results. Respirology. 2013;18:866–73. Larsson K, Janson C, Lisspers K, Jorgensen L, Stratelis G, Telg G, et al. Combination of budesonide/formoterol more effective than fluticasone/salmeterol in preventing exacerbations in chronic obstructive pulmonary disease: the PATHOS study. J Intern Med. 2013;273:584–94. Martinez FJ, Boscia J, Feldman G, Scott-Wilson C, Kilbride S, Fabbri L, et al. Fluticasone furoate/vilanterol (100/25; 200/25 mug) improves lung function in COPD: a randomised trial. Respir Med. 2013;107:550–9. Magnussen H, Disse B, Rodriguez-Roisin R, Kirsten A, Watz H, Tetzlaff K, et al. Withdrawal of inhaled glucocorticoids and exacerbations of COPD. N Engl J Med. 2014;371:1285–94. Spina D: PDE4 inhibitors: current status.Br J Pharmacol 2008, 155:308-315. Calverley PM, Rabe KF, Goehring UM, Kristiansen S, Fabbri LM, Martinez FJ: Roflumilast in symptomatic chronic obstructive pulmonary disease: two randomised clinical trials.Lancet 2009, 374:685-694. Fabbri LM, Calverley PM, Izquierdo-Alonso JL, Bundschuh DS, Brose M, Martinez FJ, et al. Roflumilast in moderate-to-severe chronic obstructive pulmonary disease treated with longacting bronchodilators: two randomised clinical trials. Lancet. 2009;374:695–703. Chong J, Poole P, Leung B, Black PN: Phosphodiesterase 4 inhibitors for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2011. doi:10.1002/14651858.CD002309.pub3. Вам также может понравиться Если вы ищете захватывающее путешествие в мир фэнтези Как мужчина в свои 26 лет, я всегда искал игры, которые Как любитель компьютерных игр и поклонник вселенной Привет, друзья! Меня зовут Макс, и сегодня я хочу поделиться |