Сосуды головы и шеи. Анатомия. Видеоатлас доктора Роберта Акланда. Часть 1, 2.
Сосуды головы и шеи. Анатомия. Видеоатлас доктора Роберта Акланда. Часть 1, 2.
Сосуды головы и шеи. Часть 1. Автор лекции профессор В. А. Изранов
Сосуды головы и шеи. Часть 2. Автор лекции профессор В. А. Изранов
АРТЕРИИ ГОЛОВЫ И ШЕИ
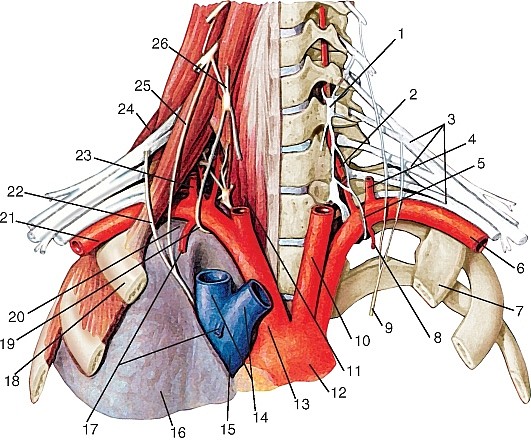
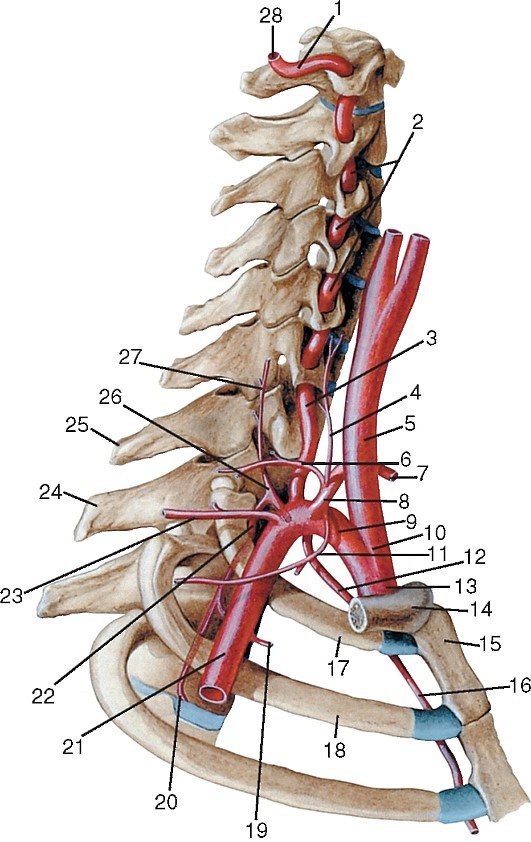
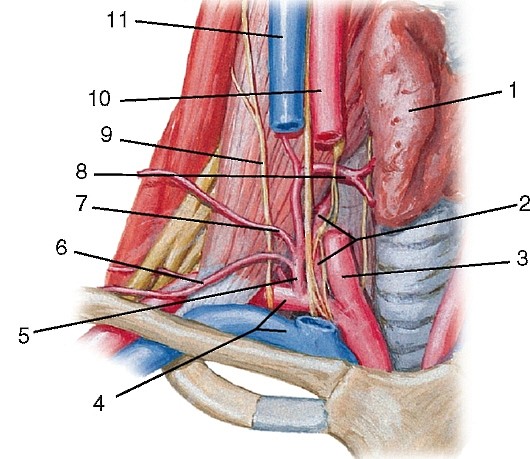
Ветви первого отдела (рис. 179):
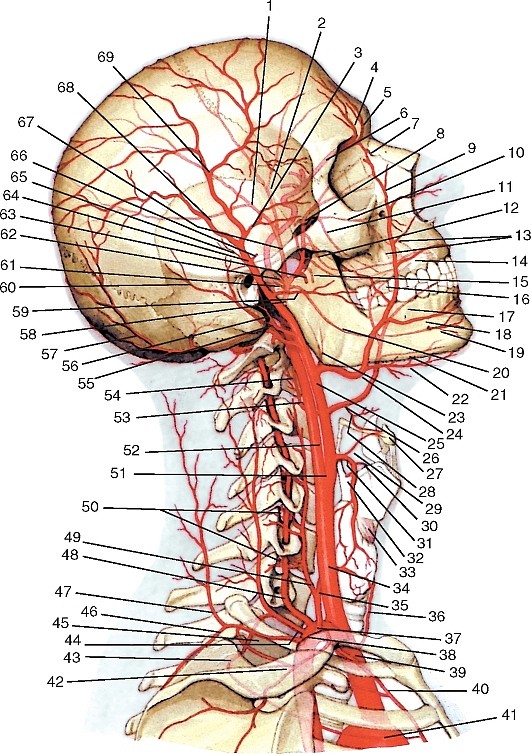
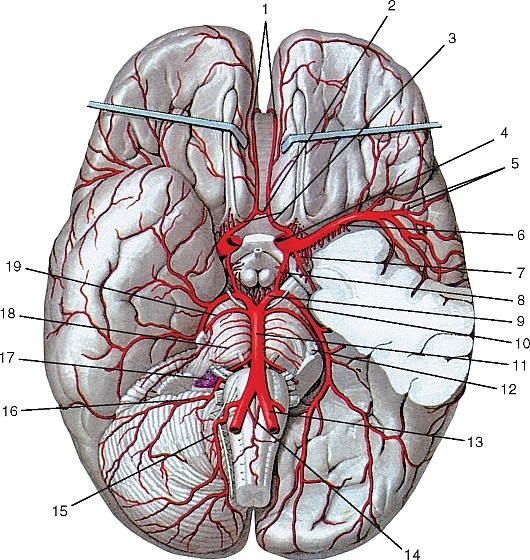
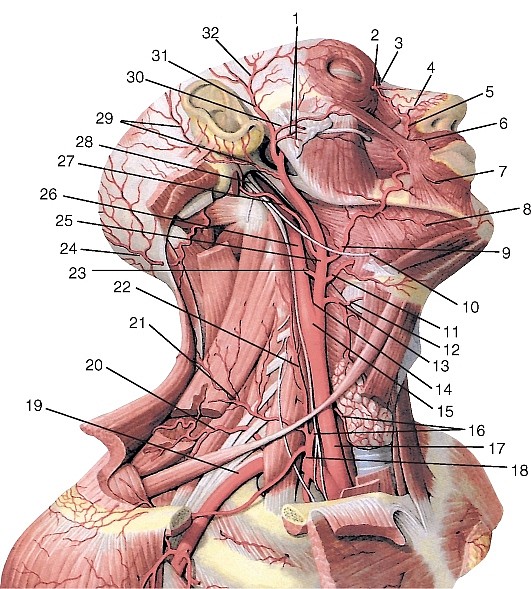
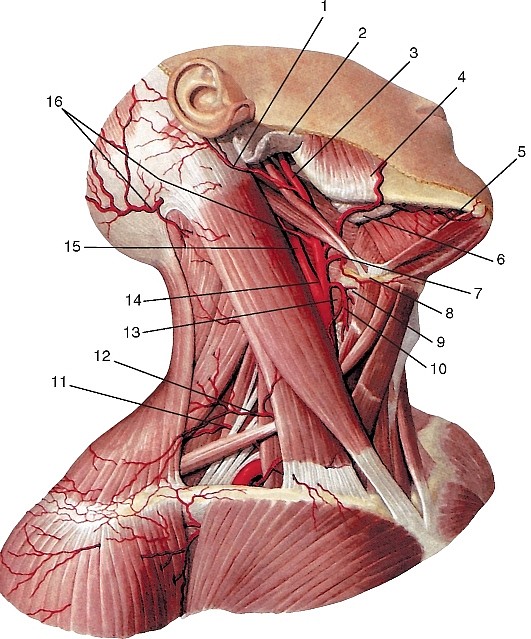
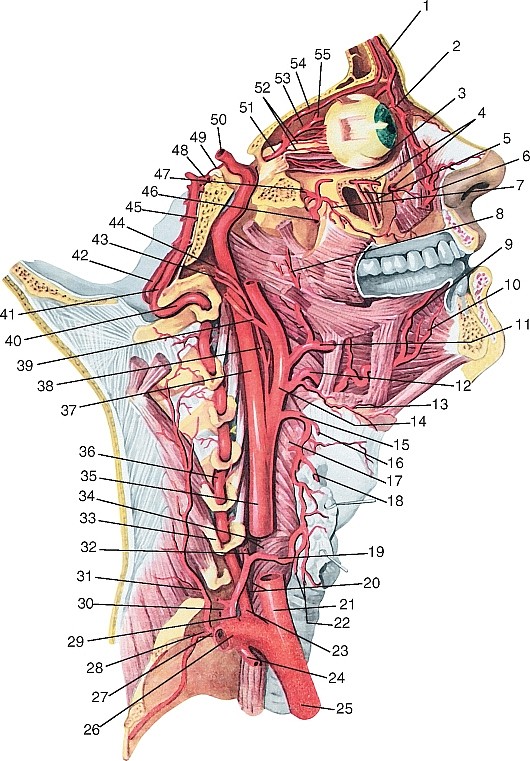
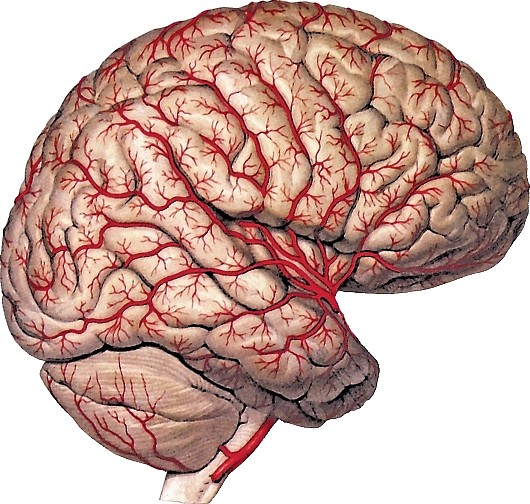
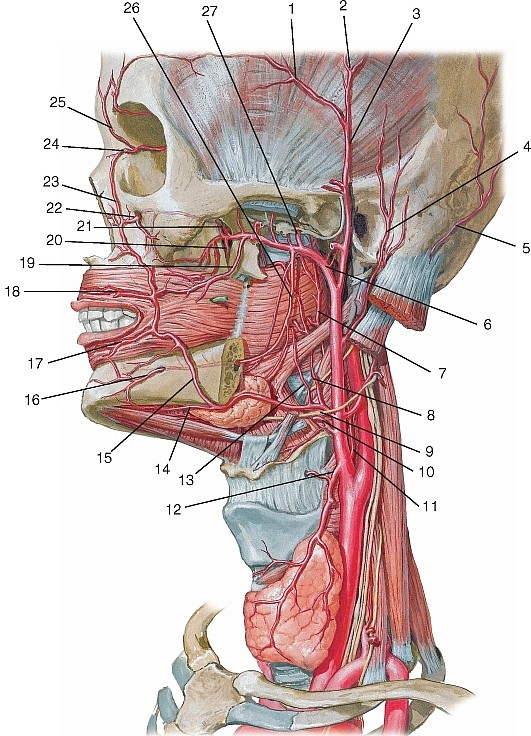
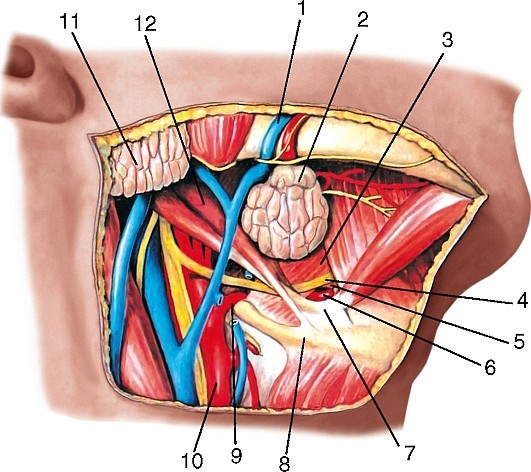
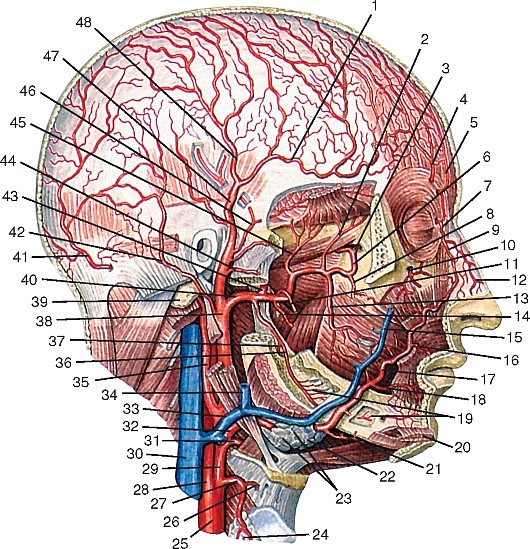
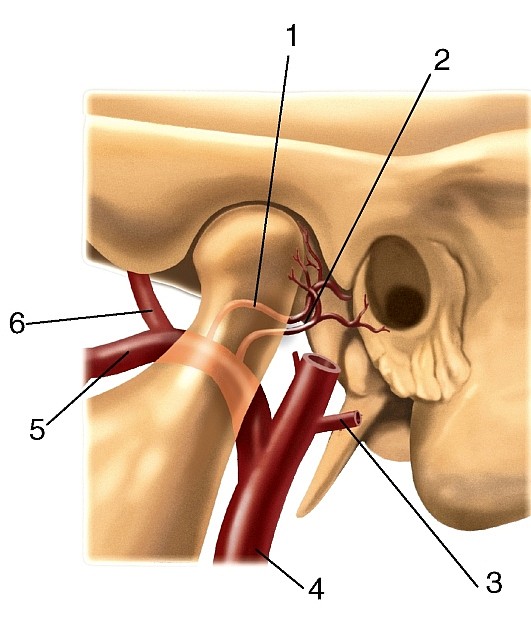
Рис. 177. Общий вид артерий головы и шеи, вид справа (схема):
Ветви базилярной артерии:
3) задняя мозговая артерия (a. cererbriposterior), посылающая артерии затылочной доле конечного мозга.
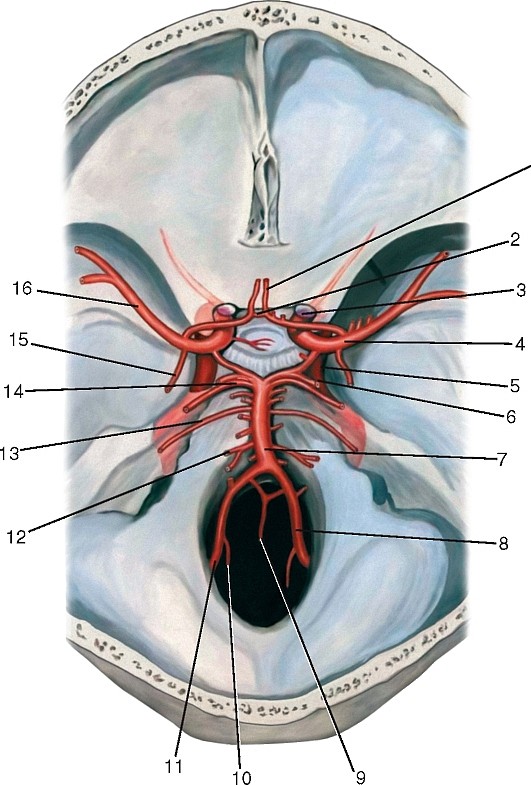
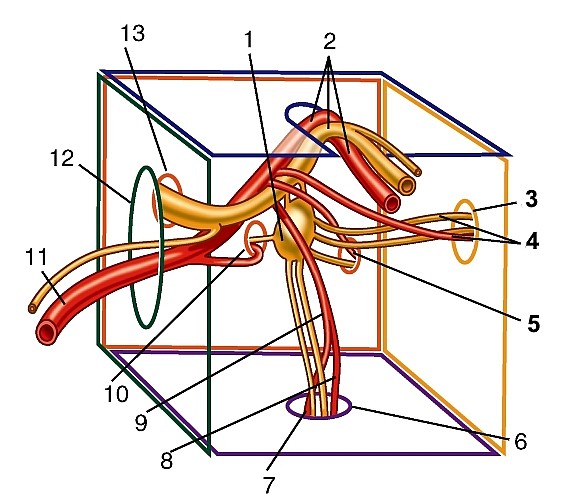
Рис. 180. Ветви базилярной и внутренней сонной артерий в полости черепа, вид со стороны полости черепа:
2) восходящую шейную (a. cervicalis ascendens);
Артерии третьего отдела (см. рис. 179).
Внутренняя сонная артерия (a. carotis interna) парная, отходит от общей сонной артерии на уровне верхнего края щитовидного хряща; в артерии выделяют 4 части: шейную, каменистую, пещеристую и мозговую (рис. 186, 187, см. рис. 177, 180, 181).
На шее внутренняя сонная артерия сначала располагается латеральнее наружной сонной артерии, затем направляется кверху и медиальнее ее, идет между внутренней яремной веной (снаружи) и глот кой (изнутри) и достигает наружной апертуры сонного канала. На шее ветвей не отдает. Каменистая часть (pars pertrosa) расположена в сонном канале пирамиды височной кости и окружена густыми венозным и нервным сплетениями; здесь артерия переходит из вертикального положения в горизонтальное. В пределах канала от нее отходят сонно-барабанные артерии (аа. caroticotimpanicae), проникающие через отверстия в стенке канала в барабанную полость, где они анастомозируют с передней барабанной и шилососцевидной артериями.
Задняя соединительная артерия (a. communicans posterior) соединяет внутреннюю сонную артерию с задней мозговой артерией (см. рис. 180, 181).
Передняя мозговая артерия (a. cerebri anterior) идет на медиальную поверхность лобной доли мозга, прилегая сначала к обонятельному треугольнику, затем в продольной щели большого мозга переходит на верхнюю поверхность мозолистого тела; кровоснабжает конечный мозг. Недалеко от своего начала правая и левая передние мозговые артерии соединяются посредством передней соединительной артерии (a. communicans anterior) (см. рис. 181, 188).
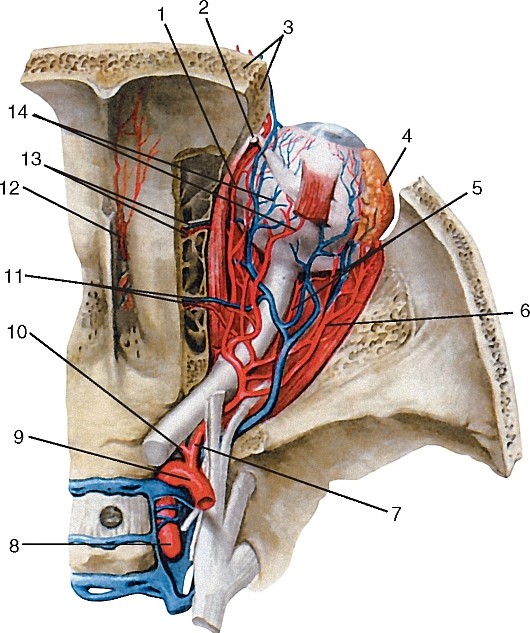
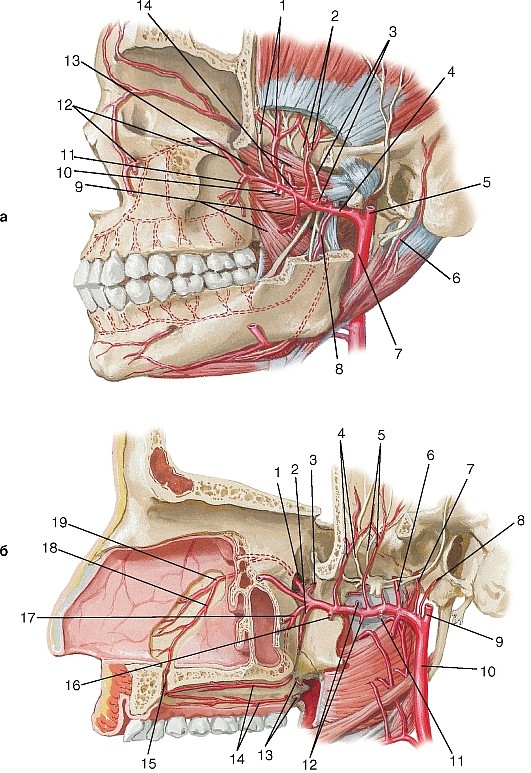
Рис. 186. Внутренняя сонная артерия, вид справа:
Средняя мозговая артерия (a. cerebri media) более крупная, располагается в латеральной борозде, по которой восходит вверх и латерально; отдает ветви к конечному мозгу (см. рис. 181, 189).
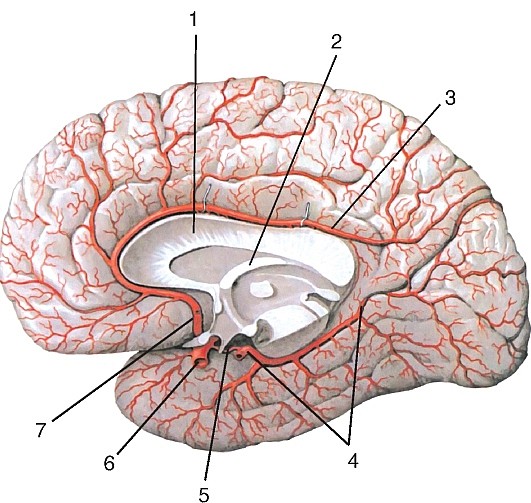
Рис. 188. Артерии на медиальной и нижней поверхностях полушария головного мозга:
Рис. 189. Ветви средней мозговой артерии на дорсолатеральной поверхности полушария головного мозга
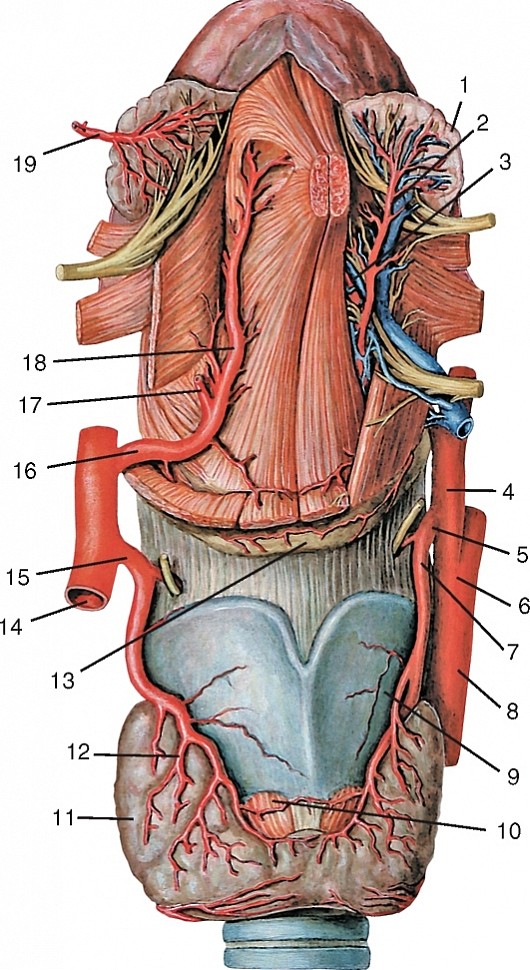
Верхняя щитовидная артерия (a. thyroidea superior) отходит вблизи бифуркации общей сонной артерии ниже большого рога подъязычной кости, идет дугообразно вперед и вниз к верхнему полюсу щитовидной железы (рис. 191, см. рис. 177, 184, 186). Анастомозирует с нижней щитовидной артерией и верхней щитовидной артерией противоположной стороны. Отдает подподъязычную ветвь (r. infrahyoideus), грудино-ключично-сосцевидную ветвь (r. sternocleidomastoideus) и верхнюю гортанную артерию (а. laringea superior), сопровождающую верхний гортанный нерв и кровоснабжающую мышцы и слизистую оболочку гортани выше голосовой щели.
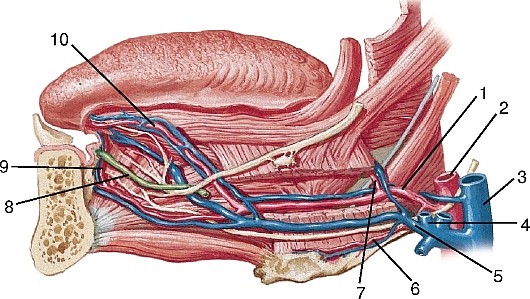
Рис 192. Язычная артерия, вид слева:
От лицевой артерии отходят артерии к соседним органам:
1) восходящая нёбная артерия (а. palatina ascendens) идет кверху между шилоглоточной и шилоязычной мышцами, проникает через глоточно-базилярную фасцию и снабжает кровью мышцы глотки, нёбную миндалину, мягкое нёбо;
2) миндаликовая ветвь (r. tonsillaris) прободает верхний констриктор глотки и разветвляется в глоточной миндалине и корне языка (см. рис. 186);
3) железистые ветви (rr. glandulares) идут к поднижнечелюстной слюнной железе;
4) подподбородочная артерия (а. submentalis) отходит от лицевой артерии у места ее перегиба через основание нижней челюсти и идет кпереди под челюстно- подъязычной мышцей, отдавая ветви к ней и к двубрюшной мышце, затем подходит к подбородку, где разделяется на поверхностную ветвь к подбородку и глубокую ветвь, перфорирующую челюстно-подъязычную мышцу и кровоснабжающую дно полости рта и подъязычную слюнную железу;
5) нижняя губная артерия (а. labialis inferior) ответвляется ниже угла рта, извилисто продолжается между слизистой оболочкой нижней губы и круговой мышцей рта, соединяясь с одноименной артерией другой стороны; дает ветви к нижней губе;
6) верхняя губная артерия (а. labialis superior) отходит на уровне угла рта и проходит в подслизистом слое верхней губы; анастомозирует с одноименной артерией противоположной стороны, составляя околоротовой артериальный круг.
Отдает ветви к верхней губе.
На лице наружная сонная артерия располагается в занижнечелюстной ямке, в паренхиме околоушной слюнной железы или глубже нее, кпереди и латеральнее внутренней сонной артерии. На уровне шейки нижней челюсти она разделяется на конечные ветви: верхнечелюстную и поверхностную височную артерии.
1) поперечная артерия лица (a. transversa faciei) ответвляется в толще околоушной слюнной железы ниже наружного слухового прохода, выходит из-под переднего края железы вместе со щечными ветвями лицевого нерва и разветвляется над протоком железы; кровоснабжает железу и мышцы лица. Анастомозирует с лицевой и подглазничной артериями;
2) скулоглазничная артерия (а. zygomaticifacialis) отходит выше наружного слухового прохода, идет вдоль скуловой дуги между пластинками височной фасции к латеральному углу глазной щели; кровоснабжает кожу и подкожные образования в области скуловой кости и глазницы;
3) средняя височная артерия (a. temporalis media) отходит над скуловой дугой, перфорирует височную фасцию; кровоснабжает височную мышцу; анастомозирует с глубокими височными артериями.
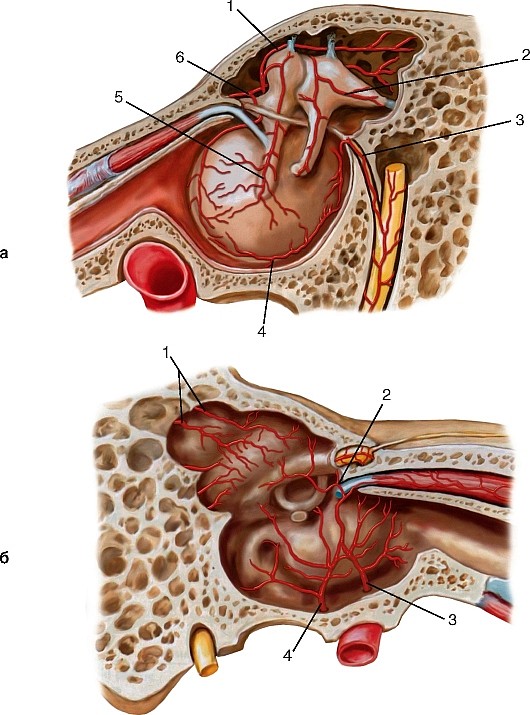
Рис. 195. Артерии среднего уха:
Глубокая ушная артерия (a. auricularis profunda) проходит назад и кверху к наружному слуховому проходу, отдаёт ветви к барабанной перепонке.
Передняя барабанная артерия (a. tympanica anterior) проникает по барабанно- чешуйчатой щели в барабанную полость, снабжает кровью её стенки и барабанную перепонку. Нередко отходит общим стволом с глубокой ушной артерией.
Анастомозирует с артерией крыловидного канала, шилососцевидной и задней барабанной артериями.
Средняя менингеальная артерия (a. meningea media) поднимается между крыловидно-нижнечелюстной связкой и головкой нижней челюсти по медиальной поверхности латеральной крыловидной мышцы, между корешками ушно- височного нерва к остистому отверстию и через него входит в твёрдую оболочку головного мозга. Обычно залегает в борозде чешуи височной кости и борозде теменной кости. Разделяется на ветви: теменную (r. parietalis), лобную (r. frontalis) и глазничную (r. orbitalis). Анастомозирует с внутренней сонной артерией через анастомотическую ветвь со слезной артерией (r. anastomoticum cum a. lacrimalis). Отдаёт также каменистую ветвь (r. petrosus) к тройничному узлу, верхнюю барабанную артерию (a. tympanica superior) к барабанной полости.
Глубокие височные артерии, передняя и задняя (aa. temporales profundae anterior et posterior) идут в височную ямку, располагаясь между височной мышцей и костью. Кровоснабжают височную мышцу. Анастомозируют с поверхностной и средней височными и слезной артериями.
Крыловидные ветви (rr. pterygoidei) снабжают кровью крыловидные мышцы.
Щечная артерия (a. buccalis) проходит вместе со щечным нервом вперед между медиальной крыловидной мышцей и ветвью нижней челюсти к щечной мышце, в которой разделяется; анастомозирует с лицевой артерией.
Ветви крыловидно-нёбной части (рис. 198, см. рис. 186):
Задняя верхняя альвеолярная артерия (a. alveolaris superior posterior) отходит в месте перехода верхнечелюстной артерии в крыловидно- нёбную ямку позади бугра верхней челюсти. Через задние верхние альвеолярные отверстия проникает в кость; разделяется на зубные ветви (rr. dentales), проходящие вместе с задними верхними альвеолярными нервами в альвеолярные каналы в заднелатеральной стенке верхней челюсти к корням верхних больших коренных зубов. От зубных ветвей отходят околозубные ветви (rr. peridentales) к тканям, окружающим корни зубов.
Подглазничная артерия (a. infraorbitalis) ответвляется в крыловидно- нёбной ямке, являясь продолжением ствола верхнечелюстной артерии, сопровождает подглазничный нерв. Вместе с подглазничным нервом через нижнюю глазничную щель входит в глазницу, где располагается в одноименной борозде и в канале.
Выходит через подглазничное отверстие в клыковую ямку. Конечные ветви снабжают кровью прилежащие лицевые образования. Анастомозируют с глазной, щечной и лицевой артериями. В глазнице посылает ветви к глазным мышцам, слёзной железе. Через одноименные каналы верхней челюсти отдает передние верхние альвеолярные артерии (aa. alveolares superiors anterior et posterior), от которых к корням зубов и околозубным образованиям (rr. peridentales) направляются зубные ветви (rr. dentales).
Артерия крыловидного канала (a. canalis pterygoidei) нередко отходит от нисходящей нёбной артерии, направляется в одноименном канале вместе с одноименным нервом к верхнему отделу глотки; кровоснабжает слуховую трубу, слизистую оболочку барабанной полости и носовую часть глотки.
Нисходящая нёбная артерия (a. palatine descendens) проходит в большом небном канале, где разделяется на большую нёбную артерию (a. palatine major) и малые нёбные артерии (aa. palatinae minores), выходящие, соответственно, через большое и малые нёбные отверстия на нёбо. Малые нёбные артерии идут к мягкому нёбу, а большая распространяется кпереди, кровоснабжает твердое нёбо и оральные поверхности десен. Анастомозирует с восходящей нёбной артерией.
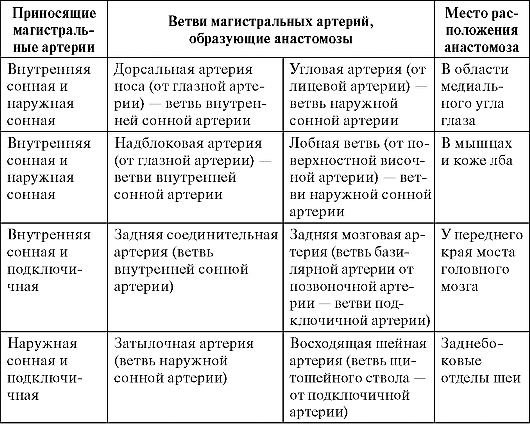
Клиновидно-нёбная артерия (a. sphenopalatina) идет через одноименное отверстие в носовую полость и разделяется на задние носовые латеральные артерии (aa. nasalis posteriors laterales) и задние перегородочные ветви (rr. septales posteriors). Кровоснабжает задние ячейки решетчатого лабиринта, слизистую оболочку боковой стенки носовой полости и перегородки носа; анастомозирует с большой нёбной артерией (табл. 13).
Таблица 13. Межсистемные анастомозы артерий головы и шеи
Вопросы для самоконтроля
1. Какие ветви отходят от подключичной артерии в каждом из отделов?
2. Какие ветви позвоночной артерии вы знаете? С какими артериями она анастомозирует?
4. Какие части топографически различают во внутренней сонной артерии?
5. Какие ветви отходят от каждой части внутренней сонной артерии?
6. Какие артерии кровоснабжают содержимое глазницы?
7. Какими артериями образуется артериальный круг большого мозга?
8. Как можно представить себе топографию наружной сонной артерии?
9. Какие передние ветви наружной сонной артерии вам известны?
11. Какие артерии отходят от лицевой артерии? Какие анастомозы имеет лицевая артерия?
12. Какие артерии отходят от верхнечелюстной артерии в каждой ее части?
13. Какие вы знаете анастомозы верхнечелюстной артерии?
Вентрикулоперитонеальное шунтирование
Данная операция выполняется при лечении гидроцефалии
Гидроцефалия – грозное заболевание, сопровождающееся увеличением желудочковой системы головного мозга, обусловленное нарушением нормального оттока спинномозговой жидкости (ликвора), либо дисбалансом в процессе ее формирования и резорбции.
В настоящее время применяются несколько видов ликворошунтирующих операций в зависимости от типа гидроцефалии. Наиболее распространённым и общепринятым методом лечения является методика вентрикулоперитонеального шунтирования (ВПШ), направленная на создание дополнительного «обходного» пути для оттока ликвора из желудочковой системы головного мозга. С этой целью могут быть использованы более 200 разновидностей шунтирующих систем, известных в настоящее время.
Вне зависимости от технических нюансов выполнения операции, конечным итогом ВПШ является создание искусственного оттока ликвора из расширенных желудочков в брюшную полость. В некоторых случаях с целью снижения риска травматизации органов брюшной полости, при наличии спаечного процесса после перенесенных ранее полостных операций, возможно использование лапароскопических методик.
Вне зависимости от моделей, все клапанные шунтирующие системы разделяются на три основных типа в зависимости от уровня ликворного давления или, другими словами, «пропускной способности». Выбор оптимального давления для конкретного пациента всегда является краеугольными камнем в достижении необходимого лечебного эффекта, так как неправильный подбор системы может приводить к недостаточному или, напротив, избыточному дренированию спинномозговой жидкости.
Существенным подспорьем в решении данной проблемы явилось появление современных шунтирующих систем с программируемыми клапанами. Технически, данная операция не отличается существенно от стандартного вентрикулоперитонеального шунтирования. Секрет заключается в специальном антисифонном устройстве в клапане шунта с возможностью дистанционного контроля за степенью дренирования и соответственно, внутричерепным давлением пациента.
Во время нахождения в стационаре, лечащим врачом осуществляется стартовый подбор необходимого уровня давления. Однако, для достижения оптимального лечебного эффекта могут потребоваться несколько повторных визитов к врачу с целью коррекции и подбора необходимой «пропускной способности». Этот фактор является ограничивающим для иногородних пациентов, проживающих на большом отдалении от клиники.
142. Анатомия и топография мозолистого тела, свода мозга, спайки, внутренней капсулы, их место в функциях центральной нервнойсистемы.
Под мозолистым телом находится свод, fornix (рис. 141). Свод состоит из двух дугообразно изогнутых тяжей, соединенных в средней своей части при помощи поперечно идущих волокон — спайки, comissura. Средняя часть свода носит название тела, corpus; кпереди и книзу оно продолжается в округлый парный тяж — столб, columna, свода. Столб свода направляется вниз и несколько латерально до основания мозга, где заканчивается в правом и левом сосцевидных телах. Кзади тело свода продолжается в также парный плоский тяж — ножку свода, crus fornicis, сращенную с нижней поверхностью мозолистого тела. Парная ножка свода на правой и на левой стороне постепенно уходит латерально и вниз, отделяется от мозолистого тела, еще больше уплощается и одной своей стороной срастается с гиппокампом, образуя бах ромку гиппокампа, fimbria hippocampi. Другая часть бахромки свободна и обращена в полость нижнего рога бокового желудочка. Оканчивается бахромка гиппокампа в крючке, соединяя, таким образом, височную долю конечного мозга с промежуточным мозгом.
Впереди свода в сагиттальной плоскости располагается прозрачная перегородка, septum pellucidum, которая состоит из двух пластинок, лежащих параллельнр друг другу. Каждая пластинка прозрачной перегородки, lamina septi pellucidi, натянута между телом и столбом свода сзади, мозолистым телом вверху, коленом и клювом мозолистого тела спереди и снизу. Между пластинками прозрачной перегородки находится щелевидная полость прозрачной перегородки, cavum septi pellucidi, содержащая прозрачную жидкость. Пластинка прозрачной перегородки служит медиальной стенкой переднего рога бокового желудочка. Впереди столбов свода находится передняя спайка, comissura rostralis [anterior>, волокна которой ориентированы поперечно. На сагиттальном разрезе спайка имеет форму небольшого овала. Передняя часть спайки тонкая, соединяет серое вещество обонятельных треугольников обоих полушарий. Большая задняя часть содержит нервные волокна, связывающие кору переднемедиальных отделов височных долей.
К белому веществу полушария относятся волокна, которые соединяют различные участки коры в пределах одного полушария (ассоциативные волокна) или кору с подкорковыми центрами дан-, ного полушария. Наряду с короткими ассоциативными нервными волокнами в белом веществе различают крупные длинные пучки, имеющие продольную ориентацию и соединяющие далеко отстоящие друг от друга участки коры большого мозга.
Патогенез
Наиболее значимым фактором риска поражения мелких сосудов головного мозга является артериальная гипертензия [23]. При дисциркуляторной энцефалопатии встречаются как первичные сосудистые, так и вторичные дегенеративные изменения вещества головного мозга.
Выделяют несколько видов патологических изменений вещества головного мозга, ассоциированных с хроническим ишемическим повреждением [2,29,42].
Атеросклероз поражает артерии эластического и крупные артерии мышечного типа. В большинстве случаев атеросклероз приводит к развитию острых нарушений мозгового кровообращения с быстрым развитием выраженных очаговых симптомов. В патогенезе хронических сосудистых заболеваний головного мозга основное значение имеет поражение микроциркуляторного русла. Оно образовано терминальными ветвями крупных артерий каротидного и вертебрально-базилярного бассейна, а также притоками церебральных вен. Артерии микроциркуляторного русла подвержены изменениями при резких перепадах артериального давления поскольку на этом уровне не образуются анастомозы.
Болезнь мелких сосудов или микроангиопатия может иметь различной этиологии:
В ряде случаев, нарушения микроциркуляции могут быть вызваны патологией со стороны системы крови, без поражения кровеносных сосудов. Истинная полицитемия, гемоглобинопатии или протеинопатии могут повышать вязкость крови, что приводит к сопротивлению кровотоку и агрегации форменных элементов, является причиной церебральной ишемии. В редких случаях возможно развитие микроэмболии. Важными дополнительными факторами могут быть нарушения обмена веществ, прежде всего, сахарный диабет и нарушение венозного оттока.
Нарушения ауторегуляции мозгового кровообращения являются как причиной, так и следствием поражения микрососудов, принимая участие в порочном круге патологических изменений.
Лейкоареоз — нейровизуализационный термин (снижение рентгеновской плотности на КТ головного мозга, повышение интенсивности сигнала по данным МРТ в Т2/FLAIR режимах), описывающий неспецифические изменения подкоркового белого вещества головного мозга. Выявляются двусторонние очаговые, иногда сливные изменения. В основе лейкоареоза лежит поражение мелких артерий и артериол вследствие липогиалиноза (также обозначается как артериосклероз) и микроатероматоза [11].
Факторами риска развития лейкоареоза являются возраст, повышенное артериальное давление и сахарный диабет [18]. Повышение внутрижелудочкового давления рассматривается в качестве дополнительного механизма развития лейкоареоза, оно приводит к нарушению микроциркуляции в прилегающих к желудочкам участках головного мозга. У пациентов с нормотензивной гидроцефалией отмечаются распространённые изменения подкоркового белого вещества [21].
Доказана связь распространенности диффузных изменений белого вещества головного мозга с выраженностью депрессии и когнитивных нарушений [9,43].
В препаратах головного мозга лейкоареоз часто сочетается с расширением периваскулярных (Вирхова-Робина) пространств — криблюрами (‘etát criblé’). Этот феномен связывают с повторными эпизодами ишемии и плазматического пропитывания участков ткани, окружающих микрососуды.
Липогиалиноз — дистрофический процесс, поражающий пенетрирующие артерии и артериолы диаметром до 200 мкм. Протекает под действием повышения артериального давления, гипергликемии, а также вследствие возрастных изменений. Повышение тканево-сосудистой проницаемости в субэндотелиальном пространстве сосуда приводит к поступлению туда белков плазмы и адсорбции их на изменённых волокнистых структурах соединительной ткани с последующей преципитацией и образованием белка гиалина. В последующем, гиалин оттесняет и разрушает эластичную мембрану, средняя оболочка истончается, и перфорирующая артерия приобретает вид стекловидной трубочки. Просвет артерии резко сужается, возможно развитие окклюзии.
При развитии липогиалиноза фоне сахарного диабета субэндотелиально часто откладывается не только гиалин, но и липиды. Сосудистая стенка инфильтрируется макрофагами с включениям фагоцитированных липидов — пенистыми клетками. В изменённых тканях происходит отложение фибриноида (сложного вещества, состоящего из белков и полисахаридов, распадающихся коллагеновых волокон, межклеточного вещества и плазмы крови). В неблагоприятных условиях происходит гибель окружающих тканей — фибриноидный некроз. Этот патологических процесс выявляется в артериолах и капиллярах головного мозга, сетчатки и почек часто сочетается с гиалинозом.
Этот патологический процесс, видимо является реактивным феноменом. Он не рассматривается, как ведущая причина гипертонического внутричерепного кровоизлияния, так как в препаратах головного мозга в случаях острого внутричерепного кровоизлияния не обнаруживается на отдалении от гематомы. В лабораторных исследованиях выраженные изменения по типу фибриноидного некроза выявлялись вокруг стереотаксически введенных тромбов в опытах у грызунов, что могло указывать на его реактивное происхождение.
Вследствие нарушения работы ассоциации эндотелиоцит-глиальная клетка (астроцит)-нейрон (»нейроваскулярное звено«) страдают механизмы ауторегуляции мозгового кровотока на уровне капилляров и микроартериол. Это приводит к сужению диапазона допустимых показателей перфузии. Из-за того, что мелкие сосуды утрачивают способность расширяться, становится невозможным перераспределение кровотока в пользу активно работающих отделов мозга, а это в свою очередь приводит к их функциональной инактивации, а затем – и к необратимому повреждению. Преимущественное поражение белого вещества в перивентрикулярном и глубинных отделах при церебральной гипоперфузии объясняется особым характером их кровоснабжения сосудами терминального типа, не имеющими коллатералей.
Клетки нервной ткани различаются по чувствительности к ишемии. При нарушении кровотока, некротические изменения развиваются сначала в нейронах, затем олигодендроцитах, миелинизированных аксонах, астроцитах и наконец в эндотелиальных клетках [38]. После гибели наиболее чувствительных типов клеток — нейронов и олигодендроцитов, относительно резистентные к ишемии астроциты, выполняющие в головном мозге опорную функцию, замещают дефект за счёт увеличения в объёме своих отростков. Формируется глиальный рубец (»неполный» инфаркт») [33]. При тотальной гибели всех элементов участка мозговой ткани формируется участок некроза (лакуна), на периферии регенерация глиальных клеток формирует его «оболочку».
В патологоанатомических исследованиях отмечена связь липогиалиноза мелких артерий с лакунарными инфарктами головного мозга. Указывается на более высокую распространённость расширенных периваскулярных пространств у пациентов с сосудистой деменцией, чем у пациентов с болезнью Альцгеймера [30]. У здоровых пожилых пациентов с выявленными расширенными периваскулярными пространствами отмечались худшие результаты тестирования когнитивных функций.
Микроатероматоз — атеросклеротическое поражение артериол, приводит к развитию более крупных лакунарных инфарктов. В зависимости от локализации, инфаркты могут проявляться клиникой инсульта, но чаще (примерно в 80 % случаев) протекают субклинически (»немые» инфаркты)[40]. У части пациентов основные патологические процессы вызываются церебральной амилоидной ангиопатией (ЦАА) — отложением амилоидных пептидов (прежде всего Аβ — амилоида) в мышечной оболочке и адвентиции микрососудов и сосудов среднего калибра, значительно реже в стенках капилляров и вен.
Частота выявления амилоидоза церебральных артерий на аутопсии с возрастом увеличивается: на основании серии из 784 аутопсийных материалов, признаки умеренной и тяжёлой ЦАА встречались с частотой 2.3% в возрасте от 65 до 74 лет, 8.0% в возрасте от 75 до 84 лет, и 12.1% в возрасте старше 85 лет [14].
Значимых половых различий во встречаемости амилоидоза не выявлено. Несмотря на то, что вопрос связи ЦАА с артериальной гипертензией продолжает обсуждаться, очевидно, что в большом количестве случаев у пациентов при жизни отмечалось нормальное артериальное давление[3].
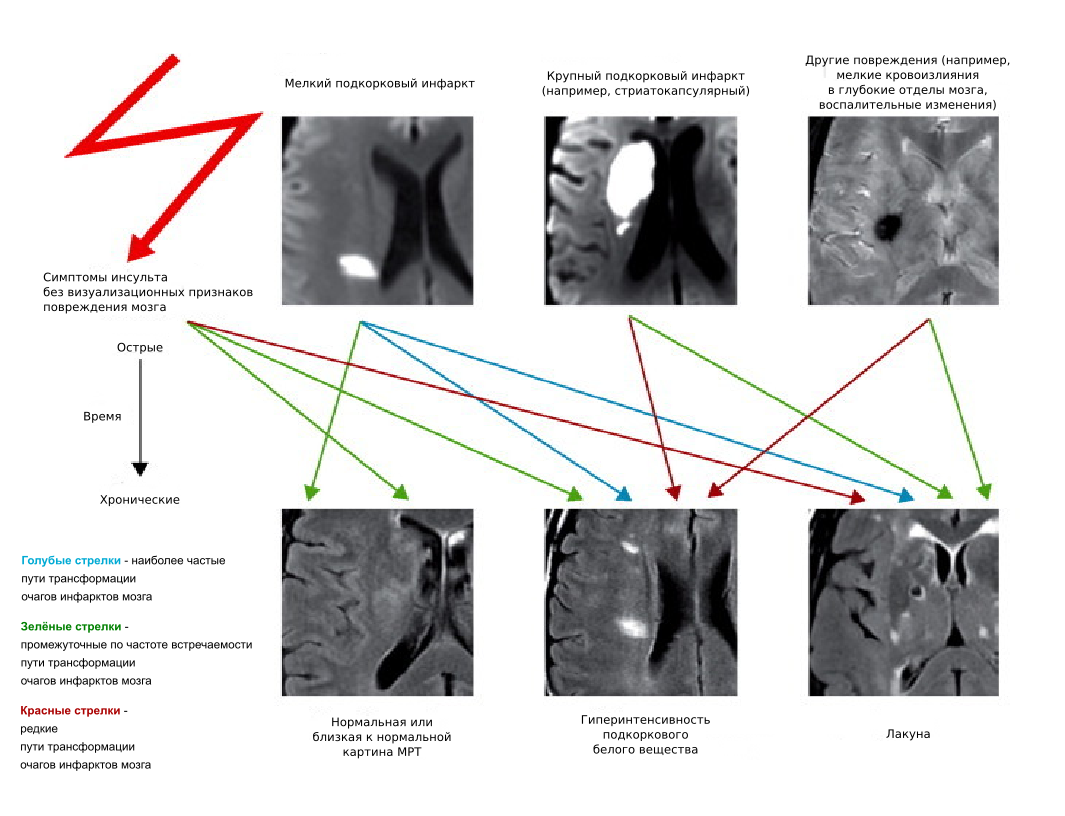
Рисунок 1. Пути трансформации мелких сосудистых очагов и сходство МРТ картины отдалённых последствий поражения мозга различной природы
Предполагается, что амилоидные пептиды, блокируют отток по переваскулярным пространствам, выполняющим в головном мозге дренажную функцию. Повышение ломкости стенки сосудов при отложении амилоида значительно увеличивает риск внутримозговых кровоизлияний. Они, как правило, имеют небольшие размеры и располагаются кнаружи от внутренней капсулы, в белом веществе больших полушарий, для сравнения, гипертонические кровоизлияния поражают преимущественно область подкорковых ядер. В связи с таким расположением микрокровоизлияний при ЦАА, подкорковые структуры остаются относительно интактными, поэтому, экстрапирамидные симптомы не характерны для клиники этого состояния. По данным Фрамингемского исследования установлена связь деменции и внутримозговых микрокровоизлияний, которая не зависела от выраженности других сердечно-сосудистых факторов риска. Наличие ЦАА предполагается у пациентов старше 55–60 лет с множественными лобарными кровоизлияниями без другой явной причины.
Бостонские критерии для кровоизлияний, связанных с церебральной амилоидной ангиопатией [19]
* приём варфарина с превышением целевого значения МНО (> 3,0), перенесённые инсульты и черепно-мозговые травмы, опухоли головного мозга, сосудистые аномалии и васкулиты, патология системы крови, коагулопатии [41].
У пациентов с подозрением на церебральную амилоидную ангиопатию, развитие острых и транзиторных неврологических нарушений может быть связано с геморрагическими осложнениями, что стоит принимать во внимание при планировании их обследования.
У пациентов с выраженным лейкоареозом и множественными лакунарными инфарктами в отсутствии факторов риска сосудистых заболеваний стоит предположить наличие церебральной аутосомно-доминантной артериопатии с подкорковыми инфарктами и лейкоэнцефалопатией (CADASIL) — наследственного заболевания, вызванного мутацией гена Notch 3 на 19-й хромосоме. У трети пациентов, страдающих этим заболеванием, отмечается мигрень с аурой, которая рассматривается как раннее проявление заболевания. Приблизительно у 75% лиц, носителей мутации, в конечном счёте развивается деменция[27].
Таким образом, хронические сосудистые поражения головного мозга определяются большим количеством факторов риска, как генетических, так и средовых. Профиль факторов риска развития дисциркуляторной энцефалопатии и инсульта не тождественны. Поражение артерий мозга может быть и изолированным — встречается у пациентов без поражения прецеребральных артерий и артериальной гипертензии.
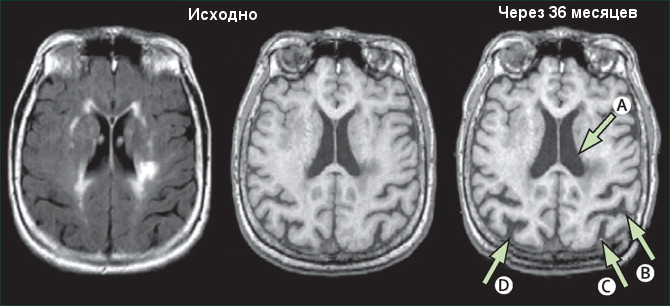
Рисунок 2. Динамика атрофических изменений вещества головного мозга
В патогенезе развития основных симптомов дисциркуляторной энцефалопатии (когнитивных нарушений, нарушений ходьбы, пирамидных и мозжечковых знаков, псевдобульбарного синдрома) лежит разобщение корковых и подкорковых структур вследствие поражения подкоркового белого вещества больших полушарий. Нарушается работа корково-подкорковых кругов, обеспечивающих последовательную избирательную активизацию отдельных участков коры головного мозга при выполнении сложных многоэтапных действий, поддерживающих общий уровень активности коры, несущих информацию для коррекции действий на стадии афферентного синтеза и исполнения (функции I [энергетического] и III [программирование, регуляция и контроль] блоков по А. Р. Лурия).
Клинико-нейровизуализационные соответствия
Термин «энцефалопатия» предполагает наличие не только субъективных жалоб, но и объективных признаков органического поражения мозга, выявляемых при неврологическом или нейропсихологическом исследовании [2]. Вместе с тем, обнаружение подобных признаков, даже вкупе с сосудистыми факторами риска, клиническими или параклиническими признаками цереброваскулярной патологии является необходимым, но недостаточным признаком ДЭП. Важнейшим принципом диагностики ДЭП должна стать констатация причинно-следственной связи между имеющимися у больного клиническими проявлениями и цереброваскулярным заболеванием.
Подобный принцип впервые был заложен в критерии клинической диагностики сосудистой деменции NINDS-AIREN. Представляется, что только следование этому принципу позволит избежать гипердиагностики ДЭП и отделить случаи ДЭП от нейродегенеративных заболеваний, широко представленных у лиц пожилого возраста (в первую очередь от болезни Альцгеймера или болезни Паркинсона, набор симптомов которых на начальных стадиях может соответствовать последствиям хронического сосудистого поражения головного мозга).
Доказательством причинно-следственной связи могут служить:
КТ или МРТ головного мозга при ДЭП могут выявить: двустороннее более или менее симметричное диффузное поражение белого вещества (лейкоареоз) в перивентрикулярной зоне, зрительной лучистости, семиовальном центре; множественные лакунарные очаги (размером 3–15 мм) в базальных ганглиях, таламусе, мосте, мозжечке, внутренней капсуле, белом веществе лобных долей; более крупные корковые и подкорковые инфаркты, отражающие патологию крупных артерий. Церебральная атрофия, выявляемая при КТ или МРТ у больных ДЭП, обычно сопровождает лейкоареоз, лакунарые или территориальные инфаркты [2]. Как правило, расширение желудочковой системы при ДЭП более выражено, чем расширение корковых борозд, и может отражать не только убыль мозгового вещества в глубинных отделах мозга, но и, возможно, снижение резистентности перивентрикулярных тканей к ликвородинамическим воздействиям [2].
В ряде исследований выявлена связь между тяжестью и/или локализацией нейровизуализационных изменений и выраженностью когнитивных и двигательных нарушений [18]. Так, показано, что умеренное когнитивное расстройство возникает, когда распространенность лейкоареоза превышает как минимум 10% белого вещества полушарий, а деменция – если распространенность лейкоареоза превысит 1/4 объема белого вещества полушарий. При наличии лакун выраженность когнитивных нарушений зависит не столько от числа лакунарных очагов, сколько от их локализации (глубинные отделы лобных долей, головка хвостатого ядра и переднее бедро внутренней капсулы, таламус). Выраженность когнитивных нарушений увеличивается при двустороннем поражении указанных структур и сочетании лакунарных очагов с лейкоареозом. Более того, должно быть соответствие между нейровизуализационными изменениями и профилем когнитивных нарушений. Например, в отсутствие соответствующих корковых очагов на КТ и МРТ у пациентов не должны выявляться признаки очагового поражения корковых функций: афазии, апраксии и агнозии. Отмечена также связь между распространенностью лейкоареоза, особенно в передних отделах мозга, локализацией лакунарных очагов в чечевицеобразном ядре и выраженностью нарушений ходьбы и равновесия.
Выраженность когнитивных и двигательных нарушений при ДЭП коррелирует и со степенью расширения боковых желудочков и особенно их передних рогов. С другой стороны, отсутствие сосудистых изменений на МРТ при клинической картине I-III стадий ДЭП и КТ при клинической картине II – III стадий ДЭП может заставлять усомниться в диагнозе. Данные КТ и МРТ имеют значение не только в диагностике ДЭП, но и могут помочь отслеживать динамику заболевания, быть маркером эффективности мер по коррекции факторов риска сердечно-сосудистых осложнений [2]. Отдельные нейровизуализационные феномены считаются нормальным проявлением старения: [12,42]