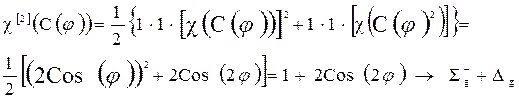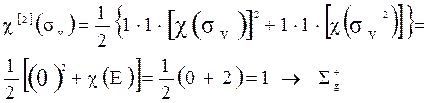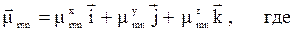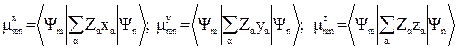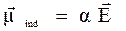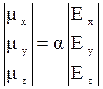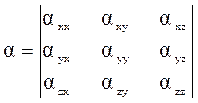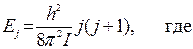Что такое линейные молекулы
Одним из важнейших свойств ковалентной связи является её направленность. Она определяет пространственную структуру молекул. Если в молекуле имеется больше одной ковалентной связи, то двухэлектронные облака связей вступают во взаимодействие друг с другом. Представляя собой заряды одного знака, они отталкиваются друг от друга, стремясь занять такое положение в пространстве, когда их взаимное отталкивание будет минимальным. Если в первом приближении считать отталкивание всех облаков одинаковым, то в зависимости от числа взаимодействующих облаков (связей) наиболее выгодным расположением будет:
Это наиболее распространенные геометрические формы многоатомных молекул (рис. 8).
Часто в образовании связей участвуют различные электроны, например `s` и `p`—электроны. Казалось бы, образующиеся связи тоже должны быть неравноценными. Однако опыт показывает, что все связи одинаковы. Теоретическое обоснование этого факта было предложено Слейтером и Полингом, которые ввели понятие гибридизации атомных орбиталей. Они показали, что при участии в образовании связей нескольких различных орбиталей, незначительно отличающихся по энергии, можно заменить их тем же количеством одинаковых орбиталей, называемых гибридными. При этом орбитали смешиваются и выравниваются по энергии. Изменяется и первона-чальная форма электронных облаков: гибридные орбитали асимметричны и сильно вытянуты по одну сторону от ядра.
В этом соединении атому бериллия нужно образовать две связи с атомами хлора. Он переходит в возбужденное состояние и его электронная пара, находящаяся на `2s`-орбитали, распаривается:
Орбитали, занятые валентными электронами, гибридизуются по типу `sp`-гибридизации, в результате чего изменяется их первоначальная форма, они становятся одинаковыми как по форме, так и по энергии, и в таком состоянии способны образовывать более прочные связи за счёт наиболее полного перекрывания с `p`-орбиталями атомов хлора:
Однако нужно отметить, что для данного соединения употреблять термин «молекула» можно только тогда, когда хлорид бериллия находится в газообразном состоянии.
`3sp^2(«B»)+p(«Cl»)+p(«Cl»)+p(«Cl»)->3` ковалентные связи `»B»-«Cl»`.
Разница между линейными и изогнутыми молекулами
В ключевое отличие между линейными и изогнутыми молекулами заключается в том, что линейные молекулы имеют атомы, связанные друг с другом, образуя прямую молекулу, тогда как изогнутые молекулы имеют ат
Содержание:
В ключевое отличие между линейными и изогнутыми молекулами заключается в том, что линейные молекулы имеют атомы, связанные друг с другом, образуя прямую молекулу, тогда как изогнутые молекулы имеют атомы, расположенные в форме изгиба под углом.
Термины линейные молекулы и изогнутые молекулы описывают формы различных молекул. Мы можем разделить различные химические соединения на разные группы в зависимости от формы молекулы; линейные, угловые / изогнутые, плоские, пирамидальные и т. д. Линейные и изогнутые формы являются самыми простыми среди них.
Что такое линейные молекулы?
Что такое изогнутые молекулы?
Обычно мы можем наблюдать нелинейное расположение молекул в трехатомных молекулах и ионах, содержащих только основные элементы группы. Искривленная структура этих молекул является результатом наличия неподеленных электронных пар в центральном атоме. Наиболее распространенные примеры изогнутых молекул включают воду, диоксид азота, CH2 и т. Д.
В чем разница между линейными и изогнутыми молекулами?
Ключевое различие между линейными и изогнутыми молекулами заключается в том, что в линейных молекулах атомы связаны друг с другом, образуя прямую молекулу, тогда как в изогнутых молекулах атомы расположены в форме изгиба под углом. Кроме того, линейные молекулы представляют собой прямые молекулы, имеющие угол связи 180 градусов, в то время как изогнутые молекулы представляют собой угловые молекулы, имеющие угол связи менее 180 градусов.
Следующая инфографика резюмирует разницу между линейными и изогнутыми молекулами.
Разница между линейными и нелинейными молекулами
В ключевое отличие между линейными и нелинейными молекулами заключается в том, что линейные молекулы имеют прямую химическую структуру, тогда как нелинейные молекулы имеют зигзагообразную или поперечн
Содержание:
В ключевое отличие между линейными и нелинейными молекулами заключается в том, что линейные молекулы имеют прямую химическую структуру, тогда как нелинейные молекулы имеют зигзагообразную или поперечно-сшитую химическую структуру.
Все известные нам молекулы можно разделить на два типа: линейные и нелинейные, в зависимости от формы молекулы. Если химическая структура молекулы имеет линейную геометрию, которая выглядит как прямая линия, то это линейная молекула. Все остальные молекулы относятся к категории нелинейных молекул.
Что такое линейные молекулы?
При рассмотрении органических соединений, имеющих линейную геометрию, в центре молекулы находится атом углерода, и лиганды связываются с атомом углерода посредством двойных или тройных связей. Здесь центральный атом имеет sp-гибридизацию атомных орбиталей, например. ацетилен. Помимо них существуют также линейные неорганические соединения; например, диоксид углерода, цианистый водород и др.
Что такое нелинейные молекулы?
При рассмотрении сложных молекул, таких как полимеры, они также могут быть линейными или нелинейными. Большинство нелинейных полимеров представляют собой разветвленные или сшитые полимеры. Разветвленные полимеры имеют боковые группы или боковые группы, присоединенные к прямой линии атомов. Сшитые полимеры имеют поперечные связи между прямыми линиями полимерных цепей, образуя сетчатые структуры.
В чем разница между линейными и нелинейными молекулами?
Все известные нам молекулы можно разделить на два типа: линейные и нелинейные, в зависимости от формы молекулы. Ключевое различие между линейными и нелинейными молекулами состоит в том, что линейные молекулы имеют прямую химическую структуру, тогда как нелинейные молекулы имеют зигзагообразную или сшитую химическую структуру.
Ацетилен, диоксид углерода, цианистый водород и т. Д. Являются некоторыми примерами линейных молекул, тогда как разветвленные и сшитые полимеры, такие как вулканизированный каучук, являются примерами нелинейных молекул.
В следующей таблице приведены различия между линейными и нелинейными молекулами.
Резюме: линейные и нелинейные молекулы
Все известные нам молекулы можно разделить на два типа: линейные и нелинейные, в зависимости от формы молекулы. Ключевое различие между линейными и нелинейными молекулами состоит в том, что линейные молекулы имеют прямую химическую структуру, тогда как нелинейные молекулы имеют зигзагообразную или сшитую химическую структуру.
Линейные молекулы



В молекулах, как и в атомах, используется метод молекулярных орбиталей (МО) для представления волновой функции:
и неприводимое представление, к которому относится Yмол., определяется в виде произведения неприводимых представлений орбиталей:
В этом произведении нужно рассматривать только представления МО, заполненных одним электроном. Посколько двухкратнозанятые МО всегда дают полносимметричное представление. Т.о. симметрия молекул с замкнутыми оболочками, т.е. когда на каждой Мо находится по два электрона, всегда отвечает полносимметричному представлению точечной группы симметрии.
Симметрия электронного состояния систем с открытыми оболочками наиболее просто определяется в случае заполнения неспаренными электронами МО, соответствующих одномерным неприводимым представлениям. Здесь для определения симметрии состояния нужно перемножить только неприводимые представления, соответствующих МО.
Более сложный случай определения симметрии систем с открытыми оболочками – неспаренные электроны расположены на вырожденной МО. Например: молекула О2, у которой два электрона расположены на дважды вырожденной Мо (pg). Методика нахождения симметрии терма здесь такая же, как и в случае атомов. Представление записывается как:
| D¥h | Е | C(j) | C2 | sh | S(j) | i | sv |
| Г(О2) | 4cos 2 j | 4cos 2 j | |||||
| 2+2cos2j | 2+2cos2j |
Учёт спинов приводит к триплетным или синглетным состояниям.
Рассмотрим синглетное состояние.
Теория кристаллического поля.
Это простейшая теоретическая модель используемая обычно для описания электронных спектров переходных металлов. По сути, это просто модель возмущения атомных орбиталей центрального атома электростатическим полем лигандов. Основная идея её состоит в отображении орбитальных представлений центрального атома (Rh(3)) на соответствующую группу точечной симметрии комплекса. Эта модель является достаточно грубой и т.о. позволяет описать наиболее важные характеристики спектров этих молекул. Комплексы с переходными металлами обладают частично-заполненной d-оболочкой, поэтому, необходимо рассматривать отображение представления d-орбиталей в группе Rh(3) на соответствующую точечную группу. Этим представлением является Dg(2).
[Далее в задачах рассмотреть молекулы MF3(D3h), MF4(Td), MF5(D3h). Система d-уровней. Определить термы MF3(M=Ti, V, Gr, Mn, Fe, Co.]
Правила отбора.
В соответствии с положениями квантовой механики любая наблюдаемая величина может быть вычислена в виде интеграла:
Если величина А – скаляр, то очевидно она не должна изменяться при всех операциях симметрии. Т.е. А должна быть инвариантна по отношению ко всем операциям симметрии. Это возможно, если интеграл áYi½Â½Yj ñ преобразуется по полносимметричному представлению группы. Если это условие не выполняется, то интеграл равен нулю. Таким образом, если через Гi, Г и Гj обозначить неприводимые представления, по которым преобразуются Yi,  и Yj, то представление по которому преобразуется интеграл будет вычисляться как

Представление Г содержит полносимметричное неприводимое представление в том случае, если произведение любых двух представлений содержит третье:
Именно на этом свойстве основаны правила отбора, позволяющие исходя из симметрии молекулы определить наблюдаемые полосы в электронных, колебательные и вращательных спектрах. Переходы между различными энергетическими уровнями связана с поглощением или испусканием кванта энергии. Интенсивность перехода пропорциональна величине дипольного момента перехода:
mmn, где 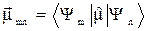
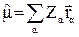
Компоненты дипольного момента – проекции на осо координат – скалярные величины. Следовательно, для того, чтобы они отличались от нуля необходимо выполнение условия:
Проникающие в вещество излучение может вызывать явления, отличные от поглощения или испускания, но сопровождающиеся изменением энергии системы. Это явление рассеяния света (спектры комбинационного рассеяния или рамановские). В этом случае в системе индуцируется переменный диполь. Величина этого индуцированного диполя пропорциональна величине напряженности падающей электромагнитной волны:
Используя декартово представление векторов это выражение можно записать как:
Правила отбора в электронном спектре.
Т.о. DJ = J’-J = ±1 при J=0 и
DJ = J’-J = 0, ±1 при J¹0.
В молекулах правила отбора для электронных переходов аналогичны атомным. Т.е. при DS=0 необходимо, чтобы выполнялось условие:
Однако нужно иметь в виду, что присутствие в молекуле тяжелых атомов может нарушить правило отбора по DS.
Вращательные спектры. В приближении жесткого ротатора энергия вращательных уровней определяется по формуле:
I – момент инерции, j – вращательное квантовое число. Волновые функции, вычисленные в приближении жесткого ротатора, имеют вид подобный волновым функциям, описывающим электронные состояния атома водорода. Поэтому и правила отбора аналогичны полученным ранее для электронных переходом в атомах. При этом, однако, нужно иметь в виду, что изменение вращательного квантового числа Dj=0 не имеет физического смысла (энергия не изменяется). Т.о. единственным имеющим физический смысл ограничением будет: Dj=±1.
В модели жесткого ротатора внутренние координаты молекулы не изменяются. Следовательно, постоянный дипольный момент молекулы так же не изменяется. В случае отсутствия у молекулы постоянного дипольного момента вращетельный спектр можно наблюдать только в спектрах комбинационного рассеяния.
Колебательные спектры. Колебания в молекулах представляют собой смещения ядер от положения равновесия. При равновесном положении конфигурация молекулы остается неизменной при любой операции симметрии соответствующей точечной группы. Т.о. волновая функция описывающая колебание молекулы на нулевом колебательном уровне, соответствующем неискаженной равновесной геометрии, преобразуется всегда по полносимметричному представлению. В то время как волновая функция в колебательно возбужденном состоянии преобразется по некому неприводимому представлению Г(Yn=n’) часто отличному от полносимметричного. Тогда произведение представлений волновых функций, отвечающих нулевому и возбужденному колебательным состояниям, равно:
Т.о переход из нулевого состояния в возбужденное будет виден в колебательном спектре поглощения или испускания если:
Большая Энциклопедия Нефти и Газа
Линейная молекула
Линейные молекулы или конденсируются друг с другом с образованием длинных цепей, или циклизуются. [1]
Линейная молекула является частным случаем симметричного волчка. [2]
Линейная молекула может принимать в растворе вид рыхлого, имеющего форму эллипсоида клубка 3, что приводит к получению заниженных молекулярных весов при измерении вязкости. Роговин и полагает, что форма цепей в растворах главным образом зависит от химической природы высокомолекулярного вещества, от природы растворителя и от концентрации раствора. [3]
Линейные молекулы обладают симметрией D mh или С, в зависимости от того, имеют ли они плоскость симметрии, перпендикулярную к оси молекулы, или не имеют ее. [5]
Линейные молекулы имеют только две вращательные степени свободы, поскольку они обладают осевой симметрией, а вращение вокруг оси симметрии не приводит к изменению положения; аналогично атомы, обладающие сферической симметрией, не имеют вращательных степеней свободы. [6]
Линейная молекула имеет эффект Штарка второго порядка. [7]
Линейные молекулы и молекулы типа симметричного волчка имеют одну ось симметрии порядка выше второго. [8]
Линейная молекула имеет эффект Штарка второго порядка. [11]
Линейная молекула имеет всего две вращательные степени свободы, соответствующие двум углам Эйлера 0 и ф, необходимым для описания ориентации молекулярной оси ( т.е. оси г) в пространстве, и отсутствие третьего угла Эйлера вызывает определенные трудности. Здесь для читателя было бы полезно еще раз вернуться к гл. [12]
Линейные молекулы обладают только двумя вращательными степенями свободы, которые соответствуют вращению молекулы относительно двух взаимно перпендикулярных осей. Легко понять, почему вопрос о третьей вращательной степени свободы даже не возникает. В двухатомной молекуле атомы имеют шесть степеней свободы, три из которых соответствуют смещению молекулы как целого, одна ответственна за колебания атомов вдоль линии связи, и, таким образом, для описания вращения остаются только две степени свободы. Аналогичные рассуждения применимы к любой линейной молекуле. Величину й2 / 2 / обычно обозначают буквой В и называют вращательной постоянной молекулы. Важно отметить, что расстояние между вращательными уровнями уменьшается с увеличением момента инерции ( так как при этом уменьшается В) и что уровень / расположен на расстоянии 2В ( / 1) от следующего уровня. [14]