Что такое кофактор фермента
Сукцинатдегидрогеназа (СДГ и КФ 1.3.5.1) представляет собой гетеротетрамерный ферментативный комплекс, который одновременно участвует в цикле Кребса и дыхательной цепи переноса электронов. Фермент играет центральную роль в клеточном метаболизме и преобразовании энергии. На шестой стадии цикла Кребса сукцинатдегидрогеназа катализирует реакцию окисления сукцината до фумарата с восстанавлением убихинона до убихинола. СДГ содержит ковалентно связанный кофактор ФАД. Активность фермента выявлена практически во всех исследованных организмах. Даже некоторые анаэробные прокариоты содержат множественные гены, кодирующие II комплекс дыхательной цепи. Впервые очищенный препарат растворимой СДГ из животных тканей был получен Сингером в 1954 г. [1].
В исследовании сукцинатдегидрогеназы важную роль играет выяснение механизмов регуляции активности СДГ не только на уровне белковой молекулы (воздействие на скорость ее функционирования различных метаболитов), но и регуляция фермента путем действия на генетический аппарат. Известно, что комплекс СДГ связан с внутренней мембраной митохондрий, имеет сложную структуру и состоит из 4 субъединиц, включая 2 гидрофильные субъединицы – СДГ-А и СДГ-Б, которые вместе образуют каталитический центр энзима, и 2 гидрофобные субъединицы – СДГ-С и СДГ-Д [2].
2.Сукцинатдегидрогеназа: структура, механизм катализа, регуляция активности
СДГ состоит из четырёх субъединиц, кодируемых ядерным геномом. Молекулярная масса составляет от 125кД до 140 кД. СДГ-С и СДГ-Д содержат гидрофобные компоненты, которые закрепляют комплекс на внутренней мембране митохондрий. Гидрофобные субъединицы С и Д — трансмембранные белки. Вместе они образуют цитохром b560, в шести трансмембранных α-спиралях которого расположен гем b и сайт связывания убихинона. Две молекулы фосфолипидов, один кардиолипин и один фосфатидилэтаноламин, которые заполняют гидрофобное пространство между субъединицами С и Д ниже гема b [2]. В сторону матрикса обращены субъединицы СДГ-А и СДГ-Б. Субъединица СДГ-А содержит ковалентно связанный ФАД и сайт для связыввания сукцината, а субъединица СДГ-Б содержит 3 железо-серных кластера: [2Fe-2S], [4Fe-4S] и [3Fe-4S], которые обеспечивают перенос электрона от сукцината к убихинону. В комплексе СДГ есть два убихинон-связывающих сайта. Сайт с высоким сродством образован субъединицами СДГ-Б, СДГ-С и СДГ-Д, расположенными вблизи со стороны матрицы внутренней митохондриальной мембраны. Сайт с низким сродством образован субъединицами СДГ-С и СДГ-Д, расположенными ближе к межмембранному пространству внутренней митохондриальной мембраны. Наконец, гем B, который расположен между СДГ-С и СДГ-Д, предположительно поглощает свободные электроны, чтобы предотвратить образование активных форм кислорода [4].
На субъединице A расположен сайт связывания и окисления сукцината. Сайт связывания сукцината и сайт связывания убихинона соединены цепочкой из редокс-центров, состоящей из ФАД и трёх железосерных кла-стеров. Эта цепочка простирается на 40 Å через всё тело фермента. Прибли-зительная дистанция между кофакторами не превышает физиологический предел для переноса электронов в 14 Å [2].
Установлено, что присутствие в структуре комплекса II всех субъединиц является необходимым требованием для обеспечения его стабильности. Исследования на дрожжах показали, что отсутствие одной из гидрофобных субъединиц СДГ приводит к значительному снижению обеих гидрофильных субъединиц, следовательно, каталитический центр, не может существовать как свободная димерная структура, без мембранного домена [5].
Все больше свидетельств указывает на то, что дыхательный комплекс II является источником и модулятором активных форм кислорода (АФК). Как потеря функций II комплекса, так и его фармакологическое ингибирование могут приводить к образованию активных форм кислорода в клетках, что оказывает существенное влияние на развитие патофизиологических состояний, то есть рака и нейродегенеративных заболеваний. Несмотря на то, что участие II комплекса в производстве АФК была определена, тонкие детали все еще ожидают прояснения. Важно разрешить эти аспекты, чтобы полностью понять роль II комплекса в патологии и изучить его терапевтический потенциал при раке и других заболеваниях [6].
2.2. Механизм катализа сукцинатдегидрогеназы
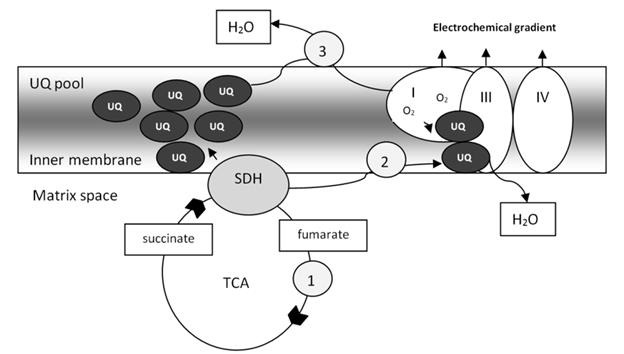
Сукцинатдегидрогеназа является ключевым ферментом в промежуточном метаболизме и преобразовании энергии в живых клетках. Митохондриальный комплекс СДГ катализирует окисление сукцината до фумарата в цикле Кребса и подает электроны в пул убихинона (UQ) дыхательной цепи (рис.1.). Этот фермент катализирует окисление сукцината до фумарата в цикле Кребса (1), а полученные электроны поступают в дыхательный комплекс III для восстановления кислорода и образования воды (2). Это создает электрохимический градиент через внутреннюю мембрану митохондрий, что позволяет синтезировать АТФ. Альтернативно, электроны могут быть направлены для уменьшения пула убихинона (пула UQ) и обеспечения восстанавливающих эквивалентов, необходимых для уменьшения супероксидных анионов, происходящих либо из экзогенного источника, либо из самой дыхательной цепи (3) [7].
Рисунок 1. Подача электронов в пул убихинона дыхательной цепи. [7].
В реакции окисления сукцината до фумарата два атома водорода удаляются из субстрата с помощью ФАД, протезной группы, которая тесно связана с сукцинатдегидрогеназой.
Два электрона из восстановленного комплекса СДГ-ФАДН2 переносятся на убихинон (Q). Затем убихинон восстанавливается до убихинола (QH2). Восстановленный убихинол окисляется комплексом III, а затем электроны переносятся через цитохром c в комплекс IV, где молеку-лярный кислород восстанавливается до воды. Протонная накачка комплекса-ми I, III и IV генерирует электрохимический градиент, который затем ис-пользуется для синтеза АТФ комплексом V (АТФ-синтаза).
Биохимические исследования выявили, что в СДГ митохондрий эука-риот имеется два сайта связывания убихинона [8]. Первый сайт – проксимальный (Qp) располагается на стороне матрицы митохондрий, обладает высоким сродством к убихинону и образован фрагментами СДГБ, СДГС и СДГД, а второй – дистальный (Qd) близок к межмембранному пространству, имеет слабое сродство к убихинону [2,9]. Восстановление убихинона протекает в два этапа: на первом происходит неполное восстановление семихинона (в качестве стабилизатора выступает проксимальный сайт) который восстанавливается до убихинола [2]. В реакции окисления сукцината до фумарата два атома водорода удаляются из субстрата флавинадениндинуклеотидом, протеиновой группой, прикрепленной к сукцинатдегидрогеназе. Два электрона из восстановленного комплекса СДГ ФАДH2 затем переносятся на убихинон растворимой части фермента электронно-транспортной системы. Происходит восстановление убихинона до убихинола. ФАД является неотъемлемым кофактором сукцинатдегидрогеназы. АТФ в митохондриях связывается с окисленным НАДН и ФАДH2 и восстановленным кислородом в воде дыхательной цепи митохондрий [10].
Транспортирование электронов от центра связывания сукцината с пер-вым или проксимальным хинонсвязывающим сайтом осуществляется вдоль цепи окислительно-восстановительных групп, которые включают ковалентно присоединенные ФАД и три кластера железо-серы [12].
В комплексе II расположены два различных активных центра и коор-динированный катализ на этих участках связывает два ключевых биологических пути, то есть окисление сукцината в цикле трикарбоновых кислот и восстановление хинона в цепи переноса электронов. Субъединица СДГА содержит ковалентно присоединенный ФАД-редокс-фрагмент и сайт связывания дикарбоксилата, где сукцинат окисляется до фумарата. Протоны этого окисления переносятся на растворитель, а фумарат действует как следующий субстрат в цикле Кребса. Электроны продукта катализа переносятся на 40 Å через три кластера железо-серы в белке СДГБ. Эти электроны действуют как сосубстраты на втором активном центре, расположенном на границе интегральных мембранных субъединиц. На этом хинон-восстанавливающем сайте, 2Н + и 2е- уменьшают убихинон до убихинола. Полученный пул хинола поддерживает синтез АТФ [13].
Два электрона, абстрагированные от дегидрирования сукцината, последовательно направляются в цепь переноса электронов от флавин-адениндинуклеотида до захваченного мембраной убихинона через кофакторы [2Fe-2S], [4Fe-4S], [3Fe-4S] и, возможно, гем b. Этот дальний, линейно-линейный электронный канал простирается более чем на 40 Å от растворимого каталитического домена СДГ до мембранно-закрепляющего домена фермента [2]. Участие гема b как части цепи переноса электронов не было четко установлено, поэтому функциональная значимость гема неясна [14].
2.3.Регуляция активности фермента сукцинатдегидрогеназы
Активность СДГ можно модулировать с помощью конкурентов сукцината, ингибиторов убихинона или посттрансляционных модификаций. Конкурентными ингибиторами сукцината являются малонат, малат и оксалоацетат. По структуре эти соединения похожи на сукцинат, что объясняет их способность конкурировать за связывание с активным центром СДГ. Примечательно, что как малат, так и оксалоацетат являются метаболитами цикла трикарбоновых кислот. Карбоксин и теноилтрифторацетон являются синтетическими ингибиторами убихинона, которые блокируют перенос электрона от комплекса СДГ к убихинону [4].
Что касается посттрансляционных модификаций, было показано, что фосфорилирование и ацетилирование остатков лизина субъединицы СДГA модулируют активность СДГ [15,16]. Например, снижение SIRT3, обладающий деацетилазной активностью, приводил к накоплению ацетилированного лизина СДГА. Это снизило активность комплекса СДГ. После повторной экспрессии SIRT3 ацетилирование лизина СДГA было удалено, а активность СДГ восстановлена [16]. Точно так же фосфорилирование остатков лизина СДГА оказывает аналогичное влияние на активность СДГ [15]. Недавно сообщалось о сукцинилировании остатков лизина СДГА в клетках, обработанным ингибитором СДГ или при снижение активности сукцинил-КоА-синтетазы. Модификация сукцинил-лизина может модулировать активность СДГ. [17,18]
Установлено, что в условиях in vitro ингибирующим эффектом на сук-цинатдегидрогеназную активность митохондрий обладают все исследован-ные производные 1,3,4-тиадиазинов. Максимальное ингибирующее влияние показано для L-9 и L-10 1,3,4-тиадиазиновых соединений, под воздействием которых активность СДГ снизилась в 6 раз по сравнению с нативными митохондриями. Высказано предположение о том, что сходный ингибирующий эффект на активность СДГ обусловлен наличием 1,3,4-тиадиазиновых колец и колец морфолина, тогда как разная степень ингибирующей активности СДГ, вероятно, связана с различием заместителей в пятом положении 1,3,4-тиадиазинового кольца [19].
За последние несколько лет комплекс СДГ стал предметом нового интереса. Это было обусловлено, прежде всего, открытием его роли в различных заболеваниях, а также открытием новых факторов сборки. Как и большинство важных открытий, эти новые открытия дают больше вопросов, чем ответов. Предстоящие годы, вероятно, станут свидетелями нового понимания сборки СДГ, включая новые факторы и большую ясность в отношении механизмов [20].
Таким образом, изучая заболевания человека, связанных с СДГ, позволяет предположить, что фермент играет не только центральную роль в цикле Кребса и дыхательной цепи, но также отличается от других митохондриальных дегидрогеназ благодаря своим уникальным окислительно-восстановительным свойствам. В партнерстве с убихиноном СДГ будет представлять собой важный антиоксидантный фермент в митохондриях [7].
Роль эссенциальных микроэлементов в жизнедеятельности человека
Минеральный состав внутриклеточной жидкости строго поддерживается на определенном уровне.
Элементы вместе с водой являются строительным материалами, кофакторами и катализаторами биохимических реакций, стабилизаторами белков и ферментов, обеспечивая постоянство осмотического давления, кислотно-щелочного баланса, процессов всасывания, секреции, кроветворения, костеобразования, свертывания крови. Благодаря присутствию элементов осуществляется процесс мышечного сокращения, нервной проводимости и внутриклеточного дыхания. Химические элементы в организме находятся в виде различных соединений и солей, их влияние на организма обусловлено дозой элемента. Для каждого элемента существует свой физиологический рабочий диапазон концентраций, обеспечивающий нормальное протекание физиологических реакций в организме.
Нарушенная экология, возросший темп жизни с неизбежным нарастанием стрессовых ситуаций, методы обработки продуктов питания, «убивающие» биологически активные вещества ведут к нарушению металло-лигандного гомеостаза и сдвигу равновесия в сторону увеличения или уменьшения концентрации элемента. Накопление элементов или их дефицит способствует активации альтернативных путей метаболизма, который в ряде случаев приводят к патологическим состояниям.
Химические элементы классифицируются в зависимости от их роли в организме. 98% тела человека состоит из органических элементов: H, C, N, O. Вместе с неорганическими элементами Na, Mg, K, Ca, P, S, Cl они составляют основу клеток и тканей, выполняя структурообразующую функцию. К эссенциальным или жизненно необходимым микроэлементам относятся Mn, Fe, Co, Ni, Cu, Zn, Mo, Se, I, при их отсутствии нарушаются базовые реакции деления и размножение клеток. К условно-эссенциальным микроэлементам относятся Li, V, Cr, B, F, Si, As, их роль до конца не определена. Существуют также «токсические металлы», которые в минимальных концентрациях способны оказывать стимулирующее воздействие на организм, но в высоких концентрациях проявляют токсические эффекты.
Микроэлементы составляют лишь 0,02% организма, но способны изменять протекание важнейших биологических реакций. Анализ волос или мочи позволяет выявить избыточное накопление микроэлементов или их дефицит. Содержание микроэлементов в волосах отражает микроэлементный статус организма в целом, поэтому пробы волос являются интегральным показателем минерального обмена. Волосы помогают диагностировать хронические заболевания, когда они себя еще ничем не проявляют.
Железо (Fe)
Железо является жизненно необходимым элементом для организма. Железо входит в состав гемсодержащих белков (гемоглобин и миоглобин) и участвует в переносе кислорода. Железо также входит в состав цитохромов (сложные белки, относящиеся к классу хромопротеидов), участвующих в процессах тканевого дыхания.
Общее содержание железа в организме человека составляет 3-5 г. Из этого количества 57% находится в гемоглобине крови, 23% — в тканях и тканевых ферментах (ферритин и гемосидерин), а остальные 20% — депонированы в печени, селезенке, костном мозге, мышцах и представляют собой «физиологический резерв» железа. Железо существует в двух формах: окисленной (Fe3+) и воcстановленной (Fe2+). Восстановленная форма лучше усваивается организмом. Только 10 % поступившего железо всасывается в кишечнике.
Недостаток железа приводит к тяжелым расстройствам, наиболее важным из которых является железодефицитная анемия. Железодефицитная анемия может привести к сердечной недостаточности.
Избыточное накопление железа приводит к отложению металла в органах (печень, поджелудочная железа, суставы, сердце). Явления отравления железом выражаются рвотой, диареей, падением артериального давления, параличом ЦНС и воспалением почек. При лечении железом могут развиться запоры, так как железо связывает сероводород, что ослабляет моторику кишечника. Избыток железа в организме может привести к дефициту меди, цинка, хрома и кальция, а также к избытку кобальта.
Йод необходим на всех этапах жизнедеятельности. Период младенчества и раннего детства являются критическими в отношении дефицита йода. Йод входит в состав гормонов щитовидной железы тироксина (T4) и трийодтиронина (T3). Йод необходим для роста и дифференцировки клеток всех тканей организма человека, внутриклеточного дыхания, регуляции трансмембранного транспорта натрия и гормонов.
Общее количество йода в организме составляет 25 мг, из них 15 мг аккумулирует щитовидная железа. Значительное количество йода содержится в печени, почках, коже, волосах, ногтях, яичниках и предстательной железе.
При недостаточном поступлении йода у взрослых увеличиваются размеры щитовидной железы, замедляется основной обмен, наблюдается падение артериального давления. У детей недостаток йода сопровождается резкими изменениями всей структуры тела: ребенок отстает в умственном и физическом развитии.
Избыток йода в организме наблюдается при гипертиреозе. Развивается Базедова болезнь, сопровождающаяся экзофтальмом, тахикардией, раздражительностью, мышечной слабостью, потливостью, исхуданием, склонностью к диарее. Повышение основного обмена ведет к гипертермии, дистрофическим изменениям кожи и ее придатков, раннему поседению, депигментации кожи на ограниченных участках (витилиго), атрофии мышц.
Марганец (Mn)
Важен для репродуктивных функций и нормальной работы центральной нервной системы. Марганец участвует в синтезе нейромедиаторов, улучшает мышечные рефлексы, обеспечивает развитие соединительной и костной ткани, увеличивает утилизацию жиров, усиливает эффекты инсулина.
3–5 % поступившего марганца всасывается. Наиболее богаты марганцем трубчатые кости и печень, поджелудочная железа. Марганец содержится в клетках, богатых митохондриями.
При недостатке марганца нарушаются процессы окостенения во всем скелете, трубчатые кости утолщаются и укорачиваются, суставы деформируются. Нарушается репродуктивная функция яичников и яичек.
Избыток марганца усиливает дефицит магния и меди.
Медь принимает участие в поддержание эластичности связок, сухожилий, кожи и стенок легочных альвеол, стенок капилляров, а также прочности костей. Медь входит в состав защитных оболочек нервных волокон, участвует в процессах пигментации, так как входит в состав меланина. Медь влияет на углеводный обмен, посредством усиления процессов окисления глюкозы и торможения распада гликогена мышц и печени. Медь обладает противовоспалительными действиями, помогает при борьбе с бактериальными агентами. Медь является кофактором ферментов антиоксидантной защиты и помогает нейтрализовать действие свободных радикалов.
Общее содержание меди в организме человека составляет примерно 100–150 мг. Лучше всего организм усваивает двухвалентную медь. В тонком кишечнике всасывается до 95% меди, поступившей с пищей. Основное «депо» меди в организме — печень, поскольку синтезирует белок-переносчик меди церулоплазмин.
При недостатке меди в организме наблюдаются: задержка роста, анемия, дерматозы, депигментация волос, частичное облысение, потеря аппетита, сильное исхудание, понижение уровня гемоглобина, атрофия сердечной мышцы. Избыток меди приводит к дефициту цинка и мoлибдена, а также марганца.
Молибден (Мо)
Способствует метаболизму углеводов и жиров, является важной частью фермента, отвечающего за утилизацию железа, в связи с чем помогает предупредить анемию. Принимает участие в обмене мочевой кислоты, включении фтора в состав эмали зубов, гемопоэзе.
Биодоступность молибдена составляет 50%. Молибден не депонируется в организме, а распределяется между клетками крови.
Селен (Sе)
Элемент антиоксидантной защиты, хорошо сочетается с витамином Е. Селен помогает поддерживать должную эластичность тканей. Селен усиливает иммунитет, поэтому активно используется в онкологической практике, в лечении гепатитов, панкреатитов, кардиомиопатий. Селен защищает организм от тяжёлых металлов.
Всасывается в тонком кишечнике, депонируется в почках, печени, костном мозге.
При дефиците селена в организме усиленно накапливаются мышьяк и кадмий, которые, в свою очередь, еще больше усугубляют его дефицит.
Избыток селена приводит к гепато- и холецистопатиям, изменениям работы нервно-мышечного аппарата (боли в конечностях, судороги, чувство онемения). Избыток может привести к дефициту кальция.
Цинк (Zn)
Цинк входит в состав более 300 ферментов, чем объясняет его влияние на углеводный, жировой и белковый обмен веществ, на окислительно-восстановительные процессы, регуляцию активности генов. Цинк связан с правильным функционированием репродуктивной, неврологической, иммунной систем, ЖКТ и кожи. Присутствие микроэлемента важно для нормального сперматогенеза, органогенеза, работы нейромедиаторов и панкреатических ферментов, правильного развития тимуса, эпителизации ран в процессе заживления и ощущения вкуса.
В организме содержится около 1,5–3 г цинка. Цинк всасывается в тонком кишечнике. Медь является антагонистом цинка, и конкурирует с цинком за всасывание в кишечнике. 99% цинка находится внутриклеточно, 1% — в плазме. Цинк присутствует во всех органах и тканях, но в большей степени цинк депонируют предстательная железа, семенники, мышцы, кожа, волосы.
Физиологическая потребность в цинке составляет: 12 мг/сут для взрослых, 3–2 мг/сут для детей.
При дефиците цинка наблюдается задержка роста, перевозбуждение нервной системы и быстрое утомление. Поражение кожи происходит с утолщением эпидермиса, отеком кожи, слизистых оболочек рта и пищевода, ослаблением и выпадением волос. Недостаточное поступление цинка приводит к бесплодию. Дефицит цинка может приводить к усиленному накоплению железа, меди, кадмия, свинца.
При цинковом отравлении наступает фиброзное перерождение поджелудочной железы. Избыток цинка задерживает рост и нарушает минерализацию костей.
Кобальт (Co)
Входит в состав витамина В12, участвует в обмене гормонов щитовидной железы, подавляет обмен йода, регулирует гемопоэз, усиливает всасываемость железа.
В организме 1,5 г кобальта. Биодоступность кобальта 20%. В организм кобальт депонируется в печени, костной ткани и мышцах.
Физиологическая потребность в кобальте составляет: 10 мкг/сут для взрослых.
Кобальт содержится в печени, молоке, овощах.
Дефицит кобальта связан с В12-дефицитной анемией, вегетарианством или паразитарной инвазией. Избыток кобальта наблюдается при интоксикации кобальта (вредное производство, разрушение ортопедических имплантантов).
Никель (Ni)
Никель пролонгирует эффекты инсулина, участвует в окислении аскорбиновой кислоты, ускоряет образование дисульфидных групп.
Никель всасывается в кишечнике, биодоступность от 1 до 10 %. Запасы никеля находятся в поджелудочной железе, легких, сердце.
Физиологическая потребность в никеле составляет: 100–200 мкг/сут для взрослых.
Богаты никелем чай, гречиха, морковь и салат.
Дефицит никеля не описан. Избыток никеля наблюдается при его токсическом поступлении, злокачественных новообразованиях легких, ожогах, инсультах и инфарктах. Избыток может проявлять потерей пигментацией кожи.
РАЗДЕЛ 2. ЭНЗИМОЛОГИЯ
III. Кофакторы и коферменты
Большинство ферментов для проявления ферментативной активности нуждается в низкомолекулярных органических соединениях небелковой природы (коферментах) и/или в ионах металлов (кофакторах).
Термин «кофермент» был введён в начале XX века и обозначал часть некоторых ферментов, которая легко отделялась от белковой молекулы фермента и удалялась через полупроницаемую мембрану при диализе. Несколько позже было выяснено, что большинство ферментов состоит из термолабильной белковой части и термостабильного небелкового фактора — кофермента. Белковая часть получила название «апофермент», который в отсутствие кофермента не обладает каталитической активностью. Кофермент с белковой молекулой (апоферментом) формируют молекулу холофермента, обладающую каталитической активностью.
Более 25% всех ферментов для проявления полной каталитической активности нуждается в ионах металлов. Рассмотрим роль кофакторов в ферментативном катализе.
1. Роль металлов в присоединении субстрата в активном центре фермента
Ионы металла выполняют функцию стабилизаторов молекулы субстрата, активного центра фермента и конформации белковой молекулы фермента, а именно третичной и четвертичной структур.
Ионы металлов — стабилизаторы молекулы субстрата
Схематично роль кофактора при взаимодействии фермента и субстрата можно представить, как комплекс Е-S-Ме, где Е — фермент, S — субстрат, Ме — ион металла.
В качестве примера можно привести расположение субстратов в активном центре гексокиназы (рис. 2-3).
Гексокиназа катализирует перенос концевого, y-фосфатного остатка молекулы АТФ на глюкозу с образованием глюкозо-6-фосфата:
Ион Мg 2+ участвует в присоединении и «правильной» ориентации молекулы АТФ в активном центре фермента, ослабляя фосфоэфирную связь и облегчая перенос фосфата на глюкозу.
Ионы металла — стабилизаторы активного центра фермента
К металлоэнзимам относят, например, фермент пируват киназу (рис. 2-4), катализирующий реакцию:
Рис. 2-4. Участие ионов магния в присоединении субстрата в активном центре пируваткиназы. Активный центр пируваткиназы имеет участки связывания для фосфоеноппирувата и АДФ. Мg 2+ участвует в стабилизации активного центра, что облегчает присоединение фосфоеноппирувата. В ходе ферментативной реакции образуется пируват и АТФ.
2. Роль металлов в стабилизации третичной и четвертичной структуры фермента
Ионы металлов обеспечивают сохранение вторичной, третичной, четвертичной структуры молекулы фермента. Такие ферменты в отсутствие ионов металлов способны к химическому катализу, однако они нестабильны. Их активность снижается и даже полностью исчезает при небольших изменениях pH, температуры и других незначительных изменениях внешнего окружения. Таким образом, ионы металлов выполняют функцию стабилизаторов оптимальной конформации белковой молекулы.
Рис. 2-5. Роль ионов цинка в стабилизации четвертичной структуры алкогольдегидрогеназы.
3. Роль металлов в ферментативном катализе
Не менее важную роль отводят ионам металлов в осуществлении ферментативного катализа.
Участие в электрофильном катализе
Протон и гидроксильная группа последовательно присоединяются к диоксиду углерода с образованием угольной кислоты (см. схему А).
В ходе электрофильного катализа ионы металлов часто участвуют в стабилизации промежуточных соединений.
Участие в окислительно-восстановительных реакциях
Ионы металлов с переменной валентностью могут также участвовать в переносе электронов. Например, в цитохромах (гемсодержащих белках) ион железа способен присоединять и отдавать один электрон:
Благодаря этому свойству цитохромы участвуют в окислительно-восстановительных реакциях.
Другой пример участия ионов металлов в окислительно-восстановительных реакциях — работа фермента дофамингидроксилазы, катализирующего реакцию образования норадреналина при участии витамина С (см. схему Б).
За окислительно-восстановительные свойства у дофамингидроксилазы отвечает ион меди (рис. 2-6).
4. Роль металлов в регуляции активности ферментов
Иногда ионы металлов выступают в роли регуляторных молекул. Например, ионы Са 2+ служат активаторами фермента протеинкиназы С, катализирующего реакции фосфорилирования белков (см. раздел 5). Ионы Са 2+ также изменяют активность ряда кальций-кальмодулинзависимых ферментов (см. подраздел V).
Как уже было сказано, для проявления каталитической активности большинству ферментов необходимо наличие кофермента. Исключение составляют гидролитические ферменты (например, протеазы, липазы, рибонуклеаза), выполняющие свою функцию в отсутствие кофермента.
Кофермент, локализуясь в каталитическом участке активного центра, принимает непосредственное участие в химической реакции, выступая в качестве акцептора и донора химических группировок, атомов, электронов. Кофермент может быть связан с белковой частью молекулы ковалентными и нековалентными связями. В первом случае он называется простетической группой (например, FAD, FMN, биотин, липоевая кислота). Вместе с тем известны примеры, когда кофермент присоединяется к ферменту нековалентными связями настолько прочно, что не диссоциирует от белковой молекулы, например, тиаминдифосфат.
Апофермент обеспечивает специфичность действия и отвечает за выбор типа химического превращения субстрата. Один и тот же кофермент, взаимодействуя с различными апоферментами, может участвовать в разных химических превращениях субстрата. Например, пиридоксальфосфат в зависимости от того, с каким апоферментом взаимодействует, участвует в реакциях трансаминирования или декарбоксилирования аминокислот.
Химическая природа коферментов, их функции в ферментативных реакциях чрезвычайно разнообразны. Традиционно к коферментам относят производные витаминов, хотя помимо них есть значительный класс небелковых соединений, принимающих участие в проявлении каталитической функции ферментов.
К коферментам относят следующие соединения:
✵ гемы, входящие в состав цитохромов, каталазы, пероксидазы, гуанилатциклазы, NO- синтазы и являющиеся простетической группой ферментов;
✵ нуклеотиды — доноры и акцепторы остатка фосфорной кислоты;
✵ убихинон, или кофермент Q, участвующий в переносе электронов и протонов в ЦПЭ;
✵ фосфоаденозилфосфосульфат, участвующий в переносе сульфата;
✵ S-аденозилметионин (SAM) — донор метальной группы;
✵ глутатион, участвующий в окислительновосстановительных реакциях.
Строение и функции этих коферментов подробно рассмотрены в соответствующих разделах учебника.
В. Мультисубстратные реакции
Большинство ферментов катализирует реакции, в которых участвует более чем один субстрат. В случае если кофермент не является простетической группой, его также можно рассматривать как ещё один субстрат. Следовательно, участников ферментативной реакции может быть несколько: непосредственно фермент, несколько субстратов и кофермент.
В этих случаях механизм ферментативной реакции, как правило, может идти по одному из двух путей: по механизму «пинг-понг» (механизму двойного замещения) или последовательному. Рассмотрим оба механизма.
1. Механизм «пинг-понг»
Схематично механизм «пинг-понг» может быть представлен следующим образом:
Субстрат А, взаимодействуя с ферментом (Е), превращается в продукт (Р1). Фермент остаётся в результате этого преобразования не в нативной форме, а в изменённой (Е’) в результате модификации кофермента. Далее к активному центру Е’ присоединяется субстрат В, подвергающийся преобразованию в продукт (Р2) с высвобождением нативной формы фермента (Е).
Хороший пример механизма «пинг-понг» — реакции трансаминирования с участием ферментов аминотрансфераз (кофермент пиридоксальфосфат). Аминотрансферазы, открытые отечественным учёным А. Е. Браунштейном, катализируют обратимые реакции переноса аминогруппы с аминокислоты на кетокислоту. Механизм «пинг-понг» данной реакции схематично представлен на рис. 2-7.
Рис. 2-7. События в активном центре аминотрансферазы как пример механизма «пинг-понг». Кофермент пиридоксальфосфат (ПФ), связанный с ферментом, принимает α-аминогруппу от первой аминокислоты (АК1) которая при этом превращается в α-кетокислоту 1 (КК1) и высвобождается из активного центра фермента. Далее в активный центр фермента присоединяется α-кетокислота 2 (КК2), которая забирает аминогруппу от кофермента и превращается в α-аминокислоту (АК2).
Другой пример механизма «пинг-понг» — реакции дегидрирования с участием кофермента FAD (флавинадениндинуклеотид) или FMN (флавинмононуклеотид), которые прочно связаны с ферментом и, следовательно, не могут рассматриваться в качестве второго субстрата.
Схематично структура этих коферментов и соответствующие им химические формулы представлены на рис. 2-8.
Рис. 2-8. Структура (А) и химическое строение (Б) коферментов FMN и FAD.
Схему реакции дегидрирования (как пример механизма «пинг-понг» с участием коферментов FMN и FAD) можно представить в следующем виде:
где АН2 — донор водорода, окисляемый субстрат 1; А — окисленная форма субстрата 1; В — акцептор водорода — субстрат 2; ВН2 — восстановленная форма субстрата 2; Е (FAD), Е (FADH2) — окисленная и восстановленная формы кофермента FAD, входящего в состав фермента Е.
В качестве примера FAD-зависимой реакции можно привести сукцинатдегидрогеназную реакцию. В этой реакции в качестве второго субстрата участвует убихинон — один из посредников ЦПЭ (см. схему).
2. Последовательный механизм
В случае последовательного механизма для протекания ферментной реакции требуется одновременно взаимодействие двух субстратов. В этом случае возможно присоединение субстратов двумя различными путями:
Механизм упорядоченного взаимодействия субстрата с активным центром фермента:
Первым в активный центр фермента присоединяется субстрат А, облегчая присоединение субстрата В. После химической модификации также наблюдают определённый порядок высвобождения продуктов реакции.
Механизм случайного взаимодействия субстрата с активным центром фермента:
Приоритетности за взаимодействие субстратов А и В в активном центре фермента нет (каждый субстрат имеет свой центр связывания в активном центре). Также нет строгой закономерности высвобождения продуктов реакции.
Схематично структура и химические формулы этих коферментов представлены на рис. 2-9.
Оба кофермента функционируют как посредники переноса двух электронов и одного протона от донора к акцептору, другого протона — в среду (см. схему А).
Донор и акцептор не обязательно участвуют в одном метаболическом пути. Другими словами, восстановленная форма этих нуклеотидов действует как общий пул электронов, образованный в результате окислительных реакций, и может быть использована в различных восстановительных реакциях. Такие реакции называют сопряжёнными (см. схему Б).
В качестве примера можно рассмотреть следующие сопряжённые реакции (см. схему), где Е1 — глицеральдегидфосфат дегидрогеназа; Е2 — лактатдегцдрогеназа.
Наш сайт не претендует на авторство размещенных материалов. Мы только конвертируем в удобный формат материалы, которые находятся в открытом доступе и присланные нашими посетителями.
Если вы являетесь обладателем авторского права на любой размещенный у нас материал и намерены удалить его или получить ссылки на место коммерческого размещения материалов, обратитесь для согласования к администратору сайта.
Разрешается копировать материалы с обязательной гипертекстовой ссылкой на сайт, будьте благодарными мы затратили много усилий чтобы привести информацию в удобный вид.
© 2018-2021 Все права на дизайн сайта принадлежат С.Є.А.