Что такое первичный рак неизвестного происхождения?
Раковая опухоль возникает в случаях, когда клетки начинают бесконтрольно расти. Такую особенность могут приобрести клетки практически любого органа. Кроме того, по мере роста опухоли они с током крови или лимфы могут переноситься в другие области тела, оседать там и давать начало росту новых очагов. Такие очаги называют вторичным раком, или метастазами, а начальную опухоль, соответственно, первичным раком.
Метастазы в любых органах классифицируют в зависимости от того, из какого органа изначально происходит опухоль. Например, вторичный очаг рака легких в печени все равно будет называться раком легких, только получит приставку «вторичный». Иногда не получается определить, в каком именно органе сначала возникла опухоль. Однако при исследовании выявляются ее метастазы в других частях тела. Если их первичный очаг определить не удается, то врачи говорят про первичный рак неизвестного происхождения, или скрытый первичный рак.
Пример выявления
Скрытый первичный рак встречается нечасто. Более того, в ходе дальнейших обследований первичный очаг может обнаружиться. Если так происходит, то опухоль более не считается первичным раком неизвестного происхождения. Ей присваивают название в соответствии с органом происхождения и, опираясь на новые данные, модифицируют схему лечения онкологического заболевания.
На практике это происходит следующим образом:
Однако в ряде случаев даже самое тщательное обследование не позволяет обнаружить первичный очаг. Более того, его не всегда получается найти даже при патологоанатомическом исследовании.
Типы раковых опухолей
Обычно опухоли классифицируют по их первичной локализации. Однако их также можно сгруппировать по типам клеток, по тому, как раковые клетки выглядят под микроскопом. Знание типа клетки может дать врачам ключ к пониманию того, из каких тканей или органов происходит данная опухоль.
Карциномы
Карцинома — это рак, который происходит из клеток, выстилающих внутреннюю или внешнюю поверхности различных органов нашего тела. Такие клетки называются эпителиальными. Наиболее распространенные типы карцином:
1) Плоскоклеточный рак
Самым ярким примером плоских клеток являются клетки, встречающиеся на поверхности кожи. Кроме того, они составляют часть слизистых оболочек многих полых органов. Плоскоклеточный рак может возникать в ротовой полости, в горле, пищеводе, легких, прямой кишке, на шейке матки, во влагалище и некоторых других органах.
2) Аденокарциномы
Эти злокачественные новообразования развиваются из железистых клеток, то есть из тех, которые способны производить какие-либо вещества. Железистые клетки входят в состав очень многих органов нашего тела, в том числе и тех, которые формально не считаются железами. Например, большинство видов раковых опухолей желудка, кишечника и толстой кишки представляют собой именно аденокарциномы и примерно 4 из 10 случаев рака легких также являются аденокарциномами.
Другие виды злокачественных опухолей
Из других типов клеток раковые новообразования возникают реже. К таким опухолям относятся:
Итак, при первичном раке неизвестного происхождения не всегда получается установить орган, где изначально возникла опухоль. Однако, исследуя под микроскопом клетки вторичного очага, чаще всего удается отнести их к одной из пяти категорий:
В дальнейшем эта информация поможет более точно идентифицировать опухоль и в конечном итоге обнаружить ее первичный очаг.
Зачем нужно искать первичный очаг?
Основная причина для поисков начальной опухоли — выбор правильной тактики лечения. Вторичные метастатические очаги состоят из тех же клеток, что и начальная опухоль, даже если развиваются в совершенно других органах. Значит, для их лечения будут эффективны те же препараты, что и для терапии первичного рака, а не те, которые используются при лечении онкопатологий органа, где развился метастаз.
Это имеет особенно важное значение при некоторых формах рака, которые хорошо поддаются лечению определенными химиотерапевтическими или гормональными препаратами. Например, такими особенностями характеризуются многие опухоли молочной железы. Их можно эффективно лечить гормональными средствами. А значит, такие же препараты подойдут и для терапии их метастазов в костях, головном мозге, печени.
К сожалению, предугадать развитие злокачественного заболевания пока практически невозможно. А потому наиболее эффективным способом борьбы с опухолями является выявление рака на 1 стадии развития. В этом случае успешному лечению поддаются более 90% всех злокачественных новообразований. Обнаружить опухоль на начальных этапах возникновения можно только при помощи периодических скринигов. Такие скрининговые программы действуют и в медицинском центре «Анадолу». На первичной консультации специалист-онколог оценит риск развития у вас онкологического заболевания и составит индивидуальный план прохождения профилактических обследований для ранней диагностики рака.
Материал подготовлен по согласованию с врачом «Анадолу», терапевтом и медицинским онкологом Шерефом Комурджу.
Диссеминация в легких
Под диссеминированными процессами в легких понимается довольно обширная группа заболеваний и патологических состояний (более 100, известных современной медицине), при которых в дыхательном органе диагностируют множественные воспалительные очаги и(или) фиброзные изменения, расположенные, как правило хаотично и с обеих сторон. Патологические изменения могут затрагивать практически все легочные сегменты, а могут быть сконцентрированы только в определенных местах, например, вокруг бронхов, в периферических отделах легких и т.д.
Первично диссеминированные заболевания легких выявляются по результатам аппаратных медицинских обследований (КТ, рентген). На посрезовой компьютерной томографии легких (МСКТ) в высоком разрешении очаги диссеминации и фиброза визуализируются лучше всего. Врач-рентгенолог может оценить объем поврежденной легочной ткани, выявить фиброзные тяжи (соединительнотканные спайки и рубцы), скопление жидкости и(или) гноя в альвеолярных пузырьках, сопутствующие патологии дыхательных путей, артерий, лимфатической системы.
В этой статье мы подробнее расскажем о легочной диссеминации и заболеваниях, при которых этот симптом наблюдается.
Что такое диссеминация в легких?
Диссеминация представляет собой множественные патологические очаги (уплотнения) диаметром 1-10 мм. На КТ-сканах они выглядят как светлые пятна, в то время как в норме легочная ткань визуализируется практически однородным темным цветом. Очаги могут быть абсолютно разными по размеру, форме (эллипсообразные, с неровными краями) и морфологии. Нередко вокруг очагов обнаруживается перифокальное воспаление. Они могут сливаться и в таком случае напоминают инфильтративные процессы при пневмонии. Диссеминация также проявляется в виде очаговых микро повреждений с кровью и отеками.
При диссеминирующих процессах в легких дыхательный орган частично (в зависимости от объема поражения) перестает выполнять свою главную функцию — дыхание и транспортировка кислорода к другим органом, в частности к сердцу и головному мозгу. При тотальном диссеминированном поражении легких пациент может погибнуть.
Симптомы легочной диссеминации
Как и большинство легочных заболеваний, диссеминированное поражение легких не обладает специфическими симптомами, по которым было бы точно поставить диагноз. При диссеминации пациентов могут беспокоить стандартные респираторные симптомы:
Причины легочной диссеминации
При обнаружении диссеминации в легких, важно точно установить причину и выявить специфику патологического процесса. Причинами патологических процессов, в зависимости от формы, плотности и характера распространения очагов могут быть:
Отметим, что к одним только возбудителям инфекционно-воспалительных заболеваний легких, которые могут вызвать диссеминированное поражение легких, относится обширная группа вирусов, бактерий и грибков (mycobacterium tuberculosis, SARS-CoV-2, сoccidioides immitis) и др. Иногда выявить точную причину диффузных воспалительных очагов и фиброза не представляется возможным. Если заболевание обладает признаками, сходными с туберкулезом или пневмонией, или имеется выраженный фиброз, но даже после медицинских обследований причина остается не ясна, то такие патологические изменения называют «идиопатическими», а тактика лечения подбирается индивидуально на основании полученных данных и анамнеза пациента.
Поэтому диссеминированные заболевания легких считаются довольно сложными в диагностике. КТ легких значительно информативнее обычной рентгенографии, однако даже этот метод изолированно от лабораторных анализов, не позволяет получить достаточно сведений для назначения терапии. Если у пульмонолога или врача-рентгенолога есть подозрения на злокачественный процесс, пациенту может быть рекомендована биопсия.
Для каких заболеваний характерен симптом легочной диссеминации?
Рассмотрим наиболее распространенные заболевания, которые могут проявляться диссеминированным патологическим процессом в легких.
Туберкулез
Туберкулез легкий представляет собой довольно распространенное, опасное и тяжелое заболевание. Его возбудителем являются бактерии — палочки Коха, которые легко передаются контактным и воздушно-капельным путем, могут годами жить в уличной пыли и даже в легких человека, не вызывая никаких симптомов.
Болезнь проявляется тогда, когда иммунная система человека не может самостоятельно сдержать активную фазу и рост микобактерий mycobacterium tuberculosis. Бактериальное поражение легких при туберкулезе обычно визуализируется как множественные воспалительные очаги — гранулемы.
В центре туберкулезных гранулем расположены очаги некроза. Вокруг них формируются уплотнения — легочные альвеолы заполняются жидким субстратом, в котором содержатся сами бактерии клетки эпителия и плазмы, мертвые лимфоциты, крупные клетки Лангханса, макрофаги.
На начальных стадиях туберкулез прогрессирует практически бессимптомно, со временем пациент начинает отмечать слабость, ухудшение общего самочувствия, кашель и изменение дыхания.
При этом на аускультации редко отмечается что-то подозрительное. Анализ мокроты не показывает микобактерии. Диагностика туберкулеза возможна по результатам рентгенографического обследования и кожной туберкулиновой пробы.
Гранулематозы и диффузно расположенные «матовые стекла» на КТ не являются специфическим признаком туберкулеза. Первые обнаруживаются и при саркоидозе, а вторые — при пневмониях и других заболеваниях.
Для лечения туберкулеза пациенту назначается курс антибактериальной терапии. Важно предотвратить фиброз (рубцевание легких), поскольку такие изменения могут носить необратимый характер.
Пневмокониоз
Пневмокониозы – это диссеминированное поражение легких, причиной которого является вдыхание строительной или промышленной пыли. Чаще всего патологические процессы протекают с выраженным развитием первичного диффузного фиброза, при котором легочные альвеолы «склеиваются», поскольку в них разрастается соединительная ткань.
Пневмокониоз тоже носит гранулематозный характер. На КТ-сканах отчетливо видны множественные узелковые уплотнения разной плотности. Такие уплотнения следует проверять на предмет того, является ли процесс доброкачественным, нет ли онкологической угрозы.
Пневмокониоз относится к так называемым «профессиональным» заболеванием. Чаще всего от него страдают:
Силикоз — распространенное и тяжелое заболевание легких, при котором диагностируют множественный диффузный фиброз и узелковые уплотнения. В результате у больного существенно сокращается функциональный объем легких. Возникает из-за продолжительного вдыхания пыли со свободным диоксидом кремния (содержится в кварцевом песке и окружающем воздухе). Поэтому в группе риска находятся пескоструйщики, работники соответствующих (абразивоструйных) предприятий, жители «песчаных» регионов.
Асбестоз — хроническое заболевание легких, при котором также манифестируется множественный легочный фиброз. Возникает из-за вдыхания асбестовой пыли или волокон асбеста. В группе риска находятся работники асбестодобывающих и асбестоперерабатывающих предприятий.
Пневмонии и осложнения пневмоний
Пневмонии – группа воспалительных заболеваний легких. На фоне этого заболевания у пациента могут возникнуть более опасные осложнения, для которых также характерна диссеминация: острый респираторный синдром (ОРДС), интерстициальное поражение легких, симптом «булыжной мостовой», «сотовое легкое», отек легких, фиброз и др.
При пневмонии со множественными диффузно расположенными локусами поражения существенно снижается жизненная емкость легких, поскольку воспалительные очаги и инфильтраты крупные, альвеолы заполнены жидким экссудатом, а не воздухом.
Пневмония с диссеминацией может быть следствием кандидоза легких, пневмокониоза и других заболеваний. Необходимо точно установить причину патологических изменений. Иногда необходимо также исключить злокачественный процесс (по результатам лабораторной диагностики).
Саркоидоз
Саркоидоз легких – это онкологическое заболевание. Его основными признаками на КТ являются диссеминация и медиастинальная лимфаденопатия. Диссеминация на сканах выражена не так ярко как при прогрессирующем туберкулезе, однако определенное сходство есть. Диагностику затрудняет легочный фиброз. Вместе с дессиминированнным поражением дыхательного органа присутствуют васкулиты, периваскулиты, перибронхит.
Множественные очаги (от 2 мм до 1 см) часто расположены вдоль бронхососудистых пучков, междольковых щелей, костальной плевры, в междольковых перегородках (перилимфатический тип диссеминации). При саркоидозе гранулематоз часто (около 35% случаев) обнаруживают не только в легких, но и в бронхах. При этом их слизистая оболочка может быть не изменена – на поражение бронхов при саркоидозе указывают отек, гиперемия, участки утолщения эпителия.
На ранних сроках саркоидоз развивается бессимптомно, на более поздних пациента начинают беспокоить непродуктивный кашель, проблемы с дыханием (без явных причин), дискомфорт и жжение в области спины, в тяжесть в груди.
Текст подготовил
Котов Максим Анатольевич, главный врач центра КТ «Ами», кандидат медицинских наук, доцент. Стаж 19 лет
Если вы оставили ее с 8:00 до 22:00, мы перезвоним вам для уточнения деталей в течение 15 минут.
Если вы оставили заявку после 22:00, мы перезвоним вам после 8:00.
Рак из невыявленного первичного очага
Лечение рака из невыявленного первичного очага
Рак из невыявленного первичного очага (НПО) — это злокачественное новообразование (подтвержденное морфологически), происхождение которого не представляется возможным установить ни на основании анамнеза, ни в ходе обследований, то есть отсутствует первичный очаг. Для такого злокачественного процесса, также характерны диссеминация (распространение клеток опухоли по всему органу/органам) на ранней стадии, агрессивное течение процесса, непредсказуемый характер метастазирования. По существующим данным такие пациенты составляют 3-15% онкологических больных.
Хотя метастазы без выявленного первичного очага отличаются своим происхождением из разных органов, биологическое поведение их приблизительно одинаково. Эта нозологическая форма отражает наиболее агрессивный тип злокачественных опухолей, метастазирование которых возникает на самых ранних этапах развития.
Так как заболевание уже на первых этапах проявляется метастазами, можно говорить о первично генерализованном процессе, который к моменту обращения пациента за медицинской помощью, как правило, выходит за пределы одного органа.
В зависимости от локализации и распространенности метастатического поражения больных делят на следующие группы:
Клинические проявления заболевания неспецифичны и зависят от локализации очагов метастатического поражения и распространенности опухолевого процесса. Первым симптомом чаще всего является увеличение размеров периферических лимфоузлов. Общие проявления: слабость, потливость, похудание, гипертермия более характерны при поражении органов — легких, печени. При обращении за медицинской помощью часто встречаются следующие изменения: наличие того или иного опухолевого образования, боль, увеличение печени, боли в костях, патологические переломы, респираторные нарушения, потеря веса, неврологические расстройства.
В ходе обследования после анализа данных рентгенографии органов грудной клетки, ультразвуковой томографии органов брюшной полости, забрюшинного пространства и малого таза, радиоизотопного исследования скелета и лимфоузлов, компьютерной томографии головного мозга оценивается распространенность метастатического поражения. Далее проводится морфологическое исследование материала, взятого при пункции или биопсии опухоли. Морфологическое исследование является наиболее значимым и должно выполняться как можно раньше. Полученные данные позволяют подтвердить злокачественность процесса, определить гистогенез опухоли, степень дифференцировки клеток, а иногда и предположительную локализацию первичной опухоли, что значительно облегчает поиск первичного очага и сокращает количество диагностических манипуляций.
Существенную помощь в определении характеристик опухоли может оказать выполнение иммуногистохимического исследования, которое позволит в каждом конкретном случае выработать индивидуальную лечебную тактику.
На заключительном этапе исследований осуществляется поиск первичной опухоли (если ее не смогли обнаружить ранее) в соответствии с гистологической структурой метастазов и распространенностью поражения. Эти два фактора существенно влияют на индивидуальную программу обследования конкретного пациента.
Стандартные методы лечения рака из НПО — это лучевая терапия, возможно в комплексе с химиотерапией, лимфаденэктомия (хирургическая операция, заключающаяся в иссечении лимфатических узлов, пораженных злокачественным процессом).
В медицинском центре ООО «Эдис Мед Ко» научились бороться с разными гистологическими формами злокачественных заболеваний, в том числе и рак из НПО, применяя авторский метод лечения фотодинамической терапией (ФДТ) в сочетании с омелотерапией. Применяемый на протяжении многих лет, этот метод доказал свою эффективность в борьбе с заболеваниями, которые считались неизлечимыми.
Курсы лечения ФДТ в медицинском центре помогут пациенту выйти на ремиссию болезни, восстановить иммунитет и защитные силы своего организма, чтобы патологический процесс не смог появиться вновь.
Смотрите также другие научные статьи:
Что такое диссеминация опухоли
В структуре онкологической заболеваемости женского населения России РМЖ устойчиво занимает первое ранговое место, составляя при этом 20,4 % [5]. Средняя продолжительность жизни больных диссеминированным РМЖ не превышает 24 месяцев. По данным B. Fisher, около 35 % больных РМЖ во время выявления первичной опухоли имеют клинически определяемые метастазы, кроме того, еще 30–35 % больных имеют микрометастазы, которые в дальнейшем клинически манифестируют [7]. В итоге результаты лечения больных РМЖ остаются неудовлетворительными (прирост грубого показателя смертности за последние 10 лет составил 7,56 %) [5].
Диагностика гематогенного распространения эпителиальных опухолей на ранних стадиях – одна из главных проблем онкологии. Морфологически единичные разрозненные опухолевые клетки не определяются – требуется применение высокочувствительных иммунологических методов. К ним в настоящее время относятся иммуноцитологические (иммуноцитохимический, проточная цитометрия) методы и молекулярно-биологические (RT-PCR) методы. Иммунологические методы исследования костного мозга значительно различаются по своей чувствительности и специфичности, технической сложности и стоимости. Для того чтобы контролировать эффективность воздействия лекарственных средств на микрометастазы нужно, в первую очередь, стандартизировать методы количественной оценки единичных диссеминированных опухолевых клеток. Речь идет об иммунологическом стадировании рака [4]. В клинической практике пока не найдено рутинных методов обнаружения микрометастазов. Методы исследования костного мозга нуждаются в дальнейшем развитии. Однако уже накапливаются данные о том, что количественное определение и характеристика диссеминированных опухолевых клеток позволяют получить важную прогностическую информацию и проводить мониторинг эффективности терапии. По мере того как методы исследования станут стандартизированными, с приемлемой чувствительностью и специфичностью, это позволит сделать еще один шаг к индивидуализации антиметастатической терапии [1].
В связи с тем, что диссеминированные опухолевые клетки присутствуют в костном мозге в малых количествах, для увеличения чувствительности иммунологических методов исследования были разработаны методы обогащения популяции клеток-мишеней. Техника обогащения включает большую панель технологий, в основе которых лежат различные свойства диссеминированных опухолевых клеток, отличающие их от нормальных гематопоэтических клеток. Стандартной процедурой считается метод градиентной сепарации Ficoll. Кроме того, большинство современных технологий основано на экспрессии молекулы адгезии эпителиальных клеток (EpCAM). Применение, в частности, метода иммуномагнитного обогащения клеток и проточной цитометрии позволяет оценивать до 50 млн миелокариоцитов у одного больного. Для сравнения ‒ иммуноцитологически на цитоцентрифужных препаратах можно оценить обычно 1–2 млн миелокариоцитов [1].
Ранее нами было проведено исследование, в котором изучался костный мозг у 50 больных РМЖ с помощью цитологического, гистологического и иммуноцитохимического методов. От общего числа больных, включенных в исследование, микрометастазы в костный мозг были обнаружены у 19 (38 %) пациенток. Комбинация различных методов диагностики существенно не повысила вероятность выявления опухолевых клеток в костном мозге. Наиболее информативными в плане определения оккультных метастазов в костный мозг были иммуноцитохимический (63,2 %) и гистологический (57,9 %) методы. Таким образом, чтобы максимально повысить вероятность диагностики метастазов в костный мозг, целесообразно одновременно пользоваться обоими методами. Что становится весьма актуальным для правильного стадирования опухолевого процесса и составления дальнейшего плана лечения [3].
Целью настоящей работы явилось установление степени гематогенной диссеминации РМЖ на основании обнаружения диссеминированных опухолевых клеток высокочувствительным иммуноцитологическим методом с применением моноклональных антител к эпителиальным антигенам.
Материалы и методы исследования
В работе использованы материалы клинического, морфологического, иммуноцитологического обследования 28 больных РМЖ, находящихся на лечении в ГУЗ «Областной клинический онкологический диспансер» с ноября 2011 г. по настоящее время. На проведение данного исследования было получено разрешение этической комиссии ФГБОУ ВПО «Ульяновский государственный университет». Исследования проводились с соблюдением законодательства РФ, этических норм и принципов Декларации Хельсинки (1964) со всеми последующими дополнениями и изменениями, регламентирующими научные исследования на биоматериалах, полученных от людей, а также международным руководством для биомедицинских исследований с вовлечением человека (International ethical guidelines for biomedical research involving human subjects) Совета международных организаций медицинских наук (CIOMS). Все первичные данные пациенток были обезличены в соответствии с требования п. 3 ст. 6 действующего Федерального закона РФ 152-ФЗ «О персональных данных».
В исследуемую группы вошли женщины в возрасте от 33 до 74 лет. Средний возраст составил 56 ± 11,0 лет. На момент постановки первичного диагноза пациентки распределились по стадиям следующим образом: I стадия была диагностирована у 1 (3,6 %) больной, IIА – у 7 (25 %), IIВ – у 3 (10,7 %), IIIА – у 6 (21,4 %), IIIВ – у 3 (10,7 %), IIIC – у 4 (14,3 %), IV – у 4 (14,3 %). Наиболее частым гистологическим вариантом был инфильтративный смешанный рак (42,9 %). Отмечена достаточно высокая частота инфильтративного протокового рака (28,6 %). Реже встречались инфильтративный дольковый рак (21,4 %) и другие формы рака (медуллярный, папиллярный, тубулярный) – 7,1 %. Больным было проведено стандартное клиническое обследование. Исследование костного мозга до начала лечения выполнялось как стандартными цитологическим и гистологическим методами, так и методом проточной цитометрии с применением МКА к цитокератинам EpCAM (CD326). Материал для цитологического исследования и проточной цитометрии получали с помощью стернальной пункции. Объем костномозгового пунктата не превышал 0,5 мл, т.к. при большем объеме возможно разбавление образца периферической кровью. Проточная цитометрия проводилась на базе лаборатории иммунологии гемопоэза ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» РАМН (руководитель – д.м.н., проф. Н.Н. Тупицын). Исследование проводилось в координатах CD45/CD326. Предварительно было проведено иммуномагнитное обогащение клеток, связывающих антитела CD326 (EpCAM). Это позволило оценивать до 50 млн миелокариоцитов у одного больного. Подсчет клеток миелограммы и их анализ производился в клинической лаборатории. Для гистологического исследования выполнялась трепанбиопсия задне-верхней ости подвздошной кости с двух сторон.
Результаты исследования и их обсуждение
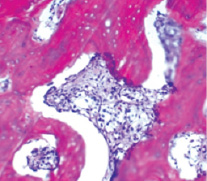
При стандартном цитологическом исследовании метастазы в костный мозг не были выявлены ни у одной из 28 пациенток. У 5 из 28 больных в микропрепаратах были обнаружены «единичные недифференцированные клетки неясного происхождения, возможно, негемопоэтической природы». При проточной цитометрии у 2 из этих 5 пациенток выявлены микрометастазы в костном мозге. При гистологическом исследовании трепанобиоптатов лишь у 1 (3,6 %) пациентки были обнаружены метастазы в костный мозг (рис. 1). Исходная стадия у этой пациентки была расценена как T4N3aM0 (IIIC), после гистологического обнаружения метастазов в костный мозг стадия была изменена на IV. При дополнительной остеосцинтиграфии у этой пациентки были выявлены множественные остеопластические метастазы в кости, не подтвержденные рентгенологически. Метастазы в костный мозг в данном случае были подтверждены методом проточной цитометрии.
Рис. 1. Микрофото метастаза инфильтрирующего рака молочной железы в костном мозге больной Д., 58 лет. Окр. гематоксилином и эозином, ×200
У 3 из 28 больных в трепанобиоптатах были обнаружены единичные клетки, подозрительные на раковые, что не было подтверждено иммуноцитологически. Еще у 7 больных в трепанобиоптатах были обнаружены единичные плазматические клетки или микроочаговое их скопление, что является косвенным признаком поражения костного мозга. При проточной цитометрии у 2 из этих 7 пациенток были обнаружены микрометастазы.
Эпителиальные (опухолевые) клетки в образцах костного мозга были выявлены у 24 (89,3 %) из 28 пациенток с помощью проточной цитометрии с применением моноклональных антител ЕрСАМ (CD326). Важно то, что количество опухолевых клеток, определяемых иммуноцитологически, было очень низким и варьировалось от 1 до 118 клеток в образце, что в 82,2 % случаев составило менее 1 клетки на 1 млн миелокариоцитов. Лишь у 5 (17,8 %) из 28 больных было выявлено ≥ 1 (максимум – 10) эпителиальных клеток на 1 млн миелокариоцитов. У двух пациенток была установлена IV стадия РМЖ (T4N3сM1). У одной имелись метастазы в позвоночнике, грудине, легких, плевре. У другой было выявлено поражение селезенки, внутрибрюшных, забрюшинных лимфатических узлов, яичников. Костный мозг обеих пациенток, как показали миелограммы и трепанобиоптаты, был гипоклеточным (особенно это касалось красного ростка). У двух других пациенток изначально была диагностирована IIA стадия РМЖ. Еще у одной больной изначально была диагностирована IIIB стадия, причем у нее были выявлены метастазы в трепанобиоптате, что потребовало проведения рестадирования – была выставлена IV стадия заболевания (об этом было сказано ранее).
Если считать положительной реакцию при наличии 1 метастатической клетки среди 1 миллиона мононуклеарных клеток (МНК) костного мозга (сумма количества лимфоцитов, моноцитов и плазматических клеток), то число таких пациенток составило 21 (75 %) из 28. При этом только у 3 (10,7 %) из 28 больных число клеток было ≥ 10. У двух больных было выявлено наибольшее число клеток на 1 млн МНК – 32 и 35 соответственно.
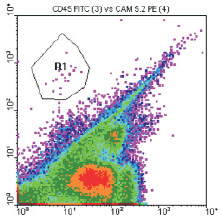
Четкий кластер опухолевых клеток при проведении проточной цитометрии был диагностирован у 4 (14,3 %) из 28 пациенток (рис. 2).
При этом число клеток в образцах костного мозга было очень низким: у одной пациентки (IIA стадия) число опухолевых клеток на 1 млн миелокариоцитов равнялось одной, у трех остальных (IIB, IIIA и IIIB стадии) – менее одной клетки. При пересчете на 1 млн МНК это число составило 6, 2, 6 и 4 клетки соответственно.
Полагая, что обнаружение одной изолированной опухолевой клетки может быть диагностически незначимым, ряд исследователей попытался количественно определить «критическую» опухолевую нагрузку, превышение которой достоверно было бы связано с ростом частоты рецидива заболевания. Было показано, что количество рецидивов рака молочной железы резко возрастает при обнаружении в костном мозге 10 или 15 изолированных опухолевых клеток [6]. В нашем исследовании не была прослежена общая и безрецидивная выживаемость в связи с небольшим сроком от начала исследования. Однако одна больная с IV стадией РМЖ, у которой были подтверждены микрометастазы в костный мозг, погибла от прогрессирования заболевания во время проведения ей второго курса химиотерапии.
Рис. 2. Цитограмма больной раком молочной железы Б., 74 лет, IIB стадия, с микрометастазом в костном мозге, выявленным методом проточной цитометрии. Область R1 – это «кластер» из 20 CD45-негативных клеток (ось абсцисс), положительных в реакции с антителами к молекуле адгезии эпителиальных клеток EpCAM (CD326) – ось ординат
В работе Крохиной О.В. и соавт. (ФГБУ «РОНЦ им. Н.Н. Блохина» РАМН) было сделано предположение, что к наиболее ранним проявлениям реакции костного мозга на присутствие отдельных опухолевых клеток можно отнести следующие изменения кроветворения по данным миелограмм: гипоклеточность костного мозга, скопления плазматических клеток, обнаружение крупных клеток с гиперхромным ядром и множественными нуклеолами, повышение лейко-эритробластического отношения, повышенные средние значения количества моноцитов и лимфоцитов [2].
В нашем исследовании в целом у пациенток были обнаружены следующие изменения в миелограммах: снижение клеточности костного мозга (28,6 %), повышение, а также снижение лейко-эритробластического соотношения (25,0 % и 14,3 %, соответственно), повышенные значения количества моноцитов (42,9 %), лимфоцитов (46,4 %) и плазмацитов (10,7 %). У 5 (17,9 %) пациенток из 28 были обнаружены «единичные недифференцированные клетки неясного происхождения, возможно, негемопоэтической природы». У 2 из них были выявлены микрометастазы. Поскольку все эти изменения кроветворения с различной частотой имелись как у пациенток с микрометастазами, так и без них, мы пока не можем утверждать об ассоциации этих признаков с присутствием отдельных опухолевых клеток в костном мозге.
Возможность выявления единичных опухолевых клеток в костном мозге вследствие большей чувствительности является главным преимуществом метода проточной цитометрии в диагностике диссеминированных опухолевых клеток рака молочной железы в костный мозг по сравнению с морфологическими методами исследования: в 5 (17,8 %) и 1 (3,6 %) случаях из 28 соответственно. Следовательно, метод проточной цитометрии позволяет более точно судить о степени гематогенной диссеминации РМЖ в костный мозг, чем стандартные морфологические методы. В то же время обнаружение малого количества опухолевых клеток при проведении проточной цитометрии сложно трактовать в тех случаях, где они не формируют четкого кластера. При наличии такого кластера микрометастазы могут быть констатированы даже при наличии менее 1 опухолевой клетки на 1 миллион миелокариоцитов. Пока остается неясным диагностически значимое пороговое значение количества единичных опухолевых клеток в костном мозге у больных РМЖ. Нет четких данных о том, какова «критическая» опухолевая нагрузка костного мозга, превышение которой было бы связано с ростом частоты рецидива заболевания. На основании анализа миелограмм пока не удалось выявить косвенные признаки присутствия опухолевых клеток рака молочной железы. Работа в данном направлении будет продолжена.
Представленные нами данные демонстрируют необходимость внедрения в клиническую практику иммунологического исследования костного мозга, особенно на ранних стадиях рака молочной железы, для оценки распространенности опухолевого процесса. Методы исследования костного мозга нуждаются в дальнейшем развитии, а оценка значимости обнаружения диссеминированных опухолевых клеток и микрометастазов в костном мозге возможна после анализа результатов общей и безрецидивной выживаемости у данных больных.
Авторы заявляют об отсутствии каких бы то ни было конфликтов интересов с кем бы то ни было в отношении идеи, планирования, выполнения и опубликования результатов настоящего исследования и их последующего использования в коммерческих или иных целях.
Работа поддержана гос. заданием Минобрнауки РФ. Шифр гос. задания 4. 1219. 201.
Рецензенты:
Чарышкин А.Л., д.м.н., профессор, заведующий кафедрой факультетской хирургии, ФГБОУ ВПО «Ульяновский государственный университет», г. Ульяновск;
Хайруллин Р.М., д.м.н., профессор, заведующий кафедрой анатомии человека, ФГБОУ ВПО «Ульяновский государственный университет», г. Ульяновск.