Обзор онкологических заболеваний метастазы рака и меланомы в головной мозг
Вам поставили диагноз: метастазы рака и меланомы в головной мозг?
Наверняка Вы задаётесь вопросом: что же теперь делать?
Подобный диагноз всегда делит жизнь на «до» и «после». Все эмоциональные ресурсы пациента и его родных брошены на переживания и страх. Но именно в этот момент необходимо изменить вектор «за что» на вектор «что можно сделать».
Предлагаем Вашему вниманию краткий, но подробный обзор метастаз рака и меланомы в головной мозг?
Ежегодно в России выявляют более 8 тысяч новых заболеваний опухолей мозговой оболочки, головного и спинного мозга и других частей центральной нервной системы. Почти такое же количество граждан умирает от данных локализаций.
Филиалы и отделения, где лечат метастазы рака и меланомы в головной мозг
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отделение нейроонкологии
Заведующий – к.м.н. ЗАЙЦЕВ Антон Михайлович
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отделение протонной и фотонной терапии
Заведующий – д.м.н. ГУЛИДОВ Игорь Александрович
Тел: 8 (484) 399 31 30
Метастазы рака и меланомы в головной мозг
Частый вопрос, который приходится слышать врачу от своих пациентов: «Как вылечить метастазы в головной мозг или как выявить рак головного мозга?». К сожалению, это сложная и до конца не решенная проблема, решение которой находится на стыке общей онкологии, нейрохирургии и радиологии.
В России ежегодно регистрируется до 70 тысяч новых случаев метастатических опухолей мозга у онкологических больных. Развитие метастазов в головном мозге, вызывает физические и психические нарушения, приводит к быстройинвалидизации пациентов и значительной социальной дезадаптации. Основная задача, стоящая перед онкологами и нейрохирургами на данной стадии заболевания – не просто продление жизни, но и сохранение ее качества.
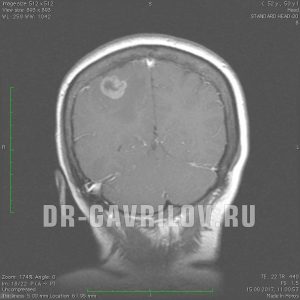
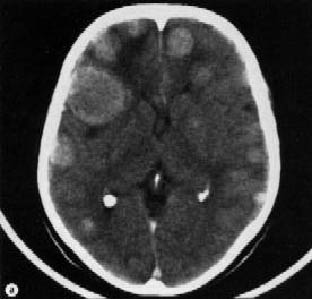
Наиболее информативным методом выявления метастазов в головном мозге является магнитно-резонансная томография (МРТ) высокого разрешения с контрастным усилением. Попытки поставить диагноз метастатического поражения мозга на основании рентгеновской компьютерной томографии или МРТ без контрастного усиления не могут считаться оптимальными.
Методы лечения метастатического поражения головного мозга:
1. Нейрохирургическое вмешательство.
Проведение нейрохирургической операции показано, как правило, при наличии единичного, крупного (более 3 см в диаметре) метастаза или метастаза любого размера, вызывающего симптомы сдавления структур мозга (головная боль, тошнота, нарушение сознания). При наличии опухоли большого объема, вызывающей грубое сдавливание головного мозга, а также при наличии выраженного перифокального отека, удаление опухоли мозга (метастаза) способствует улучшению состояния больного и достаточно быстрому регрессу отека.
Вероятность рецидива опухоли в зоне оперативного вмешательства составляет около 20%. Минимальная длительность госпитализации при лечении метастаза хирургическим путем составляет около 7-10 дней. Фактором, ограничивающим возможность проведения операции, является наличие другой сопутствующей патологии (ишемическая болезнь сердца, декомпенсированный сахарный диабет и т п.). Наличие множественных, и/или мелких, и/или глубинно расположенных метастазов рака в головной мозг в большинстве случаев является противопоказанием для оперативного лечения.
2. Облучение всего головного мозга (ОВГМ).
Известная и широкодоступная методика лечения метастазов в головном мозге. До недавнего времени ОВГМ являлась фактически единственной методикой, позволявшей бороться с множественным метастатическим поражением головного мозга. В связи с возможным развитием нейрокогнитивных расстройств, ОВГМ проводится только один раз в течение всего курса болезни. ОВГМ не имеет явной альтернативы при множественных (свыше 10) метастазах и метастатическом распространении по оболочкам мозга или его желудочковой системе. Часто применяется после хирургического удаления опухолей, для снижения вероятности рецидива в месте операции. Однако, в среднем, контроль роста метастазов после проведения ОВГМ, ограничивается 4-6 месяцами, после чего возможен как продолженный рост облученных метастазов, так и появление новых очагов. Бытующее мнение, в первую очередь среди онкологов, о целесообразности «профилактического» ОВГМ, в настоящее время считается спорным, и, по сути, может быть показано лишь при мелкоклеточном раке легкого. В то же время, некоторые гистологические виды злокачественных опухолей, например, меланома, почечно-клеточный рак, саркомы – невосприимчивы к ОВГМ. Таким образом, ОВГМ остается важным методом лечения онкологических пациентов с метастатическим поражением головного мозга в определенных клинических ситуациях.
Применение лекарственных препаратов является важной составляющей терапии онкологических больных. Однако, при метастатическом поражении головного мозга, возможности и эффективность данного метода лечения резко ограничиваются наличием т.н. гемато-энцефалического барьера (ГЭБ). Он представляет собой клеточную ультраструктуру, отделяющую мозговое вещество от кровотока. Основное его назначение – ограничить поступление в мозг различных вредных веществ, а также исключить контакт с собственной иммунной системой организма. Подавляющее большинство современных химиотерапевтических препаратов, эффективных в отношении первичных вне мозговых опухолей, оказываются не в состоянии воздействовать на их метастазы в мозге, т.к. не проникают через ГЭБ. Те же препараты, которые преодолевают ГЭБ и используются, в частности, в лечении первичных внутримозговых (не метастатических) опухолей, далеко не всегда эффективны в отношении опухолей метастатических. Из побочных эффектов следует отметить частые реакции в виде тошноты, рвоты, выпадения волос, а в более тяжелых случаях – угнетение кроветворной функции костного мозга. В настоящее время ведутся различные исследования и разработка схем химиотерапии внутримозговых метастазов, однако эффективность их не превышает 55-60%. В последние годы сформировалось новое лекарственное направление – таргетная (целевая) терапия, когда препарат воздействует только на определенную мишень (цель)в опухолевой клетке. Такая терапия показала высокую эффективность у пациентов с метастазами в головном мозге.
Лучевая терапия на аппарате «Кибер-нож» или линейных ускорителях одиночных и множественных метастазов имеет своей целью, прежде всего, обеспечение контроля их роста с сохранением максимально возможного качества жизни пациента и, в определенных клинических ситуациях является прямой альтернативой хирургическому лечению. Проведение лучевой терапии увеличивает продолжительность жизни, не ухудшая ее качество.
Все пациенты после проведения лечения по поводу метастазов в головном мозге наблюдаются каждые 3 месяца с оценкой состояния болезни в головном мозге и в остальных органах тела. С этой целью в большинстве случаев используется общепринятый онкологический поиск – рентгенография легких, УЗИ органов брюшной полости, лимфатических узлов. При необходимости уточнения распространённости болезни применяется компьютерная томография внутренних органов и другие методы обследования. В последнее время, с появлением позитронно-эмиссионных томографов, появилась дополнительная возможность выявления небольших очагов, но широкое применение данного метода диагностики сдерживается высокой стоимостью исследования и ограниченной доступностью.
Одним из основных преимуществ лучевой терапии внутримозговых метастазов является незначительная лучевая нагрузка на здоровую мозговую ткань, что делает возможным многократное проведение данного лечения. Такая необходимость возникает при локальном рецидивировании или появлении новых очагов на расстоянии. Повторное лечение – фактор, благоприятно сказывающийся на увеличении продолжительности жизни пациентов с вторичным поражением головного мозга
Филиалы и отделения, в которых лечат опухоли головного и спинного мозга, а также отделы центральной нервной системы
ФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, химиотерапевтического и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.
Метастазы рака в головном мозге
Оглавление
Метастазами называется миграция канцерогенных клеток от первичной опухоли в другие органы, что характерно для большинства онкологических новообразований. Это приводит к формированию вторичных очагов в других тканях. Для различных видов рака характерна разная интенсивность метастатического процесса, что зависит от степени злокачественности и особенностей первичной опухоли. Чем интенсивнее распространение, тем агрессивнее рак. К примеру, при меланоме кожи метастазы в головной мозг случаются часто, в отличие от базальноклеточного рака. Метастатический процесс начинается, как правило, на третьей стадии канцерогенеза, а на четверной стадии он проявляется уже достаточно сильно. Есть два пути миграции раковых клеток: через кровь и лимфу. Вид метастатических новообразований будет идентичен виду клеток первичной опухоли. При обнаружении неоплазий головном мозге важно убедиться в том, что это вторичные опухоли. С этой целью проводят полное обследование организма. При наличии метастаз в головном мозге прогноз ухудшается, продолжительность жизни оценивается месяцами, в некоторых случаях неделями.
Образование метастаз
Метастазы формируются после развития первичного злокачественного новообразования в других органах. Последние образуются в результате мутагенеза или ошибок в генетическом материале соматических клеток. На начальных стадиях метастатический процесс отсутствует, но по мере его прогрессирования, ткани первичной опухоли прорастают в близко расположенные органы. В дальнейшем болезнь усугубляется, раковые клетки начинают отрываться от первичного очага и мигрировать по кровяному или лимфатическому руслу (повреждается целостность сосудов). Метастатическая клетка закрепляется в каком-либо органе, прорастает и дает начало новому очагу – вторичной опухоли.
Важно. У разных лиц характер, сроки и интенсивность формирования вторичных метастатических очагов различны, что объясняется уровнем противоопухолевого иммунитета.
Особенности метастазирования
На интенсивность метастатического процесса, степень злокачественности, особенности формирования рецидивов, лечение метастаз в головном мозге и агрессивность рака влияют следующие обстоятельства:
Метастазы в головной мозг
Приводят к формированию вторичных опухолей в различных участках головного мозга. Почти всегда это становится причиной летального исхода. В общем, к этому может привести любой вид рака, однако есть опухоли, которые дают метастазы чаще остальных видов рака:
Кроме этих видов рака, метастатические поражения мозга могут формироваться и при других злокачественных новообразованиях, например, на терминальных стадиях рака гортани или щитовидной железы, при прорастании опухоли в крупные магистральные артерии.
Симптомы и признаки
При прогрессировании рака он переходит на поздние (3 и 4) стадии. В этом случае метастазы образуются в головном мозге, поэтому начинают проявляться характерные клинические признаки. Проявления будут зависеть от зоны поражения головного мозга. Во многих случаях свойственна зеркальность признаков, т. е. если опухоль в правом полушарии, то клиника будет проявляться с левой стороны и наоборот.
Основные признаки:
Диагностика
Поскольку образование вторичных опухолей в головном мозге становится причиной смерти больного, важно как можно раньше выявить наличие патологического образования. При наличии рака диагностика пациента должна проводится постоянно для мониторинга ситуации и своевременного выявления вторичных новообразований в головном мозге. Если опухоль в голове будет небольшого размера, она уже, как правило, имеет выраженную клинику, однако, ее можно диагностировать на самых ранних этапах при помощи компьютерной (КТ) или магнитно-резонансной томографии (МРТ). Важное значение имеет биопсия для установления метастатического процесса и выяснения всех нюансов патогенеза. Наличие метастаз можно заподозрить даже при биохимическом анализе крови.
Лечение
Что делать при метастазах в головном мозге решает консилиум врачей на основании диагностики и истории болезни пациента. Лечение метастаз в голове проходит весьма сложно, что связано с труднодоступностью локации вторичных очагов в головном мозге, наличием множественных опухолей в других органах, состоянием больного на поздних стадиях, возраста и еще целого ряда факторов. Сегодня при наличии вторичных опухолей в голове применяют стереотаксические радиохирургические методики, которые останавливают или замедляют рост патологической ткани. Самый лучший результат достигается при удалении опухолей оперативным путем, но на данных стадиях лечение всегда проходит трудно. Способ лечения будет зависеть от локации опухоли, интенсивности поражения других органов и общего состояния больного.
Основные виды лечения
Прогноз жизни
При наличии метастаз в головном мозге прогноз неблагоприятный. Ситуация осложняется трудностью в лечении в основном из-за обширного распространения патогенных клеток, образованием множественных вторичных очагов и слабостью пациента. Продолжительность жизни на терминальной стадии с наличием вторичных опухолей в головном мозге, как правило, от нескольких месяцев до одного года, в редких случаях больные проживают более года.
РЕЦИДИВ
История пациента
В период полного локдауна мы заметили у папы шишечку на шее. Возможности дойти до больницы не было, врачи на дом приезжали с большим опозданием. Если участковый терапевт еще мог хоть что-то сказать, то невролог просто поразил своей некомпетентностью. Онколог в платной клинике могла разговаривать только по телефону, на приеме не работала — проконсультироваться по новообразованию было просто не с кем. Приходящие врачи говорили, что это воспаление лимфоузла и можно не паниковать. Когда же шишечка стала расти, то стало понятно: нужен специалист.
Самостоятельно доехать до врача в Европейскую клинику мы с папой смогли только в августе. Там после осмотра и по результатам биопсии выяснилось, что это рецидив меланомы.
Удалять было нельзя, но лечить нужно срочно. Нам озвучили сумму на капельницы: минимум 6 капельниц по 200 тысяч каждая. Таких денег у нас не было. Благо, на вопрос, а можно ли лечиться по ОМС, ответили утвердительно.
Опять встал опять вопрос, где и как попасть к нужному врачу. Идти снова в поликлинику не хотелось: разговаривать с онкологом было бесполезно, направления быстро не даст, начнет тянуть время. А времени ждать не было: врачи сказали, что лечить нужно срочно. Я позвонила в институт Герцена, но результат оказался неутешительным: один врач в отпуске, запись на прием ко второму на месяц вперед расписана, а в нашем городе специализированного отделения нет.
РЕЦИДИВ: Ответы врача
Как часто возникают рецидивы меланомы кожи?
Какие симптомы рецидива могут быть при меланоме кожи?
В какой период лечения чаще всего возникают рецидивы меланомы кожи?
д.м.н., профессор РАН, онколог, хирург, президент Российского общества специалистов по опухолям головы и шеи, заведующий отделением опухолей головы и шеи клинического госпиталя «Лапино», председатель Проблемной комиссии по опухолям головы и шеи при РАН
Например, пациенты, у которых имеются метастазы в регионарных лимфоузлах, излечивается примерно 60% пациентов. У пациентов, у которых есть отдалённые метастазы, примерно 25% пациентов имеют шансы на излечение. Вся остальная популяция — это пациенты, у которых диагностируются рецидивы, прогрессирование заболевания, неудачи в лечении.
Даже в тех случаях, когда заболевание прогрессирует, есть возможность смены тактики лечения, смены лекарственной терапии и переход на более эффективную схему лечения. Но, конечно, успех уже будет в значительно меньшей степени, если мы говорим о лечении первичного пациента.
Наблюдение пациента, безусловно, зависит от стадии заболевания. Если изначально было небольшое образование, 1 стадия, условно говоря, 2 стадия, то как может проявляться прогрессирование заболевания? Это может быть местный рецидив, локальный, в зоне уже ранее иссечённой опухоли, и это могут быть регионарные метастазы. Например, если изначально меланома локализовалась в области кожи головы, то метастазы могут появиться на шее или в околоушной области. Может быть немножко по-другому. Бывает, что прогрессирование проявляется сразу в виде появления отдалённых метастазов.
Органы-мишени для меланомы это, как правило, лёгкие, головной мозг и кости — чаще всего поражаемые органы. Соответственно, нужно уделять внимание этим всем проявлениям. Часто как раз-таки при меланоме кожи назначается такое исследование, как ПЭТ или ПЭТ/КТ. Это позитронно-эмиссионная томография, которая позволяет оценить наличие или отсутствие каких-либо опухолевых очагов практически во всём теле человека. Так как мы знаем, что меланома обладает одним из самых высоких индексов отдалённого метастазирования, то как раз-таки нашим пациентам в подавляющем числе случаев назначается ПЭТ в плане обследования или наблюдения для того, чтобы контролировать это заболевание уже после первичного лечения.
Чаще всего прогрессирование наступает в течение первых 2−3 лет существования заболевания, существования меланомы или после уже проведённого лечения. Поэтому основной акцент ставится на этот срок наблюдения, но, как и при любых других онкологических заболеваниях, мы говорим
о пятилетнем минимальном сроке наблюдения пациентов, потому что считается, что если пациент прожил без каких-то проявлений заболевания в течение этого срока, в течение 5 лет, в таком случае риск появления повторно этого заболевания становится минимальным.
к.м.н., научный сотрудник отделения опухолей головы и шеи НИИ КО им. Н.Н. Трапезникова, НМИЦ онкологии им. Н.Н. Блохина
Частота возникновения рецидивов при меланоме кожи и их проявление
По результатам проведенного нами исследования местные рецидивы после проведенных ранее радикальных операций составляют не более 1,5−2%. Таким образом, можно сказать, что локальный рецидив для меланомы кожи головы и шеи — нехарактерное явление.
Болезнь проявляется реализацией регионарных и отдаленных метастазов, что укладывается в общую биологическую суть меланомы, что она является болезнью не местного прогрессирования, а регионарного и отдаленного.
Сегодня в понятие местного рецидива также входят подкожные и внутрикожные метастазы (транзитные и сателлитные метастазы). Они возникают на разном расстоянии от послеоперационного рубца до регионарного лимфоколлектора. Это подкожные округлые образования с темным пигментом внутри.
к.м.н., старший научный сотрудник, отделение онкодерматологии ФГБУ «НМИЦ онкологии имени Н.Н.Блохина» Минздрава России
Что делать, если назначенное лечение не помогает?
Лечение будет зависеть от того, что было использовано в первую линию. Например, если в первую линию использовали иммунотерапию, то далее будет назначена таргетная терапия (если есть мутация в гене BRAF) либо химиотерапия (если нет мутации), либо другой вариант иммунотерапии (после анти-PD1 назначение анти-CTLA4 или комбинации анти-PD1 и анти-CTLA4).
Наоборот, если у пациента в качестве терапии первой линии была назначена таргетная терапия, то в дальнейшем ему может быть предложена иммунотерапия или химиотерапия. Все зависит от общего состояния пациента, наличия метастазов в головной мозг, уровня ЛДГ, сопутствующих заболеваний и терапии.
В случае, если были использованы все варианты лечения и они не помогли, можно рассмотреть вопрос о возврате к тому варианту терапии, который ранее приносил пользу (будь то таргетная терапия или иммунотерапия). Если и это было назначено и не привело к результату, можно подумать о проведении широкого молекулярного тестирования опухоли для того, чтобы попытаться найти необычную мутацию и подобрать к ней «ключик» или таргетный препарат, у которого в инструкции, скорее всего, не будет указаний на меланому, но будет указание на наличие специфического молекулярного изменения в опухоли. Сегодня возможно проведение такого тестирования Foundation One или его аналоги в России, но у него высокая стоимость, и она пока не покрывается программой государственных гарантий.
Какие дополнительные обследования проводятся при рецидиве?
Стандартный объем обследования обязательно должен включать в себя выполнение КТ органов грудной клетки, брюшной полости и малого таза с внутривенным контрастированием либо ПЭТ/КТ в режиме «все тело» с ФДГ и МРТ головного мозга с внутривенным контрастированием.
Материалы конгрессов и конференций
X РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
ЛУЧЕВАЯ ТЕРАПИЯ В КОМБИНИРОВАННОМ И КОМПЛЕКСНОМ ЛЕЧЕНИИ МЕТАСТАЗОВ
В ГОЛОВНОЙ МОЗГ: ОСНОВНЫЕ ЭТАПЫ, ПЕРСПЕКТИВЫ
З.П. Михина, С.И. Ткачев, О.П. Трофимова, В.С. Данилова, О.П. Извекова,
В.А. Горбунова, М.Б Бычков, Р.Б. Карахан, В.Б. Крат
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва
Метастатическое поражение головного мозга – серьезное осложнение течения опухолевого процесса, которое отмечается примерно у 50% онкологических больных и чаще всего встречается при раке легкого (34–66%), молочной железы (10–33%), почки, колоректальном раке, меланоме. Пик метастазов приходится на возрастную группу 55-65 лет. В детском возрасте метастазы в мозг возникают чаще при саркоме Юинга, рабдомиосаркоме, нейробластоме и остеогенной саркоме (1, 2).
При подозрении или выявлении метастазов в головной мозг должно проводиться полное общее обследование, и оно особенно показано пациентам с поражением мозга без выявленной первичной опухоли и больным с известным первичным диагнозом рака, у которых была некоторое время ремиссия. Начальная оценка состояния больного с поражением ЦНС должна проводиться с использованием шкалы Карновского или системы ВОЗ. Обе системы позволяют количественно определить функциональное состояние больного, прогнозировать качество и время жизни, определять объем обследования.
Клинический осмотр больного должен включать тщательную пальпацию всех периферических лимфатических узлов, щитовидной железы, молочных желез, выслушивание легких, обследование брюшной и тазовой области, включая яички, ректальное исследование, осмотр всей кожи для выявления меланомы. Следует выяснить жалобы на боли в костях, потому что метастазы в кости и мозг нередко встречаются вместе.
Тщательная неврологическая оценка часто показывает дефициты, которые пациент не сознавал, особенно локальную слабость и умственные изменения. Следует исследовать зрение, которое отражает кортикальную функцию и внутричерепное давление. До 25% больных с метастазами в мозг имеют отек диска зрительного нерва, изолированный паралич VI (отводящего) нерва может быть неправильно истолкован как локальный симптом, хотя он отражает внутричерепную гипертензию.
При подозрении или установления диагноза метастаза в мозг у онкологического больного следует начать терапию с учетом степени тяжести неврологических симптомов. При выраженном внутричерепном давлении с признаками, предполагающими наличие вклинения мозга, или при эпилептическом состоянии показан маннитол 1 г/кг внутривенно и дексаметазон от 32 до 64 мг внутривенно струйно. Поддерживающие дозы маннитола (0.5-2 г/кг) и дексаметазона (4-10 мг в/в) вводятся, разделенные на 4 дозы. При эпилептическом статусе последовательно вводятся противосудорожные препараты: лоразепам от 1 до 4 мг в/в, далее фосфенитоин 20 мг/кг, в/в, фенобарбитал, пропофол, вплоть до общей анестезии, если нет стойкого эффекта.
Дексаметазон – глюкокортикоид, наиболее часто используемый для уменьшения отека мозга. Уменьшение отека с последующим клиническим улучшением обычно наблюдается в пределах 1-2 дней. Стандартный подход у больных с симптомами заключается в подведении высокой начальной дозы, от 16 до 32 мг в/в или в/м с последующим снижением дозы до 4-8 мг в/в или per os. При наступлении устойчивого клинического улучшения следует начать медленное снижение доза дексаметазона до самой низкой эффективной, например, по 2 мг каждые 5-7 дней. Следует не забывать, что длительное использование кортикостероидов связано с высокой частотой побочных эффектов, таких как кандидоз полости рта, повышение кислотности желудка, язвенная болезнь, условно-патогенные инфекционные процессы, отсутствие толерантности к глюкозе или свершившийся диабет, артериальная гипертензия, кушингоидные изменения, нарушения сна, личности, остеопороз, аваскулярный некроз, риск тромбоза глубоких вен. Не рекомендуется использовать кортикостероиды у пациентов с отсутствием или минимальными симптомами (1, 2).
Облучение всего головного мозга в самостоятельном варианте используется у больных с милиарной диссеминацией метастазов, с множественным или ограниченным числом очагов (2-4), но при неблагоприятном прогнозе. Весь мозг облучается при метастазах лимфосарком, мелкоклеточного рака легкого (МРЛ), герминогенных опухолей, при которых хирургическое лечение проводить нецелесообразно, но лучевая терапия обязательно дополняется химиотерапией, к которой опухоли данных локализаций высоко чувствительны.
WBRT проводится с профилактической целью после хирургического удаления одиночных метастазов или при МРЛ, аденокарциноме легкого, лейкозах, учитывая высокий потенциал интракраниального метастазирования при указанных формах первичной опухоли.
Параллельно с лучевой терапией у больных с одиночными метастазами использовался хирургический метод в самостоятельном варианте. При числе метастазов 2-3 хирургическое лечение считалось противопоказанным (3).
После представленных итогов возникли вопросы относительно роли лучевой терапии: необходима ли вообще лучевая терапия после «полной» резекции одиночного метастаза, должна ли послеоперационная лучевая терапия быть локальной или ее следует проводить в виде WBRT.
Ретроспективные исследования, которые изучали роль послеоперационной лучевой терапии при одном метастазе, не сумели ответить на этот вопрос из-за противоречивых результатов. Четко отмечалась меньшая частота рецидива в зоне операции и в других отделах мозга при использовании WBRT, не было единого мнения о пользе для выживаемости, оставалась высокая вероятность развития поздних лучевых повреждений мозга, снижающих качество жизни больных.
Patchell и соавт. опубликовали результаты рандомизированного исследования, определяющего важность включения WBRT. Больные в общем состоянии >70 баллов по шкале Карновского были рандомизированы после полного удаления единичного метастаза в головном мозге. Для увеличения эффекта и снижения возможного нейрокогнитивного ухудшения использовалась классическая лучевая терапия (СОД 50,4 Гр; РОД 1,8 Гр). Анализа данных показал достоверное уменьшение частоты рецидивов (18% против 70%) и причин смерти от неврологической болезни (14% против 44%) у больных с WBRT после хирургического удаления по сравнению с хирургией в самостоятельном варианте. Однако пользы для выживаемости или функциональной независимости больных отмечено не было. Авторы рекомендовали применять WBRT для уменьшения частоты локальных или новых метастазов в головном мозге и снижения вероятности смерти по неврологическим причинам.
WBRT обычно назначается всем пациентам после резекции 2-3 метастазов, даже, когда послеоперационные исследования (КТ и МРТ) не показывают наличие болезни. Высокая вероятность появления новых метастазов в мозге оправдывает применение WBRT после операции, не смотря на потенциальный риск постлучевых изменений. В настоящее время окончательное решение принимается с учетом полноты резекции очагов, чувствительности опухоли к облучению, наличия экстракраниальных метастазов и прогнозирования длительности выживания.
Оценка больших клинических материалов показала, что приблизительно 50% пациентов с метастазами в мозг умирают от неврологических причин (4). Было высказано предположение, что если подводить к метастазам бoльшие дозы, выживаемость может быть увеличена. Были проверены стратегии по увеличению доз облучения с использованием ускоренной гиперфракционной радиотерапии, брахитерапии, фракционированной стереотаксической радиохирургии и стереотаксической радиохирургии (SRS) в виде одной дозы. В последнем десятилетии наиболее активно использовалась SRS с подведением к опухоли всей дозы за один сеанс с минимальной дозой в нормальной ткани мозга.
SRS радиохирургия использует множество мелких, хорошо коллимированых пучков ионизирующего излучения линейного ускорителя или «гамма-ножа» для уничтожения внутричерепных очагов. Анализ 40 нерандомизированных исследований, включавших 2,697 пациентов и 3,922 метастатических очагов, выявил среднюю частоту непосредственного эффекта в 81% случае при использовании SRS.
Активное внедрение в ряде стран SRS для лечения интракраниальных метастазов позволило высказать сомнения в целесообразности использовании WBRT у пациентов с несколькими метастазами.
В настоящее время продолжаются или уже опубликованы предварительные результаты ряда рандомизированных исследований, касающихся более детальной и ясной оценки роли WBRT в сочетании с радиохирургией. Исследование Aoyama и соавт. (5) было проведено в Японии с участием больных с 1-4 метастазами, состоянием ≥70 баллов по шкале Карновского, размерами метастазов по МРТ ≤3 см, получивших радиохирургию в сочетании или без WBRT. Проведено сравнение в группах в зависимости от числа метастазов (1 против 2-4), вида первичной опухоли (легкое против других опухолей), состояния экстракраниальной болезни (есть – нет). WBRT проводилась по схеме 30 Гр за 10 фракций, дозы SRS уменьшались на 30-40% на краях метастазов в группе WBRT+SRS. Первично изучалась выживаемость, вторично – сохранение системных функций (KRS ≥70%), сохранение неврологического статуса (RTOG, стадия ≤2), время, свободное от новых интракраниальных метастазов, поздние неблагоприятные последствия, причины смерти по определению Patchell, частота локального контроля в области поражения.
Начиная с 80 гг., с внедрением новых диагностических методов (КТ, МРТ), основное внимание уделялось совершенствованию методов диагностики внутримозговых метастазов, определению прогностических групп, разработке методов лечения с учетом прогноза. На основе изучения прогностических факторов 1176 больных исследователи RTOG, используя статистический метод, названный рекурсивным парциальным анализом (RPA), выделили три подгруппы (классы). Рекурсивный класс I включал пациентов до 65 лет, в общем состоянии по шкале Карновского ≥70%, излеченной или контролируемой основной опухолью и отсутствием внечерепных метастазов. Эта группа составляла меньше 20% от общей численности пациентов с метастазами в мозг. Класс III включал пациентов в общем состоянии по шкале Карновского 90% пациентов с метастазами в мозг до лучевой терапии всего черепа имелиcь нарушения познавательной функции, которые в значительной степени зависели от объема опухоли, но не от числа метастазов, и исходный уровень этой функции был значительным прогностическим признаком выживаемости, помимо обычных используемых показателей прогноза.
Поздние изменения мозга после WBRT имеют особый интерес, поскольку они включают возможность появления деменции. Важно, что деменции, частота которой с течение первого года после WBRT составляла 11%, была выявлена только у пациентов, леченных большими ежедневными фракциями (больше 3 Гр). В то же время приведены веские доводы в пользу того, что лечение крупными фракциями позволяет быстрее получить эффект с улучшением неврологических симптомов и уменьшить время приема поддерживающих лекарств. Кроме того, больные с неблагоприятным прогнозом имеют небольшую выживаемость, и у них не успевает развиться такое серьезное осложнение как деменция. Однако выживаемость у части больных растет, и при хорошем прогнозе больные могут дожить до поздних повреждений, что заставляет изучать факторы, определяющие позднюю нейротоксичность.
Таблица 2.
Лучевые осложнения после облучения черепа.
| Фаза | Признаки | Время появления | Вероятная причина | Лечение |
|---|---|---|---|---|
| Острая | Усталость, головная боль, тошнота, алопеция, эритема кожи черепа, обострение локального неврологического дефицита | Первые 2 недели лучевой терапии | Отек | Кортикостероиды |
| Ранняя отсроченная | Усталость, сонливость, головная боль → познавательная дисфункция → замедленная обработка информации → снижение внимания → неспособность обучения; нарушение памяти → исполнительная дисфункция → нарушение моторной ловкости | 1-6 мес. после лучевой терапии | Демиелинизация | Кортикостероиды, возможно спонтанное улучшение |
| Поздние нарушения | Деменция, изменение личности, лейкоэнцефалопатия, судороги, повышение черепно-мозгового давления, атаксия, дизартрия, несдержанность, оптическая невропатия, индуцированные опухоли | От 6 мес. до нескольких лет после лучевой терапии | Ангиопатия, демиелинизация, некроз | Кортикостероиды, антикоагулянты, вит. Е |
В заключение следует отметить, что решение клинической проблемы должно основываться на оценке прогностических показателей. Это позволяет разделить больных на благоприятные, промежуточные, и неблагоприятные категории и предложить методы лечения (резекцию, облучение, радиохирургию, химиотерапию), которые разработаны в конкретном учреждении и доступны больным.
В странах с большим опытом применения стереотаксической радиохирургии до конца не определено место метода в лечении метастазов: должна ли радиохирургия использоваться в сочетании с WBRT для предупреждения рецидивов и новых метастазов или во время рецидива после WBRT, или использоваться самостоятельно, резервируя WBRT для облучения обширных мозговых рецидивов. В России только набирается опыт лечения с использованием гамма-ножа, нет пока исследований по обоснованному сочетанию радиохирургии с различными методами лечения. В связи с этим общее облучение мозга проводится практически всем больным (после операции, самостоятельно), и при показаниях добавляется локальное облучение отдельных очагов на линейных ускорителях. Дальнейшие исследования должны обязательно включать оценку реакций на облучение всего мозга с изучением познавательной функции путем анкетирования больных с различными первичными новообразованиями, имеющими шанс прожить более 3 мес.
1. Evaluation and management of brain metastases. /Mehta M., Tremont-Lukats I.W Educational Lection of the 38th ASCO Annual Meeting 18-21 May, 2002, Orlando, FL, USA — 2002. — P.375—82.
2. Treatment of brain metastases. / Patchell R.A. Educational Lection of the 38th ASCO Annual Meeting 18-21 May, 2002, Orlando, FL, USA — 2002. — P. 383—91.
3. Management of cerebral metastases: the role of surgery/ Lang F.F., Wildrick D.M., Sawaya R. — Cancer Control. — 1998, Mar. — Vol. 5. — No. 2. — P.124—9.
4. Focal management of single or multiple brain metastasis without whole-brain radiotherapy. / Kleinberg L.R Educational Lection of the 42nd ASCO Annual Meeting, 2006 — P. 93—9.
5. Interim report of the JROSG99-1 multi-institutional randomized trial, comparing radiosurgery alone vs. radiosurgery plus whole brain irradiation for 1-4 brain metastases. /Aoyama H, Shirato H, Nakagawa K, et al. J Clin Oncol.—2004—22 (suppl; abstr 1506)14s.
6. Phase II trial of radiosurgery for one to three newly diagnosed brain metastases from renal cell carcinoma, melanoma, and sarcoma. / Manon R, O’Neill A, Knisely J, et al. An Eastern Cooperative Oncology Group study (E 6397). J Clin Oncol.— 2005. —23. — P. 8870-8876.
7. Clinical practice guideline on the optimal radiotherapeutic management of brain metastases/ Tsao M.N., Lloyd N.S., Wong R.K.S. and the Supportive Care Guidelines Group of Cancer Care Ontario’s Program in Evidence-based Care. — BMC Cancer. — 2005. — Vol. 5 — P.34.
8. Neurocognitive sequelae оf whole-brain radiotherapy in patients with brain metastase. /Jeffrey S. Educational Lection of the 42nd ASCO Annual Meeting, 2006 — P.100—4.