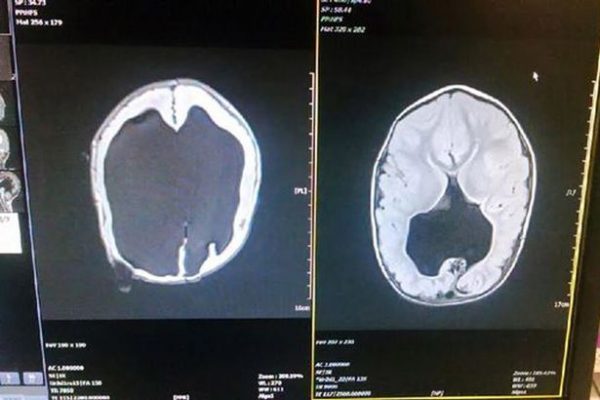
Анэнцефалия
Анэнцефалия — это порок развития нервной системы, при котором у плода отсутствуют большие полушария мозга, недоразвиты кости свода черепа, мягкие ткани головы. Аномалия возникает под действием химических, биологических или физических тератогенных факторов. Большинство плодов с анэнцефалией погибают во внутриутробном периоде, и даже при живорождении срок жизни ребенка не превышает нескольких часов. Диагностика выполняется пренатально с помощью УЗИ, МРТ, амниоцентеза, биохимического скрининга. В такой ситуации показано прерывание беременности, при отказе родителей от аборта — оказание паллиативной помощи ребенку.
МКБ-10
Общие сведения
По данным ВОЗ, пороки развития ЦНС занимают первое место среди врожденных аномалий у плода (25%). Анэнцефалов стоит отличать от ацефалов (акефалов), у которых вовсе отсутствует головной мозг. Анэнцефалия встречается в США и России с частотой 1 на 10000 новорожденных, в Великобритании — 5:10000, в Китае — 8:10000. Заболевание чаще наблюдается у плодов женского пола. Риск повторения анэнцефалии при следующей беременности составляет до 5%, а при рождении женщиной двух детей с этим пороком ЦНС — возрастает до 10%. Вероятность аномалии у кровных родственников составляет не более 3%.
Причины
Порок формируется при нарушениях внутриутробной закладки нейроструктур в эмбриональном периоде формирования плода. Он считается мультифакториальным, точные причины такого состояния окончательно не установлены. Ученые предполагают, что появление анэнцефалии связано с воздействиями негативных факторов на ранних этапах беременности. Типичными тератогенными влияниями считаются:
К предрасполагающим факторам со стороны родителей относят генетические — наличие различных генных мутаций, частые случаи родственных браков и кровосмешения. Риск аномалий развития ЦНС у ребенка повышается, если в организме матери низкий уровень йода, фолатов и других витаминов группы В. Вероятность анэнцефалии повышается при тяжелом течении гестации, наличии у беременной женщины экстрагенитальных патологий: сахарного диабета, сердечной недостаточности, гипотиреоза.
Патогенез
Симптомы анэнцефалии
У живорожденных младенцев с анэнцефалией резко уменьшена мозговая часть черепа, отсутствуют плоские кости, недоразвиты мягкие ткани. На месте головного мозга находится аномальная сосудистая ткань, которая может быть покрыта кожей.
Такие дети пребывают в бессознательном состоянии, они слепые и глухие, не реагируют ни на какие внешние стимулы. Зачастую есть сопутствующие пороки: спинномозговые грыжи, патологии надпочечников, расщелины неба.
Хотя большинство живорожденных пациентов погибает практически сразу, в медицине описано по крайней мере три случая, когда дети смогли прожить более 2-х лет. Долгожителем среди анэнцефалов считается девочка Стефани Кин (более известная по прозвищу Бэби Кей), которая прожила 2,5 года и умерла от остановки сердца. У нее были проблемы с дыханием, которые требовали проведения ИВЛ. Двухлетний рубеж также преодолели Джексон Буэлл из Бостона, Виктория де Кристо из Бразилии.
Однако продление срока жизни анэнцефалов возможно только при постоянной кардиореспираторной поддержке, восполнении нутритивных потребностей. Ввиду отсутствия большей части мозга состояние младенцев остается стабильно тяжелым вплоть до смерти. Объем и необходимость паллиативной помощи для таких новорожденных поднимает важные вопросы биомедицинской этики.
Осложнения
Диагностика
Аномалия обнаруживается антенатально во время плановых ультразвуковых скринингов беременности. Такой диагноз является абсолютным показанием к прерыванию беременности независимо от возраста плода, поэтому на акушеров-гинекологов ложится большая ответственность — необходимо как можно раньше установить диагноз, чтобы снизить риски для женщины. Для обнаружения порока применяются следующие методы:
Женщинам, которые планируют прервать беременность при выявленной анэнцефалии плода, требуется расширенная диагностика. Назначается стандартное гинекологическое исследование, а также набор анализов: клиническое исследование крови, анализы на вирусные гепатиты, ВИЧ-инфекцию. Впоследствии пациенткам рекомендовано медико-генетическое консультирование, чтобы оценить риски врожденных пороков при последующих беременностях.
Лечение анэнцефалии
Решение о прерывании беременности должны принимать родители. Единственным исключением является мертвый плод, когда женщине требуется экстренное хирургическое вмешательство. Живорожденным детям с анэнцефалией можно оказать только паллиативную помощь. Около 66% таких детей живут несколько часов после рождения, остальные погибают в первые минуты. Основные направления медицинской помощи при анэнцефалии:
Важной составляющей является психологическая помощь родителям на всех этапах от момента диагностики аномалии у плода, поскольку это становится тяжелым испытанием для семьи, у женщин зачастую возникают депрессии, апатии, суицидальные мысли. Помощь оказывают психологи, психиатры (в случае серьезных нарушений психоэмоционального состояния), верующим людям можно порекомендовать обратиться к представителям религии.
Прогноз и профилактика
Прогноз неблагоприятный, поскольку анэнцефалия заканчивается внутриутробной смертью плода или летальным исходом вскоре после того, как родился живой ребенок. Современные возможности медицины позволяют обеспечить такому младенцу достойный уход из жизни, если родители приняли решение не прерывать беременность.
Учитывая разнообразие предрасполагающих факторов, эффективные меры профилактики этого состояния пока не разработаны. Положительным для предупреждения тяжелых аномалий плода является прием беременной по назначению гинеколога витаминных добавок с солями фолиевой кислоты, дополнение рациона зелеными листовыми овощами, фасолью, апельсиновым соком, содержащими фолаты.
Родители купили гроб: сын родился с 2% мозга
Они купили детский гроб и приготовились…
Находясь на третьем месяце беременности, Шелли Уолл узнала, что у ее ребенка расщепление позвоночника, редкие хромосомные аномалии и гидроцефалия – скопление жидкости в мозгу.
Состояние ребенка было настолько серьезным, что врачи предупредили родителей мальчика, Шелли и Роба – их сын вряд ли выживет или родится с серьезными умственными и физическими недостатками. Врачи также рассказали супружеской паре, что у ребенка останется массивное отверстие в позвоночнике.
Пять раз Шелли предлагали прервать беременность, но с емья решила оставить ребенка.
Шелли рассказывает, что они купили маленький детский гроб для Ноя и приготовились к худшему.
Фото: Newcastle Chronicle
Мозг начал расти!
Когда Ной родился, у него было меньше 2 процентов от мозга. Кроме практически полного отсутствия мозга, у него была также парализована нижняя часть туловища от груди. Врачи провели 5-часовую операцию, зашивая отверстие в спине Ноя, а затем установили шунт в череп, чтобы откачивать лишнюю жидкость из мозга.
Через десять дней после рождения Ноя выписали из больницы. Родители продолжали регулярно посещать с Ноем медицинский центр, чтобы откачивать жидкость из мозга мальчика, и не переставали верить, что Ной выживет.
Шелли и Роб окружали мальчика любовью, лаской и заботой. И мозг Ноя начал расти, расти и расти – занимая пространство, в котором раньше была жидкость.
Когда Ною исполнилось 3 года, сканирование мозга показало, что его мозг «расширился до 80% от состояния нормального мозга».
Ной с доктором Клэр Николсон. Фото: Channel 5
«Мам, все в порядке?» – он считает и ходит в школу
На снимках видно, каким был мозг Ноя при рождении, и каким стал в возрасте 3-х лет.
Нейрохирург Клэр Николсон, наблюдающая Ноя с рождения, называет его «необыкновенным ребенком с необыкновенными родителями» и подчеркивает, что история Ноя стала открытием для медицинского сообщества.
Сегодня Ною 4 года, и его мозг продолжает развиваться. Родители и старшая сестра Ноя Стеф помогают стимулировать его мозг, они называют это «тренировкой». Благодаря постоянному вниманию и заботе Ной научился считать до десяти, может держать ручку и даже посещает местную начальную школу – невероятный успех, о котором никто даже не мог мечтать.
Ной очень улыбчивый и заботливый мальчик, – когда Шелли начинает плакать, рассказывая о нем, он спрашивает: «Мам, все в порядке?»
Ной с мамой. Фото: Newcastle Chronicle
Отец верит, что Ной сможет ходить
Аномалия развития позвоночника спина бифида привела к параличу от груди до ног, поэтому Ной вынужден передвигаться в инвалидном кресле. Но после серии болезненных и сложных операций появилась надежда, что в один прекрасный день он сможет ходить.
Отец Ноя Роб говорит, что «верит в то, что Ной сможет ходить, – либо с помощью механических средств, либо самостоятельно».
И вера родителей творит чудеса – спустя четыре года после рождения Ной продолжает жить и радовать своих близких вопреки прогнозам врачей.
Фото: Newcastle Chronicle
Перевод Марии Строгановой специально для портала «Православие и мир»
Реанимация и интенсивная терапия новорожденных с асфиксией
Общепринятого определения асфиксии новорожденного пока не существует. Наиболее информативной и объективной представляется дефиниция асфиксии, представленная Н. П. Шабаловым и соавторами (2003). Они считают асфиксией новорожденного синдром, характеризующ
Общепринятого определения асфиксии новорожденного пока не существует. Наиболее информативной и объективной представляется дефиниция асфиксии, представленная Н. П. Шабаловым и соавторами (2003). Они считают асфиксией новорожденного синдром, характеризующийся отсутствием эффективности газообмена в легких сразу после рождения, неспособность самостоятельно дышать при наличии сердцебиений и (или) других признаков живорожденности (спонтанное движение мышц, пульсация пуповины).
До середины 1980-х гг. основным критерием диагностики асфиксии была оценка по шкале Апгар, что нашло отражение в Международной классификации болезней 9-го пересмотра (1975). Однако в 1986 г. Американская академия педиатрии и Американский колледж акушеров и гинекологов на основании многочисленных катамнестических исследований пришли к заключению о том, что баллы по шкале Апгар через 1 и 5 мин после рождения слабо коррелируют как с причиной данного состояния, так и с прогнозом и сами по себе не должны рассматриваться как показатели проявления или последствия асфиксии.
В то же время при состоянии с низкой оценкой по шкале Апгар (0–3 балла), сохраняющемся в течение 15 мин, детский церебральный паралич наблюдается у 10%, а в течение 20 мин — у 60% пациентов.
Несмотря на критическое отношение к шкале Апгар и вопреки мнению о том, что она не должна рассматриваться в качестве критерия диагностики и степени тяжести асфиксии в родах (Н. П. Шабалов и соавт., 2003), целесообразо обратиться непосредственно к Международной классификации болезней 10-го пересмотра (1993).
Рубрика Р 21. Асфиксия при родах
Примечание. Эту рубрику не следует использовать при низких показателях по шкале Апгар без упоминания об асфиксии и других дыхательных расстройствах.
Р 21.0. Тяжелая асфиксия при рождении.
Пульс при рождении менее 100 уд./мин, замедляющийся или устойчивый, дыхание отсутствует или затруднено, кожа бледная, мышцы атоничны. Асфиксия с оценкой по шкале Апгар 0–3 балла через минуту после рождения. Белая асфиксия.
Р 21.1. Средняя и умеренная асфиксия при рождении.
Нормальное дыхание в течение первой минуты после рождения не установилось, но частота сердцебиений составляет 100 уд./мин или более, незначительный мышечный тонус, незначительный ответ на раздражение.
Оценка по шкале Апгар 4–7 баллов через минуту после рождения. Синяя асфиксия.
Различают также острую асфиксию, являющуюся проявлением интранатальной гипоксии, и асфиксию, развившуюся на фоне хронической внутриутробной антенатальной гипоксии.
Частота встречаемости асфиксии новорожденных, по данным различных авторов, колеблется в весьма широких пределах, что, очевидно, связано с отсутствием общепринятой дефиниции. Так, Саrter и соавторы (1993) полагают, что частота асфиксии составляет 1–1,5%. Еще в 10–15% случаев низкая оценка по шкале Апгар оказывается обусловлена кардиореспираторной депрессией. В сумме названные состояния составляют до 16,5%. Примерно такие же показатели за 2003 г. опубликованы Министерством здравоохранения и социального развития РФ. При этом летальность от асфиксии среди доношенных детей составляет 0,2%, а среди недоношенных — 1,16%.
По данным С. Г. Эзутаган (1999), частота перинатальной асфиксии у недоношенных детей составляет 30%, а у доношенных новорожденных — 20%.
Н. Н. Володин и С. О. Рогаткин (2004) сообщают, что ежегодно в мире рождаются в состоянии асфиксии 4 млн детей: 840 тыс. из них умирают, еще столько же в дальнейшем страдают от стойких нарушений функциональной деятельности центральной нервной системы.
Выделяют пять главных причин асфиксии новорожденного.
Гипоксемия, гиперкапния и связанный с ними ацидоз являются ведущими звеньями патогенеза асфиксии. Они активируют гемодинамическое перераспределение объемов крови, секрецию гормонов стрессового типа, продукцию цитокинов, молекул адгезии и факторов роста, каскадную систему плазменных протеаз. Эти же факторы после реоксигенации активируют перекисное окисление липидов клеточных мембран с образованием метаболитов арахидоновой кислоты (простагландинов и лейкотриенов) и повышением содержания клеточных метаболитов (аденозина, оксида азота, эндотелина и др.).
Напряжение кислорода в крови ниже 40 мм рт. ст. включает так называемый «ишемический рефлекс», хеморецепторный механизм которого приводит к возбуждению одновременно вазомоторного и дыхательного центров, централизации кровообращения, т. е. ишемии кожи, легких, почек, печени, желудочно-кишечного тракта, ради обеспечения жизненно важных органов (сердца, мозга, диафрагмы, надпочечников).
В процессе централизации кровообращения, кроме адреналина и норадреналина, участвуют ангиотензин II и вазопрессин.
Высокое сопротивление сосудов малого круга, поддерживаемое гипоксемией и гиперкапнией, является причиной легочной гипертензии и шунтирования крови, дыхательной недостаточности, а также перегрузки правых отделов сердца давлением, а левых отделов — объемом.
Отрицательным эффектом гипоксемии, гиперкапнии и централизации кровообращения является накопление недоокисленных продуктов и тяжелый смешанный ацидоз. Компенсаторная активация анаэробного гликолиза с накоплением лактата еще больше усиливает ацидоз. Последний крайне отрицательно влияет на системную гемодинамику, микроциркуляцию, гемореологию, водно-электролитный баланс, обменные процессы.
Нарастание гипоксии и смешанного ацидоза вызывает раскрытие прекапиллярных сфинктеров, децентрализацию кровообращения с падением артериального давления, т. е. гемодинамический коллапс, снижающий тканевую перфузию в жизненно важных органах.
В сосудах ишемизированных тканей активизируются тромбоциты, эндотелиоциты, моноциты, что приводит к активации каскада плазменных протеаз, а также освобождению клеточных ферментов, про- и антикоагулянтов, метаболитов арахидоновой кислоты, активных форм кислорода и оксида азота, которые причастны к повреждению функции органов.
Активация тромбиновой, фибринолитической, кининовой и системы комплемента ведет к эндотоксикозу продуктами протеолиза и наряду с ацидозом — к повреждению мембран клеток, митохондрий, лизосом, гематоэнцефалического барьера, повышению сосудистой проницаемости, падению сосудистого тонуса, деструкции клеток, отеку интерстициального пространства, сладж-феномену, запуску внутрисосудистого свертывания, тромбозу, блокаде микроциркуляции, дистрофическим процессам, в конечном счете — к полиорганной недостаточности.
Клинические признаки и симптомы
При асфиксии средней тяжести ребенок рождается с апноэ или с единичными гаспами, с частотой сердцебиений 90–160 уд./мин, со сниженным мышечным тонусом и рефлекторным ответом на назофарингеальный катетер, с выраженным цианозом (синяя асфиксия). Общее состояние оценивается как тяжелое или средней тяжести. В первые минуты жизни ребенок вял, быстро охлаждается. Слабо реагирует на осмотр и раздражения. Спонтанная двигательная активность низкая. Физиологические рефлексы угнетены. При аускультации сердца часто выявляют тахикардию, приглушенность тонов, акцент II тона над легочной артерией. Дыхание нередко с участием вспомогательной мускулатуры, аускультации — ослабленное, с обилием сухих и разнокалиберных влажных хрипов.
Нередко уже в первые часы жизни появляются гипервозбудимость, крупноразмашистый тремор рук, гиперстезия, спонтанный рефлекс Моро, кратковременные судороги. В то же время у некоторых пациентов нарастают клинические признаки угнетения центральной нервной системы. Динамика мышечного тонуса, физиологические рефлексы, признаки угнетения или повышенной возбудимости нервной системы весьма индивидуальны и во многом зависят от адекватности оказания помощи.
Тяжелая асфиксия характеризуется наличием при рождении признаков II или III стадии шока: дыхание отсутствует или наблюдаются неэффективные гаспы, пульс менее 100 уд./мин, кожные покровы очень бледные (белая асфиксия), мышцы атоничны, реакция на назофарингеальный катетер отсутствует, симптом «белого пятна» более 3 с, артериальная гипотония.
Общее состояние оценивается как тяжелое или крайне тяжелое.
В первые часы и дни жизни клиническая картина обусловлена полиорганной недостаточностью. Со стороны центральной нервной системы: гипоксически-ишемическая энцефалопатия, отек мозга, внутричерепные кровоизлияния, судороги.
Со стороны легких: синдром аспирации меконием, легочная гипертензия, синдром дыхательных расстройств II типа.
Со стороны сердечно-сосудистой системы: шок, гипотензия, полицитемия, гиперволемия или гиповолемия, патологическое шунтирование крови, трикуспидальная недостаточность, ишемические некрозы эндокарда/миокарда.
Со стороны выделительной системы: олигурия, острая почечная недостаточность с тромбозами сосудов почек или без них.
Со стороны желудочно-кишечного тракта: функциональная непроходимость, рвота, срыгивания, печеночные дисфункции, некротизирующий энтероколит.
Со стороны эндокринной системы: транзиторная недостаточность симпато-адреналовой системы, щитовидной железы, надпочечников.
Все это сопровождается нарушениями гомеостаза (декомпенсированный ацидоз, гипогликемия, гипокальциемия, гипоантриемия, гипомагниемия) и гемостаза (тромбоцитопения, ДВС-синдром).
Вторичный иммунодефицит, сопровождающий полиорганную недостаточность, способствует активации и генерализации внутриутробных инфекций, а также развитию госпитальных инфекций.
Диагностика и рекомендуемые клинические исследования
Критериями тяжелой асфиксии являются:
Важными критериями тяжести асфиксии являются ответ на адекватную терапию, а также течение и исход патологии в раннем неонатальном периоде, отражающие выраженность повреждения витальных функций. Следовательно, окончательно тяжесть асфиксии диагностируют не сразу после родов, а по окончании раннего неонатального периода.
Необходимый объем исследований:
В оптимальном варианте — допплерографическое определение центральной и церебральной гемодинамики.
С учетом необходимости проведения дифференциального диагноза с тяжелыми инфекционными заболеваниями показано микробиологическое, вирусологическое исследование.
Дифференциальный диагноз в первую очередь необходимо проводить со следующими состояниями:
Общие принципы лечения
Проведение реанимационных мероприятий при асфиксии новорожденных регламентируется приказом министра здравоохранения и медицинской промышленности РФ «Первичная и реанимационная помощь новорожденному в родильном зале» (1995 г.).
При оказании реанимационной помощи новорожденному необходимо строго соблюдать следующую последовательность действий:
Лекарственные средства (ЛС) при первичной реанимации назначаются при отсутствии сердцебиения и в тех случаях, когда несмотря на искусственную вентиляцию легких (ИВЛ) 100% кислородом и непрямой массаж сердца, проведенные в течение 30 с, у ребенка сохраняется брадикардия ниже 80 уд./мин.
Используются следующие ЛС: раствор адреналина гидрохлорида, препараты, восполняющие объем циркулирующей жидкости (раствор альбумина 5%, изотонический раствор натрия хлорида, раствор рингера), раствор гидрокарбоната натрия 4%.
Адреналина гидрохлорид является синтетическим аналогом адреналина надпочечников. Обладает адренопозитивным действием, оказывая стимулирующее влияние на α- и β-адренорецепторы. Инотропное кардиотоническое действие адреналина связано с воздействием на β1-адренорецепторы, локализующиеся в миокарде. Это ведет к повышению силы и частоты сердечных сокращений. Наряду с этим адреналин, воздействуя на α-адренорецепторы, повышает периферическое сосудистое сопротивление и артериальное давление крови, тем самым увеличивая коронарный кровоток и кровоснабжение миокарда.
Бронхорасширяющее действие адреналина обусловлено воздействием на β2-адренорецепторы.
Адреналин вводится новорожденным в разведении 1:10 000 в объеме 0,1–0,3 мл/кг массы тела (0,01–0,03 мг/кг) внутривенно или эндотрахеально. При введении через эндотрахеальную трубку требуется дополнительное разведение физиологическим раствором (1:1). Внутривенно адреналин вводится струйно.
В результате должно наблюдаться увеличение частоты сердечных сокращений до 100 уд./мин и выше через 30 с после введения ЛС. Если частота сердечных сокращений остается менее 100 уд./мин, следует повторить введение адреналина. При отсутствии эффекта и признаков общей кровопотери или гиповолемии необходимо ввести восполнители объема циркулирующей крови.
Показаниями к восполнению объема циркулирующей крови служат кровопотеря и гиповолемия. При этом наблюдаются следующие симптомы:
Восполнители объема циркулирующей крови (изотонический раствор натрия хлорида, раствор альбумина 5%, раствор рингера) вводятся новорожденным при первичной реанимации в вену пуповины из расчета 10 мл/кг массы тела в течение 5–10 мин.
Показания к применению гидрокарбоната натрия:
Используется 4% раствор гидрокарбоната натрия, содержащий 0,5 мэкв/мл. Назначается в дозе 2 мэкв (4 мл 4% раствора) на кг массы тела. Вводится в вену пуповины на фоне ИВЛ со скоростью не выше 1 мэкв /кг/мин.
Ожидаемый эффект: увеличение частоты сердечных сокращений до 100 и более ударов в минуту на фоне уменьшения метаболического ацидоза.
Положительный эффект от реанимационных мероприятий — в течение первых 20 мин после рождения восстанавливаются адекватное дыхание, нормальные частота сердечных сокращений и цвет кожных покровов — служит основанием к прекращению ИВЛ и непрямого массажа сердца. Однако реанимация в родильном зале является лишь первым этапом оказания помощи детям, родившимся c асфиксией.
Дальнейшее наблюдение и лечение новорожденных, перенесших асфиксию, в том числе и детей, у которых не восстановилось адекватное дыхание, наблюдаются судороги, центральный цианоз, проводится в отделении интенсивной терапии.
При внутривенном введении раствора гидрокарбоната натрия на фоне неадекватной вентиляции возможно усиление ацидоза, а избыточное введение этого ЛС ведет к гипернатриемии и риску развития внутрижелудочковых кровоизлияний.
Эффективная сердечно-легочная реанимация при асфиксии является главным фактором, улучшающим прогноз. При средней и умеренной асфиксии прогноз, как правило, благоприятный. При тяжелой асфиксии персистирующая низкая оценка по шкале Апгар (0–3 балла) на 10, 15 и 20-й минутах достаточно тесно коррелирует с неблагоприятным исходом и указывает на повышенный риск смерти (60% — у доношенных новорожденных и 50–100 % — у детей с очень малой массой тела).
Литература
А. Г. Антонов, доктор медицинских наук, профессор
НЦАГиП РАМН, Москва