Нарушение мозгового кровообращения
Диагностика головной боли – комплексное обследование
Кровоснабжение головного мозга – это его питание. Мозгу для нормального функционирования необходима высокая скорость клеточного метаболизма (обмена веществ), что требует отличной циркуляции крови, несущей кислород. Ведь именно мозг потребляет 25% поступающего при дыхании кислорода.
Причины ухудшения кровообращения головного мозга
При некоторых патологиях происходит стеноз (сужение) просвета сосуда или его обтурация (закупорка). В результате замедляется скорость кровотока, в отдельных участках мозга возникает ишемия (кислородное голодание ткани), приводящее к некрозу (омертвлению) ткани.
Факторами риска являются:
Симптомы ухудшения кровообращение головного мозга
Различают острое (ОНМК – инсульт) и хроническое (ХНМК – дисциркуляторная энцефалопатия) нарушение мозгового кровообращения (МК).
Для ОМНК характерны следующие симптомы:
При ХНМК развивается следующая симптоматика:
Последствия нарушения кровообращения головного мозга
Мозг – наиболее уязвимый к нехватке кислорода орган. Циркуляционный объем крови в головном мозге остается практически неизменным и составляет порядка 750 мл. Так как нервная ткань не способна сохранять кислород, его запаса хватает на 8–10 секунд. Когда клетки мозга лишены кровоснабжения, т. е. нет доступа жизненно важных питательных веществ и кислорода, они умирают – происходит инсульт.
Последствия инсульта могут варьировать в широких пределах в зависимости от участка головного мозга, серьезности нарушений, общего состояния здоровья человека.
Нарушения кровообращения головного мозга включают:
Они, как правило, являются результатом ранее существовавших сосудистых заболеваний, врожденной патологии или могут быть спровоцированы травмой.
Лечение и профилактика нарушений мозгового кровообращения
Инсульт – одна из ведущих причин смерти и наиболее распространенная причина инвалидности.
Профилактика инсульта включает:
Адекватная терапия нарушений мозгового кровообращения начинается с обследования и установления точной причины патологии. Нельзя заниматься самолечением и бессистемно сбивать давление – это нарушает скоординированную работу сердечно-сосудистой системы, повышает нагрузку на стенки сосудов, что приводит к образованию аневризм, стенозов и как следствие, нарушению почечной фильтрации, усугубляя тем самым течение гипертонической болезни, повышая риск инсультов и инфарктов. При нерегулярном и неправильно приеме гипотензивных средств, падает церебральное перфузионное давление, что вызывает закупорку кровеносных сосудов и гипоксию мозга. Присутствие малейших симптомов нарушения МК – повод незамедлительно обратиться к врачу.
К большому сожалению, на фоне постоянных стрессов, неправильного питания, несвоевременного обследования, бесконтрольного приема лекарственных средств, нарушение мозгового кровообращения стало поражать людей молодого возраста. Иногда, частые головные боли могут свидетельствовать о начале изменений в сосудах головного мозга, в связи, с чем прием обезболивающих средств может затруднять своевременную диагностику и приводить к осложнениям.
Начальное обследование кровоснабжения головного мозга должно включать:
Это обязательный перечень для базового исследования для определения рисков или степени нарушения мозгового кровообращения, но врач на основании полученных данных осмотра, анамнеза и результатов исследований может порекомендовать более глубокие обследования, вплоть до КТ и МРТ, для установки степени тяжести состояния, установки правильного диагноза и подбора лечебно-профилактических мероприятий.
Для более подробной консультации, осмотра и обследований обращайтесь к специалистам медицинского центра «Президент-Мед».
Органическое поражение мозга
Понятие «органическое поражение мозга у детей» не имеет четкого и однозначного определения.
Но принято считать, что это – целый комплекс нарушений, связанных со структурными патологическими изменениями в тканях головного мозга.
Они могут быть как диффузными (например, появиться вследствие энцефалопатии) так и локализованными (возникнуть в результате опухоли или травмы головного мозга)
У таких детей нарушены функции многих тканей в мозгу и не только, нужно немало времени, чтобы они поменялись на другие или здоровые, которые будут выполнять свои функции правильно.
В современной педиатрии такое явление, к сожалению, это не редкость.
Головной мозг детей подвержен целому ряду негативных воздействий
Более того, невропатологи утверждают, что диагноз «органическое повреждение головного мозга» сегодня можно ставить 9 из 10 пациентов любого возраста.
Просто большая часть таких поражений не дает о себе знать.
Симптомы ОПМ ярко проявляются тогда, когда изменением подверглись от 20 до 50% органа.
Если же повреждение охватило больше половины мозга, тогда стоит говорить о серьезных признаках болезни, носящих стойкий патологический характер.
Но есть и другая сторона медали: часто не слишком квалифицированные специалисты просто злоупотребляют данным диагнозом, не желая глубоко анализировать характер неврологической патологии у ребенка.
В медицине существует классификация недугов, которые можно объединить под термином ОПМ (органическое поражение мозга).
Заболевания, относящиеся к органическим поражениям головного мозга:
Гидроцефалии
Врожденные аномалии развития головного мозга
Детский церебральный паралич ДЦП
Нарушения, вызванные внутриутробными инфекциями
Группа заболеваний, вызванных поражением центральной нервной системы (ЦНС)
Каждый недуг, входящий в эту группу, характеризуется множеством нюансов – имеет свою природу и развивается особым образом
От причины развития болезни во многом зависит и характер его лечения
Существует несколько основных причин возникновения органического поражения головного мозга у детей
Патогенез
Наиболее значимым фактором риска поражения мелких сосудов головного мозга является артериальная гипертензия [23]. При дисциркуляторной энцефалопатии встречаются как первичные сосудистые, так и вторичные дегенеративные изменения вещества головного мозга.
Выделяют несколько видов патологических изменений вещества головного мозга, ассоциированных с хроническим ишемическим повреждением [2,29,42].
Атеросклероз поражает артерии эластического и крупные артерии мышечного типа. В большинстве случаев атеросклероз приводит к развитию острых нарушений мозгового кровообращения с быстрым развитием выраженных очаговых симптомов. В патогенезе хронических сосудистых заболеваний головного мозга основное значение имеет поражение микроциркуляторного русла. Оно образовано терминальными ветвями крупных артерий каротидного и вертебрально-базилярного бассейна, а также притоками церебральных вен. Артерии микроциркуляторного русла подвержены изменениями при резких перепадах артериального давления поскольку на этом уровне не образуются анастомозы.
Болезнь мелких сосудов или микроангиопатия может иметь различной этиологии:
В ряде случаев, нарушения микроциркуляции могут быть вызваны патологией со стороны системы крови, без поражения кровеносных сосудов. Истинная полицитемия, гемоглобинопатии или протеинопатии могут повышать вязкость крови, что приводит к сопротивлению кровотоку и агрегации форменных элементов, является причиной церебральной ишемии. В редких случаях возможно развитие микроэмболии. Важными дополнительными факторами могут быть нарушения обмена веществ, прежде всего, сахарный диабет и нарушение венозного оттока.
Нарушения ауторегуляции мозгового кровообращения являются как причиной, так и следствием поражения микрососудов, принимая участие в порочном круге патологических изменений.
Лейкоареоз — нейровизуализационный термин (снижение рентгеновской плотности на КТ головного мозга, повышение интенсивности сигнала по данным МРТ в Т2/FLAIR режимах), описывающий неспецифические изменения подкоркового белого вещества головного мозга. Выявляются двусторонние очаговые, иногда сливные изменения. В основе лейкоареоза лежит поражение мелких артерий и артериол вследствие липогиалиноза (также обозначается как артериосклероз) и микроатероматоза [11].
Факторами риска развития лейкоареоза являются возраст, повышенное артериальное давление и сахарный диабет [18]. Повышение внутрижелудочкового давления рассматривается в качестве дополнительного механизма развития лейкоареоза, оно приводит к нарушению микроциркуляции в прилегающих к желудочкам участках головного мозга. У пациентов с нормотензивной гидроцефалией отмечаются распространённые изменения подкоркового белого вещества [21].
Доказана связь распространенности диффузных изменений белого вещества головного мозга с выраженностью депрессии и когнитивных нарушений [9,43].
В препаратах головного мозга лейкоареоз часто сочетается с расширением периваскулярных (Вирхова-Робина) пространств — криблюрами (‘etát criblé’). Этот феномен связывают с повторными эпизодами ишемии и плазматического пропитывания участков ткани, окружающих микрососуды.
Липогиалиноз — дистрофический процесс, поражающий пенетрирующие артерии и артериолы диаметром до 200 мкм. Протекает под действием повышения артериального давления, гипергликемии, а также вследствие возрастных изменений. Повышение тканево-сосудистой проницаемости в субэндотелиальном пространстве сосуда приводит к поступлению туда белков плазмы и адсорбции их на изменённых волокнистых структурах соединительной ткани с последующей преципитацией и образованием белка гиалина. В последующем, гиалин оттесняет и разрушает эластичную мембрану, средняя оболочка истончается, и перфорирующая артерия приобретает вид стекловидной трубочки. Просвет артерии резко сужается, возможно развитие окклюзии.
При развитии липогиалиноза фоне сахарного диабета субэндотелиально часто откладывается не только гиалин, но и липиды. Сосудистая стенка инфильтрируется макрофагами с включениям фагоцитированных липидов — пенистыми клетками. В изменённых тканях происходит отложение фибриноида (сложного вещества, состоящего из белков и полисахаридов, распадающихся коллагеновых волокон, межклеточного вещества и плазмы крови). В неблагоприятных условиях происходит гибель окружающих тканей — фибриноидный некроз. Этот патологических процесс выявляется в артериолах и капиллярах головного мозга, сетчатки и почек часто сочетается с гиалинозом.
Этот патологический процесс, видимо является реактивным феноменом. Он не рассматривается, как ведущая причина гипертонического внутричерепного кровоизлияния, так как в препаратах головного мозга в случаях острого внутричерепного кровоизлияния не обнаруживается на отдалении от гематомы. В лабораторных исследованиях выраженные изменения по типу фибриноидного некроза выявлялись вокруг стереотаксически введенных тромбов в опытах у грызунов, что могло указывать на его реактивное происхождение.
Вследствие нарушения работы ассоциации эндотелиоцит-глиальная клетка (астроцит)-нейрон (»нейроваскулярное звено«) страдают механизмы ауторегуляции мозгового кровотока на уровне капилляров и микроартериол. Это приводит к сужению диапазона допустимых показателей перфузии. Из-за того, что мелкие сосуды утрачивают способность расширяться, становится невозможным перераспределение кровотока в пользу активно работающих отделов мозга, а это в свою очередь приводит к их функциональной инактивации, а затем – и к необратимому повреждению. Преимущественное поражение белого вещества в перивентрикулярном и глубинных отделах при церебральной гипоперфузии объясняется особым характером их кровоснабжения сосудами терминального типа, не имеющими коллатералей.
Клетки нервной ткани различаются по чувствительности к ишемии. При нарушении кровотока, некротические изменения развиваются сначала в нейронах, затем олигодендроцитах, миелинизированных аксонах, астроцитах и наконец в эндотелиальных клетках [38]. После гибели наиболее чувствительных типов клеток — нейронов и олигодендроцитов, относительно резистентные к ишемии астроциты, выполняющие в головном мозге опорную функцию, замещают дефект за счёт увеличения в объёме своих отростков. Формируется глиальный рубец (»неполный» инфаркт») [33]. При тотальной гибели всех элементов участка мозговой ткани формируется участок некроза (лакуна), на периферии регенерация глиальных клеток формирует его «оболочку».
В патологоанатомических исследованиях отмечена связь липогиалиноза мелких артерий с лакунарными инфарктами головного мозга. Указывается на более высокую распространённость расширенных периваскулярных пространств у пациентов с сосудистой деменцией, чем у пациентов с болезнью Альцгеймера [30]. У здоровых пожилых пациентов с выявленными расширенными периваскулярными пространствами отмечались худшие результаты тестирования когнитивных функций.
Микроатероматоз — атеросклеротическое поражение артериол, приводит к развитию более крупных лакунарных инфарктов. В зависимости от локализации, инфаркты могут проявляться клиникой инсульта, но чаще (примерно в 80 % случаев) протекают субклинически (»немые» инфаркты)[40]. У части пациентов основные патологические процессы вызываются церебральной амилоидной ангиопатией (ЦАА) — отложением амилоидных пептидов (прежде всего Аβ — амилоида) в мышечной оболочке и адвентиции микрососудов и сосудов среднего калибра, значительно реже в стенках капилляров и вен.
Частота выявления амилоидоза церебральных артерий на аутопсии с возрастом увеличивается: на основании серии из 784 аутопсийных материалов, признаки умеренной и тяжёлой ЦАА встречались с частотой 2.3% в возрасте от 65 до 74 лет, 8.0% в возрасте от 75 до 84 лет, и 12.1% в возрасте старше 85 лет [14].
Значимых половых различий во встречаемости амилоидоза не выявлено. Несмотря на то, что вопрос связи ЦАА с артериальной гипертензией продолжает обсуждаться, очевидно, что в большом количестве случаев у пациентов при жизни отмечалось нормальное артериальное давление[3].
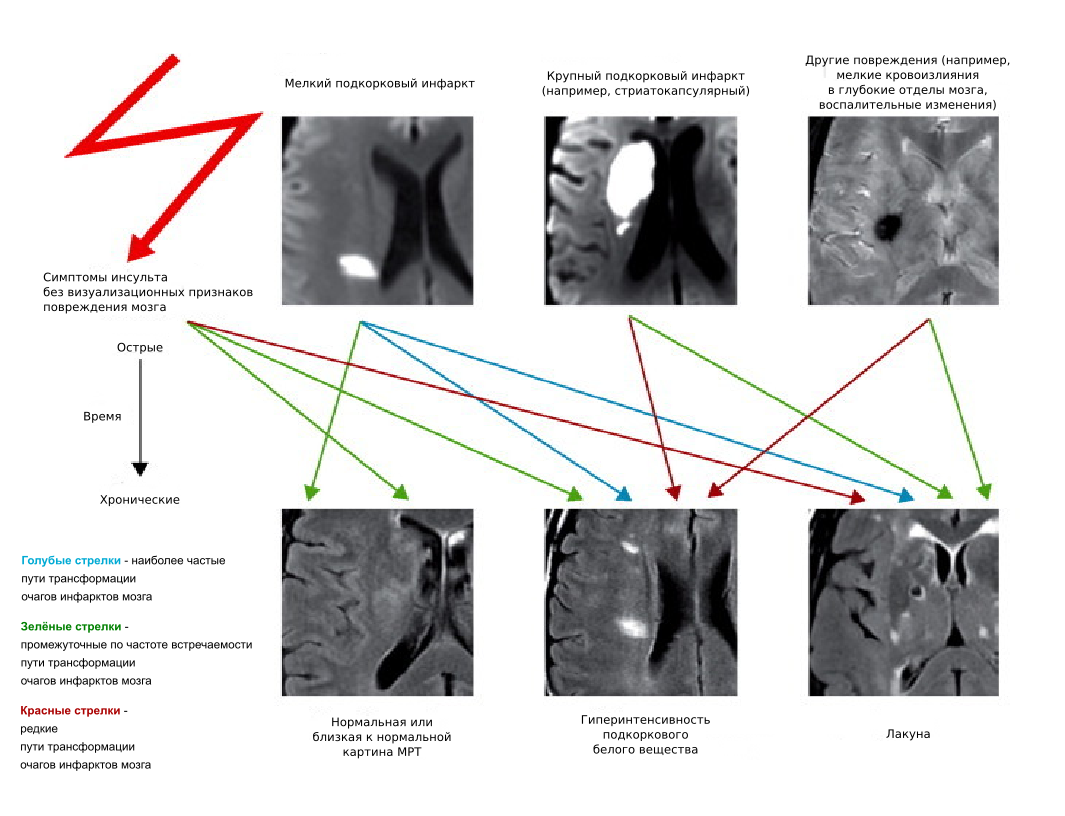
Рисунок 1. Пути трансформации мелких сосудистых очагов и сходство МРТ картины отдалённых последствий поражения мозга различной природы
Предполагается, что амилоидные пептиды, блокируют отток по переваскулярным пространствам, выполняющим в головном мозге дренажную функцию. Повышение ломкости стенки сосудов при отложении амилоида значительно увеличивает риск внутримозговых кровоизлияний. Они, как правило, имеют небольшие размеры и располагаются кнаружи от внутренней капсулы, в белом веществе больших полушарий, для сравнения, гипертонические кровоизлияния поражают преимущественно область подкорковых ядер. В связи с таким расположением микрокровоизлияний при ЦАА, подкорковые структуры остаются относительно интактными, поэтому, экстрапирамидные симптомы не характерны для клиники этого состояния. По данным Фрамингемского исследования установлена связь деменции и внутримозговых микрокровоизлияний, которая не зависела от выраженности других сердечно-сосудистых факторов риска. Наличие ЦАА предполагается у пациентов старше 55–60 лет с множественными лобарными кровоизлияниями без другой явной причины.
Бостонские критерии для кровоизлияний, связанных с церебральной амилоидной ангиопатией [19]
* приём варфарина с превышением целевого значения МНО (> 3,0), перенесённые инсульты и черепно-мозговые травмы, опухоли головного мозга, сосудистые аномалии и васкулиты, патология системы крови, коагулопатии [41].
У пациентов с подозрением на церебральную амилоидную ангиопатию, развитие острых и транзиторных неврологических нарушений может быть связано с геморрагическими осложнениями, что стоит принимать во внимание при планировании их обследования.
У пациентов с выраженным лейкоареозом и множественными лакунарными инфарктами в отсутствии факторов риска сосудистых заболеваний стоит предположить наличие церебральной аутосомно-доминантной артериопатии с подкорковыми инфарктами и лейкоэнцефалопатией (CADASIL) — наследственного заболевания, вызванного мутацией гена Notch 3 на 19-й хромосоме. У трети пациентов, страдающих этим заболеванием, отмечается мигрень с аурой, которая рассматривается как раннее проявление заболевания. Приблизительно у 75% лиц, носителей мутации, в конечном счёте развивается деменция[27].
Таким образом, хронические сосудистые поражения головного мозга определяются большим количеством факторов риска, как генетических, так и средовых. Профиль факторов риска развития дисциркуляторной энцефалопатии и инсульта не тождественны. Поражение артерий мозга может быть и изолированным — встречается у пациентов без поражения прецеребральных артерий и артериальной гипертензии.
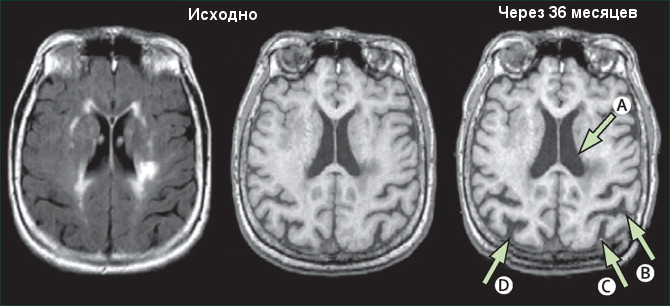
Рисунок 2. Динамика атрофических изменений вещества головного мозга
В патогенезе развития основных симптомов дисциркуляторной энцефалопатии (когнитивных нарушений, нарушений ходьбы, пирамидных и мозжечковых знаков, псевдобульбарного синдрома) лежит разобщение корковых и подкорковых структур вследствие поражения подкоркового белого вещества больших полушарий. Нарушается работа корково-подкорковых кругов, обеспечивающих последовательную избирательную активизацию отдельных участков коры головного мозга при выполнении сложных многоэтапных действий, поддерживающих общий уровень активности коры, несущих информацию для коррекции действий на стадии афферентного синтеза и исполнения (функции I [энергетического] и III [программирование, регуляция и контроль] блоков по А. Р. Лурия).
Клинико-нейровизуализационные соответствия
Термин «энцефалопатия» предполагает наличие не только субъективных жалоб, но и объективных признаков органического поражения мозга, выявляемых при неврологическом или нейропсихологическом исследовании [2]. Вместе с тем, обнаружение подобных признаков, даже вкупе с сосудистыми факторами риска, клиническими или параклиническими признаками цереброваскулярной патологии является необходимым, но недостаточным признаком ДЭП. Важнейшим принципом диагностики ДЭП должна стать констатация причинно-следственной связи между имеющимися у больного клиническими проявлениями и цереброваскулярным заболеванием.
Подобный принцип впервые был заложен в критерии клинической диагностики сосудистой деменции NINDS-AIREN. Представляется, что только следование этому принципу позволит избежать гипердиагностики ДЭП и отделить случаи ДЭП от нейродегенеративных заболеваний, широко представленных у лиц пожилого возраста (в первую очередь от болезни Альцгеймера или болезни Паркинсона, набор симптомов которых на начальных стадиях может соответствовать последствиям хронического сосудистого поражения головного мозга).
Доказательством причинно-следственной связи могут служить:
КТ или МРТ головного мозга при ДЭП могут выявить: двустороннее более или менее симметричное диффузное поражение белого вещества (лейкоареоз) в перивентрикулярной зоне, зрительной лучистости, семиовальном центре; множественные лакунарные очаги (размером 3–15 мм) в базальных ганглиях, таламусе, мосте, мозжечке, внутренней капсуле, белом веществе лобных долей; более крупные корковые и подкорковые инфаркты, отражающие патологию крупных артерий. Церебральная атрофия, выявляемая при КТ или МРТ у больных ДЭП, обычно сопровождает лейкоареоз, лакунарые или территориальные инфаркты [2]. Как правило, расширение желудочковой системы при ДЭП более выражено, чем расширение корковых борозд, и может отражать не только убыль мозгового вещества в глубинных отделах мозга, но и, возможно, снижение резистентности перивентрикулярных тканей к ликвородинамическим воздействиям [2].
В ряде исследований выявлена связь между тяжестью и/или локализацией нейровизуализационных изменений и выраженностью когнитивных и двигательных нарушений [18]. Так, показано, что умеренное когнитивное расстройство возникает, когда распространенность лейкоареоза превышает как минимум 10% белого вещества полушарий, а деменция – если распространенность лейкоареоза превысит 1/4 объема белого вещества полушарий. При наличии лакун выраженность когнитивных нарушений зависит не столько от числа лакунарных очагов, сколько от их локализации (глубинные отделы лобных долей, головка хвостатого ядра и переднее бедро внутренней капсулы, таламус). Выраженность когнитивных нарушений увеличивается при двустороннем поражении указанных структур и сочетании лакунарных очагов с лейкоареозом. Более того, должно быть соответствие между нейровизуализационными изменениями и профилем когнитивных нарушений. Например, в отсутствие соответствующих корковых очагов на КТ и МРТ у пациентов не должны выявляться признаки очагового поражения корковых функций: афазии, апраксии и агнозии. Отмечена также связь между распространенностью лейкоареоза, особенно в передних отделах мозга, локализацией лакунарных очагов в чечевицеобразном ядре и выраженностью нарушений ходьбы и равновесия.
Выраженность когнитивных и двигательных нарушений при ДЭП коррелирует и со степенью расширения боковых желудочков и особенно их передних рогов. С другой стороны, отсутствие сосудистых изменений на МРТ при клинической картине I-III стадий ДЭП и КТ при клинической картине II – III стадий ДЭП может заставлять усомниться в диагнозе. Данные КТ и МРТ имеют значение не только в диагностике ДЭП, но и могут помочь отслеживать динамику заболевания, быть маркером эффективности мер по коррекции факторов риска сердечно-сосудистых осложнений [2]. Отдельные нейровизуализационные феномены считаются нормальным проявлением старения: [12,42]
Аутоиммунные заболевания в неврологии
Разнородная группа заболеваний, в основе которых лежит аутоагрессия иммунной системы организма и выработка активных клеток — антител, разрушающих собственные здоровые клетки и ткани.
Аутоиммунные заболевания могут поражать любые системы и органы, в том числе и нервную систему.
Симптомы аутоиммунных заболеваний нервной системы разнообразны, поскольку для каждого из них характерна выработка специфических антител, поражающих только определенные структуры клеток.
Классификация аутоиммунных заболеваний в неврологии
Основные аутоиммунные заболевания, поражающие центральную нервную систему:
Аутоиммунные заболевания, поражающие периферическую нервную систему (нервные корешки и нервы):
Аутоиммунные заболевания, поражающие мышцы и нервно-мышечный аппарат:
Лечение аутоиммунных заболеваний нервной системы
Общим для всех аутоиммунных заболеваний является подход к лечению. Терапия направлена не столько на коррекцию симптомов поражения нервной системы, сколько на модуляцию работы иммунной системы: применяются кортикостероиды, иммуноглобулины и моноклональные антитела, цитостатики, плазмаферез.
Преимущества лечения аутоиммунных заболеваний нервной системы в клинике Рассвет
Неврологи клиники Рассвет не назначают симптоматические препараты с недоказанной эффективностью. Схемы длительного лечения и профилактики аутоиммунных заболеваний разрабатываются в рамках амбулаторных консультаций. Терапия в дневном стационаре направлена на борьбу с обострениями.
Обзор онкологических заболеваний менингиомы
Вам поставили диагноз: менингиома?
Наверняка Вы задаётесь вопросом: что же теперь делать?
Подобный диагноз всегда делит жизнь на «до» и «после». Все эмоциональные ресурсы пациента и его родных брошены на переживания и страх. Но именно в этот момент необходимо изменить вектор «за что» на вектор «что можно сделать».
Предлагаем Вашему вниманию краткий, но подробный обзор одной из разновидности опухолей головного мозга.
Ежегодно в России выявляют более 8 тысяч новых заболеваний опухолей мозговой оболочки, головного и спинного мозга и других частей центральной нервной системы. Почти такое же количество граждан умирает от данных локализаций.
Филиалы и отделения, где лечат менингиомы
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отделение нейроонкологии
Заведующий – к.м.н. ЗАЙЦЕВ Антон Михайлович
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отделение протонной и фотонной терапии
Заведующий – д.м.н. ГУЛИДОВ Игорь Александрович
Тел: 8 (484) 399 31 30
Менингиомы
Симптомы менингиомы
Симптомы заболевания во многом зависят от места локализации опухоли и могут проявляться в виде:
головных болей; нарушения координации движений; глазодвигательных нарушений (косоглазие, двоение, опущение верхнего века); нарушений зрения – снижения остроты или ограничения периферического зрения чувствительных или двигательных нарушений в конечностях противоположной стороны тела, эпилептических приступов различной структуры, психо-эмоциональных нарушений.
Менингиомы больших размеров могут сопровождаться симптомами повышения внутричерепного давления (головная боль с тошнотой и рвотой), могут вызывать клинические симптомы сдавления мозга и ликворопроводящих путей и угрожать жизни пациента.
Диагностика менингиомы
Лечение менингиомы
В настоящее время выделяют несколько основных методов лечения менингиом.
Хирургическое удаление. Успешность хирургического вмешательства зависит от нескольких факторов – от расположения опухоли по отношению к функционально важным отделам мозга, от близости сосудов и черепно-мозговых нервов, а также от размера менингиомы. Оперативное удаление менингиомы в большинстве случаев заканчивается благополучно. Пациенты относительно быстро могут вернуться к нормальному образу жизни. Однако, вероятность рецидива (повторного образования опухоли) может достигать 20% и более в сроки свыше 10 лет наблюдения и зависит в первую очередь от гистологического подтипа опухоли и радикальности ее удаления.
Альтернативой хирургическому вмешательству при лечении менингиом является лучевая терапия. Этот современный метод облучения отлично себя зарекомендовал при лечении опухолей с локализацией в труднодоступных местах, когда удаление сопряжено с высоким риском функциональных нарушений и хирургических осложнений. Лучевой терапии поддаются опухоли различной величины с максимальной точностью, за один раз или несколькими сеансами лечения, необходимых для получения желаемого результата.
Данные литературы свидетельствуют, что контроль роста доброкачественных менингиом составляет 92-95% (т.е. всего 5-8% рецидивов) при наблюдении свыше 10 лет после лучевой терапии с сохранением высокого уровня качества жизни. Менингиомы 2-й и 3-й степени злокачественности рецидивируют чаще, однако важным преимуществом применения лучевой терапии перед другими методами лечения является возможность неоднократного использования и низкий (в сравнении с другими методами) уровень осложнений.
Таким образом, при менингиомах внутричерепной локализации применение лучевой терапии является оптимальным методом лечения, потому что:
ведет к продолжительному контролю опухолевого роста, который проявляется стабилизацией размеров или уменьшением опухоли;
имеет минимальный риск появления новой или усугубления имеющейся неврологической симптоматики;
позволяет быстро вернуться к повседневной жизненной активности.
Лучевая терапия противопоказана при: больших опухолях (должно быть проведено удаление); наличии выраженной неврологической симптоматики связанной или нет с наличием масс-эффекта; опухолях зрительного нерва с сохранным зрением (проводится фракционированное облучение).
Филиалы и отделения, в которых лечат опухоли головного и спинного мозга, а также отделы центральной нервной системы
ФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, химиотерапевтического и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.