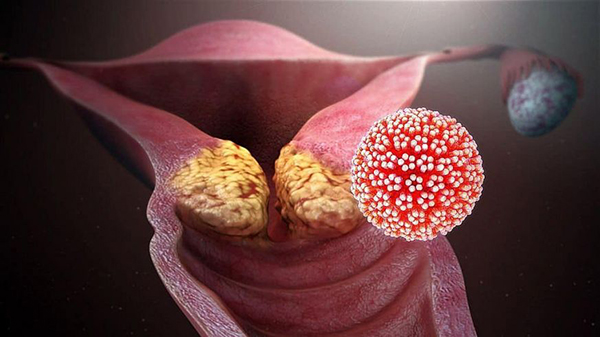
Количественное определение ДНК вируса папилломы человека высокого канцерогенного риска
В лаборатории медицинского центра «Консультант» проводится новое исследование — «Количественное определение ДНК вируса папилломы человека высокого канцерогенного риска (HPV ВКР) 16,18,31,33,35,39,45,51,52,56,58,59,66,68 генотипов (16, 18 и 45 типы определяются отдельно) с выявлением вероятности интеграции вируса в геном человека».
Современные данные о взаимосвязи ВПЧ и рака шейки матки (РШМ)
| Наименование | Цена, руб. |
|---|---|
| Количественное определение ДНК вируса папилломы человека высокого канцерогенного риска (HPV ВКР) 16,18,31,33,35,39,45,51,52,56,58,59,66,68 генотипов (16, 18 и 45 типы определяются отдельно) с выявлением вероятности интеграции вируса в геном человека | 1050 |
| Забор биоматериала | 200 |
Общая информация об ВПЧ высокого канцерогенного риска
Вирусы папилломы человека (ВПЧ) представляют собой широко распространённую и вариабельную группу вирусов, поражающих эпителий кожи и слизистых оболочек и обладающих онкогенным потенциалом. ВПЧ передаётся при тесном контакте с инфицированным эпителием, поэтому основные пути заражения – половой и контактно-бытовой. Возможна передача ВПЧ от инфицированной матери к плоду.
Инкубационный период может длиться от 2 месяцев до 2-10 лет.
Характерно скрытое течение заболевания, при котором отсутствуют клинические проявления. В 30 % случаев в течение 6-12 месяцев может произойти избавление от вируса. Диагностика скрытой ВПЧ-инфекции осуществляется только методом ПЦР.
ВПЧ может по-разному воздействовать на эпителий: способствовать возникновению доброкачественных образований (папиллом, кондилом) или объединению ДНК папиллома-вируса с геном клетки, что приводит к дисплазии (неоплазии) и в дальнейшем к раку (чаще всего в зоне трансформации).
По данным исследований количественное содержание вируса в материале коррелирует со степенью неоплазии: чем выше вирусная нагрузка, тем выраженнее цитологические изменения в эпителии.
При обследовании необходимо учитывать генотип вируса, наличие и степень цитологических и гистологических изменений в тканях, увеличение или снижение вирусной нагрузки через несколько месяцев (6 месяцев и более) после предыдущего обследования, оценить эффективность терапии в процессе лечения.
Показания к назначению теста:
— Первичный скрининг перед цитологическим исследованием.
— Первичный скрининг вместе с цитологическим исследованием для женщин старше 30 лет.
— Для ведения женщин с неопределенным результатом цитологии(ASC-USи ASC-H).
— Для разрешения дискордантных результатов цитологии и кольпоскопии.
— Для контроля эффективности терапии предраковой патологии шейки матки.
— При выявлении цитологических изменений в мазке на атипию.
— При кондиломах и других морфологических изменениях половых путей.
Что означают результаты?
Уровень вирусной нагрузки интерпретируется с учетом результатов цитологического исследования мазков, гистологических изменений в биоптате и генотипа вируса, изменении его количества с течением времени.
Количество ДНК ВПЧ не определяется при отсутствии вируса в исследуемом образце или его минимальном количестве. При этом риск развития патологического процесса, связанного с ВПЧ, минимальный.
— Клинически малозначимая концентрация вируса (менее 10 в третьей степени копий ДНК ВПЧ на 10 в пятой степени клеток) – минимальный риск развития дисплазии, транзиторное течение вирусного процесса.
— Клинически значимая концентрация вируса (более 10 в третьей степени копий ДНК ВПЧ на 10 в пятой степени клеток) – хроническая инфекция с высоким риском развития дисплазии и РШМ.
— Более 10 в пятой степени копий ДНК ВПЧ на 10 в пятой степени клеток при установленном факте персистентного течения инфекции (ВПЧ выявляется более 1 года) – усиленная вирусная нагрузка, ассоциированная с повышенным риском тяжелой дисплазии, часто встречается при РШМ.
Важные замечания
— Снижение вирусной нагрузки в 10 раз за 6 месяцев – транзиторная инфекция.
— Рост вирусной нагрузки через 6 и более месяцев после лечения указывает на возможность рецидива.
— Инфицирование ВПЧ не всегда приводит к раку шейки матки.
— Возможно одновременное заражение несколькими генотипами ВПЧ.
— Результат анализа должен интерпретироваться с учетом заключений цитологического и гистологического исследований и клинической картины.
Клинически не значимо что это
Исследование используется для диагностики папиллома-вирусной инфекции, с одновременным определением количества вирусной ДНК в исследуемом материале. Анализ позволяет сделать вывод о степени поражения слизистой, оценить эффективность терапии в процессе лечения. Определяется суммарное количество ДНК 14 типов ВПЧ высокого канцерогенного риска (ВКР) с отдельным определением ДНК ВПЧ 16-го, 18-го и 45-го генотипов. Тест также позволяет оценить вероятность интеграции ВПЧ 16-го, 18-го и 45-го типа в геном человека (что является опасным и прогностически неблагоприятным фактором).
Папиллома-вирусы высокого канцерогенного риска, вирусы папилломы высокого канцерогенного риска, ВПЧ высокого канцерогенного риска.
Human Papillomavirus, DNA; HPV, Viral Load.
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Вирусы папилломы человека (ВПЧ) представляют собой широко распространённую и вариабельную группу вирусов, поражающих эпителий кожи и слизистых оболочек и обладающих онкогенным потенциалом. ВПЧ передаётся при тесном контакте с инфицированным эпителием, поэтому основные пути заражения – половой и контактно-бытовой. Возможна передача ВПЧ от инфицированной матери к плоду.
К факторам, провоцирующим развитие ВПЧ-инфекции, относятся ранее начало половой жизни, большое количество половых партнеров, сниженный иммунитет, применение оральных контрацептивов, авитаминозы, инфекции, передаваемые половым путём, курение и проживание в крупных городах.
Инкубационный период может длиться от 2 месяцев до 2-10 лет. Характерно скрытое течение заболевания, при котором отсутствуют клинические проявления, а при кольпоскопическом, цитологическом и гистологическом обследовании выявляется норма. В 30 % случаев в течение 6-12 месяцев может произойти избавление от вируса. Диагностика скрытой ВПЧ-инфекции осуществляется только методом ПЦР.
ВПЧ может по-разному воздействовать на эпителий: способствовать возникновению доброкачественных образований (папиллом, кондилом) или объединению ДНК папиллома-вируса с геном клетки, что приводит к дисплазии (неоплазии) и в дальнейшем к раку (чаще всего в переходной зоне шейки матки).
К папиллома-вирусам высокого онкогенного риска относятся ВПЧ типов 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68.
Для выявления возбудителя используется метод полимеразной цепной реакции, которая позволяет обнаружить ДНК вируса. Принцип метода основан на многократном увеличении числа копий специфичного для данного возбудителя участка ДНК.
Полимеразная цепная реакция (ПЦР) – это метод молекулярной диагностики, позволяющий выявлять генетический материал возбудителя на ранних этапах заболевания. Он характеризуется высокими показателями диагностической чувствительности и специфичности, быстротой получения конечного результата и доступностью. Особенностью метода является возможность выявлять ДНК вируса даже при малом содержании её в исследуемом биологическом материале. Метод основан на многократном увеличении числа копий специфичного для данного возбудителя участка ДНК. Для диагностики может использоваться разнообразный биологический материал, взятый у детей, взрослых лиц, людей с патологией иммунной системы, беременных женщин. Метод позволяет определять количество молекул ДНК исследуемого вируса, что является важным в диагностике острой формы инфекции, реактивации персистентной инфекции, носительстве вируса, а также при контроле эффективности проводимой противовирусной терапии.
По данным исследований, количественное содержание вируса в материале коррелирует со степенью неоплазии: чем выше вирусная нагрузка, тем выраженнее цитологические изменения в эпителии. При обследовании необходимо учитывать генотип вируса, наличие и степень цитологических и гистологических изменений в тканях, увеличение или снижение вирусной нагрузки через несколько месяцев (6 месяцев и более) после предыдущего обследования.
В исследовании проводится определение суммарного количества ДНК 14 типов ВПЧ высокого канцерогенного риска (ВКР) с отдельным определением ДНК ВПЧ 16, 18 и 45 генотипов. ВПЧ ВКР являются главной этиологической причиной развития РШМ и предшествующей ему тяжелой дисплазии. ВПЧ обнаруживается в 95 % случаев РШМ, из них 16, 18, 45 генотипы в совокупности являются причиной 75 % плоскоклеточных раков и 94 % аденокарцином шейки матки.
Известно, что развитие РШМ часто ассоциировано с интеграцией ДНК вируса в геном клетки-хозяина. Наиболее часто интегрируют ВПЧ 16 и 18 генотипов, при этом происходит разрыв участка Е1/Е2 при сохранении онкогена Е6/Е7. В тест-системе, на которой выполняется данное исследование, по разным каналам прибора детектируются разные участки генома ВПЧ 16, 18 и 45 типов. Выявление области Е6 при отсутствии области Е1/Е2 позволяет косвенно судить о возможности интеграции вируса в геном человека. В случае обнаружения возможности интеграции вируса в геном в бланк ответа выводится соответствующая информация.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Уровень вирусной нагрузки интерпретируется с учетом результатов цитологического исследования мазков, гистологических изменений в биоптате и генотипа вируса, изменении его количества с течением времени.
Кто назначает исследование?
СОДЕРЖАНИЕ
Типы значимости
Статистическая значимость
Практическое значение
Хотя клиническое значение и практическое значение часто используются как синонимы, использование более технических ограничений означает, что это ошибочное. Такое техническое использование в психологии и психотерапии не только является результатом тщательно проработанной точности и специфики языка, но и позволяет сместить точку зрения с групповых эффектов на специфику изменений внутри индивидуума.
Специальное использование
Напротив, когда он используется в качестве технического термина в психологии и психотерапии, клиническая значимость дает информацию о том, было ли лечение достаточно эффективным, чтобы изменить диагностический ярлык пациента. С точки зрения клинических исследований лечения, клиническая значимость отвечает на вопрос: «Достаточно ли эффективное лечение, чтобы вызвать у пациента нормальное состояние [в отношении рассматриваемых диагностических критериев]?»
В психологии и психотерапии клиническое значение было впервые предложено Якобсоном, Фоллеттом и Ревенсторфом как способ ответить на вопрос, достаточно ли эффективны терапия или лечение, чтобы клиент не соответствовал критериям диагноза? Якобсон и Труакс позже определили клиническую значимость как «степень, в которой терапия выводит кого-либо за пределы неблагополучной популяции или за пределы функциональной популяции». Они предложили два компонента этого индекса изменений: статус пациента или клиента после завершения терапии и «сколько изменений произошло во время курса терапии».
Клиническая значимость также принимается во внимание при интерпретации результатов психологической оценки человека. Часто разница в оценках или промежуточных оценках будет статистически значимой и вряд ли возникнет чисто случайно. Однако не все эти статистически значимые различия клинически значимы, поскольку они не объясняют существующую информацию о клиенте и не дают полезного направления для вмешательства. Небольшие по величине различия обычно не имеют практического значения и вряд ли будут клинически значимыми. Различия, которые распространены среди населения, также вряд ли будут клинически значимыми, потому что они могут просто отражать уровень нормальной человеческой изменчивости. Кроме того, врачи ищут информацию в данных оценки и истории клиента, которая подтверждает актуальность статистической разницы, чтобы установить связь между результатами конкретного теста и более общим функционированием человека.
Расчет клинической значимости
Якобсон-Труакс
Гулликсен-Лорд-Новик
Эдвардс-Наннелли
Метод Эдвардса-Наннелли для расчета клинической значимости является более строгой альтернативой методу Якобсона-Труакса. Показатели надежности используются для приближения оценок перед тестированием к среднему значению, а затем рассчитывается доверительный интервал для этой скорректированной оценки перед тестированием. Доверительные интервалы используются при расчете перехода от предварительного теста к послетестовому, поэтому для демонстрации клинической значимости необходимо большее фактическое изменение баллов по сравнению с методом Якобсона-Труакса.
Хагеман-Арринделл
Расчет клинической значимости Хагемана-Арринделла включает индексы групповых и индивидуальных изменений. Надежность изменений показывает, улучшилось ли состояние пациента, осталось прежним или ухудшилось. Второй индекс, клиническая значимость изменения, указывает на четыре категории, аналогичные тем, которые использовал Якобсон-Труакс: ухудшение, ненадежное изменение, улучшение, но не выздоровление, и выздоровление.
Иерархическое линейное моделирование (HLM)
HLM включает анализ кривой роста вместо сравнений до и после тестирования, поэтому для каждого пациента требуется три точки данных, а не только две точки данных (до и после тестирования). Компьютерная программа, такая как иерархическое линейное и нелинейное моделирование, используется для расчета оценок изменений для каждого участника. HLM также позволяет анализировать модели кривых роста диад и групп.
Стадии рака: классификация онкологических заболеваний
Стадия онкологического заболевания дает информацию о том, насколько велика опухоль и распространилась ли она по организму. Это помогает врачам определять прогноз пациента и план лечения.
С помощью врача-онколога, резидента Высшей школы онкологии Сергея Югая разбираемся, как врачи устанавливают стадии рака и что каждая из них означает.
На что влияет стадия онкологического заболевания?
Стадирование нужно, чтобы спрогнозировать, какие у пациента шансы на выздоровление, а также чтобы определить, какой метод лечения будет наиболее эффективен в конкретном случае, — поясняет Сергей Югай.
Все начинается с медицинского осмотра и обследований — УЗИ, КТ, МРТ, ПЭТ-КТ и других методов в зависимости от вида рака. Затем врач берет кусочек опухоли — биопсию или удаляет опухоль целиком во время операции, а после отправляет материал на гистологический анализ, чтобы поставить диагноз.
Стадии рака по TNM-классификации
Стадии онкологического процесса описывают разными способами — это зависит от вида опухоли. Один из самых распространенных способов — стадирование с помощью TNM-классификации.
Т характеризует первичную опухоль, ее размеры и вовлечение окружающих структур в опухолевый рост, например, прорастание в стенку кишки или желудка. N говорит о наличии в лимфоузлах метастазов и количестве пораженных лимфоузлов, а М — о наличии отдаленных метастазов (во внутренних органах, костях, ЦНС или лимфоузлах, которые расположены далеко от первичной опухоли), — объясняет Сергей Югай.
Индекс Т принимает значения от 0 до 4. 0 означает, что первичная опухоль не обнаружена, 1 — опухоль маленькая, а 4 — опухоль проросла в прилегающие ткани. Таким образом, чем больше цифра рядом с Т, тем ситуация сложнее. При некоторых видах рака N принимает значение 0 или 1, при других — 0, 1 или 2, а иногда — 0, 1, 2 и 3. 0 означает, что опухоль не проникла в ближайшие лимфоузлы, а 3 — что поражено множество лимфоузлов. M0 показывает, что метастазов нет, а 1 — что метастазы есть.
Онкологи выставляют стадию по TNM клинически — до операции или когда операция не планируется и патоморфологически — при изучении удаленной во время операции опухоли, — объясняет Сергей.
Клиническая стадия обозначается буквой «c», например, cT2. Патоморфологическая — буквой «p», например, pN1.
От правильной стадии зависит тактика лечения. Например, пациент — мужчина с раком желудка и стадией cT1N0M0. Это значит, что опухоль прорастает в слизистую и подслизистый слой стенки желудка. В этом случае пациенту показана операция. Если же стадия выше (cT2N1M0, например), то есть опухоль пациента прорастает в мышечный слой, и есть метастазы в лимфоузлах, то может понадобиться химиотерапия перед операцией, которая позволит улучшить результаты лечения, — добавляет Сергей.
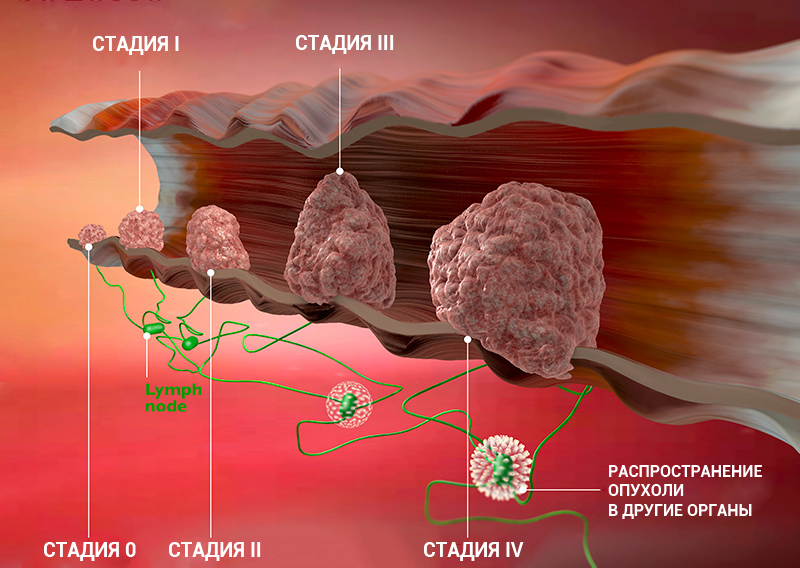
Стадию рака могут обозначать с помощью цифр — 0, I, II, III, IV. Что это значит?
Клинические стадии (0, I, II, III, IV) тесно связаны с системой TNM. Как правило, одна клиническая стадия включает в себя несколько вариантов стадирования по TNM. Эти варианты характеризуются схожими прогнозом и подходом к лечению. Например, стадии T1N3M0, T2N3M0, T3N2M0 рака легкого объединяются в IIIВ стадию, так как при любой из этих ситуаций пациент будет иметь примерно одинаковый прогноз и тактику лечения. В этом конкретном примере необходима химиолучевая терапия, а не операция, — комментирует Сергей Югай.
Меняется ли стадия после лечения, при прогрессировании заболевания?
Нет, стадия выставляется один раз. Но есть нюансы:
Например, мы хотим посмотреть, как опухоль ответила на лечение, чтобы понять, можно ли делать операцию. После лечения опухоль уменьшилась, и мы добавляем к стадии новые данные. При прогрессировании опухолевого процесса первоначальная стадия также остается прежней, но, к сожалению, прогноз будет менее благоприятный. Например, у человека II стадия рака желудка. Он прооперирован, и прогноз у него хороший. Через 2 года врачи обнаруживают у пациента метастазы в легких. Стадия остается II, но рак у пациента уже метастатический, что очень усложняет положение, — говорит Сергей.
Бывает, что люди сравнивают свою ситуацию с историями других пациентов. Если речь идет о разных онкологических заболеваниях, то такие сравнения некорректны — это заболевания с разными прогнозами и схемами лечения:
Например, с нейроэндокринным раком поджелудочной железы люди могут жить десятилетиями, а при метастатической стадии рака поджелудочной железы — полгода или год, — объясняет врач-онколог.
Что может повлиять на прогноз людей с одинаковой стадией и одним видом рака?
Сергей Югай выделяет три фактора:
Главное меню
Главное меню
Клинически незначимый ракпредстательной железы: современная тактика выбора терапии
По оценкам ВОЗ, к 2030 г. глобальная смертность от рака вырастет на 45% по сравнению с уровнем 2007 г. (с 7,9 млн до 11,5млн случаев). Отчасти это произойдет из-за роста численности и старения населения мира. При этом за этот же период времени число новых случаев заболевания раком возрастет с 11,3 млн в 2007 г. до 15,5 млн случаев в 2030 г.
Значительный прирост забо-леваемости РПЖ был отмечен в конце 1980-х гг., что связывают с началом эры диагностики при помощи простат-специфического антигена (ПСА). По последним эпидемиологическим данным американских исследователей, РПЖ развивается у каждого шестого человека, а риск смерти от мета-статического РПЖ составляет 1 к 29[1]. В Европе уровень смертности от РПЖ оценивается в 23,2 на 100 000 мужчин [3].
Согласно этим данным, можно представить, какое значение приобретают вопросы профилактики, возможности вакцинации, адекватной диагностики и лечения РПЖ.
Однако, в настоящее время до конца не понятен естественный ход развития РПЖ. Так, при пато-логоанатомическом исследовании у половины мужчин 40-49 лет был выявлен РПЖ, который не мани-фестировал до летального исхода и не явился его причинной [4]. У 80% из них РПЖ был неболь- □ шого размера (менее 0,5 см3), высокой степени дифференцировки и мог быть расценен как незначимый рак предстательной железы по критериям Epstein [5, 6].
Считается, что в первые 15 лет после установки диагноза течение заболевания относительно вялотекущее, а значительный рост смертности от РПЖ наблюдается после 15 лет [7]. Именно этот аспект рассматривался как основная причина немедленного лече-ния пациентов с предполагаемой длительной продолжительностью жизни.
Таким образом, в настоящее время уровень гипердиагностики РПЖ составляет около 56% [7,8]. С другой стороны, в развитых странах с программами скрининга РПЖ все чаще выявляется на более ранней стадии, что потенциально должно привести к снижению смертности [13].
По современным нормам, активное лечение выявленного РПЖ должно проходить по золотым стандартам, даже с учетом его раннего выявления [14]. Однако всем методам лечения присущи такие осложнения, как нарушения сексуальной функции и мочеиспускания, что, безусловно, приводит к снижению качества жизни [15].
В настоящее время выделяют различные группы риска, в связи с чем в некоторых центрах начались исследования по выделению группы пациентов с низким риском прогрессии РПЖ. Таким пациентам показано динамическое наблюдение с отсроченной терапией, что, по предварительным данным, не ухудшает эффективность лечения и не увеличивает смертность от рака, но улучшает качество жизни. При этом вы-явлено, что лишь определенным пациентам потребовалось проводить лечение по результатам динамического наблюдения. Однако результаты этих исследований предварительны и недолговременны [16].
В данном обзоре будут рассмотрены вопросы возможности и длительности динамического наблюдения при клинически незначимом РПЖ.
ОПРЕДЕЛЕНИЕ НЕЗНАЧИМОГО РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
Понятие «незначимый рак предстательной железы» появилось в современной литературе недавно. Под ним понимается такой РПЖ, который является клинически незначимым, т.е. с низкой вероятностью прогрессирования заболевания до клинических симптомов и/или летального исхода.
Для максимальной эффективности динамического наблюдения ключевым фактором является правильный отбор пациентов, так как пациентов с низким риском прогрессии, вероятно, не потре-буется лечение. Как же отобрать этих пациентов? В настоящее время довольно часто используются критерии Epstein, основанные на результатах биопсии простаты. Для определения незначимого РПЖ необходимо наличие следующих фактов: клиническая стадия Т1с, плотность ПСА меньше 0,15 нг/мл, раковые клетки выявлены менее чем в 3 биоптатах, при этом поражено 50% и менее каждого положительного биоптата, ни в одном биоптате не выявлены опухоли 4 или 5 баллов по Глисону [17]. Однако по данным последних исследований, проведенных с использованием критериев Epstein, выявлено, что они не являются достаточно точным инструментом для определения незначимого РПЖ и отбора пациентов для ди-намического наблюдения. В связи с этим были предложены много-численные варианты критериев для отбора пациентов.
Так, DAmico с соавт. [18] пред-ложили следующие критерии: уровень ПСА не более 10 нг/мл, ни в одном биоптате не выявлены опухоли 4 или 5 баллов по Глисо-ну, клиническая стадия Т2а или меньше. Patel M.I. c соавт. [19] опубликовали работу, в которой использовали и другие критерии незначимого РПЖ: клиническая стадии Т3 или менее, сумма баллов по Глисону не более 7.
Van den Bergh c соавт. в ис-следовании PRIAS (Междуна-родное исследование по РПЖ: динамическое наблюдение) при-меняли следующие критерии от-бора пациентов: клиническая стадия Т1с-Т2Ь, отсутствие опу-холей 4 или 5 баллов по Глисону в биоптате, плотность ПСА менее 0,20 нг/мл, уровень ПСА менее 10 нг/мл, выявляется патологические изменения менее чем в 3биоптатах. Наиболее часто в последних исследованиях при-меняются критерии, предложенные Dall’Era c соавт. [15], которые предполагают наличие следующих фактов: сумма по Глисону 6 или менее, отсутствие паттернов 4или 5 по Глисону в биоптате, уровень ПСА менее 10 нг/мл и стабильная кинетика ПСА, пора-жение захватывает не более 50% каждого положительного био- птата, всего менее трети (33%) положительных биоптатов из всех, взятых при биопсии пред-стательной железы.
Эффективность использования этих критериев по данным разных исследований колеблется в пределах 73%.
ОЦЕНКА РИСКА НЕЗНАЧИМОГО РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
Современные статистические данные по заболеваемости РПЖ свидетельствуют о смещении (ми-грации) распространенности ста-дий этого онкологического забо-левания. За последние десять лет значительно повысилось количе-ство случаев выявляемого лока-лизованного РПЖ, что привело к логичному снижению доли мест-нораспространенного рака ПЖ [20]. В связи с этим, а также с уче-том распространения программ скрининга РПЖ, значительно изменилось время между моментом выявления РПЖ и временем, когда он становится клинически значимым. Draisma с соавт. [21] сообщили, что по данным Евро-пейского рандомизированного исследования по скринингу РПЖ данный период времени изменился с 9,9 лет до 13,3 лет, что также было подтверждено другими ра-ботами [22, 23].
Лечение необходимо проводить только у потенциально излечимых пациентов с клинически значимым РПЖ и значительным риском прогрессирования заболевания. Однако правильное выявление данной группы пациентов остается сложной задачей для урологов. В настоящее время среди клинических врачей становится популярным использование моделей прогнозирования для определения риска прогрессиро-вания РПЖ [24]. В них использу-ются значения исходного уровня ПСА, суммы баллов по Глисону, клинической стадии. Наиболее популярными являются таблица Partin [12], классификация риска DAmico [25], номограмма Kattan [18]. Точность применения данных моделей оценивается в 73-79%. Эти номограммы напоминают критерии Epstein, так как позволят предсказать патогистологически подтвержденный незначимый РПЖ, однако одним из важных преимуществ является то, что с их помощью можно оценить риски, основываясь на исходной клинической информации [26].
Среди последних публикаций заслуживает внимания номо-грамма Chun, в которой исполь-зуются данные исходного уровня ПСА, сумма баллов по Глисону, общая длина пораженной ткани, доля положительных биоптатов. Точность ее использования со-ставляет до 90%, однако в связи с чем достигается такое повышение точности пока неясно, и требуется дальнейшее изучение этого феномена [26]. Следует отметить, что авторы не считают эту номо-грамму достаточным инструмен-том для отбора пациентов в группу динамического наблюдения.
Schroder с соавт. опубликовали обзор по номограммам, использу-емым при РПЖ и сообщили, что большинство моделей требуют дополнительной проверки и не могут использоваться самодоста-точно [27].
Таким образом, в настоящее время не существует стандартных критериев для отбора пациентов в группу динамического наблюдения и становится очевидным необходимость проведения муль-тицентровых проспективных ис-следований по сравнению этих критериев для выбора наиболее оптимальных [15]. Это становится особенно важным в России с учетом социальной и экономиче-ской обстановки.
НЕОБХОДИМЫЕ ИССЛЕДОВАНИЯ в ПЕРИОД ДИНАМИЧЕСКОГО НАБЛЮДЕНИЯ И ВЫЯВЛЕНИЯ ПРОГРЕССИИ рпж
В современной литературе су-ществуют различные протоколы ведения пациентов в группе динамического наблюдения. Тактика ведения варьирует незна-чительно в зависимости от по-литики учреждения и протокола исследования, в целом отличаясь только временными рамками. Так, исследователи из госпиталя Джона Хопкинса проводят повторные биопсии ПЖ каждый год, в то время как исследователи в Торонто предлагают проводить повторные биопсии в 12-18 месяцев [28, 29]. Помимо регулярной биопсии ПЖ предполагается периодическое определение уровня ПСА (раз в 3-6 месяцев), выполнение пальцевого ректального исследования (раз в 3-6 месяцев) и трансректального ультразвукового исследования (ТРУЗИ). Последнее исследование не входит в число обязательных и, как правило, выполняется при необходимости.
Таким образом, именно уровень ПСА и его изменения являются основным параметром для определения возможности про-должения активного наблюдения или начала активного лечения. Следует иметь в виду, что у па-циентов с быстром ростом ПСА до начала лечения гораздо выше риск летального исхода от РПЖ [30, 9]. Также по данным многочисленных исследований именно кинетика ПСА является одним из независимых факторов прогноза смертности после различных видов лечения [31, 32].
Современные визуализацион- ные техники, такие как ультразву-ковое исследование и магнитная резонансная томография, воз-можно, тоже могут быть исполь-зованы для отбора пациентов и перевода их на активное лечение, однако их прогностическая роль сегодня не доказана. Также необ-ходимо изучение новых техник, одной из которых является уль-тразвуковое исследование с кон-трастированием.
РЕЗУЛЬТАТЫ ДИНАМИЧЕСКОГО НАБЛЮДЕНИЯ
Как уже было упомянуто выше, в современной литературе опубликованы результаты 9 ис-следований, однако данные эти предварительны, и при их оценке следует учитывать небольшой интервал наблюдения за пациен-тами.
У большинства пациентов, ко-торым было выполнено радикаль-ное лечение, при патогистоло-гическом исследовании выявлен локализованный РПЖ. Более чем у половины пациентов установлена стадия заболевания Т1.
ПСИХОСОЦИАЛЬНЫЕ АСПЕКТЫ ДИНАМИЧЕСКОГО НАБЛЮДЕНИЯ И ОТСРОЧЕННОГО ЛЕЧЕНИЯ
Первое исследование психосо-циальных последствий динамиче-ского наблюдения было проведено около 15 лет назад группой под руководством Litwin M.S. [42]. Од-нако с тех пор в литературе появи-лось лишь несколько сообщений на эту тему. При проведении мета-анализа психосоциальных аспек-тов всех методов терапии РПЖ не найдено достаточного количества рандомизированных исследований [43]. Некоторые авторы сообщали о различных формах беспокойства, неопределенности по поводу онкологического заболевания, о снижении качества жизни 44. Остается неясным, можно ли сравнивать эти данные с по-казателями качества жизни муж-чин, получивших активную тера-пию [15]. В рандомизированном шведском исследовании не было выявлено разницы этого показа-теля в течение 5 лет между паци-ентами в группах динамического наблюдения и активного лечения. Волнение, беспокойство и депрес-сия отмечались в обеих группах со сравнимой частотой [48]. Все пациенты одинаково волновались по поводу возможности рецидива или прогрессии онкологического заболевания. Однако именно фак-тор беспокойства, а не рост уровня ПСА, может оказаться главным стимулом для перехода пациента от динамического наблюдения к активной терапии [49]. Наиболее важным моментом для разрешения психологических проблем является информирование пациента отом, что РПЖ является медленно прогрессирующим онкологическим заболеванием [50].
Становится очевидной необ-ходимость улучшения консуль-тирования и информирования пациентов в современных услови-ях, так как лишь небольшое коли-чество пациентов действительно выбирает эту форму терапии [51]. Также необходимо проведение дальнейших исследований этих аспектов динамического наблюде-ния, так как скудные данные в до-ступной литературе не позволяют сделать вывод о преимуществах или недостатках динамического наблюдения по сравнению с ак-тивной терапией.
В дальнейшем можно предпо-ложить более частое использова-ние этого терапевтического пула возможностей в связи с разра-боткой новых биомаркеров рака предстательной железы, которые позволят улучшить как отбор па-циентов с РПЖ низкого риска, так и более эффективно определять время перехода к активной тера-пии 55. Также следует прини-мать во внимание активную раз-работку вакцин против РПЖ [56].
В последние годы проведено три рандомизированных исследо-вания по эффективности и безо-пасности динамического наблюде-ния (START, PRIAS, ProtecT) [57].
ЗАКЛЮЧЕНИЕ
Таким образом, основываясь на современных данных, динами-ческое наблюдение при незначи-мом РПЖ является одним из ме-тодов ведения больных указанной категории. Этот метод имеет свои социальные, психологические и экономические преимущества, которые могут оказаться очень важными для пациента, особенно с небольшой прогнозируемой продолжительностью жизни, так как при этом сохраняется прием-лемый образ и качество жизни. Также применение этого метода может оказаться чрезвычайно важным для системы здравоохра-нения в целом, так как снижаются необоснованные затраты на лече-ние основного заболевания и ос-ложнений активного лечения.
Однако следует помнить о се-рьезных недостатках подобной тактики ведения пациентов, ко-торые, на наш взгляд, обусловлены недостатком диагностического пула определения РПЖ низкого риска и его прогрессии. Так, остается вероятность прогрессии или метастазирования РПЖ до начала лечения, что приведет к упущению возможности излечения РПЖ на ранней стадии. Некоторые авторы упоминают о том, что при отсроченном лечении осложнения являются более выраженными, однако эти данные не подтверждены рандо-мизированными исследованиями. Также следует иметь в виду психосоциальные аспекты, так как тревога и депрессия пациента по поводу присутствующего он-кологического заболевания могут серьезно ухудшить качество жизни. Также может повлиять на качество жизни и необходимость достаточно частого медицинского обследования и периодического проведения биопсии простаты. На сегодняшний день нет достоверных данных о естественном течении РПЖ и его последствиях. Также не определены стандарты и критерии отбора пациентов для динамического наблюдения и перевода их на активное лечение.
Актуальна необходимость про-ведения исследования эффектив-ности и безопасности динамиче-ского наблюдения больных раком предстательной железы, определе-ния критериев отбора пациентов для динамического наблюдения или начала активной терапии, что в дальнейшем должно привести к оптимизации лечения данной группы пациентов.
Ключевые слова: рак предстательной железы, динамическое наблюдение, клинически незначимый рак предстательной железы, скрининг, ПСА, биопсия.
Keywords: prostate cancer, dynamic monitoring, Clinically Insignificant Prostate Cancers screening, PSA, biopsiae.