Что такое дисплазия шейки матки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Игнатенко Т. А., гинеколога со стажем в 13 лет.
Определение болезни. Причины заболевания
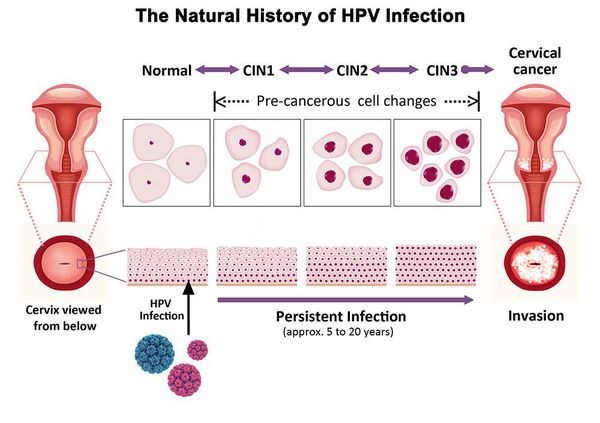
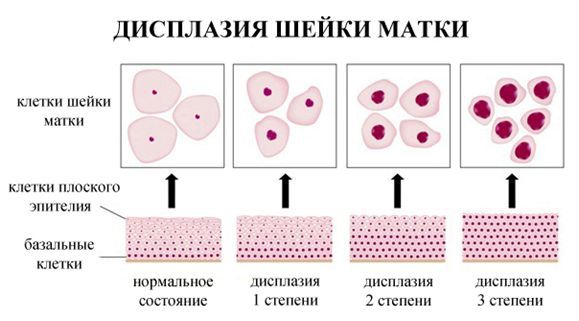
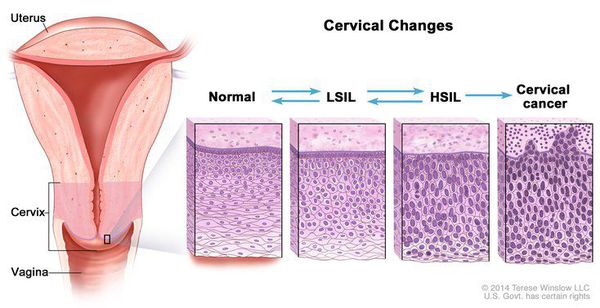
Дисплазия шейки матки, или цервикальная интраэпителиальная неоплазия (ЦИН), или Cervical Intraepithelial neoplasia (CIN) — это патологический процесс, при котором в толще клеток, покрывающих шейку матки, появляются клетки с различной степенью атипии (неправильного строения, размера, формы).
Основной фактор развития дисплазии и рака шейки матки — папилломавирусная инфекция (ПВИ), причем длительное персистирование именно ВПЧ высокого канцерогенного риска. У женщин с риском развития цервикальной неоплазии распространенность онкогенных типов ВПЧ чрезвычайно велика. ВПЧ становится причиной CIN 2-3 и рака шейки матки в 91,8% и 94,5% случаев соответственно. [1]
Риск цервикальной CIN 2 особенно высок у женщин, которые до этого имели опыт пересадки органов, у них выявлена ВИЧ-инфекция или они принимают иммунодепрессанты. [2]
Кроме того, была выявлена связь между пассивным курением среди некурящих и повышенным риском возникновения CIN 1. [3]
Симптомы дисплазии шейки матки
Дисплазия шейки матки, как правило, имеет бессимптомное течение, поэтому пациентки не предъявляют никаких специфических жалоб.
Патогенез дисплазии шейки матки
Критический фактор развития цервикальной интраэпителиальной неоплазии — инфицирование вирусом папилломы человека. Во многих случаях цервикальная интраэпителиальная неоплазия легкой степени отражает временную реакцию организма на папиломавирусную инфекцию и без лечения исчезает в течение полугода-года наблюдения. При цервикальной интраэпителиальной неоплазии умеренной и тяжелой степени высока вероятность встраивания вируса папилломы человека в клеточный геном. Инфицированные клетки начинают продуцировать вирусные белки E6 и Е7, которые продлевают жизнь клетки, сохраняя ее способность к неограниченному делению. Неизбежно формирующиеся на этом фоне мутации клеток ведут к формированию предрака (дисплазии) и рака шейки матки, влагалища и вульвы.
Онкогенные белки ВПЧ (Е6, Е7) взаимодействуют с регуляторными белками клеток шейки матки, приводя к повышению активности онкомаркера p16INK4A, что свидетельствует о неконтролируемом размножении клеток шейки матки. Таким образом, сверхэкспрессия p16INK4A, определяемая в материале шейки матки, который получают при биопсии, является биомаркером интеграции вируса папилломы человека высокого риска в геном и трансформации эпителиальных клеток под действием вируса, что делает эту информацию полезной при оценке прогноза развития предраковых и злокачественных поражений, связанных с инфицированием генитального тракта вирусом папилломы человека. [5]
Классификация и стадии развития дисплазии шейки матки
Для постановки цитологического диагноза (по результатам цитологического исследования соскобов шейки матки и цервикального канала с окрашиванием по Папаниколау (Рар-тест) или жидкостной цитологии) используется классификация Бетесда (The Bethesda System, 2014), основанная на термине SIL (Squamous Intraepithelial Lesion) – плоскоклеточное интраэпителиальное поражение. [10]
Выделяют три вида результатов соскобов с поверхности шейки матки (экзоцервикса):
Классификация Папаниколау
Существуют также гистологические классификации для оценки материала, полученного при биопсии.
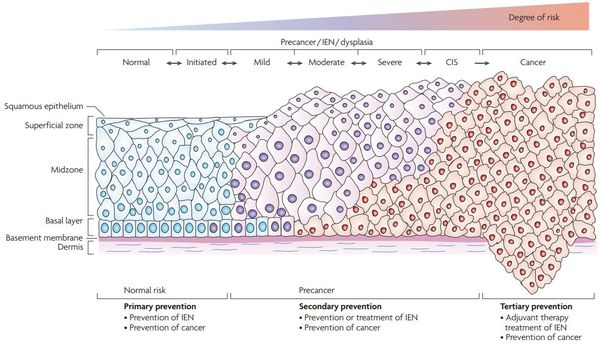
По классификации R. M. Richart (1968) в зависимости от глубины поражения поверхностного клеточного слоя шейки матки выделяют:
В приведенной ниже таблице даны соотношения классификаций предраковых поражений шейки матки. [9]
Осложнения дисплазии шейки матки
Основное и самое опасное осложнение цервикальной интраэпителиальной неоплазии заключается в развитии рака шейки матки, любой случай развития которого — результат упущенных возможностей диагностики и лечения дисплазии шейки матки. [7]
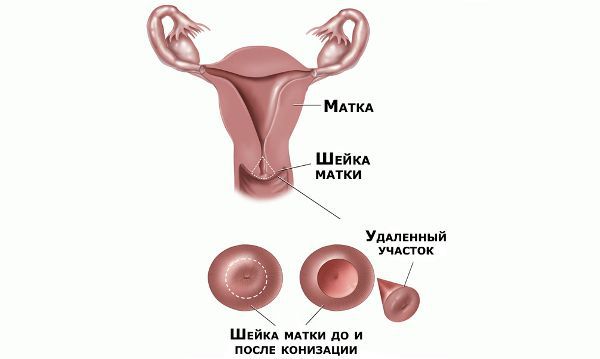
Проводились длительные, систематические исследования риска рака шейки матки у женщин с диагнозом цервикальной интраэпителиальной неоплазии 3 степени (CIN3) по сравнению с женщинами, у которых были нормальные цитологические результаты. Согласно полученным данным, долгосрочный относительный риск развития рака шейки матки зависит от различных гистологических типов CIN3 и выше всего он для аденокарциномы in situ. Даже через 25 и более лет после конизации (хирургического иссечения патологических тканей шейки матки) риск злокачественного перерождения клеток был значительным. [4]
Диагностика дисплазии шейки матки
Для ранней диагностики предраковых поражений шейки матки во многих странах мира существует система цервикального скрининга.
В России данная система включает последовательность действий:
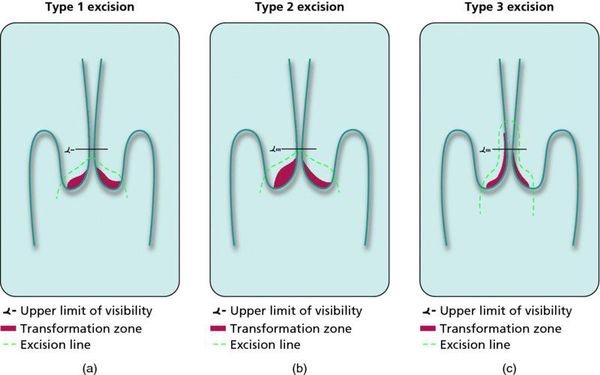
При кольпоскопии должна быть тщательно оценена зона трансформации (переходная зона стыка двух видов покровного эпителия шейки матки).
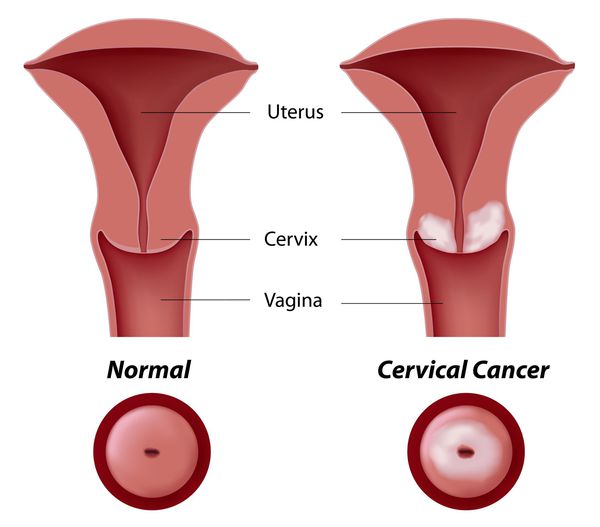
Влагалищная часть шейки матки (экзоцервикс) покрыта многослойным плоским эпителием. В канале шейки матки (цервикальном канале, эндоцервиксе) — цилиндрический эпителий. Место перехода цилиндрического эпителия цервикального канала в многослойный плоский эпителий поверхности шейки матки носит название зоны трансформации. Эта область имеет большое клиническое значение, поскольку именно в ней возникает более 80% случаев дисплазии и рака шейки матки.
Лечение дисплазии шейки матки
Динамическому наблюдению подлежат молодые пациентки (до 35 лет) с LSIL (ВПЧ, ЦИН 1, ЦИН 2, если при биопсии не обнаружен белок р16, являющийся признаком проникновения ВПЧ высокого риска в геном и трансформации опухолевых клеток под действием вируса). Наблюдать возможно пациенток только с 1 и 2 кольпоскопическим типом зоны трансформации.
Контрольные осмотры, цитологическое и ВПЧ-тестирование показаны через 6 и 12 месяцев после первичного обнаружения патологии. При выявлении HSIL (ЦИН 2 c обнаружением белка р16 при биопсии, ЦИН 3) неизбежно хирургическое лечение в виде абляции («прижигания») или эксцизии (удаления) поврежденной ткани. Для абляции используют электро-/радио-, крио- и лазерные воздействия. Эксцизия возможна электро-/радиоволновая или ножевая.
Немаловажно, что при выявлении по кольпоскопии 3 типа зоны трансформации на фоне положительного РАР-теста гинеколог обязан провести выскабливание слизистой канала шейки матки и/или широкую эксцизионную биопсию (конизацию шейки матки) для исключения опухолевого процесса, потенциально располагающегося вне зоны кольпоскопического обзора. Немаловажно наблюдение после операции через 6 и 12 месяцев с выполнением цитологического соскоба и ВПЧ-теста.
Следует отметить, что процедура хирургического иссечения патологических тканей на шейке матки увеличивает риск преждевременных родов. А сама по себе цервикальная интраэпителиальная неоплазия первой степени на течении беременности и родов никак не отражается и зачастую опасности не представляет. [12]
Средний возраст женщин, когда может потребоваться хирургическая коррекция цервикальной внутриэпителиальной неоплазии — около 30 лет. Хирургическое лечение нередко ассоциировано с неблагоприятным течением последующей беременности. Частота и тяжесть неблагоприятных осложнений возрастают с увеличением глубины иссекаемых тканей. [13]
Прогноз. Профилактика
При своевременном выявлении и лечении дисплазии шейки матки прогноз благоприятный. Основным фактором развития и прогрессирования дисплазии шейки матки является длительное инфицирование канцерогенными типами ВПЧ. Для предупреждения заражения ВПЧ существуют профилактические вакцины «Церварикс» (защита от 16, 18 типов ВПЧ), «Гардасил» (профилактика инфицирования 6, 11, 16, 18 типами вируса), в декабре 2014 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов одобрило использование вакцины «Гардасил9», защищающей от инфицирования 9 типами ВПЧ (6, 11, 16, 18, 31, 33, 45, 52, 58). Однако на российском рынке данный продукт ещё не доступен. «Церварикс» зарегистрирована для вакцинации женщин от 10 до 25 лет; «Гардасил» показана к применению детям и подросткам в возрасте от 9 до 15 лет и женщинам от 16 до 45 лет.
Дополнительными факторами риска прогрессирования ПВИ с формированием предраковой патологии являются:
Устранение и профилактика данных факторов способны снизить вероятность развития предраковой патологии шейки матки.
Рак шейки матки поражает преимущественно женщин репродуктивного возраста. Скрининг является важной стратегией вторичной профилактики. Длительный процесс канцерогенной трансформации от появления в организме вируса папилломы человека (ВПЧ) до инвазивного рака дает широкие возможности для выявления заболевания на стадии, когда лечение высокоэффективно. Подходящими скрининговыми тестами в мире признаны цитологическое исследование, визуальный осмотр после применения уксусной кислоты и тесты на выявление ВПЧ. Всемирная организация здравоохранения рекомендует проводить скрининг женщин по крайней мере один раз в жизни в возрасте от 30 до 49 лет. [14]
Согласно приказу Министерства здравоохранения РФ от 03.02.2015. N36ан «Об утверждении порядка проведения диспансеризации определенных групп взрослого населения», осмотр со взятием мазка (соскоба) с поверхности шейки матки и цервикального канала на цитологическое исследование производится 1 раза в 3 года для женщин в возрасте от 21 года до 69 лет включительно.
Что такое атипичные клетки шейки матки
» data-image-caption=»» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2019/02/atipichnye-kletki.png?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2019/02/atipichnye-kletki.png?fit=829%2C550&ssl=1″/>
Нарушение строения эпителиальных клеток — это термин для обозначения клеток необычного размера или формы, обнаруженных на шейке матки. Этот результат теста, чаще всего полученный после мазка Папаниколау, не обязательно указывает на злокачественный рост опухоли, но уже говорит о том, что могут быть предраковые клетки или начальные раковые клетки.
Особенности анализа на атипичные клетки
Типы аномалий
Атипичные эпителиальные клетки делятся на две широкие категории: плоскоклеточные и железистые.
Наиболее распространенными типами являются атипичные плоскоклеточные клетки (ASC), плоскоклеточные интраэпителиальные образования (SIL) или плоскоклеточный рак. Проблемы, возникающие обнаружением железистых клеток обычно классифицируются как атипичные железистые клетки (AGC) или аденокарцинома.
Из обнаруженных плоскоклеточных и железисто-клеточных аномалий только имеющие признаки плоскоклеточного рака и аденокарциномы почти наверняка указывают на развитие рака.
ASC-клетки
ASC-клетки явно не нормальны, но не совсем понятно, почему. Клетки в этой категории могут быть либо атипичными плоскоклеточными неопределенного значения (ASCUS), либо атипичными плоскоклеточными клетками с возможными изменениями высокого уровня риска рака (ASC-H).
Кольпоскопия — диагностический тест, при котором гинеколог визуально исследует внутреннюю часть влагалища на наличие патологий или повреждений.
SIL-клетки
SIL — это клетки, образующие наросты на поверхности шейки матки, которые могут привести к раку. Они относятся к категории среднего или высокого риска в зависимости от вероятности возникновения рака.
После обнаружения SIL-клеток специалист обычно рекомендует кольпоскопию или биопсию, чтобы подтвердить уровень риска, связанного с обнаружением данной клетки.
Плоскоклеточный рак
Плоскоклеточный рак — наиболее распространенный тип рака шейки матки и может быть смертельным, если его не лечить.
Если на него указывает мазок Папаниколау, гинекологи срочно проводят кольпоскопию или биопсию, чтобы определить, на какой стадии находится рак, начиная с «in situ», что означает, что раковые клетки существуют, но еще не распространились в ткани, до стадии 4, на которой рак распространился за пределы шейки матки.
Как только это будет определено, женщина может начать лечение.
AGC-клетки
Их обнаружение может указывать на то, что у железистых клеток в шейке матки или слизистой оболочке матки, также называемой эндометрием, могут возникнуть проблемы. Около половины случаев обнаружения AGC-клеток не вызывают беспокойства, как ASCUS. Однако они могут быть предраковыми, поэтому также нужно пройти биопсию для уверенности.
Аденокарцинома
Это довольно редкий тип рака, который похож на плоскоклеточный рак, но поражает железистые клетки.
Как и в случае обнаружения плоскоклеточного рака, необходимо срочное дополнительное тестирование для определения стадии рака, а затем начинают лечение.
Причины
Одна из причин появления аномальных эпителиальных клеток — дисплазия шейки матки. В этом случае шеечные клетки растут ненормально, и они либо имеют странную форму, либо разрастаются в огромных количествах.
Рост клеток не является однозначно злокачественным симптомом, но со временем аномальная клетка может переродиться в рак в течение примерно 10 лет или немного дольше. Дисплазия шейки матки чаще встречается у женщин от 25 до 35 лет и обычно не имеет симптомов.
Иногда сообщается о необычных клетках, возникающих из-за инфекций, таких как герпес и вирус папилломы человека. ВПЧ — один из ведущих факторов риска развития рака шейки матки.
Наличие паразитов или грибковых инфекций также может дать положительный результат. Клеточная ткань может оказаться ненормальной из-за травмы. Если есть подозрение на инфекцию или травму, то, как правило, не возникает проблем с диагностикой рака в результате обнаружения такой аномалии эпителиальных клеток.
Лечение
Лечение аномалий эпителиальных клеток зависит от конкретной проблемы.
Атипичные клетки в отчете о биопсии
Иногда Вы можете увидеть отчет о биопсии, в котором имеется фраза, что “присутствуют атипичные клетки”. Это может заставить Вас волноваться, что это означает рак, но атипичные клетки не обязательно означают злокачественные клетки.
Наличие атипичных клеток в отчете о биопсии иногда называют “дисплазия“. Многие факторы могут приводить к появлению из нормальных клеток атипичных, включая воспаление и инфекции. Даже естественное старение может привести к появления ненормальных клеток.
Атипичные клетки могут подвергнуться обратному развитию и вернуться к нормальным клеткам в случае, если первопричина устранена или разрешена. Это может произойти и спонтанно. Или это может быть результатом специфического лечения.
Наличие атипичных клеток в отчете о биопсии не обязательно означает, что это рак. Тем не менее, остается важным убедиться, что в этом очаге не присутствуют структуры рака или, что рак не начинает развиваться.
Если врач выявляет атипичные клетки в отчете о биопсии, то важно тщательное наблюдение. В некоторых случаях, врач может просто следить за атипичными клетками, чтобы убедиться, что они не стали еще более ненормальными. Другие тесты и проверки могут быть полезны в данном случае, в зависимости от конкретных обстоятельств.
В других случаях врач может рекомендовать какое-то конкретное лечение, чтобы попытаться переломить процесс, который вызывает атипичные клетки. Возможно, потребуется получить другой образец ткани — дополнительную биопсию — чтобы убедиться, что в данном случае нет рака или другого серьезного заболевания.
Атипическая гиперплазия эндометрия
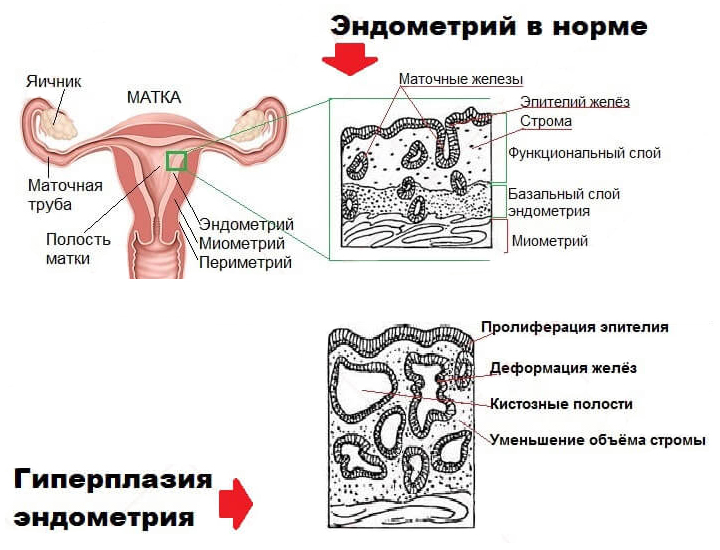
При атипической гиперплазии внутренний слой матки — эндометрий —разрастается, что ведет к увеличению его толщины и объема. При этом морфология клеток изменяется, появляются атипичные — клетки, изменившие свои свойства. Вид и особенности таких клеток становятся нехарактерными тем, из которых они появились. Заболевание может развиваться у женщин любой возрастной категории, но вероятность ее появления выше в постменопаузе.
Это гинекологическое заболевание относится к предраковым состояниям, если адекватное лечение отсутствует, то болезнь в 40% переходит в злокачественную форму. Появление эндометрия с атипической железистой гиперплазией может означать начало преобразования в аденокарциному — злокачественное заболевание. Появление атипичных клеток в функциональном слое слизистой характерно для начального этапа атипической гиперплазии эндометрия матки, их обнаружение в базальном слое и строме — признак начинающегося рака эндометрия.
Как появляется заболевание
Развитие заболевания тесно связано с уровнем гормонов в организме. У здоровой женщины функциональный слой эндометрия увеличивается в 1-й половине цикла. Когда зачатия не наступает, происходит его отторжение, затем он естественным путем удаляется из матки. При гормональных отклонениях этот процесс нарушен, происходит активное деление клеток, однако своевременного отторжения и выведения частиц эндометрия нет. Наблюдается его утолщение и разрастание. Патологические очаги могут появляться на отдельных участках или же избыточное разрастание будет равномерным. Когда все же происходит отторжение эндометрия, появляется обильное кровотечение.
Гиперплазия — прогрессирующее заболевание, со временем свойства эндометрия изменяются, что способствует появлению нехарактерных клеток, развивается атипическая гиперплазия эндометрия. Однако существуют факторы, увеличивающие вероятность появления заболевания:
К группе риска относятся женщины с лишним весом. Сахарный диабет, гипертония также увеличивают риск развития заболевания.
Симптомы
Основным признаком атипической гиперплазии эндометрия является кровотечение. Более продолжительные, чем менструация, нередко продолжающиеся около 3-х недель, кровотечения могут быть цикличными (чаще у женщин репродуктивного возраста) или ацикличными. Не отделившиеся частицы эндометрия могут стать причиной межменструальных выделений. Нередко кровотечения возникают после задержки; после незначительной — выделения носят умеренный характер, после длительной — они становятся обильными. У четверти пациенток возникают ановуляторные кровотечения — нерегулярные, большей продолжительности и кровопотери.
Отсутствие лечения приводит к осложнениям. В результате длительных и обильных кровотечений развивается анемия. К наиболее тяжелым последствиям атипической гиперплазии эндометрия относится переход болезни в рак.
Однако заболевание не всегда сопровождается характерными признаками, при бессимптомном течении женщина может долго и безуспешно пытаться забеременеть. Гиперплазия эндометрия в таком случае впервые диагностируется, когда женщина обращается к врачу по поводу бесплодия.
Диагностика
Чтобы своевременно обнаружить болезнь даже при бессимптомном течении, важно регулярно проходить гинекологическое обследование даже при отсутствии каких-либо жалоб. В настоящее время существуют различные методики, позволяющие безошибочно диагностировать заболевание даже на ранней стадии. Сюда входят:
Для уточнения диагноза также может быть рекомендовано проведение МРТ, назначено обследование у эндокринолога, что важно для пациенток, входящих в группу риска. Комплексное обследование позволяет обнаружить не только атипическую гиперплазию эндометрия, но и диагностировать другие заболевания: как половой сферы (миому, кисты яичников и т.п.), так и другие отклонения (сахарный диабет, гипертонию и др.).
Лечение
Выбор тактики лечения при атипической гиперплазии эндометрия зависит от возраста пациентки, тяжести состояния, наличия сопутствующих заболеваний, осложнений, а также желания женщины сохранить функцию репродукции. Лечение может быть консервативным или хирургическим.
При консервативной терапии назначаются гормональные препараты, направленные на подавление разрастания эндометрия, нормализацию цикла, восстановление гормонального баланса. При наличии кровотечений показано выскабливание эндометрия во время гистероскопии.
Хирургическое лечение — какие существуют варианты
Операция при атипической гиперплазии эндометрия назначается, если:
Не так давно единственным методом лечения было удаление матки. Я выполняю радикальную операцию в том случае, если патоморфологически подтвержден рак эндометрия, в остальных ситуациях возможно проведение органосохраняющего вмешательства.
Одним из эффективных методов является гистерорезектоскопия, рекомендованная женщинам репродуктивного возраста или в пременопаузальном периоде. Процедура относится к малотравматичным и выполняется с использованием эндоскопического оборудования, оснащенного видеокамерой. Возможность визуализации позволяет проводить манипуляции максимально бережно и с высокой точностью, без риска развития осложнений. Длительность процедуры — около получаса, период восстановления занимает не более 14 дней.
Однако для проведения гистерорезектоскопии, как и при любом хирургическом вмешательстве, имеются противопоказания:
При лечении гиперплазии неплохо зарекомендовала себя малоинвазивная процедура — абляция — трансцервикальная деструкция эндометрия. Во время ее проведения можно удалить базальный и функциональный слой эндометрия, а также часть миометрия на глубину 3-5 мм. Абляция может быть проведена с помощью лазерной или электрохирургической методики, но в любом случае процедура выполняется с использованием гистероскопического оборудования, поэтому является безопасной и эффективной.
При наступлении менопаузы женщине рекомендована гистерэктомия — удаление матки. Если патологические изменения в яичниках отсутствуют, то операция проводится без удаления придатков. В случае, если имеется аденомиоз или подтвержден злокачественный процесс в матке, то гистерэктомия проводится с удалением придатков. Органуносящая операция также показана пациенткам в постменопаузе при рецидиве после гормонального лечения.
Мною проведено более 4000 гинекологических операций, в том числе по поводу гиперплазии эндометрия. К каждой пациентке я подбираю тактику лечения, учитывая целый ряд деталей: возраст и наличие других болезней, желание сохранить матку как орган и проведенное ранее лечение. Если существует возможность, я всегда стремлюсь провести малотравматичную органосохраняющую операцию, после которой женщина сможет быстро вернуться к привычному образу жизни. После такой операции восстановление занимает не более двух недель, а госпитализация не превышает трех дней.
Сегодня возможность сохранить матку имеется даже у пациенток с сопутствующими гинекологическими заболеваниями (например, с миомой, кистами, полипами). Однако проведение органосохраняющей операции окажется невозможным, если процесс перейдет в злокачественный. Чтобы избежать подобного, следует регулярно проходить осмотры. В нашей клинике даже полное обследование займет минимум времени.
Безоперационное лечение атипической гиперплазии эндометрия за 1 сеанс фотодинамической терапии
Аденоматоз эндометрия
Д.м.н., профессор Сеченовского университета, онколог, хирург, онкогинеколог, гинеколог-иммунолог, эксперт по лечению атипической гиперплазии и рака матки, а также предраковых и опухолевых заболеваний шейки матки.
Атипическая гиперплазия эпителия – это диагноз, который в онкогинекологии однозначно классифицируется как предраковое заболевание с высокой степенью канцерогенности – способностью перерождаться в рак.
Женщин репродуктивного возраста врачи стараются лечить. Проводят тяжелую гормональную терапию или хирургическую процедуру – лазерную абляцию эндометрия. Оба эти метода имеют достаточно серьезные последствия.
На фоне приема гормонов женщина погружается в состояние, свойственное менопаузе, и испытывают такие осложнения, как набор лишнего веса, усталость, снижение либидо и повышенный риск тромбоэмболии (1, 2).
Частым же осложнением абляции является развитие так называемого синдрома Джозефа Ашермана, когда в процессе заживления полость матки срастается.
К сожалению, атипичная гиперплазия матки – это очень серьезное заболевание, которое тяжело поддается лечению. Абляция и гормонотерапия гиперплазии эндометрия с очагами атипии эффективны лишь в определенном проценте случаев.
При неэффективности гормонотерапии и абляции, медицина сегодня может предложить фактически единственный способ избежать озлокачествления процесса и сохранить жизнь. Этот способ – удаление матки. Зачастую показания требуют удаления матки вместе с придатками – то есть, вместе с маточными трубами и яичниками. Поэтому отсутствие эффекта на фоне гормонального лечения или абляции всегда заканчивается одинаково – радикальной рекомендацией избавиться от матки.
Новый высокотехнологичный метод фотодинамической терапии (ФДТ), который я использую в своей практике, за 1-2 сеанса обеспечивает выздоровление более чем в 80% случаев.
Безоперационный метод ФДТ позволяет сохранить матку, а вместе с ней сохранить женское здоровье, возможность зачать и самостоятельно родить.
Перед тем, как продолжить наш разговор об атипической гиперплазии, давайте определимся, что скрывается за этим термином и какова природа заболевания. Это позволит понять, почему классические методы мало эффективны против атипии и оценить все преимущества ФДТ.
Что такое гиперплазия матки
Изнутри матку выстилает слизистый слой – эндометрий. Эндометрий не однороден. Он состоит из:
1. маточных желез и
2. стромы – служебной ткани, которая поддерживает железы и обеспечивает их питание.
В норме строма и железы занимают примерно равный объем, 1:1.
Каждый месяц к моменту овуляции матка готовится принять в себя яйцеклетку, и толщина эндометрия увеличивается. После выхода яйцеклетки из яичника железы эндометрия активируются и начинают вырабатывать слизь (секрет), создавая благоприятную среду для оплодотворения. Когда оплодотворения не происходит, эндометрий отслаивается и выходит вместе с кровью.
Если по каким-то причинам эндометрий не отторгается во время менструации (например, в этом цикле у женщины не было овуляции), он продолжает разрастаться. Это состояние и называется гиперплазией эндометрия.
Классификация гиперплазии эндометрия
Гиперплазия эндометрия подразделяется на:
1. простую гиперплазию эндометрия,
2. атипическую гиперплазию эндометрия.
Если толщина эндометрия увеличивается локально, на отдельных участках, такое состояние называется очаговой гиперплазией. Если повсеместно по всей полости матки – диффузной.
Но так как далеко не все гинекологи и морфологи взяли на вооружение новую классификацию, в статье я буду использовать все существующие названия этого диагноза.
Что такое простая гиперплазия эндометрия
Это начальная стадия гиперплазии, которая характеризуется утолщением эндометрия и незначительным неравномерным расположением маточных желез, некоторые из которых превращаются в кисты – закупоренные железы, расширенные изнутри собственным секретом. Соотношение маточных желез и стромы примерно соответствует здоровому – 1:1.
К простым формам гиперплазии сегодня относят следующие диагнозы:
Сочетание нескольких из указанных видов ранее относили и трактуются коллегами как сложная гиперплазия.
Гиперплазия проявляется кровотечениями или мажущими кровянистыми выделениями в период между менструациями. При УЗИ выявляется неоднородная эхоструктура эндометрия.
В силу стрессов – смены часового пояса, недосыпания, отсутствия овуляции (ановуляторный цикл) и нервного перенапряжения, – простая железистая гиперплазия может проявиться в самом обычном цикле даже у самой здоровой женщины. Поэтому можно говорить, что признаки простой гиперплазии наблюдаются в течение жизни у 90% женщин.
Это состояние достаточно легко поддаётся коррекции гестагенными препаратами, а также Дюфастоном, Норколутом, Утрожестаном и др. Молодым пациенткам для лечения часто назначают комбинированные оральные контрацептивы – Джесс, Жанин и другие.
Простая гиперплазия эндометрия не является предраковым состоянием и не требует специального противоопухолевого лечения.
Что такое атипичная гиперплазия эндометрия матки, или аденоматозная гиперплазия эндометрия (код N85.1 в МКБ-10 – международная классификация болезней 10 пересмотра)
Аденоматоз эндометрия, или атипическая гиперплазия матки – стадия развития гиперплазии, которая характеризуется появлением атипичных клеток. Слово «атипичные» означает почти то же самое, что «нетипичные»: эти клетки не похожи на нормальные.
Все наши клетки имеют четкую форму, располагаются слоями и выполняют определенную функцию. Но по каким-то причинам (ученые не пришли к единому мнению о причинах развития атипии в эндометрии матки), они изменяют свою форму, размер и перестают выполнять заложенную природой функцию.
Появление атипических клеток – очень серьезный звонок! Эта стадия развития гиперплазии в медицине относится к предраковым заболеваниям матки.
Атипичные клетки продолжают делиться и накапливать повреждения. Если процесс не остановить, атипичная форма гиперплазии приводит к появлению злокачественных клеток и переходит в рак матки.
Атипичная гиперплазия эндометрия в медицинской практике носит сразу несколько названий – сложная или комплексная гиперплазия с атипией клеток, аденоматозная гиперплазия эндометрия, атипичная железистая гиперплазии эндометрия, очаговый аденоматоз эндометрия, сложная гиперплазия с атипией, железистая гиперплазии эндометрия с атипией, кистозно-аденоматозная гиперплазия, очаговая гиперплазия с атипией клеток и атипическая железистая гиперплазия эндометрия. Некоторые из них устарели, но используются до сих пор.
И какой бы диагноз из этого списка вам не поставили, при появлении атипии все эти состояния трактуются как предраковые и лечатся одинаково.
Название «аденоматозная» эта форма гиперплазии получила не случайно. Аденома – это доброкачественная опухоль, образованная из клеток железистого эпителия, в нашем случае – из эпителия маточных желез.
Как проявляется сложная атипическая гиперплазия эндометрия
Сложная гиперплазия эндометрия с атипией клеток сопровождается разрастанием желез слизистой оболочки матки. Большое количество маточных желез на ограниченном участке располагаются очень плотно друг к другу и деформируются. Соотношение железистой ткани и стромы смещается к пропорции 2:1. Общая структура эндометрия значительно нарушается.
Многие железы закупориваются, переполняются собственным секретом, образуют кисты и аденомы.
Атипическая гиперплазия эндометрия может переходить в рак – в этом ее основная опасность
К сожалению, не только может, но и переходит – атипическая гиперплазия эндометрия имеет высокий риск озлокачествления.
Данные статистики сильно отличаются, но в общем и целом от 23 до 81%*** случаев атипической гиперплазии приводят к раку матки.
С одной стороны, такой разброс в цифрах объясняется разным периодом наблюдения за больными с атипической гиперплазией (при длительном наблюдении цифра приближается к 100%).
С другой стороны, даже квалифицированный специалист-патоморфолог, который рассматривает клетки под микроскопом и определяет степень их злокачественности, испытывает сложности при постановке диагноза.
Мы не будем вдаваться в тонкости работы патоморфолога, но, поверьте, крайне сложно однозначно дифференцировать предраковое и начальное раковое состояние эндометрия. И одни видят атипию там, где другие уже видят рак.
Атипичная гиперплазия эндометрия матки – это рак?
Атипичная гиперплазия не являются раком в истинном смысле слова:
То есть, атипичные клетки уже приобрели свойства раковых – они разного размера и с увеличенными ядрами, но еще не преодолели сопротивление организма.
Еще раз повторюсь, что вопрос атипических процессов в матке совсем непростой. Постановка диагноза по материалу биопсии или после выскабливания крайне затруднительна. Поэтому при подозрении на диагноз «атипическая гиперплазия эндометрия матки» пересмотр стекол почти всегда сопровождается новым заключением патоморфолога.
Точная диагностика характера очагов аденоматоза возможна только после удаления матки, когда специалист получает возможность прицельно исследовать структуру эндометрия на всю его глубину. То есть, провести не цитологическое исследование (исследование клеток), а гистологическое исследование (исследование тканей), которое позволяет получить более точный результат.
Между тем по литературным данным диагностика тканей матки после гистерэктомии выявляет рак эндометрия у каждой третьей и даже у каждой второй (54%) больной***!
Как раньше проводили лечение атипичной гиперплазия эндометрия
Раньше после постановки диагноза «очаговая атипическая гиперплазия эндометрия» гинекологи не могли порадовать своих пациенток наличием эффективного нехирургического метода лечения и благоприятным прогнозом на выздоровление.
Как я уже говорил, стандартный международный подход лечения аденоматоза матки у молодых женщин предусматривает приём тяжелых гормональных препаратов, таких как Депо Провера и его аналоги. Этот метод еще называется «гормональным кюретажем». Такое гормональное лечение направлено на усиление секреции – отторжение гиперплазированного эндометрия.
При отсутствии эффекта лечение аденоматозной гиперплазии эндометрия проводят хирургически – методом абляции (выпаривания) эндометрия при помощи лазера с его последующим кюретированием (выскабливанием). Кюретаж эндометрия выполняют не более трех раз, поскольку этот метод лечения имеет высокие риски развития синехий – осложнения, в результате которого внутренние стенки матки часто в процессе заживления срастаются.
Женщинам репродуктивного возраста, планирующим иметь детей, после проведения выскабливания назначается гормональное лечение прогестероном.
При этом важно понимать, что при железистой гиперплазии с атипией гормональное лечение позволяет уменьшить толщину эндометрия, но слабо при этом влияет на атипию, и атипические клетки продолжают свое деление. То есть, прогестероновая терапия не является профилактикой рака.
В случае неэффективности всех перечисленных методов, женщине выполняют удаление матки.
Да, в последние годы европейская медицина при малейшем появлении атипии часто направляет пациентку на удаление матки, исключая таким образом риск перерождения атипии в рак.
«Гистерэктомия», или удаление матки, – такова современная международная тактика ведения пациенток по поводу гиперплазии с атипией клеток, принятая в Европе и Америке. И хотя в отношении не рожавших женщин западная медицина тоже назначает горомонотерапию, финальный исход в виде гистерэктомии считается неизбежным как для рожавших, так и для не рожавших женщин любого возраста.
Такая тактика спасает жизнь, но приводит к развитию крайне серьезных осложнений.
Последствия удаления матки
По этому поводу я написал разъясняющую статью, к каким последствиям приводит удаление матки для женщины.
В первую очередь это касается другого качества жизни после операции. Как говорится, природой лишних органов не задумано. И понятно, что при утрате органа, даже по медицинским показаниям, утрачивается и функция этого органа. Но это только часть проблемы. Крайне отрицательное воздействию после операции испытывают и соседние органы.
После удаления матки серьезно страдает мочевыделительная система, нарушается работа толстой кишки, развивается высокое артериальное давление, серьезно повышаются риски инфарктов и инсультов.
Женщинам же репродуктивного возраста, ведущих активную половую жизнь, приходится адаптироваться не только к изменению ощущений во время секса, но и к изменившемуся размеру влагалища.
Стремясь найти эффективное лечение без удаления органа, я разработал протокол лечения атипической гиперплазии эндометрия методом фотодинамической терапии.
Как проходит процедура фотодинамической терапии
Именно такое избирательное воздействие обеспечивает полноценное удаление атипичных клеток и гиперплазированного эндометрия и выздоровление после процедуры.
Как происходит заживление
Спустя 6–7 недель после сеанса фотодинамической терапии слизистая заживает без рубцов. Формируется здоровый эпителий матки.
В течение полугода все пациентки проходят 3-кратный контроль, который включает:
В дальнейшем нужно будет посещать гинеколога один раз в пол года для профилактических осмотров.
Пациентка, 34 года, г. Москва, диагноз «атипическая гиперплазия эндометрия»
Обратилась с поставленным диагнозом зимой этого года. С Января 2015 года перестали приходить самостоятельно менструации. По назначению гинекологов принимала гестагенные препараты (Дюфастон) в непрерывном режиме.
| Здесь следует отметить характерные для атипической (сложной) гиперплазии эндометрия жалобы – отсутствие самостоятельных менструаций, признак патологии эндометрия. |
В мае 2016 года при проведении раздельно выскабливания матки и гистероскопии диагноз снова подтвердился. Гистологическое заключение после пересмотра в лаборатории института онкологии им. Блохина № 24730: в готовых препаратах и препаратах, приготовленных с блока в соскобе кусочки эндометриального полипа с картиной простой железистой гиперплазии без атипии и сложной атипической гиперплазии. Показано проведение специального противоопухолевого лечения в объёме гистерэктомии, гормонотерапии. Была консультирована в том же онкоцентре им. Блохина, от предложенной гормонотерапии решила воздержаться в пользу проведения сеанса фотодинамической терапии.
В октябре 2016 года проведена фотодинамическая терапия матки. Послеоперационный период без осложнений. Пайпель биопсия эндометрия от 03.02.2017 года, гистологическое заключение № 171005746: «вероятнее всего определяется фрагмент железистого полипа эндометрия гиперпластического типа с очаговым фиброзом стромы, фокусами лимфоцитарной инфильтрации».
С целью профилактики рецидива атипической гиперплазии в апреле 2017 года пациентке проведён второй сеанс ФДТ матки, перед которым проведено раздельное выскабливание матки, гистологическое заключение № 171020496: «очаговая простая железистая гиперплазия эндометрия без атипии с кисточкой трансформацией желёз».
Пациентка вылечена. Клинический признак выздоровления: с декабря 2016 года у пациентки восстановился цикл, стали приходить менструации.
На сегодняшний день пациентка здорова и планирует беременность.
Почему лечение аденоматоза эндометрия нужно проводить методом ФДТ
Я не могу гарантировать, что ФДТ способна вылечить атипическую гиперплазию эндометрия на 100%, так как причина этого заболевания – в основе своей – комплексная (гормональная).
1. Фотодинамическая терапия прицельно устраняет атипические клетки и, как следствие, избавляет от риска развития рака матки.
После правильно выполненной фотодинамической терапии с возникновением адекватных фотохимических реакций, можно говорить о том, что в зоне лечения атипичных клеток не остается. Это означает, что рецидиву взяться попросту неоткуда.
2. Фотодинамическая терапия сохраняет матку – орган, который важен не только для рождения детей, но и для нормального функционирования всего женского организма – от кишечника до сосудов.
3. Процедура не затрагивает глубокие слои матки, позволяет сохранить целостность матки и все функции здорового органа. Такая матка впоследствии позволяет зачать, выносить и родить.
При этом акушеры и гинекологи в своей практике наблюдают интересный факт – беременность и период лактации благотворно влияют на гормональный фон женщины и служат отличной профилактикой: после родов гиперплазия эндометрия развивается крайне редко.
4. Исследования** эффективности ФДТ показывают удивительную способность процедуры тормозить избыточное разрастание эпителия матки.
На протяжении 6 месяцев наблюдений после одного сеанса ФДТ гиперплазии не была обнаружена у 82 % пациентов, и еще у 7% регрессировала после повторного сеанса ФДТ.*
Это обнадеживает и дает запас времени всем планирующим беременность.
Из пяти моих пациенток с пролеченной атипической гиперплазией четыре уже прошли контроль и здоровы. Одна еще находится под наблюдением в ожидании контроля.
5. ФДТ исключает сращение внутренних стенок матки – распространенное осложнение после хирургической абляции.
Хуже не будет, а высокая – более 80 процентов – вероятность излечения – хорошее основание, чтобы устранить очаг атипической гиперплазии методом ФДТ. Принять решение об удалении матки всегда успеете.
Таким образом, из всех орагносохраняющих методов лечения гиперплазии эндометрия с атипией фотодинамическая терапия является самым результативным.
Результаты лечения пациентки 39 лет, Москва
Зарубежный опыт лечения гиперплазии матки методом ФДТ подтверждает его высокую эффективность
Основанием для усовершенствования моей методики проведения ФДТ стала работа врачей из Южной Кореи (3), которые пролечили несколько пациенток с высокодифференцированной аденокарциномой эндометрия матки и получили показательный результат.
Выше мы уже говорили о сложностях разграничения тяжёлой атипической гиперплазии эндометрия (дисплазии) и высокодифференцированной аденокарциномы эндометрия. Поэтому данные корейских коллег можно рассматривать в качестве релевантных и для случаев атипической гиперплазии.
Лечение проходила группа пациенток репродуктивного возраста 24-35 лет. У 10 из 16 пациенток удалось добиться выздоровления после одного сеанса ФДТ. Еще у двух пациенток удалось добиться выздоровления после второго и третьего сеанса ФДТ соответственно.
Таким образом, доля положительного ответа на лечение методом ФДТ составила 75% (12/16).
Из 7 пациенток, которые попытались забеременеть после лечения, у четырех пациенток (57%) прошло семь успешных беременностей, которые привели к рождению 6 живых младенцев.
Стоит также отметить, что после успешного лечения методом ФДТ на протяжении 78 месяцев наблюдения не было отмечено рецидива болезни ни у одной из пациенток. Также не было отмечено серьезных побочных эффектов, связанных с фотодинамической терапией.
Почему направление ФДТ в медицине не развивается?
Идея и опыт применения фотодинамической терапии в лечении атипической гиперплазии эндометрия и рака тела матки не нова. Работы по фотодинамической терапии проводилась еще на кафедре акушерства и гинекологии II Медицинского университета им. Н.И. Пирогова.
1. Метод технологически сложный и объединяет в себе три направления науки: медицину, биологию и физику. Ни одну из этих составляющих нельзя считать второстепенной.
Как следствие, практикующий ФДТ специалист должен исповедовать мультидисциплинарный подход и быть специалистом в разных областях знаний. Не у каждого врача это получается.
2. Врачи мало знают про этот метод или не знают совсем, хотя он уже входит в федеральный стандарт оказания медицинской помощи по акушерству и гинекологии при патологии шейки матки при CIN – смотрите Приказ Минздрава России от 01.11.2012 N 572н (ред. от 11.06.2015) «Об утверждении Порядка оказания медицинской помощи по профилю «акушерство и гинекология (за исключением использования вспомогательных репродуктивных технологий)» (Зарегистрировано в Минюсте России 02.04.2013 N 27960).
3. Сейчас не производят катетеры по форме матки. Что касается лечения матки, технология усложняется тем, что матка – полый мышечный орган треугольной формы. Около 5 лет назад в России и в Швейцарии производили баллонные катетеры по форме матки, но в последнее время их выпуск остановлен.
На сегодняшний день мной совместно с доктором физических наук, профессором Лощёновым В.Б. (ЗАО БИОСПЕК) инициирована разработка и сертифицированное производство внутриматочного баллонного световода нового поколения.
Показания к проведению фотодинамической терапии предрака матки
Чтобы получить консультацию, показана ли вам фотодинамическая терапия, и рассчитать цену процедуры, высылайте вашу историю болезни и анализы на e-mail doctor.afanasyev@mail.ru. Или звоните по телефону 8 (800) 555-77-26 в Москве.
Прием ведет Афанасьев Максим Станиславович, акушер-гинеколог, онкогинеколог, онколог, иммунолог, доктор медицинских наук, профессор и член ученого совета Первого МГМУ им. И.М. Сеченова МЗ РФ, эксперт по лечению атипической гиперплазии матки.
Прием проводится в двух клиниках в Москве, а также в Санкт-Петербурге, Махачкале, Курске, Ставрополе, Барнауле, Самаре, Набережных Челнах, Салавате, Челябинске, Сургуте и других регионах России. Уточнить дату, место приема в вашем городе и записаться на консультацию вы можете у администратора по телефону +7 (495) 204-18-93.
После лечения я поддерживаю обратную связь со всеми пациентками и решаю все возникающие вопросы. Гепатит и положительный ВИЧ статус не является противопоказаниями для лечения методом ФДТ.
1. Ramirez PT, Frumovitz M, Bodurka DC, et al. Hormonal therapy for the management of grade 1 endometrial adenocarcinoma: a literature review. Gynecol Oncol. 2004;95:133-138.
2. Banno K, Kisu I, Yanokura M, et al. Progestin therapy for endometrial cancer: the potential of fourth-generation progestin [review]. Int J Oncol. 2012;40:1755-1762.
3. Сохранение фертильности путем фотодинамической терапии у молодых пациенток с ранней стадией карциномы эндометрия. Долгосрочное исследование, основанное на последующем наблюдении пациенток. Авторы: Мин Чул Чой, Санг Геун Джунг, Хьюн Парк, Юн Хьюн Чо, Чан Ли, Сеунг Джо Ким.
5. *** Новикова Е.Г., Чулкова О.В., Пронин С.М. Лечение атипической гиперплазии эндометриия / Практическая онкология. 2004. Т. 4, № 1. С. 52-59.