NK-клетки: что значит и какую функцию в человеческом организме они выполняют
Человеческий организм наполнен различными удивительными явлениями, многие из которых не слишком известны широкому кругу людей. Одним из ярких примеров в этом плане можно привести так называемые NK-клетки, которыми интересуются многие ученые и исследователи. Что же это за клетки?
Натуральные киллеры

Данные образования способствуют грамотной регуляции иммунной системы и ее ответа на имеющиеся в теле болезни и опухоли. Благодаря их активному действию происходит генерация цитокинов, а также хемокинов, которые в свою очередь образуют важнейшую часть трехмерной белковой структуры любого живого организма.
Из сказанного понятно, что NK-клетки являются предельно важными для работы нашего тела и его защиты от неприятелей микробов.
Как образуются NK-клетки
Медицине долгое время было неизвестно происхождение натуральных киллеров, но в последние годы эту тайну удалось раскрыть. Происхождение NK-клеток и лимфоцитов оказалось одним и тем же – они формируются в красном костном мозге, а потом попадают в ткани и кровь, разносясь по всему телу. Если подходить к рассмотрению вопроса строго по-научному, то сейчас NK-клетки вообще принято считать одной из разновидностей лимфоцитов.
Структура естественных киллеров следующая:
Без этих образований наш организм был бы болезненным и не способным сопротивляться различным неприятностям.
Основные функции NK-клеток
Как уже было упомянуто – рассматриваемые образования являются разновидностью лимфоцитов и важнейшей частью естественного барьера организма против внешних микроорганизмов, инфекций, а также опухолей. Интересной особенностью NK-клеток является то, что при наличии хорошего здоровья у человека они находятся в полупассивном состоянии и особо не проявляют своего присутствия. Но как только болезнь начинает одолевать гражданина, это сигнал организму – Т-лимфоциты не справляются с инфекцией, и именно в такие моменты естественные киллеры вступают в дело.
Из сказанного понятно, что главная функция NK-клеток – борьба с агрессивными вредоносными микроорганизмами, когда обычные лимфоциты уже не в силах справиться со своей задачей и подавить их.
Анализы также показывают, когда человек здоров, то NK-клетки у него в норме, когда болен – их становится значительно больше.
ЗдоровьеКак Т-лимфоциты спасут нас от коронавируса и почему они лучше, чем антитела
В пандемию мы все научились немного больше заботиться о своём здоровье. И точно так же стали немного лучше разбираться в том, о чём раньше даже не подозревали: устройстве иммунной системы человека, взаимодействии её с вирусами разных типов и антителах. Последние особенно интересны в контексте приобретённого иммунитета, который позволяет переболевшим COVID-19 (кому-то больше, кому-то меньше) оставаться защищёнными от коронавируса.
Но вот в чём проблема: не у всех людей с симптомами коронавируса обнаруживаются антитела. Как такое возможно? Ответом на задачу со звёздочкой стали Т-лимфоциты. Учёные уже доказали, что сформированная ими защита может быть прочнее и совершеннее. Обо всём этом давайте немного подробнее.
ТЕКСТ: Марина Левичева
Иммунитет врождённый и адаптивный
Иммунная система представляет собой сложную сеть связанных между собой клеток, которая защищает организм от внутренних и внешних угроз. Сам иммунитет при этом бывает двух типов: врождённый (естественный) и адаптивный (приобретённый). В основном они отличаются друг от друга специфичностью и оперативностью реагирования на врага.
Врождённый иммунитет — наша первая линия защиты. Она может обнаружить многие патогены, как только они попадают в организм. Но, во-первых, она не всегда делает это достаточно быстро, чтобы мы успели не заболеть, во-вторых, она всё-таки не может распознать все потенциально опасные молекулы.
Если что-то идёт не так и врождённый иммунитет не справляется, система посылает сигналы, чтобы активировать адаптивную иммунную систему. Этот процесс называется презентацией антигена, потому что компоненты системы естественного иммунитета буквально представляют Т-лимфоцитам захваченный ими антиген (разве что без слов «Теперь это ваша проблема»).
Адаптивная иммунная система развивалась, чтобы обеспечить организму лучшую защиту. Но её полноценный запуск довольно медленный, так что может пройти несколько дней, прежде чем в игру вступят звёзды этой вечеринки — Т-клетки.
Т-клетки и что о них нужно знать
Из школьной программы многие помнят, что за иммунитет у нас ответственны лимфоциты. Существует два типа лимфоцитов: В-клетки, которые образуются и созревают в костном мозге, и Т-клетки, которые также образуются в костном мозге, но созревают в вилочковой железе (тимусе), расположенной в верхнем отделе грудной клетки. В организме они работают вместе, но Т-клетки всё равно круче.
Дело в том, что Т-клетки нацелены на выявление и устранение специфических инородных частиц. Вместо того, чтобы атаковать все антигены подряд (а это бактерии, вирусы, токсины и даже пыльца — всё, что заставляет организм вырабатывать антитела), Т-клетки циркулируют до тех пор, пока не столкнутся со «своим» антигеном. Они определяют его с помощью белков на поверхности, которые могут связываться с белками на поверхности антигенов. Существуют триллионы вариантов этих поверхностных белков, каждый из которых может распознать собственную мишень.
Роль Т-клеток немного меняется на протяжении жизни. В детстве с их помощью у нас формируется иммунитет к общим патогенам и создаётся запас Т-клеток памяти. Они буквально запоминают реакцию на те или другие антигены, поэтому, встречая их в будущем, реагируют быстрее и эффективнее (это называется вторичным иммунным ответом). Дальше
Т-клетки в основном занимаются иммунорегуляцией и работой с повторяющимися или постоянно присутствующими (при наличии хронических заболеваний) в организме антигенами. С возрастом их количество снижается, так что чем мы старше, тем слабее становится наш иммунитет.
Т-клетки тоже бывают разных типов. Т-хелперы, например, помогают активности других иммунных клеток, высвобождая информационные молекулы цитокины. Они стимулируют созревание В-клеток, которые уже начинают вырабатывать антитела для нейтрализации патогена. А
Т-киллеры (цитотоксические T-лимфоциты) самостоятельно убивают повреждённые или инфицированные клетки организма.
Хотя Т-клетки в основном наши друзья и защитники, иногда они могут стать причиной аутоиммунных заболеваний. Это происходит, когда путешествующие в поисках своего антигена клетки начинают атаковать собственные клеточные белки человека.
Что не так с антителами
Основная проблема антител в том, что они не очень долго сохраняются в организме. Есть данные, что уровень антител у людей, инфицированных SARS-CoV-2, снижается в течение 2–3 месяцев. Это справедливо, что так бывает не всегда, потому что срок жизни антител, по всей видимости, зависит от патогена.
Антитела к другим коронавирусам могут, постепенно уменьшаясь, сохраняться от 12 до 52 недель с момента заражения. Но в случае
с COVID-19 это может продолжаться до семи недель, а может и больше. Другое недавнее исследование показало, что при бессимптомном течении заболевания уровень антител значительно ниже и в 40 % случаев они полностью исчезают через восемь недель.
Получается, что с антителами пусть и всё так, но защита, которую они обеспечивают, не настолько продолжительная и мощная, как того хотелось бы.
Т-клетки и коронавирус
Так как большинство людей раньше не подвергались воздействию нового коронавируса (на то он и новый), у них нет Т-клеток памяти и, соответственно, защиты от инфекции. Хорошая новость в том, что инфицированные люди при этом могут генерировать COVID-специфические Т-клетки. Причём, как показало исследование шведских учёных, это происходит также у пациентов со слабыми симптомами или вообще без них. И даже в том случае, если в организме нет антител.
А ещё обнаружилось, что некоторые неинфицированные люди имеют
Т-клетки к COVID-19. Это, вероятнее всего, является перекрёстной реактивностью — совпадением с реакцией организма на предыдущие коронавирусные инфекции. Когда учёные посмотрели на образцы крови, взятые за несколько лет до начала пандемии, и обнаружили в них Т-клетки, приспособленные к обнаружению белков на поверхности COVID-19, теория подтвердилась.
Почему это всех так радует? Потому что Т-клеточные реакции могут быть довольно длительными. Когда учёные из Сингапура проанализировали показатели людей, перенёсших атипичную пневмонию в 2003 году, они увидели, что даже спустя семнадцать лет у них остались специфические
Т-клетки. Не говоря уже о том, что наличие Т-клеток более точно показывает, переболел человек коронавирусом или нет.
Что выяснили российские учёные
Совсем недавно в авторитетном научном журнале Immunity опубликовали исследование российских учёных на тему Т-клеток и коронавируса, в котором приняли участие 34 переболевших коронавирусом добровольца и две контрольные группы здоровых доноров.
«Действительно, не у всех переболевших коронавирусом обнаруживаются антитела. У части выздоровевших иммунный ответ обеспечивается только за счёт Т-клеток, чего, по всей видимости, оказывается достаточно», — объясняет Григорий Ефимов, заведующий лабораторией трансплантационной иммунологии Национального медицинского исследовательского центра (НМИЦ) гематологии Минздрава и один из авторов исследования.
Учёные также отметили, что ответ на фрагменты коронавируса есть не только у тех, кто им переболел, что может объясняться сезонными простудными заболеваниями в прошлом, которые были вызваны коронавирусами других типов. «При этом здоровые доноры, которых мы набирали во время пандемии, в среднем имели более высокий уровень ответа, чем те, образцы которых хранились в биобанке и были получены раньше. Скорее всего, это значит, что часть доноров имела контакт с вирусом, вызывающим COVID-19, не подозревая об этом», — добавляет Григорий Ефимов.
Одно из самых интересных открытий — обнаружение фрагментов вируса,
Т-клеточный ответ на которые у людей возникает особенно часто. По словам исследователей, прямо сейчас они заняты изучением этих фрагментов, так как лучшее их понимание даст информацию для разработки теста
на Т-клеточный иммунитет. Пока он используется только как научный инструмент, но если всё пойдёт хорошо, в ближайшее время может стать доступным и для диагностики тоже.
Иммунология бесплодия.
Статья Елены Клещенко в журнале «Химия и жизнь», номер 1, 1999
Жили-были царь с царицей, и не было у них детей. Не обязательно царь, может быть и купец, и бедняк — в сказке, точно так же, как и в жизни, это несчастье может случиться с кем угодно. Ну, а потом происходит чудо — на то она и сказка.
А чудеса, по определению, отличаются от обыкновенных событий всего лишь более низкой вероятностью. Диагноз «бесплодие» вовсе не означает, что ребенка никогда не будет. Но в норме вероятность зачатия довольно высока — когда супруги решают завести детей, ожидания обычно сбываются в первый же год. А если вероятность снижена в десять раз? При максимальном невезении придется ждать десять лет, но за эти десять лет шансы еще уменьшатся. В общем, рассуждения о ненулевой вероятности в подобной ситуации едва ли утешат.
Однако с этой точки зрения понятно, почему бывает так, что женщина, вроде бы ничем не болевшая, не может забеременеть. Скажем, воспалительное заболевание, ухудшившее проходимость маточных труб, небольшое нарушение функции яичников, легкие изменения гормонального цикла — каждый фактор незначительно снижает вероятность, но все вместе (что не так уж редко в нашей тяжелой жизни) они вполне способны отсрочить наступление беременности до потери последней надежды.
Не следует забывать и о мужчинах. Глава семьи, ожидающий наследника, часто не желает и слышать, что может быть сам виноват. Многие даже не помнят, болели или не болели свинкой, и понятия не имеют, какие осложнения дает это «детское» заболевание у взрослых людей. (О свинке мы еще поговорим).
Но допустим, у мужчины все в порядке, и будущая мать тоже избавилась от своих болячек, а беременность так и не наступает. Платные обследования показывают полный порядок, врач в женской консультации разводит руками, друзья и родные сыплют советами и соболезнованиями. Что делать и как быть?
Уникальный, платный, некоммерческий
В России сегодня еще не так плохо с медициной, как принято считать. Гематология, иммунология, акушерство и гинекология — все это у нас есть. А вот врачей и ученых, работающих на пересечении этих областей явно не хватает. Между тем как раз иммунологические реакции, которые происходят во время оплодотворения и ранней беременности, могут вызывать таинственное и зловещее «бесплодие неясного генеза» (а таким диагнозом сопровождаются примерно 10–15% всех случаев бесплодия!). И генитальный хламидиоз, и обычные, нехорошо нам знакомые воспалительные процессы тоже могут быть связаны с иммунологическими нарушениями. Но кто будет в этом разбираться?
Теперь пробел отчасти заполнен. В Москве работает Центр иммунологии и репродукции. Здесь занимаются не только иммунологией беременности. Один из самых важных проектов — ранняя диагностика предраковых заболеваний шейки матки, иначе говоря, именно то, что само собой разумеется в развитых странах и за отсутствие чего гражданки России (не про нас будь сказано, дорогие читательницы) расплачиваются здоровьем и жизнью. ЦИР сотрудничает с Институтом ревматологии РАМН, Кардиологическим научным центром РАМН, Гематологическим научным центром РАМН, Онкологическим научным центром.
Однако основная цель, которая была поставлена при создании центра, — организовать диагностику и лечение иммунологических форм невынашивания беременности и бесплодия, собрать и ввести в практику все существующие методики на максимально высоком уровне. Уникальные (для России) методы анализа позволяют определить многие заболевания, вызывающие якобы беспричинное бесплодие. И, что более важно, эти заболевания, оказывается, излечимы. Настрадавшиеся женщины становятся матерями. (Из «первой волны» пациенток забеременело около половины, при том, что не все прошли обследование до конца — не у всех хватает терпения.)
ЦИР — некоммерческая организация: хотя услуги здесь платные, но доход, который приносят клиенты, только-только перекрывает расходы на оказание этих услуг. Есть еще у нас непрактичные люди, которые считают, что приоритетной в таком деле должна быть организация медицинской помощи, а не материальная выгода. Дай-то Бог, чтобы в фондах, распределяющих гранты, ценили подобную непрактичность.
Впрочем, о том, как существует теоретическая и прикладная медицина в условиях экономического кризиса, можно рассказывать долго. Но давайте сейчас не будем о деньгах, которых не хватает и врачам, и пациентам, и вообще большинству наших соотечественников. Поговорим о высоком, о научном.
«И разве сперматозоид — не страшнейший из микробов?»
Так спрашивал себя, размышляя о жизни, герой романа Евгения Замятина «Мы». Микроб не микроб, а на протозойную инфекцию похож — такое «решение» принимает иммунная система женщины примерно в каждом десятом случае бесплодия. Секрет шейки матки из благоприятной среды превращается в агрессивную — в нем присутствуют антитела, которые связывают и обездвиживают сперматозоиды. Оплодотворения при этом, естественно, не происходит.
Здесь важно отметитья, что иммунизация женщины сперматозоидами партнера происходит в любом случае, поэтому обыкновенное определение уровня антител в крови не всегда помогает поставить диагноз. Искать надо именно те антитела, которые мешают движению сперматозоидов, и коль скоро они найдены — искусственное оплодотворение спермой мужа снимет все проблемы.
Бывает и так, что расправу учиняет иммунная система самого мужчины. Дело в том, что она считает «своими» только белки, которые были в организме на момент рождения. Белки, которые синтезируются позже (например, в тканях яичка), — уже как бы чужие, их приходится прятать от агрессивного внимания иммунной системы. В ткани яичка лимфоциты просто не попадают — доступ им преграждает так называемый гемато-тестикулярный барьер. А коль скоро лимфоцит не видит белкового антигена, то и антителам взяться неоткуда. (Но при травме одного яичка через некоторое время будет поражено и второе именно потому, что лимфоциты проникают через брешь в барьере и начинают производство антител.)
Однако у всех хитрых систем защиты есть и свои слабые места. Организм человека, больного свинкой, вырабатывет антитела, которые взаимодействуют с тканями органа, пораженного вирусом, — околоушной железы. Но, оказывается, в иммунологии, как и везде, бывают глупые совпадения. Те же антитела «помечают» и ткани яичка; таким образом, их атакует не вирус, а собственная иммунная система организма. Следствие — резкое снижение числа сперматозоидов.
Но вообще-то, если задуматься, самое удивительное то, что сама беременность, как правило, протекает нормально. Вспомним, с какими осложнениями связана пересадка органов и тканей, даже если донор приходится пациенту кровным родственником. Почему же организм матери терпит это чудовищное вторжение — не сердечный клапан или кусочек кости, а что-то огромное, растущее, пожирающее питательные вещества, отравляющее мать токсикозом? Откуда иммунная система узнает, что это трех-четырехкилограммовое нечто — не страшная опухоль, подлежащая немедленной ликвидации, а, наоборот, любимое дитя?
Чтобы разобраться в этом вопросе, придется напомнить, с чего все мы, уважаемые читатели, начинали. Неоплодотворенная яйцеклетка человека живет 21 час. За это время она входит в маточную трубу и ожидает прихода сперматозоида. Если дождаться ей не суждено, тут все и заканчивается — до следующей овуляции. Если же оплодотворение происходит, продукт слияния яйцеклетки и сперматозоида получает гордое имя «зародыш» и направляется по трубе в полость матки. Путешествие длится 6—7 суток, в продолжение которых зародыш живет, так сказать, своим умом, за счет собственного запаса питательных веществ, ведь связь с материнским организмом еще не установлена.
И вот в эти-то несколько дней зародыш — крохотное тельце размером 0,1 мм, ничем пока не похожее на разумное существо — посылает сигналы иммунной системе матери, синтезируя особые белки. Один из этих белков, называемый фактором ранней беременности, особым образом перенастраивает иммунную систему. Как легко догадаться, его очень мало — оцените сравнительные размеры матери и ее будущего ребенка! — и определять наличие этого фактора в крови проще не напрямую (хотя современные методы позволяют и это), а по так называемой реакции розеткообразования с эритроцитами барана.
(Кстати, это единственный признак, по которому можно определить беременность до имплантации зародыша в стенку матки. Иначе говоря, узнать, было ли, собственно, зачатие, ведь потерю зародыша в возрасте нескольких дней сама женщина воспринимает как обычную менструацию. Но пока этот метод применяют только в рамках научных исследований. Клинический метод, знакомый большинству женщин, — определение в моче хорионического гонадотропина, или ХГ, — эффективен на более поздних сроках, когда зародыш имплантируется в стенку матки и между его оболочкой и стенкой матки установлен контакт.
Агрессия? Нет, равнодушие
Как же изменяются иммунные реакции у женщины, в теле которой странствует зародыш? В начале 50-х предполагали, что зародыш (с самого начала своего существования, и позже, когда его называют плодом) получает своего рода «статус невидимости». Это предположение высказал английский биолог Питер Брайан Медавар, один из основоположников иммунологии и трансплантологии, нобелевский лауреат.
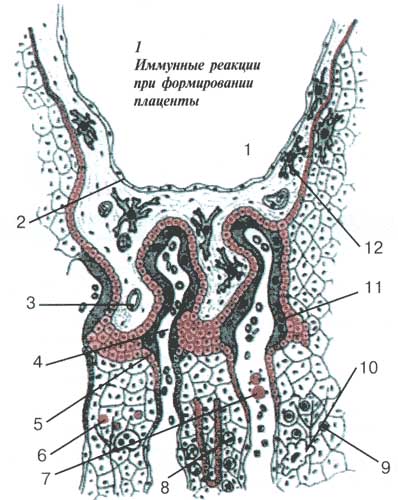 | 1 — околоплодные воды, 2 — амнион, 3 — капилляр плода, 4 — артериола матери. Клетки трофобласта (5) несут на своей поверхности так называемый антиген HLA-G — один из важнейших сигналов, который плод подает иммунной системе матери. Эти клетки попадают в толщу слизистой оболочки матки (6) и в кровяное русло (7), усиливая при этом иммунную реакцию. При благоприятном течении беременности обязательно наблюдается иммунный ответ матери: активизируются NK-клетки (8), Т-лимфоциты (9) и макрофаги (10) матери. В трофобласте идет слияние клеток — образуется синцитиотрофобласт (11). Макрофаги плода (12), в свою очередь, готовы к борьбе |
Как известно, иммунологическую индивидуальность человека определяет главный комплекс тканевой совместимости, или система лейкоцитарных антигенов (сокращенно ее называют HLA — human leucocyte antigens). При переливании крови, пересадке тканей донор предстает перед иммунной системой больного в виде множества антигенов, или, точнее. эпитопов — небольших характерных участков биомолекул, с которыми взаимодействуют антитела. Это такая же неотъемлемая часть нашей индивидуальности, как черты лица или отпечатки пальцев. Предполагалось, что эпитопы плода спрятаны от иммунной системы матери (примерно так, как ткани яичка у мужчин). Но все оказалось гораздо интереснее: чтобы беременность протекала нормально, антигены, которые плод получил от отца, ДОЛЖНЫ распознаваться иммунной системой матери!
Для исследования системы HLA, естественно, понадобились антитела к этим антигенам. Так вот, источником таких антител стала кровь беременных женщин, много рожавших: чем больше было детей у супружеской пары, тем выше содержание антител к HLA мужа. Получалось, что иммунный ответ все-таки возникает, и именно при нормальной беременности! И наоборот, если таких антител мало (например, в случае близкородственного брака, когда HLA мужа похожа на собственную HLA женщины), велика вероятность невынашивания, патологии беременности. Разумеется, тут свою долю проблем приносят и гены — возможность передать потомству две копии дефектного гена выше, если супруги связаны хотя бы отдаленным родством. Но основной причиной невынашивания приходится назвать, как это ни парадоксально, недостаточную чуждость плода.
Необходимо иметь в виду, что плод — не часть материнского организма, а отдельное существо. Когда зародыш «пускает корни» в стенку матки, это весьма агрессивное вторжение, на которое организм матери должен бы ответить резким отпором. Так и происходило, например, в эксперименте на животных: когда зародыш пересаживали под капсулу почки матери, он мгновенно отторгался. Стало быть, не вся иммунная система матери подвергается перенастройке: особыми полномочиями обладают только лимфоциты слизистой оболочки матки. Они позволяют зародышу внедряться в слизистую, разрушая ее, но лишь до определенного этапа. Затем вторжение принудительно останавливают. Если этого не происходит, последствия могут быть плачевными.
Имплантация плода — это установление контакта между трофобластом (наружной оболочкой плода) и кровотоком матки. Позднее между клетками трофобласта исчезают перегородки, он превращается в синцитий — как бы одну гигантскую многоядерную клетку. Получается своего рода мембрана, которая и ограничивает, и соединяет. Оказалось, что и слияние клеток трофобласта, и последующее формирование плаценты регулируются извне, теми же лимфоцитами матери. Лимфоциты вырабатывают особые регуляторные вещества — цитокины. Собственно, этот класс низкомолекулярных пептидов-регуляторов — отдельная большая тема. В разных тканях разные типы клеток синтезируют различные цитокины, структурно сходные, но с различными функциями. Есть и такие, которые «учат» плаценту, как ей развиваться.
Вот и выстроилась причинно-следственная цепочка: распознавание плода иммунной системой матери — размножение соответствующих клонов лимфоцитов — синтез цитокинов — нормальная плацента, нормальный обмен веществ между матерью и плодом, нормальное протекание беременности. И обратно: нет иммунной реакции у матери — нет регуляции развития плода — патологии, невынашивание.
Какие именно сочетания антигенов HLA отца и матери ведут к бесплодию, пока неясно, хотя гипотезы, конечно, есть, и некоторые из них подтверждены экспериментально. Кроме того, известно, что существуют особые белки, которые синтезируются только в эмбриональном периоде, — именно они отличают плод от пересаженного органа, сигнализируют иммунной системе матери: свои, мол. (Эти белки синтезируют и раковые опухоли, чтобы не быть уничтоженными.)
Но пока теоретики думают, практики используют в работе метод, позволяющий ответить на самый общий вопрос: достаточно ли хорошо иммунная система женщины реагирует на антигены будущего отца? Если у пациентки уже были выкидыши по непонятной причине, просто необходимо это проверить. Технически это несложно: в сыворотку крови женщины помещают лимфоциты мужа, и смотрят, сколько их выживет и сколько погибнет. А погибнуть должны не менее 30% клеток. Если этот процент снижен, скорее всего, причина невынашивания в том самом «равнодушии» материнской иммунной системы к мужу и ребенку. Значит, надо вызвать у матери иммунный ответ, иммунизировав ее антигенами мужа, — сделать своего рода прививку.
Интересно, что эта методика появилась еще в конце 70-х — начале 80-х, когда основной причиной выкидышей считалась чрезмерная агрессивность материнской иммунной системы по отношению к плоду. Методом лечения выбрали пересадку женщине кожного лоскута мужа, чтобы он «оттитровывал» избыток антител, тем самым спасая зародыш. На самом деле пересаженный лоскут стимулировал иммунный ответ — но именно это и обеспечивало нормальную беременность! Теперь, конечно, к пластической хирургии уже не прибегают: для иммунизации вполне достаточно инъекции лимфоцитов мужа.
Но есть и другой вариант развития событий, почти совпадающий с первоначальной гипотезой: иммунная система матери может быть чересчур агрессивна по отношению к плоду. Виновниками агрессии оказались так называемые естественные клетки-киллеры (по английски natural killers, NK). Наверное, все наши читатели знают про T-киллеры и сложный многоступенчатый механизм их запуска: клетка-макрофаг захватывает чужой антиген, при необходимости вычленяет из него фрагменты, которые соединяются со специальными белками (как раз из числа HLA) и уже в этом виде преподносятся T-лимфоцитам. Клеткам типа NK все эти сложности чужды. Они руководствуются правилом: «Постороннее? Разрушить». Предполагают, что это наиболее древняя форма иммунитета. — примитивная в смысле «первичная», но не в смысле «простая», ибо свои сложности есть и у «естественных убийц».
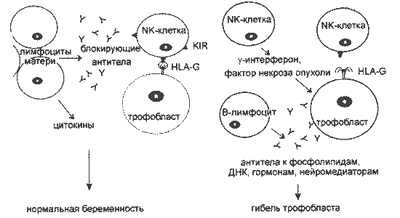
На этой схеме очень упрощенно изображены иммунные взаимодействия матери и ребенка в норме и при патологии беременности. По одной из последних теорий, если организмы матери и плода отличаются по так называемым HLA DQ и DR, NK-клетки взаимодействуют с антигенами HLA-G трофобласта (слева). После этого на поверхности NK-клеток появляются рецепторы, ингибирующие киллерную активность (KIR). NK-клетки становятся неактивными под воздействием антител к KIR. Клетки иммунной системы матери выделяют также цитокины, регулирующие рост трофобласта, и антитела, которые останавливают реакцию отторжения. При патологии (справа) взаимодействие NK-клеток с HLA-G нарушено, и киллер начинает свою работу. В отсутствие цитокинов нарушается развитие трофобласта. Другой причиной гибели плода может стать аутоиммунная реакция (антитела к фосфолипидам)
В норме NK — это основа противоопухолевого иммунитета. Их главная задача состоит в том, чтобы как можно раньше распознать «сбойные» клетки и уничтожить их. NK играют важную роль в ходе нормальной беременности. Но когда уровень NK в крови женщины повышен, повышается и вероятность выкидыша — понятно почему: зародыш принимают за раковую опухоль.
При повышенном уровне естественных клеток-киллеров в крови назначают терапию, механизм которой не совсем ясен. Женщине вводят внутривенно, через капельницу, так называемые естественные донорские иммуноглобулины — смесь белков, полученных из плазмы тысяч доноров. Что в точности происходит, пока не совсем понятно, но результаты обнадеживают: неспецифическая агрессия бывает отражена.
До сих пор мы говорили по большей части об аллоиммунных формах бесплодия, то есть таких, в основе которых лежит взаимодействие «чужой (отцовский) антиген — антитело матери». Но существуют также аутоиммунные заболевания, связанные с появлением антител против собственных антигенов матери. Например, при заболевании, которое называется антифосфолипидный синдром, антитела атакуют «родные» фосфолипиды — один из главных структурных элементов клеточных мембран. Антифосфолипидный синдром у женщин сопровождается невынашиванием беременности. Дело в том, что фосфолипиды стенок сосудов — одна из узловых точек в процессе свертывания крови, образования трехмерной сетки тромба. Антитела к фосфолипидам сбивают регуляцию свертывания/антисвертывания. В результате повышается опасность микротромбозов, нарушается формирование плаценты и опять-таки происходит выкидыш.
Но этого можно избежать. Если в сыворотке крови женщины присутствуют антитела к кардиолипину (это один из главных фосфолипидов), терапию начинают еще до зачатия. Малые дозы аспирина и гепарина корректируют коагуляционные свойства крови, и очень часто это приводит к хорошим результатам — беременность развивается нормально.
Два слова в заключение. «Черный сентябрь» минувшей осенью стал черным и для ЦИРа. Телефоны молчали, прежние больные не показывались, и новые не приходили. Собственная жизнь становилась не по карману, что говорить о жизни нерожденного ребенка! А месяц спустя прием возобновился. Слава Богу, экономическая форма бесплодия нам пока не грозит. Чтобы с нами ни делали, женщины хотят иметь детей.
Автор благодарит за предоставленную информацию Игоря Ивановича Гузова, директора АНО «Центр иммунологии и репродукции»







