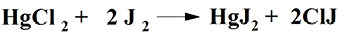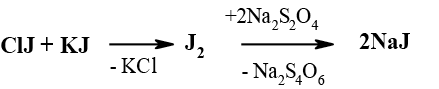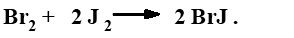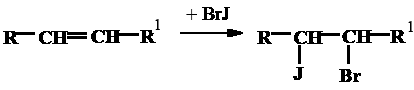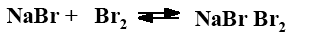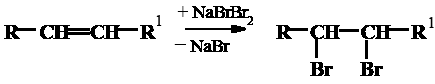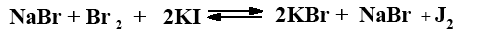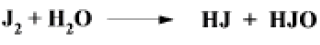ОФС.1.2.3.0005.15 Йодное число
Содержимое (Table of Contents)
ОФС.1.2.3.0005.15 Йодное число
Йодным числом (II) называют количество йода, выраженное в граммах, связываемое 100 г испытуемого вещества.
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ОБЩАЯ ФАРМАКОПЕЙНАЯ СТАТЬЯ
Йодное число ОФС.1.2.3.0005.15
Взамен ст. ГФ XI, вып.1
Йодным числом (II) называют количество йода, выраженное в граммах, связываемое 100 г испытуемого вещества. Йодное число характеризует содержание в испытуемом веществе непредельных соединений (например, непредельных жирных кислот в жирах или маслах).
Метод 1
Точную навеску испытуемого вещества в количестве, указанном в табл. 1, помещают в сухую коническую колбу с притертой пробкой вместимостью 250 мл, растворяют в 3 мл эфира или хлороформа, прибавляют 20,0 мл йода монохлорида раствора 0,1 М, закрывают колбу пробкой, смоченной 10 % раствором калия йодида, осторожно встряхивают и выдерживают в темном месте в течение 1 ч.
Прибавляют последовательно 10,0 мл калия йодида раствора 10 %, 50 мл воды и титруют натрия тиосульфата раствором 0,1 М при постоянном энергичном встряхивании до светло-желтой окраски раствора. Прибавляют 3 мл хлороформа, сильно встряхивают, затем прибавляют 1 мл раствора крахмала и продолжают титрование до обесцвечивания раствора. Проводят контрольный опыт в тех же условиях.
При анализе твердых жиров навеску испытуемого вещества растворяют в 6 мл эфира, прибавляют 20,0 мл йода монохлорида раствора 0,1 М и 25 мл воды. Дальнейшее определение проводят, как указано выше.
Таблица 1 — Величина навески испытуемого вещества в зависимости от ожидаемого йодного числа
| Ожидаемое йодное число | Навеска испытуемого вещества, г |
| Менее 30 | 1,1 – 0,7 |
| 31 – 50 | 0,7 – 0,5 |
| 51 – 100 | 0,5 – 0,25 |
| 101 – 150 | 0,25 – 0,15 |
| Более 150 | Менее 0,15 |
Йодное число вычисляют по формуле:
где V1 – объем натрия тиосульфата раствора 0,1 М, израсходованный на титрование в основном опыте, мл;
V2 – объем натрия тиосульфата раствора 0,1 М, израсходованный в контрольном опыте, мл;
a – навеска испытуемого вещества, г;
0,01269 – титр натрия тиосульфата раствора 0,1 М по йоду, г/мл.
Метод 2
Точную навеску испытуемого вещества в количестве, указанном в табл. 2, помещают в сухую коническую колбу с притертой пробкой вместимостью 250 мл и растворяют в 15 мл хлороформа. Медленно прибавляют 25,0 мл раствора йода бромида. Колбу закрывают и выдерживают в темном месте в течение 30 мин, если не указано иначе в фармакопейной статье, часто встряхивая. Прибавляют последовательно 10,0 мл калия йодида раствора 10 %, 100 мл воды и титруют натрия тиосульфата раствором 0,1 М при постоянном энергичном встряхивании до светло-желтой окраски раствора. Прибавляют 5 мл раствора крахмала и продолжают титрование, прибавляя натрия тиосульфата раствор 0,1 М по каплям, до обесцвечивания раствора. Проводят контрольный опыт в тех же условиях.
Таблица 2 — Величина навески испытуемого вещества в зависимости от ожидаемого йодного числа
| Ожидаемое йодное число | Навеска испытуемого вещества, г |
| Менее 20 | 1,0 |
| 20 – 60 | 0,5–0,25 |
| 60 – 100 | 0,25–0,15 |
| Более 100 | 0,15–0,10 |
Йодное число вычисляют по формуле, приведенной в методе 1.
Что такое йодное число?
Оно пришло к нам из аналитической химии и равно массе йода (в граммах), которой будет достаточно, чтобы химически связать 100 граммов взятого вами масла. Проще говоря, если йодное число взятого нами кунжутного масла равно 110, то для того, чтобы йодировать 100 г такого масла, потребуется 110 г молекулярного йода. (Это довольно много – в знакомом каждому флакончике со спиртовым раствором, например, содержится всего полграмма чистого йода!)
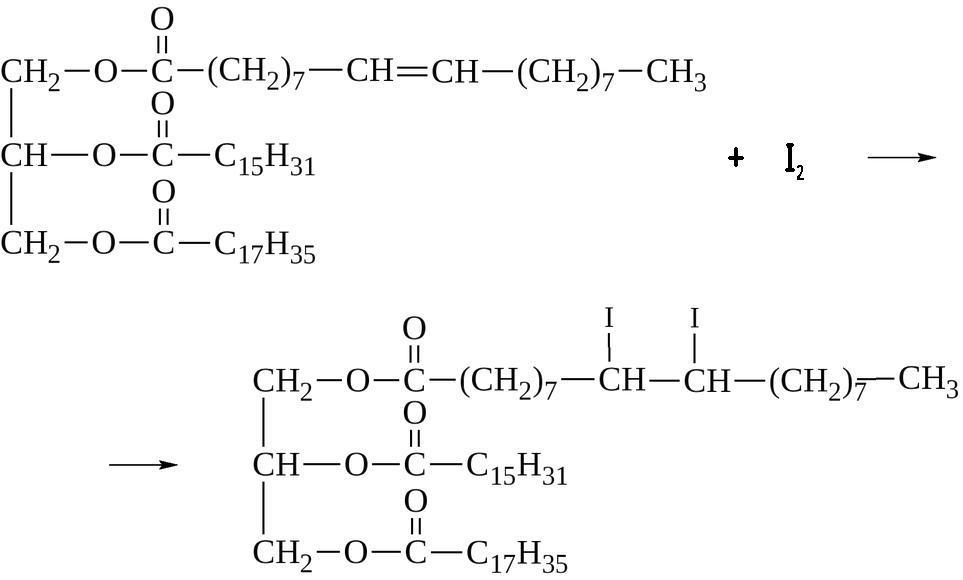
Вот как выглядит реакция йодирования:
Если в составе жира есть кислотный остаток с двойной связью – эта связь (мононенасыщенная кислота) окисляется ровно одной молекулой йода (I2). Если таких связей несколько (т.е. кислота – полиненасыщенная), то и молекул I2 требуется по одной на каждую связь.
Теперь возьмем для примера две мононенасыщенные кислоты – олеиновую (1) и нервоновую (2).
(1) 
У каждой из них есть только по одной двойной связи. Означает ли это, что их йодные числа равны? Вовсе нет!
Эти кислоты имеют разные молекулярные веса – 282 и 376. А молекулярный вес йода – 254. Немного школьной химии, и вы легко сосчитаете, что требующаяся масса йода для олеиновой кислоты будет равна 100*(254/282) = 90 граммов, а для нервоновой 100*(254/376) = 68 граммов. То есть, их йодные числа – 90 и 68.
Из всего вышесказанного нетрудно сделать вывод, что йодное число масла тем выше, чем больше:
— ненасыщенных жирных кислот в составе масла,
— молекулярная масса этих кислот (пропорциональна длине углеводородной цепочки),
— двойных связей в структуре их молекул.
А как влияют на йодное число насыщенные кислоты, вроде пальмитиновой и стеариновой? Они с йодом не взаимодействуют, поэтому, чем их в составе больше, тем йодное число меньше. Если же масло содержит ТОЛЬКО насыщенные кислоты, то его йодное число равно нулю.
Как считать йодное число для смеси масел?
Поскольку речь идет о массах, каждое масло в смеси вносит свой вклад пропорционально весу. Формула выглядит так:
Xобщ = X1*W1 + X2*W2 + … +Xn*Wn,
где Xn – йодные числа входящих в смесь масел,
Wn – соответствующие им массовые доли.
Например, нам нужно посчитать итоговое йодное число для смеси из 20% бабассу (й.ч. = 15), 65% пальмового (й.ч. = 51) и 25% льняного (й.ч. = 104) масел. Подставляем цифры в формулу: 15*0,2 + 51*0,55 + 104*0,25 = 3 + 28 + 26 = 57.
Мыльный калькулятор считает точно так же – можете проверить и в дальнейшем пользоваться им. Приведенная формула понадобится вам, только если вы по каким-то причинам не доверяете значениям йодного числа, заложенным в калькулятор, и располагаете более точными данными.
Кстати, а зачем вообще знать йодное число масла?
Чем оно ниже, тем тверже и устойчивее к прогорканию будет ваше будущее мыло. Для твердых натриевых мыл желателен показатель не более 55. Многие удачные рецепты пренебрегают этим правилом, поскольку есть и другие факторы, влияющие на твердость и сохранность мыла. Однако, на начальном этапе лучше все-таки ориентироваться на него.
Йодные числа для масел и жиров можно поискать в Интернете или в химических справочниках, однако сведения из разных источников зачастую отличаются на 10-20%. На самом деле, точное значение поможет узнать только химический анализ – ведь все зависит от индивидуального состава вашего конкретного масла, способа производств. Так что, вне зависимости от того, считаете вы на калькуляторе или вручную, будьте внимательны и осторожны, при работе с показателями «на грани». Удачи!
Йодное число и другие показатели качества жиров
Жиры специального назначения в большинстве жироемких кондитерских изделий являются структурообразователями. При их выборе технологи опираются, прежде всего, на твердость и температуру плавления.
Твердостью называют способность жиров сопротивляться проникновению в них другого тела, не получающего остаточной деформации. Этот показатель во многом определяет структурно-реологические свойства жира.
Температура плавления является определяющим показателем при формировании вкусовых качеств готового продукта. Низкая температура способствует быстрому таянию и высвобождению аромата. Этот параметр влияет и на усвояемость жира. Чем выше температура плавления, тем хуже жир усваивается организмом человека.
Температура застывания характеризует переход жира из жидкого состояния в твердое. Она представляет собой интервал значений, более низких, чем температура плавления. Данный показатель может определяться двумя методами (по Дженсену и Жукову), основанными на определении температуры жира, соответствующей максимальному выделению скрытой теплоты кристаллизации при определенных условиях охлаждения образца жира.
Важным технологическим параметром, характеризующим скорость кристализации жира, и, соответственно, определяющим производительность охлаждающего оборудования, является продолжительность застывания, под которым понимают время, за которое образец жира достигает температуры застывания (по Дженену или Жукову).
Одной из основных идентификационных характеристик липидов является их жирнокислотный состав. Согласно ГОСТу 3623-98 именно по нему можно обнаружить фальсификацию растительных масел и маргариновой продукции. Жирнокислотный состав определяется методом газовой хроматографии. С помощью данного метода определяют качественный и количественный жирнокислотный состав, количество трансизомеров, а также йодное число жира.
Йодное число является важнейшим химическим показателем. Йодное число позволяет судить о степени ненасыщенности жирных кислот, входящих в состав жира. Чем выше содержание ненасыщенных жирных кислот, тем выше значение йодного числа.
Йодное число жира – условная величина, представляющая собой число граммов йода, эквивалентное галогену, присоединившемуся к 1 г исследуемого жира, выраженное в процентах йода. Его можно определить по жирнокислотному составу как сумму произведений процентного содержания каждой ненасыщенной жирной кислоты на соответствующий ей коэффициент.
Триглицеридный состав дает информацию о том, какие триглицериды и в каком количестве входят в состав данного жира. Особую важность этот показатель приобретает при идентификации масла какао и его эквивалентов. Необходимо отметить, что даже если жирнокислотный состав и йодное число одинаковы, триглицеридный состав может быть разным, благодаря чему физико-химические показатели жиров будут отличаться. Это зависит от порядка распределения жирных кислот в триглицериде. Анализ проводится с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ).
Под воздействием таких неблагоприятных факторов, как повышенная влажность и высокие температуры при хранении и перекачке жира, происходит гидролиз, в результате которого образуются глицерин и свободные жирные кислоты. Высокомолекулярные жирные кислоты не имеют вкуса и запаха, и поэтому при увеличении их количества в продукте ощутимого изменения органолептических показателей не наблюдается, что не относится к жирам лауриновой группы (кокосовому, пальмоядровому маслам). Так как свободная лауриновая кислота имеет низкий вкусовой порог, то даже ее следов достаточно для появления «мыльного» привкуса.
В результате действия кислорода в жирах накапливаются первичные и вторичные продукты окисления. Именно их присутствие обуславливает появление характерного неприятного вкуса и запаха в жирах. Количество перекисей и гидроперекисй характеризует перекисное число, которое определяется в соответствии с ГОСТом 26593-85 и измеряется в ммоль активного кислорода/кг.Оно показывает, какое количество активного кислорода вступило в реакцию окисления жирных кислот. По ФЗ-9 перекисное число должно быть не более 1 ммоль активного кислорода/кг.
Альдегиды являются вторичными продуктами окисления жиров. Анизидиновое число–это мера концентрации вторичных продуктов окисления, встречающихся в масле и жире. Оно может характеризовать возможную устойчивость жира.
Высокое анизидиновое число исходного жира свидетельствует о продолжительном времени или неудовлетворительных условиях его хранения, либо о подвергании его длительному механическому и термическому воздействию. Даже если готовый продукт с завышенным анизидиновым числом получит высокую дегустационную оценку, при хранении может отмечаться реверсия вкуса. Стандарта на анизидиновое число для качественного жира не существует, но в мировой практике, также как и на производстве «ЭФКО», хорошим показателем считается анизидиновое число, не превышающее 3.
Таким образом, для получения качественных изделий на основе жира необходимо учитывать целый ряд показателей, охватывающих как чисто технологические свойства (твердость, температуру плавления и застывания, значение йодного чила), так и показатели порчи продукта (кислотное, перекисное и анизидиновые числа).
СОДЕРЖАНИЕ
Принцип
Химическая реакция, связанная с этим методом анализа, включает образование дииодалкана (R и R ‘символизируют алкил или другие органические группы):
Предшественник алкен (R 1 CH = CHR 2 ) бесцветно и так является органикйодистым продуктом (R 1 Х-Чир 2 ).
Методы определения йодного числа
Метод Хюбля
Основной принцип йодного числа был впервые введен в 1884 году А. В. Хюблем как « Йодзал ». Он использовал спиртовой раствор йода в присутствии хлорида ртути (HgCl 2 ) и четыреххлористого углерода (CCl 4 ) в качестве солюбилизатора жира. Остаточный йод титруют раствором тиосульфата натрия, используя крахмал в качестве индикатора конечной точки. Этот метод сейчас считается устаревшим.
Метод Вейса / Хануша
Затем к этой смеси добавляют насыщенный раствор иодида калия (KI), который реагирует с оставшимися свободными ICl / IBr с образованием хлорида калия (KCl) и дииодида (I 2 ).
ICl + 2 KI → KCl + KI + I 2
После этого высвободившийся I 2 титруют тиосульфатом натрия в присутствии крахмала для косвенного определения концентрации прореагировавшего йода.
IV (г л / 100 г) рассчитывается по формуле:
Определение IV по Вийсу является официальным методом, принятым в настоящее время международными стандартами, такими как DIN 53241-1: 1995-05, AOCS Method Cd 1-25, EN 14111 и ISO 3961: 2018. Одним из основных ограничений является то, что галогены не реагируют стехиометрически с сопряженными двойными связями (особенно в большом количестве в некоторых олифах ). Следовательно, в этой ситуации метод Розенмунда-Кунхенна обеспечивает более точное измерение.
Метод Кауфмана
Теперь количество образующегося йода определяется обратным титрованием раствором тиосульфата натрия.
Реакции необходимо проводить в темноте, так как образование радикалов брома стимулируется светом. Это привело бы к нежелательным побочным реакциям и, таким образом, к искажению результата потребления брома.
В образовательных целях Simurdiak et al. (2016) предложили использовать трибромид пиридиния в качестве реагента для бромирования, который более безопасен в химическом классе и значительно сокращает время реакции.
Метод Розенмунда-Кунхенна
Этот метод подходит для определения йодного числа в сопряженных системах ( ASTM D1541). Было замечено, что метод Вейса / Хануша дает ошибочные значения IV для некоторых стеринов (например, холестерина ) и других ненасыщенных компонентов неомыляемой фракции. В оригинальном методе в качестве галогенирующего агента используется раствор сульфата дибромида пиридина, а время инкубации составляет 5 мин.
Другие методы
Измерение йодного числа официальным методом занимает много времени (время инкубации 30 мин с раствором Вийса) и использует опасные реагенты и растворители. Было предложено несколько методов определения йодного числа без использования влаги. Например, IV чистых жирных кислот и ацилглицеринов теоретически можно рассчитать следующим образом:
IV знак равно 2 × 126,92 × нет. двойной облигации × 100 молекулярный масса <\ displaystyle <\ textrm
IV смесь знак равно ∑ А ж × IV ж <\ displaystyle <\ textrm 
Значение и ограничения
Пищевая химия: учебник для студентов вузов
Лабораторная работа 9. Титриметрические методы определения йодного числа
Йодное число, или так называемый коэффициент непредельности, характеризует степень ненасыщенности жира и выражается количеством йода в граммах, которое требуется для полного насыщения жирных кислот, содержащихся в 100 г жира (г I 2 /100 г жира). Это наиболее важная из констант жира. По величине этого показателя судят о преобладании в жирах насыщенных или ненасыщенных жирных кислот. Чем выше в жире содержание ненасыщенных жирных кислот, тем выше йодное число. Тугоплавкие жиры имеют низкое йодное число, легкоплавкие – высокое.
Йодное число дает возможность судить о склонности жира к различным изменениям (окислению, присоединению водорода и т. д.), происходящим при хранении и переработке пищевых жиров. Оно позволяет судить о чистоте и натуральности исследуемого жира. Кроме того, йодное число характеризует степень свежести жиров. При окислении жиров в процессе хранения йодное число снижается.
китовый жир (покровное сало)
Йодное число является показателем консистенции сливочного масла и должно учитываться при выборе температурных режимов обработки сливок в процессе их созревания и перемешивания. Этот показатель молочного жира зависит от кормовых рационов, стадии лактации, времени года, породы животного и т. д. Оно повышается летом и понижается зимой и лежит в пределах 28–45 г/100 г. Йодное число сливочного масла определяют при подозрении на наличие в нем примесей растительных масел.
Метод определения йодного числа основан на способности галогенов (йода, хлористого йода, бромистого йода) присоединяться по кратным связям. Непрореагировавший галоген оттитровывают тиосульфатом натрия в присутствии крахмала в качестве индикатора.
Кратные связи в полиненасыщенных жирных кислотах, входящих в состав жиров, насыщаются последовательно, причем время реакции присоединения возрастает по сравнению с мононенасыщенными. Насыщению галогенами в первую очередь подвержены кратные связи, наиболее удаленные от карбоксильной группы. Используя галогены, невозможно достичь полного насыщения сопряженных кратных связей. Величина йодного числа зависит:
§ от числа этиленовых связей в ненасыщенных жирных кислотах (с увеличением количества этиленовых связей в углеродной цепи жирных кислот при одном и том же числе углеродных атомов йодное число увеличивается);
§ от длины углеродной цепи в жирных кислотах (или от молекулярного веса);
§ от положения этиленовых связей в углеродной цепи (с приближением этиленовой связи к карбоксильной группе жирных кислот их йодное число уменьшается);
§ от наличия сопряженных связей (сопряженные этиленовые связи при использовании обычных методов определения йодного числа насыщаются не полностью).
Рекомендуемыми ГОСТ Р ИСО 3961–2010 «Жиры и масла животные и растительные. Определение йодного числа» являются следующие методы определения йодного числа: Гюбля (с хлорйодом), Кауфмана (с NaBr × Br 2 ), Гануса (с бромйодом). Методы Гюбеля и Гануса дают одинаковые и близкие к теоретическим результаты. Названные методы рекомендуются для исследовательских целей, идентификации жиров и контроля производства. Метод Гануса неприемлем для анализа жиров с сопряженными кратными связями. Результаты определения йодных чисел по методу Кауфмана обычно на 1–3% выше, чем по методу Гюбля.
Метод Гюбля основан на присоединении по кратным связям хлористого йода (раствор Гюбля), который образуется при взаимодействии сулемы с йодом в спиртовых растворах:
Хлористый йод практически полностью насыщает кратные связи жирнокислотных радикалов в жирах:
Избыток непрореагировавшего хлористого йода оттитровывают тиосульфатом натрия. Предварительно в реакционную среду необходимо внести йодид калия и воду для выделения эквивалентного количества йода из хлористого йода по следующей реакции:
Таблица 1.3.7. Рекомендуемая масса пробы и время настаивания
в зависимости от величины йодного числа
Значение йодного числа, г I 2 /100 г
Время настаивания, ч
от 5 до 20 включительно
свыше 20 до 50 включительно
свыше 50 до 100 включительно
свыше 100 до 150 включительно
свыше 150 до 200 включительно
По истечении вышеуказанного времени до титрования в колбу для анализа внести 20 мл 10%-го раствора йодида калия и 100 мл дистиллированной воды, смесь перемешать. Избыток выделившегося йода оттитровать 0,1 н раствором тиосульфата натрия до появления желто-соломенной окраски. В конце добавить несколько капель 1%-го раствора крахмала и продолжить титрование до перехода цвета анализируемого раствора из фиолетового в бесцветный.
Контрольный опыт проделать с тем же количеством реагентов в аналогичных условиях, но без добавления жира: 15 мл хлороформа, 25 мл раствора Гюбля. Колбу закрыть пробкой, смоченной в растворе йодида калия, и оставить в темном месте на 18–24 часа. Перед титрованием в колбу для анализа внести 20 мл 10%-го раствора йодида калия и 100 мл дистиллированной воды и оттитровать.
где V K – количество 0,1 н раствора тиосульфата натрия, израсходованного на титрование контрольного образца, мл;
V O – количество 0,1 н раствора тиосульфата натрия, израсходованного на титрование опытного образца, мл;
0, 01269 – титр 0,1 н раствора тиосульфата натрия, мг/мл;
m – масса исследуемого жира, г;
100 – коэффициент пересчета на 100 г анализируемого жира.
Метод Гануса основан на использовании бромистого йода, растворенного в безводной уксусной кислоте (реактив Гануса), который количественно присоединяется по кратным связям. Бромистый йод получают посредством смешения брома с йодом в безводной уксусной среде:
Бромистый йод присоединяется по кратным связям ненасыщенных жирных кислот.
Избыток бромистого йода после введения йодида калия и воды оттитровывают тиосульфатом натрия.
Избыток выделившегося йода оттитровать 0,1 н раствором тиосульфата натрия до появления желтой окраски. В конце титрования добавить несколько капель 1%-го раствора крахмала и продолжить титрование до перехода цвета анализируемого раствора из фиолетового в бесцветный. Контрольный опыт проделать в аналогичных условиях с тем же количеством реагентов, но без добавления жира.
Бром из соединения NaBr × Br 2 отщепляется и присоединяется к этиленовым связям жирных кислот, причем активность его недостаточна для замещения водорода:
При прибавлении к раствору Кауфмана йодистого калия выделяется эквивалентное количество йода, который оттитровывают тиосульфатом натрия.
По истечении указанного времени в колбу прилить 10–15 мл 10%-го раствора йодистого калия и 50–60 мл дистиллированной воды. Избыток выделившегося йода оттитровать 0,1 н раствором тиосульфата натрия до появления желтой окраски. В конце титрования добавить несколько капель 1%-го раствора крахмала и продолжить титрование до перехода цвета анализируемого раствора из фиолетового в бесцветный.
Контрольный опыт проделать с тем же количеством реагентов, но без добавления жира.
Метод Маргошеса является ускоренным методом определения йодного числа. Хотя он и уступает по точности вышеописанным методам, но может использоваться для анализа жиров, содержащих жирные кислоты с сопряженными кратными связями. В качестве реагента используется раствор Маргошеса, содержащий йодноватистую кислоту.
В спиртовых растворах образование из йода йодноватистой кислоты происходит в ничтожных количествах, но ускоряется в присутствии ненасыщенных связей и особенно в избытке воды. Образующаяся йодноватистая кислота взаимодействует по этиленовым связям быстрее галоидов:
Избыток непрореагировавшего йода оттитровывают тиосульфатом натрия.
Контрольный опыт проделать с теми же реактивами. К 10 мл смеси этилового спирта и хлороформа (10:1) добавить 25 мл 0,2 н раствора Маргошеса и оставить полученный раствор в темном месте. Спустя ровно 5 минут влить 200 мл дистиллированной воды и тщательно перемешать. Полученную эмульсию оттитровать 0,1 н раствором тиосульфата натрия в присутствии крахмала.
Необходимые реактивы, посуда, оборудование :
§ реактивы Гюбля, Гануса, Кауфмана, Маргошеса, 1%-ный раствор крахмала (индикатор), 0,1 н раствор йода, 0,1 н, 0,01 н растворы тиосульфата натрия, 10%-ный раствор йодида калия, диэтиловый эфир, хлороформ, спиртово-эфирная смесь (для рефрактометра);
§ колбы для титрования с пришлифованными пробками (500 мл), пипетки, бюретки, мерные цилиндры;
§ водяная баня, аналитические весы, термостат.
Раствор Маргошеса. В 1000 мл 96%-го этилового спирта растворить 25 г дважды возогнанного йода. Раствор можно использовать в течение 14 дней. К 30 дню титр раствора меняется более чем на 3%.