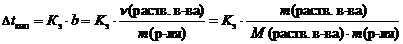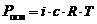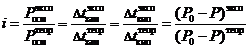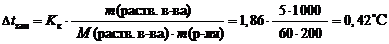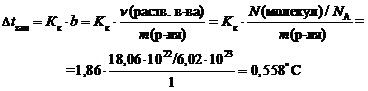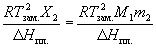Коллигативные свойства растворов
Любому раствору характерны те или иные физические свойства, к которым относятся и коллигативные свойства растворов. Это такие свойства, на которые не оказывает влияние природа растворенного вещества, а зависят они исключительно от количества частиц этого растворенного вещества.
К коллигативным свойствам растворов относятся:
Рассмотрим подробнее каждое из перечисленных свойств.
Понижение давления паров
Давление насыщенного пара (т.е. пара, который пребывает в состоянии равновесия с жидкостью) над чистым растворителем называется давлением или упругостью насыщенного пара чистого растворителя.
Если в некотором растворителе растворить нелетучее вещество, то равновесное давление паров растворителя при этом понижается, т.к. присутствие какого – либо вещества, растворенного в этом растворителе, затрудняет переход частиц растворителя в паровую фазу.
Экспериментально доказано, что такое понижение давления паров напрямую зависит от количества растворенного вещества. В 1887 г. Ф.М. Рауль описал количественные закономерности коллигативных свойств растворов.
Первый закон Рауля
Первый закон Рауля заключается в следующем:
Давление пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально мольной доле растворителя в данном растворе:
p — давление пара над раствором, Па;
p0 — давление пара над чистым растворителем, Па;
χр-ль — мольная доля растворителя.
nв-ва и nр-ля – соответственно количество растворенного вещества и растворителя, моль.
Иногда Первому закону Рауля дают другую формулировку:
относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества:
При этом принимаем, что χв-ва + χр-ль= 1
Изотонический коэффициент Вант-Гоффа
Для растворов электролитов данное уравнение приобретает несколько иной вид, в его состав входит изотонический коэффициент i:
Δp — изменение давления паров раствора по сравнению с чистым растворителем;
i – изотонический коэффициент.
Изотонический коэффициент (или фактор Вант-Гоффа) — это параметр, не имеющий размерности, который характеризует поведение какого – либо вещества в растворе.
То есть, изотонический коэффициент показывает, разницу содержания частиц в растворе электролита по сравнению с раствором неэлектролита такой же концентрации. Он тесно связан связан с процессом диссоциации, точнее, со степенью диссоциации и выражается следующим выражением:
n – количество ионов, на которые диссоциирует вещество.
α – степень диссоциации.
Повышение температуры кипения или понижение температуры затвердевания (кристаллизации). Второй закон Рауля
Равновесное давление паров жидкости имеет тенденцию к увеличению с ростом температуры, жидкость начинает кипеть, при уравнивании давления ее паров и внешнего давления.
При наличии нелетучего вещества, давление паров раствора снижается, и раствор будет закипать при более высокой температуре, по сравнению с температурой кипения чистого растворителя.
Температура замерзания жидкости также определяется той температурой, при которой давления паров жидкой и твердой фаз уравниваются.
Ф.М. Рауль доказал, что повышение температуры кипения, так же как и понижение температуры замерзания разбавленных растворов нелетучих веществ, прямо пропорционально моляльной концентрации раствора и не зависит от природы растворённого вещества. Это правило известно как Второй закон Рауля:
K — криоскопическая константа,
mв-ва — моляльность вещества в растворе.
Растворы электролитов не подчиняются Законам Рауля. Но для учёта всех несоответствий Вант-Гофф предложил ввести в приведённые уравнения поправку в виде изотонического коэффициента i, учитывающего процесс распада на ионы молекул растворённого вещества:
Осмотическое давление раствора
Некоторые материалы имеют способность к полупроницаемости, т.е. им свойственно пропускать частицы определенного вида и не пропускать частицы другого вида.
Перемещение молекул растворителя (но не растворенного, в нем вещества), через полупроницаемую мембрану в раствор с большей концентрацией из более разбавленного представляет собой такое явление как осмос.
Представим два таких раствора, которые разделены полупроницаемой мембраной, как показано на рисунке выше. Растворы стремятся к выравниванию концентраций, поэтому вода будет проникать в раствор, тем самым уменьшая его концентрацию.
Для того, чтобы осмос приостановить, необходимо приложить внешнее давление к раствору. Такое давление, которое требуется приложить, называется осмотическим давлением.
Осмотическое давление и концентрацию раствора неэлектролита позволяет связать уравнение Вант — Гоффа, которое напоминает уравнение идеального газа Клапейрона – Менделеева:
R — универсальная газовая постоянная (8,314 Дж/моль·К);
T — абсолютная температура раствора.
Преобразуем уравнение следующим образом:
C = n/V = m/(M·V)
π = т·R·T / M·V или
Для растворов электролитов осмотическое давление определяется уравнением, в которое входит изотонический коэффициент:
где i — изотонический коэффициент раствора.
Для растворов электролитов i > 1, а для растворов неэлектролитов i = 1.
Если полупроницаемой перегородкой разделены два раствора, имеющие одинаковое осмотическое давление, то перемещение растворителя через перегородку отсутствует. Такие растворы называются изотоническими.
Раствор, с меньшим осмотическим давлением, по сравнению с более концентрированным раствором, называют гипотоническим, а раствор с большей концентрацией – гипертоническим.
Что такое коллигативные свойства
Коллигативные свойства растворов
Коллигативные свойства – это свойства растворов, зависящие от числа частиц растворенного вещества. К коллигативным свойствам растворов относят:
1) понижение давления насыщенного пара растворителя над раствором,
2) понижение температуры замерзания и повышение температуры кипения растворов по сравнению с температурами замерзания и кипения чистых растворителей.
3) осмотическое давление.
1 закон Рауля. Давление насыщенного пара растворителя над раствором пропорционально мольной доле растворителя.
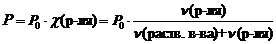
где Р – давления насыщенного пара растворителя над раствором, Па;
Р0 – давления насыщенного пара над растворителем, Па;
c (р-ля) – мольная доля растворителя;
n (раств. в-ва) – количество растворенного вещества, моль;
n (р-ля) – количество вещества растворителя, моль.
Иногда закон Рауля определяют следующим образом. Относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества.
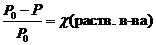
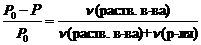
где c (раств. в-ва) – мольная доля растворенного вещества.
2 закон Рауля. Понижение температуры замерзания и повышение температуры кипения растворов по сравнению с таковыми для чистого растворителя пропорциональны моляльной концентрации растворенного вещества:
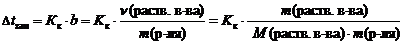
где D t кип – повышение температуры кипения раствора, ° С;
D t зам – понижение температуры замерзания раствора, ° С;
К э – эбуллиоскопическая константы растворителя, (кг ×° С)/моль;
К к – криоскопическая константы растворителя, (кг ×° С)/моль;
b – моляльная концентрация, моль/кг;
n (раств. в-ва) – количество растворенного вещества, моль;
m (р-ля) – масса растворителя, кг;
m (раств. в-ва) – масса растворенного вещества, г;
М (раств. в-ва) – молярная масса растворенного вещества, г/моль.
Зная температуры кипения и замерзания чистых растворителей и D t можно рассчитать температуры кипения и замерзания растворов:
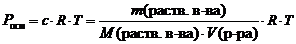
где Росм – осмотическое давление, кПа;
с – молярная концентрация растворенного вещества, моль/л;
R – универсальная газовая постоянная, 8,314 Дж/(моль × К);
Т – абсолютная температура, К;
V (р-ра) – объем раствора, л.
Осмос – односторонняя диффузия вещества через полупроницаемую мембрану.
Осмотическое давление – сила, обуславливающая осмос. Оно равно внешнему давлению, при котором осмос видимо прекращается.
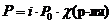
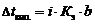
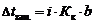
Значение изотонического коэффициента Вант-Гоффа рассчитывают как частное от деления экспериментальных и теоретических значений осмотического давления, изменения температур кипения и замерзания растворов и понижения давления растворителя над раствором:
Пример 1. Вычислите температуру кристаллизации раствора мочевины, содержащего 5 г мочевины CH 4 N 2 O в 200 г воды. Криоскопическая константа воды равна 1,86 (кг ×° С)/моль.
Пример 2. Вычислите температуру замерзания раствора, если он содержит 18,06 × 10 22 молекул неэлектролита и 1000 мл воды. Криоскопическая константа воды равна 1,86 (кг ×° С)/моль.
m ( H 2 O ) = V ( H 2 O ) × r ( H 2 O ) = 1000 мл × 1 г/мл = 1000 г = 1 кг
Пример 3. Вычислите массовую долю нафталина С10Н8 в бензольном растворе, если он кипит при температуре 81,45 ° С. Эбуллиоскопическая константа бензола равна 2,57 (кг ×° С)/моль. Температура кипения чистого бензола 80,2 ° С.
М (С10Н8) = 12 × 10 + 1 × 8 = 128 г/моль
Коллигативные
Онлайн-конференция
«Современная профориентация педагогов
и родителей, перспективы рынка труда
и особенности личности подростка»
Свидетельство и скидка на обучение каждому участнику
Описание презентации по отдельным слайдам:
Описание слайда:
Лектор: доцент, к.х.н., Иваненко О.И.
Пермская медицинская академия
Описание слайда:
Коллигативные свойства растворов – это свойства, которые зависят от числа частиц растворенного в веществе и не зависят от его природы:
Понижение давления насыщенного пара (ДНП) над раствором
2. Понижение температуры замерзания раствора (ΔТз) и повышение температуры кипения раствора (ΔТк)
3. Осмотическое давление (π).
Описание слайда:
Понижение давления насыщенного пара (ДНП)
над раствором. I закон Рауля
p0
Н2О
Описание слайда:
↑t ↑p0
H2O:
00C – 4,6 мм рт. ст.
200C – 17,4 мм рт. ст.
1000C – 760 мм рт. ст.
p0= pатм. жидкость закипает
Понижение давления насыщенного пара (ДНП)
над раствором. I закон Рауля
Описание слайда:
Понижение давления насыщенного пара (ДНП)
над раствором. I закон Рауля
p0
p
>
Н2О
раствор
Описание слайда:
Понижение давления насыщенного пара (ДНП)
над раствором. I закон Рауля
Описание слайда:
ΔТзамерзания = Тзамерзания р-ля – Тзамерзания р-ра = ΔТз
ΔТкипения = Ткипения р-ра – Ткипения р-ля = ΔТк
Повышение температуры кипения (ΔТк) и понижение температуры замерзания (ΔТз) разбавленных растворов неэлектролитов прямо пропорционально моляльной концентрации раствора.
ΔТк = Кэ·Сm; ΔТз = Кз·Сm;
Описание слайда:
II закон Рауля
Чем больше концентрация растворенного вещества, тем выше Тк и ниже Тз раствора.
ΔТк = Кэ·Сm; ΔТз = Кз·Сm;
Сm – моляльная концентрация – количество растворенного
вещества в 1 кг растворителя (моль/кг):
m вещ-ва
Cm = ————————
M · m раств-ля (кг)
Кэ – эбулиометрическая const;
Кз (КК) – криометрическая const;
Эти константы зависят от природы растворителя.
При Cm = 1 моль/кг; Кз = ΔТз; Кэ = ΔТк.
КзН2О = 1,86 кг·К/моль; КэН2О = 0,52 кг·К/моль;
Описание слайда:
Криометрия –метод определения молярной массы вещества (М) по температуре замерзания:
Кз · m вещ-ва
М вещ-ва = —————— (г/моль)
ΔТз·m раств-ля (кг)
Описание слайда:
Осмос. Осмотическое давление
Осмос – это односторонняя диффузия воды через полупроницаемою
мембрану из растворителя в раствор или из раствора с меньшей концентрацией в раствор с большей концентрацией.
Вода из сосуда переходит через
полупроницаемую мембрану (целлофан,
оболочка мочевого пузыря) в сосуд
h с более концентрированным раствором.
Уровень жидкости в этом сосуде поднимается
на высоту h.
Описание слайда:
Описание слайда:
Значение осмоса
упругость, тургор клеток
эластичность тканей, форма органов
усвоение пищи, образование лимфы, мочи, кала
За счет осмоса вода в организме распределяется между кровью, тканями, клетками.
Описание слайда:
Осмотическое давление крови
Состав плазмы крови: 90 % Н2О, 7 % белков, 0,9 % эл-отв (> NaCl), ≈
2 % (лип., а/к, глюкозы, органических кислот).
π = π НМС + π ВМС
(эл. + неэл.) (белки)
ΔТз·R·T
По ΔТз крови =0,56 Сº определяют π плазмы = ———— = Кз
0,56·0,083·(273+37º)
= ————————— = 7,65 атм
1,86
π пл вмс (белки) = 0,04 – 0,03 атм
π плазмы = π НМС + π ВМС = 7,65 + 0,03(0,04) ≈ 7,7 – 8,1 атм
Описание слайда:
Осмотическое давление, которое зависит от белков называется онкотическим (0,03 – 0,04 атм.). При длительном голодании, болезни почек концентрация белков в крови уменьшается, онкотическое давление в крови снижается и возникают онкотические отеки: вода переходит из сосудов в ткани, где πОНК больше. При гнойных процессах πОНК возрастает в 2–3 раза в очаге воспаления, так как увеличивается число частиц из-за разрушения белков.
В организме осмотическое давление должно быть постоянным (≈ 7,7 атм.). При болезнях больным вводят изотонические растворы.
Это растворы, осмотическое давление которых равно π ПЛАЗМЫ ≈ 7,7 атм. (0,9 % NaCl – физиологический раствор, 5 % раствор глюкозы). Растворы, у которых π больше, чем у π ПЛАЗМЫ, называются гипертоническими. В медицине они применяются для очистки ран от гноя (10 % NaCl), для удаления аллергических оттенков (10 % CaCl2, 20 % – глюкоза), в качестве слабительных лекарств (Na2SO4∙10H2O, MgSO4∙7H2O).
Описание слайда:
Описание слайда:
Плазмолиз – явление сжатия, высушивания клеток в гипертоническом растворе. Идет осмос воды из клетки в раствор, где π больше. Растворы, у которых π больше, чем у π ПЛАЗМЫ, называются гипертоническими.
Гемолиз – явление набухания и разрыва клеток
эритроцитов в гипотоническом растворе. Идет осмос
воды в клетки. Клетка набухает, оболочка разрывается.
Растворы, у которых π меньше, чем у π ПЛАЗМЫ, называются гипотоническими.
Описание слайда:
Коллигативные свойства растворов электролитов
В растворах электролитов число частиц больше из-за диссоциации.
Вант-Гофф дал поправочный изотонический коэффициент i,
который учитывает диссоциацию электролитов.
i = 1+ α (n – 1)
/ \
степень число частиц
диссоциации из 1 молекулы
На практике i определяют по ΔТз, ΔТк, π.
ΔТз пр ΔТк пр π пр
i = ———— = ————— = —————
ΔТз теор ΔТк теор π теор
С учетом i формулы для определения коллигативных свойств имеют вид:
РО – Р
——— = i · N(x2); ΔТз = i · Кз· Сm; ΔТк = i · Кэ · Cm; π = i · R · C(x)
РО
Описание слайда:
Для сильных электролитов (α≈1):
α=(i-1)/(n-1)
NaCl ↔ Na+ + Cl-
2 иона => n=2, i=2 при α=1
CaCl2 ↔ Ca2+ + 2Cl-
3 иона => n=3, i=3 при α=1
Описание слайда:
Спасибо за внимание.
1ое занятие 2го семестра посвящено данной теме!
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Что такое коллигативные свойства
Свойства разбавленных растворов, зависящие только от количества нелетучего растворенного вещества, называются коллигативными свойствами. К ним относятся понижение давление пара растворителя над раствором, повышение температуры кипения и понижение температуры замерзания раствора, а также осмотическое давление.
Понижение температуры замерзания и повышение температуры кипения раствора по сравнению с чистым растворителем:
где X2 – мольная доля растворенного вещества, 
где C – молярность раствора.
Уравнения, описывающие коллигативные свойства неэлектролитов, можно применить и для описания свойств растворов электролитов, введя поправочный коэффициент Вант-Гоффа i, например:
Растворимость твердого вещества в идеальном растворе при температуре T описывается уравнением Шредера:
ПРИМЕРЫ
Решение. Воспользуемся формулой 
При 150 o C 
При 200 o C 
Растворимость увеличивается с температурой, что характерно для эндотермического процесса.
ЗАДАЧИ
Рассчитать молярную массу фермента.


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
Что такое коллигативные свойства
Свойства разбавленных растворов, зависящие только от количества нелетучего растворенного вещества, называются коллигативными свойствами. К ним относятся понижение давление пара растворителя над раствором, повышение температуры кипения и понижение температуры замерзания раствора, а также осмотическое давление.
Понижение температуры замерзания и повышение температуры кипения раствора по сравнению с чистым растворителем:
где X2 – мольная доля растворенного вещества, 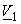
где C – молярность раствора.
Уравнения, описывающие коллигативные свойства неэлектролитов, можно применить и для описания свойств растворов электролитов, введя поправочный коэффициент Вант-Гоффа i, например:
Растворимость твердого вещества в идеальном растворе при температуре T описывается уравнением Шредера:
ПРИМЕРЫ
Решение. Воспользуемся формулой 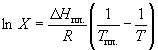
При 150 o C 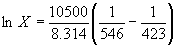
При 200 o C 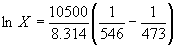
Растворимость увеличивается с температурой, что характерно для эндотермического процесса.
ЗАДАЧИ
Рассчитать молярную массу фермента.


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору