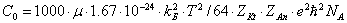Активность и коэффициент активности
Несмотря на то, что термодинамика не учитывает процессы, происходящие в реальных растворах, например, притяжение и отталкивание ионов, термодинамические закономерности, выведенные для идеальных растворов, можно применить и для реальных растворов, если заменить концентрации активностями.
Активность может быть как меньше, так и больше номинальной концентрации вещества в растворе. Активность чистого растворителя, а также растворителя в не слишком концентрированных растворах принимается равной 1. За 1 принимается также активность твёрдого вещества, находящегося в осадке, или жидкости, не смешивающейся с данным раствором. В бесконечно разбавленном растворе активность растворённого вещества совпадает с его концентрацией.
Отношение активности вещества в данном растворе к его концентрации называется коэффициентом активности.
Отклонения от идеальности в растворах сильных электролитов
Особенно заметное отклонение от идеальности имеет место в растворах сильных электролитов. Это отражается, например, на их температурах кипения, плавления, давлении пара над раствором и, что особенно важно для аналитической химии, на величинах констант различных равновесий, протекающих в таких растворах.
Для характеристики активности электролитов используют:
Величина, которая учитывает влияние концентрации (С) и заряда (z) всех ионов, присутствующих в растворе, на активность растворённого вещества, называется ионной силой (I).
Пример 3.1. В 1,00 л водного раствора содержится 10,3 г NaBr, 14,2 г Na2SO4 и 1,7 г NH3. Чему равна ионная сила такого раствора?


I = 0,5×[0,300×(+1) 2 + 0,100×(-1) 2 + 0,100×(-2) 2 ] = 0,400 моль/л
Рис. 3.1. Влияние ионной силы на среднеионный коэффициент активности HCl
На рис. 3.1 показан пример влияния ионной силы на активность электролита (HCl). Аналогичная зависимость коэффициента активности от ионной силы наблюдается также у HClO4, LiCl, AlCl3 и многих других соединений. У некоторых электролитов (NH4NO3, AgNO3) зависимость коэффициента активности от ионной силы является монотонно убывающей.
Универсального уравнения, с помощью которого можно было бы рассчитать коэффициент активности любого электролита при любой величине ионной силы, не существует. Для описания зависимости коэффициента активности от ионной силы в очень разбавленных растворах (до I
При более высоких значениях ионной силы (до
1) количественную оценку коэффициента активности можно проводить по уравнению Дэвиса.
В данном уравнении a принято равным 3,05, поэтому произведение Ba равно 1. Фактор 0,2I учитывает образование ионных пар, изменение диэлектрической проницаемости и т.д.
Пример 3.2. Рассчитать коэффициенты активности иона H + при ионной силе 0,010 и 0,10.


3.4. Виды констант химического равновесия, используемые в аналитической химии
Научная электронная библиотека
1.3.4. Коэффициенты активности
Электростатические взаимодействия приводят к значительным отклонениям в поведении системы от идеального. Учесть отклонения от идеального, т.е. предусмотреть влияние электростатических факторов можно с помощью метода активностей: вместо концентраций реагирующих частиц [A] используют величины, называемые активностями aA. Численные значения активностей выбирают таким образом, чтобы форма функциональной зависимости для свободной энергии
сохранялась и для реальных растворов:
Тогда для общей реакции
Отношение активности частицы к ее равновесной концентрации
называется коэффициентом активности. Коэффициенты активности ионов в растворах электролитов могут служить мерой электростатических взаимодействий в системе. Для идеальных растворов электростатические взаимодействия пренебрежимо малы, активности приравниваются равновесным концентрациям, тогда g = 1.
Известно несколько методов определения и расчета коэффициентов активности. Поскольку электростатические взаимодействия весьма заметны в растворах электролитов, то остановимся на расчетах коэффициентов активности ионов. Они зависят от ионной силы, вычисляемой по известному уравнению:
Одним из наиболее применяемых методов определения коэффициентов активности индивидуальных ионов является оценка по приближению Дебая-Хюккеля [8]
В разбавленных растворах (I 2 (I) 1/2 /[1+aB(I) 1/2 ]+ CI,
Экспериментально определить коэффициенты активности отдельных ионов невозможно, так как нельзя получить раствор, содержащий ионы только одного сорта. Опытным путем можно было измерить лишь средний коэффициент активности g± ионов электролита AmBn, который связан с коэффициентами активности составляющих его ионов A n+ и B m- следующим образом:
Уравнения Дебая-Хюккеля и Дэвиса пригодны в первом приближении и для расчетов коэффициентов активности незаряженных молекул (неэлектролитов). В этих случаях zi = 0 и в уравнениях Дебая-Хюккеля коэффициент активности неэлектролита равен единице при ионной силе I £ 0.1 М, при больших значениях ионной силы необходимо использовать уравнение Дэвиса, которое для неэлектролитов превращается в lgg = CI. Константа С в этом случае называется солевым коэффициентом, зависящим от диэлектрической проницаемости неэлектролита e. Для веществ с низкойe (газы, сахара, белки) C>0, g > 1. Для таких веществ наблюдается эффект “высаливания”, т.е. уменьшение их растворимости в воде в присутствии электролитов. Для веществ же с высокой e(например, для HCN e = 111) C 2 ћ 2 CiNA/m·1000· kБ 2 T 2 ) 1/2 ] (1.23)
В данной работе предложено модельное уравнение расчета оптимальных концентраций электролитов, соответствующих минимуму коэффициента активности и рассуждения 16.
Показано, что в точке минимума функции
а затем − к выражению (4):
Уравнения (1.23) и (1.24) выражают коэффициент активности для неассоциированных ионов электролита, тогда как литературные (экспериментальные) величины g± учитывают в этой точке фактические (реальные) взаимодействия сольватированных ионов с образованием молекулярной формы электролита или ионных ассоциатов по равновесию (а). Поэтому не следует ожидать полного тождества коэффициентов активности, теоретически оцененных по уравнению (1.24), с литературными, но, безусловно, важен характер зависимости коэффициентов активности от концентраций.
В табл.1.3 приведены полученные концентрации для 42 электролитов при gmin.
Что касается увеличения коэффициента активности g при больших концентрациях электролита, то не было предложено рациональной количественной теории, определяющей концентрации растворов с минимумом g и значительным увеличением его с повышением моляльности. В данной работе дается объяснение этому факту и рассчитаны оптимальные концентрации электролитов, соответствующие минимуму коэффициента активности. Так, за пределами концентрации С0, соответствующей минимуму коэффициента активности, в связи с сокращением длин свободного пробега сольватированных ионов или молекул, превалирующими становятся межионные взаимодействия, приводящие преимущественно к ионным ассоциатам в полярных с низкими значениями диэлектрических проницаемостей растворителях или к молекулярным сольватам в неполярных с низкими значениями диэлектрических проницаемостей растворителях.
Уравнение (1.24) позволяет рассчитывать теоретические значения коэффициентов активности различных электролитов в зависимости от их концентраций. Функция проходит через минимум при С0, повторяя контур зависимости фактических (реальных) g± от моляльности растворов (рис. 1.1 и 1.2).
Рис. 1.1. Зависимости рассчитанных (1) и экспериментальных (2) коэффициентов активности от моляльной концентрации водного раствора хлороводородной кислоты
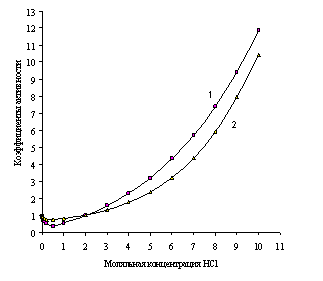
Рис. 1.2. Зависимости рассчитанных (1) и экспериментальных (2) коэффициентов активности от моляльной концентрации водного раствора хлорида лития
На рис. 1.1 и 1.2 показана приемлемость предлагаемой модельной оценки коэффициента активности в связи с достаточно заметным соответствием хода зависимости функций g = f (m) и g± = f (m) для водных растворов хлороводородной кислоты (рис. 1.1) и хлорида лития (рис. 1.2).
В табл. 1.4 в качестве примера представлены экспериментальные (литературные) и рассчитанные по уравнению (1.24) величины коэффициентов активности хлороводородной кислоты и хлорида лития.
Таким образом, в данной работе теоретически обосновываются области концентраций растворов электролитов, в которых наблюдается минимум коэффициентов активности, объясняется феномен доминирования ассоциативных явлений, приводящих к образованию ионных ассоциатов или в зависимости от свойств и природы растворителя − к преимущественному состоянию растворов в виде молекулярных сольватов.
Коэффициенты активности HCl и LiCl, оцененные по уравнению (1.24), в сравнении с экспериментальными в зависимости от концентрации С (моль/1000 г)
Коэффициент физической активности: что это такое и как его рассчитать? Шаблоны и подсказки
Эта статья поможет рассчитать личный коэффициент физической активности.
Коэффициент физической активности (PAL или КФА) определяет уровень активности человека. Чтобы похудеть, необходимо оценить нашу потребность в энергии и, таким образом, сформировать правильный план питания и тренировок. Читайте в другой статье на нашем сайте, как при помощи питания можно сформировать спортивную фигуру. Как рассчитать коэффициент PAL? Какова взаимосвязь между общей и основной скоростью метаболизма и скоростью физической активности? Ответы на эти вопросы ищите ниже.
КФА — коэффициент физической активности человека: что это такое и зачем нужно знать формулу?
Как говорилось выше, коэффициент физической активности человека — это уровень затрат энергии. Сознательная потеря веса и коррекция фигуры всегда приносят лучшие результаты. Вот почему стоит изучить некоторые базовые понятия в области диетологии. На первый взгляд они могут показаться сложными, но освоение новой информации всегда интересное, и когда вы начнете вникать в расчеты, то все будет намного проще. В этой статье будет использоваться как русская, так и английская аббревиатура слов, так как многие люди используют для получения знаний и иностранную литературу. Итак, КФА или PAL — коэффициент физической активности человека: зачем нужно знать формулу?
Также стоит выяснить, из чего состоит расход энергии. Это прежде всего влияние пищи и физической активности, а также обмена веществ. Обычно определение потребности в энергии начинается с определения PPM или Basic Metabolic (основного метаболизма). Это самый низкий уровень, напрямую связанный с энергией. Читайте далее.
Какие существуют уровни, коэффициенты физической активности человека: объяснение
Коэффициент PAL или КФА позволяет определять уровень физической активности конкретного человека. Это необходимо для расчета подробных затрат энергии. Чем точнее мы определим значение описанного фактора, тем более надежным будет результат CPM (Total Metabolic) или общего метаболизма. Это позволит определить, сколько калорий в день мы должны потреблять и сжигать. Вот объяснение, какие существуют уровни, коэффициенты физической активности человека:
Следует помнить: Каждый день фактор физической активности может иметь различное значение. Это потому, что мы делаем разные работы каждый день. Следовательно, нельзя сказать, что ежедневные затраты энергии всегда одинаковы.
Вот почему многие люди рассчитывают среднее значение за всю неделю. Это оптимальное решение.
С чего начать: как рассчитать коэффициент физической активности?
Мы не будем рассчитывать потребность в энергии без ключевых параметров — это будет неправильно. Начните с расчета PPM (основной уровень метаболизма), CPM (общий уровень метаболизма) и PAL (уровень физической активности).
Существуют различные варианты расчета. Но следует помнить, что некоторые из них в основном предназначены для опытных диетологов, которые имеют специальные знания. Если мы сами делаем расчет, тогда следует использовать более простые формулы.
Стоит отметить: Если вы будете знать соотношения своего коэффициента физической активности, то такой показатель поможет гораздо более эффективно подобрать правильную диету или спортивное питание.
Это особенно важно не только для спортсменов, которые хотят улучшить свои спортивные результаты, но и для тех, кто худеет и имеет избыточный вес. Подробнее читайте далее.
Основной метаболизм (PPM): показатель для формулы для расчета коэффициента физической активности
Основной метаболизм (PPM) — самый низкий уровень энергетического обмена. Этот фактор определяет, сколько энергии организм использует при выполнении основных физиологических действий: сердцебиение, дыхание, пищеварение, регенерация тканей и т.д.
При расчете PPM обычно используется формула Харриса-Бенедикта. Плюсом является то, что этот показатель можно рассчитать при помощи готового калькулятора, который значительно ускоряет и облегчает оформление счетов. Однако хорошо уметь рассчитывать этот параметр самостоятельно, чтобы вы могли понять, из чего он состоит.
Формула для PPM для женщин:
Формула для PPM для мужчин:
Используя приведенные выше формулы, можно рассчитать среднее значение основного обмена. Конечно, профессионалы индивидуализируют формулу так, чтобы риск нарушений был на самом низком уровне.
Общая скорость метаболизма (CPM): показатель для формулы для расчета коэффициента физической активности
Общая скорость метаболизма (СРМ) — это общая потребность организма в энергии. Это означает, что этот фактор определяет количество энергии, необходимое, когда тело остается в пассивном состоянии. Этот показатель также необходим для формулы для расчета коэффициента физической активности.
СРМ состоит из основного и вторичного обмена веществ. Во втором случае имеется в виду, что человек проводит какие-либо действия в течение дня. К примеру, физические и умственные усилия.
Формула для CPM:
Как рассчитать коэффициент k(PAL), описано ниже. Читайте далее.
Коэффициент физической активности (PAL): шаблон, подсказки в таблице
Коэффициент физической активности PAL можно рассчитать в общем или подробно. Нужно учитывать, что чем точнее вы это сделаете, тем лучше. Казалось бы, все, что вам нужно сделать, это выбрать правильное значение из готовых таблиц. Все зависит от того, какая точность необходима.
Значение коэффициента физической активности (k) для формулы вы найдете в виде подсказок в таблице ниже — шаблон расчетов:
| № | Коэффициент, k | Когда используется |
| 1 | 1,2 — 1,39 | В случае неподвижности, например, постельный режим из-за болезни |
| 2 | 1,4-1,69 | При низкой физической активности, например, сидячий образ жизни в сочетании с кратковременными походами, ездой на велосипеде, упражнениями |
| 3 | 1,7-1,99 | Для умеренной физической активности, например, физической/сидячей работы в сочетании с легкими регулярными тренировками |
| 4 | 2,0-2,4 | Активный образ жизни, который учитывает очень тяжелую физическую работу или силовую тренировку |
| 5 | свыше 2,4 | Профессиональный спорт |
Вышеуказанные значения облегчают расчет PAL. Однако показатели получатся не очень точными. Если это не устраивает, то нужно рассчитать расход энергии тела. Это требует определения количества энергии, необходимой для выполнения заданных действий, например, работы, ходьбы, тренировок. Стоит знать:
Основные затраты энергии рассчитываются по формуле PPM. Затем мы суммируем количество энергии, необходимое для повседневной физической активности. Таким образом, мы можем рассчитать CPM:
Теперь можно перейти к расчету точного коэффициента физической активности (PAL). Используйте такую формулу:
Важно: Расход энергии меняется у человека практически каждый день. Ведь мы ходим на работу или тренировки, но не каждый день. Поэтому стоит рассчитать CPM для каждого дня. Затем нужно сложить полученные значения и разделить на семь дней в неделю.
Благодаря этому вы получите среднесуточный общий уровень метаболизма, который будете использовать при расчетах. Это уменьшает риск того, что результат будет неточным.
Почему необходимо знать свой КФА — коэффициент физической активности?
В наше время все больше людей ленятся быть физически активными. У многих из них появляются большие проблемы с лишним весом или ожирением. Никого не удивит тот факт, что лишние килограммы — это настоящий бич нашего времени. Коэффициент физической активности — КФА поможет вам определить, поддерживаете ли вы оптимальный уровень физической активности. Вот почему необходимо рассчитывать этот показатель для себя.
Избыточный вес и недостаток физических упражнений являются огромным бременем для нашего организма. Это простой способ получить много серьезных патологий. Чем быстрее вы внесете изменения, тем ниже риск развития негативных изменений в организме.
Что следует запомнить: средний коэффициент физической активности — это соотношение затрат энергии к затратам организма в состоянии покоя
Казалось бы, люди, бегающие несколько раз в неделю или путешествующие на велосипеде, считаются физически активными. Но это неправильное суждение. Это все еще умеренный уровень активности. Но в этом случае, потребность в энергии выше, чем у людей, которые ведут малоподвижный образ жизни или путешествуют в основном на машине. Что следует запомнить? Вот главное правило:
Это указывает на то, что многие люди могут сопоставить спрос на энергию с другими людьми, профессионально занимающимися спортом. Как это происходит? К примеру, те, кто много работает физически (например, на стройке, на сельскохозяйственном поле), а также регулярно (5-6 раз в неделю) занимаются фитнесом или другими видом любительского спорта.
Запомните: Показатель затрат энергии CPM меняется с возрастом или состоянием здоровья.
Кроме этого стоит учитывать, что и каждая тренировка в спортзале отличается. Поэтому нельзя наверняка знать, сколько энергии наш организм будет использовать во время той или иной работы.
Важно: Внимательно выполняйте расчет затрат энергии. Известно, что у людей, занимающихся экстремальными видами спорта, больше потребностей, чем у тех, кто сжигает калории на беговой дорожке или катается на велосипеде в течение часа.
Видео: Формулы расчета основного обмена и суточного калоража. Простая альтернатива сложным расчетам
Коэффициент активности
СОДЕРЖАНИЕ
Термодинамическое определение [ править ]
μ B знак равно μ B ⊖ + р Т пер Икс B <\ displaystyle \ mu _ <\ mathrm > = \ mu _ <\ mathrm > ^ <\ ominus>+ RT \ ln x _ <\ mathrm > \,>
Это обобщается, чтобы включить неидеальное поведение, написав
μ B знак равно μ B ⊖ + р Т пер а B <\ displaystyle \ mu _ <\ mathrm > = \ mu _ <\ mathrm > ^ <\ ominus>+ RT \ ln a _ <\ mathrm > \,>
когда В это активность вещества в смеси с
а B знак равно Икс B γ B <\ displaystyle a _ <\ mathrm > = x _ <\ mathrm > \ gamma _ <\ mathrm >>
Подробно: закон Рауля гласит, что парциальное давление компонента B связано с его давлением пара (давлением насыщения) и его мольной долей x B в жидкой фазе,
Другими словами: соединение показывает неидеальное поведение в разбавленном случае.
Приведенное выше определение коэффициента активности нецелесообразно, если соединение не существует в виде чистой жидкости. Это часто бывает с электролитами или биохимическими соединениями. В таких случаях используется другое определение, в котором бесконечное разбавление рассматривается как идеальное состояние:
Здесь символ используется для различения двух видов коэффициентов активности. Обычно его опускают, так как из контекста ясно, какой вид имеется в виду. Но есть случаи, когда требуются оба вида коэффициентов активности, которые могут даже входить в одно и то же уравнение, например, для растворов солей в смесях (вода + спирт). Иногда это является источником ошибок. † <\displaystyle ^<\dagger >>
Изменение мольных долей или концентраций с помощью коэффициентов активности дает эффективные активности компонентов и, следовательно, позволяет применять такие выражения, как закон Рауля и константы равновесия, как к идеальным, так и к неидеальным смесям.
Ионные растворы [ править ]
Для электролита 1: 1, такого как NaCl, он определяется следующим образом:
где γ + и γ — коэффициенты активности катиона и аниона соответственно.
В более общем смысле, средний коэффициент активности соединения формулы A p B q определяется как [4]
γ ± = γ A p γ B q p + q <\displaystyle \gamma _<\pm >=<\sqrt[
\gamma _ <\mathrm >^>>>
Преобладающее мнение о том, что коэффициенты активности отдельных ионов невозможно измерить независимо или, возможно, даже физически бессмысленно, уходит своими корнями в работы Гуггенхайма в конце 1920-х годов. [5] Однако химики никогда не могли отказаться от идеи активности одного иона и, как следствие, коэффициентов активности одного иона. Например, pH определяется как отрицательный логарифм активности ионов водорода. Если преобладающая точка зрения на физический смысл и измеримость активности одного иона верна, то определение pH как отрицательного логарифма активности ионов водорода помещает эту величину в категорию неизмеримых. Признавая эту логическую трудность, Международный союз теоретической и прикладной химии(IUPAC) утверждает, что определение pH на основе активности является только условным определением. [6] Несмотря на преобладающее отрицательное мнение об измеримости одноионных коэффициентов, концепция активности отдельных ионов продолжает обсуждаться в литературе, и, по крайней мере, один автор представляет определение активности одного иона в терминах чисто термодинамических величин и предлагает метод измерения коэффициентов активности одиночных ионов, основанный на чисто термодинамических процессах. [7]
Концентрированные ионные растворы [ править ]
Для концентрированных ионных растворов необходимо учитывать гидратацию ионов, как это было сделано Стоксом и Робинсоном в их модели гидратации от 1948 года. [8] Коэффициент активности электролита разделен на электрические и статистические компоненты Э. Глюкауфом, который модифицирует Модель Робинсона – Стокса.
Статистическая часть коэффициента активности концентрированного раствора составляет:
ln γ s = h − ν ν ln ( 1 + b r 55.5 ) − h ν ln ( 1 − b r 55.5 ) + b r ( r + h − ν ) 55.5 ( 1 + b r 55.5 ) <\displaystyle \ln \gamma _=<\frac
<55.5>>\right)-<\frac
<55.5>>\right)+<\frac
<55.5>>\right)>>> 
Модель Стокса – Робинсона анализировалась и улучшалась также другими исследователями. [12] [13]
Экспериментальное определение коэффициентов активности [ править ]
Радиохимические методы [ править ]
Коэффициенты активности можно определить радиохимическими методами. [14]
При бесконечном разбавлении [ править ]
Коэффициенты активности для бинарных смесей часто указываются при бесконечном разбавлении каждого компонента. Поскольку модели коэффициента активности упрощаются при бесконечном разбавлении, такие эмпирические значения могут использоваться для оценки энергий взаимодействия. Приведены примеры для воды:
| Икс | γ x ∞ (К) | γ W ∞ (К) |
|---|---|---|
| Этанол | 4,3800 (283,15) | 3,2800 (298,15) |
| Ацетон | 6,0200 (307,85) |
Теоретический расчет коэффициентов активности [ править ]
Для незаряженных видов коэффициент активности γ 0 в основном соответствует модели высаливания : [24]
log 10 ( γ 0 ) = b I <\displaystyle \log _<10>(\gamma _<0>)=bI>
Для воды в качестве растворителя активность a w можно рассчитать по формуле [24]
Ссылка на ионный диаметр [ править ]
log ( γ i ) = − A z i 2 I 1 + B a I <\displaystyle \log(\gamma _)=-<\frac
Зависимость от параметров состояния [ править ]
Производная коэффициента активности по температуре связана с избыточной молярной энтальпией соотношением
H ¯ i E = − R T 2 ∂ ∂ T ln ( γ i ) <\displaystyle <\bar
Точно так же производная коэффициента активности по давлению может быть связана с избыточным молярным объемом.
V ¯ i E = R T ∂ ∂ P ln ( γ i ) <\displaystyle <\bar
Приложение к химическому равновесию [ править ]
В состоянии равновесия сумма химических потенциалов реагентов равна сумме химических потенциалов продуктов. Изменение свободной энергии Гиббса для реакций Δ r G равно разности этих сумм и, следовательно, в состоянии равновесия равно нулю. Таким образом, для такого равновесия, как
Подставьте в выражения для химического потенциала каждого реагента:
После перестановки это выражение становится
Δ r G ⊖ = − R T ln K <\displaystyle \Delta _
Этот вывод служит двум целям. Он показывает взаимосвязь между стандартным изменением свободной энергии и константой равновесия. Это также показывает, что константа равновесия определяется как отношение активности. На практике это неудобно. Когда каждое действие заменяется произведением концентрации на коэффициент активности, константа равновесия определяется как
где [S] обозначает концентрацию S и т. д. На практике константы равновесия определяются в среде таким образом, чтобы коэффициент коэффициента активности был постоянным и им можно было пренебречь, что приводит к обычному выражению
который применяется при условиях, когда коэффициент активности имеет определенное (постоянное) значение.