Химический состав воды
Основные (преобладающие) компоненты
Под влиянием климатических и других условий химический состав природных вод изменяется и приобретает характерные черты, иногда специфические для различных видов природных вод (атмосферные осадки, реки, озера, подземные воды).
Не поддаются даже приблизительной оценке громадные количества солевых частиц, поднимаемых с почв, соленых озер, поверхности льда, удобрений и, наконец, выбрасываемых химическими и металлургическими производствами, и выбрасываемые в атмосферу в результате другой деятельность людей, а в дальнейшем вымываемые осадками.
Реки с водой, относящейся к сульфатному классу, сравнительно малочисленны. Они распространены преимущественно в степной полосе и частично в полупустынях. В составе катионов природных вод сульфатного класса, так же как и в водах гидрокарбонатного класса, преобладает кальций. Однако ряд рек сульфатного класса имеет преобладание натрия. По минерализации воды сульфатного класса значительно превосходят воды гидрокарбонатного класса. Речные сульфатные воды с малой (общее количество солей до 200 мг/л) и средней (общее количество солей с 200 до 500 мг/л) минерализацией встречаются сравнительно редко. Наиболее характерна для этих рек повышенная (общее количество солей с 500 до 1000 мг/л), а иногда и высокая (общее количество солей более 1000 мг/л) минерализация воды.
Приведенная характеристика ионного состава речной воды относится к периоду летней межени. До некоторой степени она характеризует состав и в период ледостава. Существенно иная, значительно меньшая минерализация воды наблюдается в период весеннего половодья.

Чем более изолированно море от океана, тем заметнее отличается состав его воды от состава воды в океане. Первостепенное значение имеют условия водообмена с океаном, соотношение объема материкового стока с объемом моря, глубина моря и характер химического состава вод впадающих рек.
Подземные воды отличаются исключительным разнообразием химического состава, в том числе и ионного. Состав воды бывает всех классов, групп и типов. Ионный состав подземных вод прежде всего зависит от условий их формирования и залегания.
Стабилизация pH природной воды
Гидрокарбонат-ионы нейтрализуют кислоты, попадающие в водоём с атмосферными осадками или образующиеся в результате жизнедеятельности организмов. С концентрацией гидрокарбонат-ионов напрямую связана устойчивость водоёмов к кислотным дождям. Наиболее чувствительны к ним реки и озёра Карелии, Финляндии, Скандинавии, в водах которых этих ионов практически нет.
Органические вещества
Общая концентрация органического вещества в природных водах, изменяясь в широких пределах, бывает наибольшей в болотных водах (в которых при большой концентрации гумусовых веществ она иногда достигает 500 мг/л и более) и реках с болотным питанием, причем болотная вода бывает окрашенной в желтый и коричневый цвет до 300° и выше по платиново-кобальтовой шкале цветности (окраску природной воде придают гуминовые кислоты). Высокая концентрация органического вещества иногда встречается в подземных водах, связанных с нефтеносными месторождениями. Еще большая концентрация может быть в природных водах, загрязненных промышленными и хозяйственно-бытовыми сточными водами. Незагрязненные природные воды обычно содержат мало органических веществ. Например, по Б.А. Скопинцеву, в воде океанов концентрация органического вещества составляет только 2,0-5,4 мг/л (в среднем 3,0 мг/л, а в воде рек в среднем 20 мг/л).
В некоторых поверхностных водах, особенно в реках с болотным питанием, вещества гумусового происхождения являются основной частью химического состава воды. После поступления в хорошо аэрируемые реки, а затем озера и моря органические вещества воды подвергаются изменению, и начатый в почвах процесс окисления завершается для большей их части переходом в простые минеральные соединения. Другая, более устойчивая часть остается и накапливается в водных объектах.
В холодных климатических зонах (тундре) очень мало органических остатков, и там водоёмы почти не содержат гуминовых кислот. А в зоне лесов, особенно хвойных, где органических остатков образуется много и они не успевают полностью разложиться, содержание гуминоных кислот составляет несколько десятков миллиграммов на литр. Гуминовые кислоты не только подкисляют воду в водоёме, но ещё и связывают практически все тяжёлые металлы в прочные комплексные соединения.
Газы в природной воде
Кислород (O2) находится в природной воде в виде растворенных молекул. Кислород, являясь мощным окислителем, играет особую роль в формировании химического состава природных вод. Кислород поступает в воду в результате происходящих в природе процессов фотосинтеза и из атмосферы. Расходуется кислород на окисление органических веществ, а также в процессе дыхания организмов. Концентрация растворенного кислорода в природных водах колеблется в ограниченных пределах (от 0 до 14 мг/л, при интенсивном фотосинтезе, в полдень, возможна и более высокая концентрация). Вследствие зависимости концентрации кислорода в поверхностных водах от целого ряда факторов его концентрация значительно меняется в течение суток, сезона и года. Так как потребление кислорода сравнительно мало зависит от суточных изменений солнечной радиации, а фотосинтез всецело определяется ею, то в течение дня происходит накопление кислорода, а в темное время суток расходование его. Кислород необходим для существования большинства организмов, населяющих водоемы. Как сильный окислитель кислород играет важную санитарно-гигиеническую роль, способствуя быстрой минерализации органических остатков.
Диоксид углерода (CO2) находится в воде главным образом в виде растворенных молекул газа CO2. Однако часть их (около 1 %) вступает во взаимодействие с водой, образуя угольную кислоту:
Диоксид углерода расходуется также на растворение карбонатов:
Мезоэлементы
Способствует неустойчивости кремния в растворе и склонность кремниевой кислоты при определенных условиях переходить в гель. В очень мало минерализованных водах кремний составляет существенную, а иногда и преобладающую часть химического состава воды, несмотря на его малое абсолютное содержание. Присутствие кремния в воде является серьезной помехой в технике, так как при продолжительном кипячении воды кремний образует в котлах очень твердую силикатную накипь.
Алюминий поступает в водоёмы в результате действия кислот на глины (каолин):
Микроэлементы
Факторы влияющие на химический состав воды
Почти на всей европейской части России (кроме Карелии и Мурманской области) известняки, а также доломиты MgCO3•CaCO3 залегают довольно близко к поверхности. Поэтому вода здесь содержит преимущественно гидрокарбонаты кальция и магния. В таких реках, как Волга, Дон, Северная Двина, и основных их притоках гидрокарбонаты кальция и магния составляют от 3/4 до 9/10 всех растворённых солей.
Соли попадают в водоёмы и в результате деятельности человека. Так, хлоридами натрия и кальция зимой посыпают дороги, чтобы растапливать лёд. Весной вместе с талой водой хлориды стекают в реки. Треть хлоридов в реках европейской части России привнесена туда человеком. В реках, на которых стоят крупные города, эта доля гораздо больше.
Рельеф местности косвенно влияет на состав воды, способствуя вымыванию солей из толщи пород. Глубина эрозионного вреза реки облегчает поступление в реку более минерализованных грунтовых вод нижних горизонтов. Этому же способствуют и другие виды депрессий (речные долины, балки, овраги), улучшающие дренирование водосбора.
Климат же, создает общий фон, на котором происходит большинство процессов, влияющих на формирование химическою состава природных вод. Климат прежде всего определяет баланс тепла и влаги, от которого зависит увлажненность местности и объем водного стока, а следовательно, и разбавление или концентрирование природных растворов и возможность растворения веществ или выпадения их в осадок.
Огромное влияние на химический состав воды и его изменение с течением времени оказывают источники питания водного объекта и их соотношение. В период таяния снега вода в реках, озерах и водохранилищах имеет более низкую минерализацию, чем в период, когда большая часть питания осуществляется за счет грунтовых и подземных вод. Это обстоятельство используют при регулировании наполнения водохранилищ и сброса из них воды. Как правило, водохранилища наполняют в период весеннего половодья, когда приточная вода имеет меньшую минерализацию.
Катионы и анионы в химии, таблица растворимости
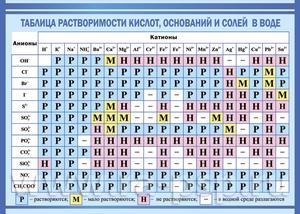
Показатели растворимости в воде
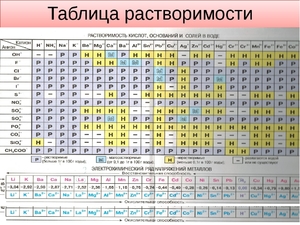
Она помогает при решении химических уравнений, где участвуют ионные реакции. Если результатом будет получение нерастворимого вещества, то реакция возможна. Существует несколько вариантов:
Это интересно: металлы и неметаллы в периодической таблице Менделеева.
Электролиты
Это растворы или сплавы, проводящие электрический ток. Электропроводность их объясняется мобильностью ионов. Электролиты можно поделить на 2 группы:
Теория электролитической растворимости
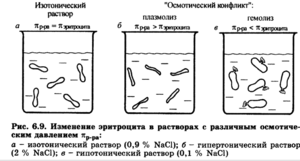
Одновременно с диссоциацией проходит противоположный процесс – соединение ионов в молекулы. Кислоты – это такие электролиты, при распаде которых образуется катион – ион водорода. Основания – анионы – это гидроксид ионы. Щелочи – это основания, которые растворяются в воде. Электролиты, которые способны образовывать и катионы и анионы, называются амфотерными.
Это такая частица, в которой больше протонов или электронов, он будет называться анион или катион, в зависимости от того, чего больше: протонов или электронов. В качестве самостоятельных частиц они встречаются во многих агрегатных состояниях: газах, жидкостях, кристаллах и в плазме. Понятие и название ввёл в обиход Майкл Фарадей в 1834 году. Он изучал воздействие электричества на растворы кислот, щелочей и солей.
Простые ионы несут на себе ядро и электроны. Ядро составляет почти всю атомную массу и состоит из протонов и нейтронов. Количество протонов совпадает с порядковым номером атома в периодической системе и зарядом ядра. Ион не имеет определённых границ из-за волнового движения электронов, поэтому невозможно измерить их размеры.
Отрыв электрона от атома требует, в свою очередь, затрат энергии. Она называется энергия ионизации. Когда присоединяется электрон, происходит выделение энергии.
Катионы
Это частицы, носящие положительный заряд. Могут иметь разную величину заряда, например: Са2+ — двузарядный катион, Na+ — однозарядный катион. Мигрируют к отрицательному катоду в электрическом поле.
Анионы
Это элементы, имеющие отрицательный заряд. А также обладает различным количеством величины зарядов, например, CL- — однозарядный ион, SO42- — двухзарядный ион. Такие элементы входят в состав веществ, обладающих ионной кристаллической решёткой, в поваренной соли и многих органических соединениях.
Химия – наука, где возможно творить практически любые чудеса. Катион вы можете узнать по ссылке.
Солёность и жёсткость природных вод. Какие анионы и катионы являются главными ионами природных вод.
Окислительно-восстановительные реакции в гидросфере.
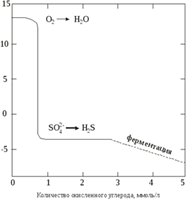
Окислительная способность природных вод характеризует их активность. ОВР – редокс реакции. большинство наиболее важных редокс-реакций катализируется микроорганизмами. Инициирование процессов окисления в воде помимо основного окисления кислорода связано также с наличием в воде сульфатов, нитратов, Ме с переменной валентностью, а так же частично с наличием свободных радикалов.
Под окислительностью элементов принимают способность системы поставлять е для ОВ реакций.
Окислительная способность зависит от ph среды. Для природной воды величина активности может различаться на 20 порядков.
Активность воды представляет через редокс, он аналогичен значению pH, но характеризует не кол-во ионов Н, а потенциальную воз-тьприрродной воды к участию ОВР.
Энергия Гиббса в ходе ОВР = 0
Потенциал, измеряемый по отношению к стандартному Н электроду называется величиной стандартной энергии р-раEhи оттого +/- значение имеет данная величина будет зависеть активность электронов в исследуемом растворе. Величина ОВ потенциала, протекающая с участием ионов Н завист от pH р-ра
Природные воды обычно находятся в контакте с воздухом, в котором парциальные давления кислорода и водорода меньше 1 атм, поэтому их ОВ потенциалы будут находиться в интервале значений, определяемых уравнениями
При окислительных процессах с участием О2 в воде, реакция идет в 2 стадии
Если на окислительные процессы израсходован весь О2, а в систему продолжают поступать органические вещества, то ОВР будут идти за счет других соединений.
Роль данной реакции состоит в превращении нитрата в биологически нейтральный азот.
Кроме молекулярного азота могут образоваться оксид, диоксид, гемеоксид азота.
2) Восстановление сульфатов или сульфат-редуксов – реакция в которых бактерти используют для окисления органических веществ сульфат иона.
Если pH воды > 7, то обр-я HS
Если в Н2О присутствует активные формы Fe, то будут образовываться его сульфиды.
3) Ферментация – процесс происходит при участии микроорганизмов и приводит к образованию более простых органических соединений.
Сорг + Н2О = СО2 + СН4
Данная реакция протекает при pH = 4.5
Особенности ОВ процессов в подземных водах:
Основными параметрами природных систем, обусловливающими редокс-уровни природных вод, являются:
Содержание кислорода в инфильтрационных водах. Если инфильтрационные воды поступают в водоносный горизонт по трещинам обнаженных пород (камням), то они обогащены кислородом и характеризуются значительной редокс-буферной емкостью и высокими значениями 
Распределение и реакционная способность органического вещества и других потенциальных восстановителей в водоносном горизонте. Так, органическое вещество осадочных пород трудно утилизируется бактериями, так как оно является устойчивым.
Распределение веществ, способных создать редокс-буферность водоносного горизонта. В подземных водах массы веществ, способных потенциально создать редокс-буферность, на единицу объема подземной воды довольно велики. Поэтому редокс-уровни подземных вод часто соответствуют величинам 
Скорость циркуляции подземных вод. Чем больше время пребывания, тем ниже конечное значение 
(26)11. Уникальные свойства воды.
Вода благодаря своему строению (наличию Н связи) имеют ряд аномальных свойств, благодаря которым поддерживается жизнь на земле.
1) Температурная зависимость плотности воды.Максимальная плотность воды наблюдается при t= 4 о С. Благодаря тому, что лед легче воды, он остается на поверхности водоемов, сохраняя в них жизнь круглогодично.
2) Теплоемкость – удельная теплоемкость воды выше, чем у у всех жидких и твердых веществ. (исключение :NH4 и Н2). Она ровна 75.3 Дж/моль*К. Благодаря этому свойству океаны сглаживают колебания t на планете.
3) Удельная энтальпия плавления, является самой высокой среди всех жидких и твердых веществ (исключение :NH3 и Н2). Благодаря данному свойству на земле сглаживаются сезонные переходы.
5) Поверхностное натяжение. Аномально высокое значение приводит к появлению ряби на воде уже при слабом ветре, в результате резко возрастает площадь водной поверхности à интенсифицируются процессы теплообмена между атмосферой и гидросферой. Также с явлением высокого натяжения связаны капиллярные силы воды, благодаря чему вода способна подниматься на высоту до 12 м от уровня грунтовых вод.
6) Диэлектрическая проницаемость. Она определяет самую большую растворяющую способность воды по отношению к веществам с полярной и ионной структурой.
(27)1. Литосфера. Строение. Свойства.
Одним из важнейших свойств почвы является её плодородие, т.е. способность обеспечивать органическое и минеральное питание растений. Плодородие зависит от физических и химических свойств почвы.
(28)2. Что такое «Кларк». Охарактеризуйте его расширенное понятие понимание в биогеохимии. Как распределены химические элементы в земной коре.
Средний химический состав земной коры (в %) характеризуется значениями кларковхимических элементов. К настоящему времени установлено, что земная кора бо- лее чем на 99 % состоит всего из 9 элементов: O, Si, Al, Fe, Ca, K, Na, Mg, Ti, на долю остальных элементов, называемых редкими и рассе-янными, приходится всего 0,52 % массы земной коры.
Ввиду неравномерности распределения элементов в земной коре для количественной оценки их распределения используются кларки концентраций: Кк = А/К, где А – содержание элемента в земной коре в данном регионе, % (мас.); К – кларк элемента в земной коре, % (мас.).
Химические элементы входят в состав различных минералов – однородных структур соединений химических элементов, образующихся в земной коре при различных физико-химических процессах. Рассеянные элементы либо изоморфно входят в кристаллические решетки минералов, образованных главными элементами, либо находятся в твердом кристаллическом веществе в неупорядоченном состоянии. Минералы в земной коре, как правило, входят в состав различных горных пород – природных совокупностей минералов более или менее постоянного минералогического состава, образующих самостоятельное тело в земной коре.
(29)3. Фазовый состав, механический состав элементарный состав почв. Условие фазного равновесия.
Почва представляет собой сложную саморегулирующуюся поликомпонентную многофазную систему. Выделяют четыре физические фазы почвы — твердую, жидкую, газовую и живую.
Твердая фаза — скелет почвы, прочная основа, состоящая из минеральной (95—99 %) и органической частей. Минеральная часть сформировалась из материнских геологических пород и содержит остаточные и вторичные.
Жидкая фаза почвы представляет собой почвенный раствор, который формируется из воды, поступающей в почву с атмосферными осадками, из грунтовых вод, при конденсации водяных паров.
Газовая фаза почвы представлена почвенным воздухом, который заполняет свободные от воды пустоты (поры) в почве. Источником почвенного воздуха являются воздух атмосферы и образующиеся в почве газы.
Живая фаза почвы представлена живыми организмами, населяющими почву и участвующими в почвообразовательном процессе. Это в первую очередь различные микроорганизмы а также простейшие, насекомые, черви и др.
В результате процессов выветривания плотные горные породы превращаются в рыхлую массу, состоящую из частиц различного размера, которые называются механическими элементами. Механические элементы, близкие по размерам, объединяются во фракции. Совокупность механических фракций представляет механический состав почвы. Механический состав почвы является важной характеристикой, необходимой для определения производственной ценности почвы, ее плодородия, способов обработки и т. д. От механического состава почвы зависят почти все физические и физико-механические свойства почвы: влагоемкость, водопроницаемость, порозность, воздушный и тепловой режим, водоподъемная сила и др.
Элементный состав – один из важнейших факторов, который обусловливает выбор методов химического и физико-химического анализа почв.
(30)4. Органические вещества почвы, гумус. Химический состав гумуса.
Органическое вещество почвы — это сложная система всех органических веществ, присутствующих в профиле в свободном состоянии или в форме органоминеральных соединений, исключая те, которые входят в состав живых организмов.
Органические остатки представлены главным образом наземным и корневым опадом высших растений, который не утратил своего анатомического строения.
Гумус представляет собой совокупность всех органических соединений, находящихся в почве, кроме входящих в состав живых организмов и органических остатков, сохранивших анатомическое строение.
В составе гумуса выделяют неспецифические органические соединения и специфические — гуминовые вещества.
Неспецифическими называется группа органических веществе известной природы и индивидуального строения. Они поступают в почву из разлагающихся растительных и животных остатков и с корневыми выделениями.
Специфическая органическая часть почвы — гуминовые вещества — представляют собой неоднородную полидисперсную систему высокомолекулярных азотсодержащих ароматических соединений кислотной природы. Гуминовые вещества образуются в результате сложного биофизико-химического процесса трансформации (гумификации) продуктов разложения органических остатков, попадающих в почву.
Важнейшими группами являются гуминовые кислоты (ГК) и фульвокислоты (ФК).
Количественной мерой типа гумуса служит отношение содержания углерода гуминовых кислот (Сгк) к содержанию углерода фульвокислот (Сфк). По величине этого отношения (Сгк/Сфк) можно различить четыре типа гумуса:
— фульватный — менее 0,5.
Гуминовые вещества почвы обладают высокой реакционной способностью и активно взаимодействуют с минеральной матрицей. Под влиянием органических веществ разрушаются неустойчивые минералы материнской породы и химические элементы становятся доступнее для растений. В процессе органо-минеральных взаимодействий образуются почвенные агрегаты, что улучшает структурное состояние почвы.
Гуминовые кислоты в противоположность ФК образуют с кальцием плохо растворимые органоминеральные соединения (гуматы кальция). Благодаря этому в почвах формируются гумусово-аккумулятивные горизонты. Гуминовые вещества почвы связывают ионы многих потенциально токсичных металлов — Al, Pb, Cd, Ni, Co, что снижает опасное влияние химического загрязнения почв.
(31) 5. Поглотительная способность почв. Почвенно-поглощающий комплекс, обменные катионы. Емкость каталитического обмена.
Почвенный поглощающий комплекс — это совокупность минеральных, органических и органоминеральных компонентов твердой части почвы, обладающих ионообменной способностью.
Катионный обмен — частный случай ионного обмена, под которым в химии понимают обратимый процесс обмена ионами между двумя контактирующими фазами. Материальным носителем катионообменной способности почв является ППК.
Реакцию обмена катионов А и Б формально можно записать так:
в ППК входят и способные к обменным реакциям катионы; в противном случае этот комплекс не смог бы выделить в ходе реакции эквивалентное количество катионов в обмен на катионы почвенного раствора. Не все твердые фазы почв способны проявлять катионообменную способность. Способность к поглощению и обмену катионов сосредоточена главным образом в илистой фракции почв.
Катионы, которые входят в состав ППК и могут быть замещены Катионами другого рода при взаимодействии с нейтральными растрами солей, называют обменными катионами, в качестве синонима употребляют термин поглощенные катионы. При характеристике ППК и обменных реакций часто используют термин обменные основания, под которым понимают только обменные катионы Са2+, Мg2+, К+ и Na+, тогда как в число обменных катионов входят кроме того, Н+, А13+ и др.
по определению Бренстеда — Лоури, основаниями называют вещества, способные соединяться с ионами водорода. Основаниями, следовательно, являются не сами катионы Са2+, Nа+ и т. д., а их гидроксиды.
Емкость катионного обмена.
Важнейшей характеристикой почвенного поглощающего комплекса и почвы в целом является емкость катионного обмена (ЕКО). Величина ЕКО существенно зависит от рН взаимодействующего с почвой раствора и несколько варьирует при замене одного вида насыщающего катиона на другой.
Под емкостью катионного обмена будем понимать общее количество катионов одного рода, удерживаемых почвой в обменном состоянии при стандартных условиях и способных к обмену на катионы взаимодействующего с почвой раствора. Величину емкости катионного обмена выражают в миллиграмм-эквивалентах на 100 г почвы или ее фракции.
• емкость катионного обмена стандартную определяют с помощью буферных растворов при постоянном значении рН.
• емкость катионного обмена реальную (или эффективную) определяют путем обработки почвы небуферными растворами солей о реальной емкости катионного обмена можно судить с достаточной точностью по сумме обменных катионов;
• дифференциальная (или рН-зависимая) емкость катионного обмена характеризует приращение емкости катионного обмена с увеличением рН равновесного раствора: ∆ЕКО/DрН. Чтобы найти дифференциальную ЕКО, почву насыщают катионами одного рода из буферных растворов с различными значениями рН (например 6,5 и 8,2), а затем рассчитывают общее приращение ЕКО или её приращение на единицу рН.
Величина ЕКО зависит от числа отрицательных зарядов, приходящихся на единицу массы или поверхности ППК. Обменные катионы компенсируют отрицательный заряд, и в отсутствие внешнего электрического поля каждая частица ППК электронейтральна.
Дата добавления: 2018-05-02 ; просмотров: 1089 ; Мы поможем в написании вашей работы!