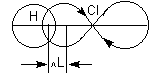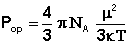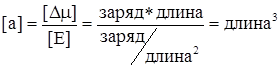Что такое индуцированный дипольный момент
Виктор Александрович КОГАН
профессор, заведующий кафедрой физической и коллоидной химии
Ростовского Государственного Университета
ИЗБРАННЫЕ ЛЕКЦИИ ПО КУРСУ «МЕТОДЫ ИССЛЕДОВАНИЯ КООРДИНАЦИОННЫХ СОЕДИНЕНИЙ»
Метод дипольных моментов в химии
Лекция посвящена одному из важнейших физических методов исследования строения вещества – методу дипольных моментов. Рассмотрена природа дипольного момента и методы его определения, а также приведены отдельные примеры применения метода дипольных моментов для выяснения строения химических соединений.
1. Общие представления о природе дипольного момента
Дипольный момент – важная молекулярная константа, характеризующая электрическую симметрию молекулы.
Знание величины дипольного момента необходимо для изучения природы химической связи, оценки прочности донорно-акцепторных и межмолекулярных связей, для квантово-химических расчетов. По величине дипольного момента можно судить об изомерии и конформации органических соединений, конфигурации координационных узлов комплексов, о взаимном влиянии атомов и связей в молекуле.
Величина электрического дипольного момента (μ) определяется соотношением:
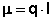
Причиной появления дипольного момента являются несколько факторов. В первую очередь – это различия в природе составляющих молекулу атомов. В простейшем случае для двухатомной молекулы μ = 0, если она состоит из двух одинаковых атомов. Это относится к H2, O2, N2 и т.д. В двухатомной молекуле с атомами разной природы проявляется постоянный дипольный момент, т. к., вследствие разной электроотрицательности, характеризующей способность атома оттягивать электронную плотность, появляется асимметрия электронной плотности. Другие причины – разные гибридные состояния орбиталей атомов. Так, например, для связи H-Cl, образованной 1s-орбиталью водорода и 3p-орбиталью хлора, вследствие различной формы s- и p-орбиталей, центр тяжести заряда перекрывания смещен в сторону водорода на ΔL, за счет чего возникает дополнительный, т. н. гомеополярный дипольный момент (рис.1):
Рис. 1. Схема происхождения гомеополярного диполя.
Естественно, молекулы HCl, HBr, HI имеют постоянные дипольные моменты, равные, соответственно, 1.95 D, 0.79 D, 0.40 D. Другие вклады в суммарный дипольный момент возникают из-за асимметрии связывающей и несвязывающей атомных орбиталей вследствие их гибридизации. Так, дипольный момент аммиака, 1.46 D, в основном обусловлен моментом несвязывающей пары электронов азота.
2. Методы определения дипольных моментов
Из всех методов получили наиболее широкое распространение методы определения дипольных моментов, основанные на измерении диэлектрической проницаемости (ε) вещества. Этими методами измерены дипольные моменты молекул более 10000 веществ. Переход от измеряемого значения ε газа, чистой жидкости или разбавленного раствора, т.е. макроскопической характеристики диэлектрика, к величине дипольного момента основан на теории поляризации диэлектриков. Считается, что при наложении электрического поля на диэлектрик его полная поляризация Р складывается из наведенной или индуцированной поляризации Рм и поляризации Рор и связана с μ уравнением Ланжевена-Дебая (2).
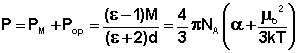
Измерения диэлектрической проницаемости проводят в постоянном поле или при низких частотах, обеспечивающих полную ориентацию молекул по полю. Кратко остановимся на типичной процедуре определения μо в разбавленных растворах. Она основана на предположении об аддитивности свойств составляющих раствор компонентов:
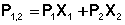
где Р1,2, Р1, Р2 – молекулярные поляризации раствора, растворителя и растворенного вещества соответственно;
Х1, Х2 – мольные доли растворителя и растворенного вещества.
С учетом уравнения (2) уравнение (3) для раствора будет выглядеть как (4):
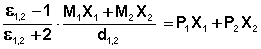
где М1 и М2 – молекулярные веса растворителя и растворенного вещества;
ε1,2 – диэлектрическая проницаемость раствора;
d1,2 – плотность раствора.
Из уравнения (4) можно вычислить Р2 – молекулярную поляризацию растворенного вещества. В этом методе допускается, что молекулы полярного вещества могут вести себя в растворах как в парообразном состоянии и свободно ориентироваться в приложенном поле только для бесконечно разбавленных растворов, поэтому значение Р2 следует экстраполировать на нулевую концентрацию (Х2 = 0) и найти значение молекулярной поляризации растворенного вещества при бесконечном разбавлении (Р2∞).
Эксперимент сводится к измерению диэлектрической проницаемости и плотности 5-7 разбавленных растворов исследуемого соединения при точно поддерживаемой температуре (обычно 25 °С) в интервале концентраций растворенного вещества от 0,001¸ 0,01 мольных долей. Выбор интервала концентраций зависит от растворимости и полярности вещества и может колебаться в сторону уменьшения мольных долей для более полярных соединений. Затем по формуле (4) находят значение молекулярной поляризации растворенного вещества для каждой концентрации и по полученным данным строят кривую зависимости Р2 от концентраций, по которой экстраполируют Р2 до нулевой концентрации и находят значение Р2∞. Эту величину можно также получить, используя различные приемы экстраполяции к нулевой концентрации для диэлектрической проницаемости и плотности.
Величину дипольного момента рассчитывают из уравнения Дебая (2)
из которого, подставляя значения N, κ, π, можно вычислить величину постоянного дипольного момента по формуле (5):
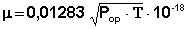
Найденное в эксперименте значение Р2∞ включает в себя электронную (Рэл) и атомную (Рат) молекулярные поляризации и поэтому Рор в уравнении (5) вычисляется как Рор = Р2∞ – Рат – Рэл.
Рэл считают равной рефракции вещества, которое вычисляется по той же схеме аддитивности на основании измерения коэффициентов преломления и плотности той же серии растворов, а Рат вследствие ее малости очень часто пренебрегают. Следует отметить, что Рэл можно рассчитать по рефракциям связей и групп, если не требуется высокая точность в значении дипольного момента.
Сходимость результатов, полученных различными методами при корректном использовании правильных расчетных формул бывает достаточно хорошей, как показано в табл. 1:
Таблица 1. Дипольные моменты молекул (в D)
Что такое индуцированный дипольный момент
μинд – индуцированный (наведенный) диполь;
μпост – индуцирующий постоянный диполь;
α – поляризуемость молекулы;
Е – напряженность электрического поля.
Диполь-дипольным взаимодействием называется взаимодействие диполей, приводящие к их взаимной ориентации и притяжению. Энергия взаимодействия двух диполей пропорциональна произведению их дипольных моментов.
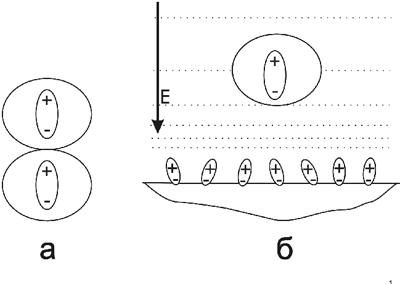
Рисунок 2.1. Диполь-дипольное взаимодействие двух частиц (а) и диполь-полевое взаимодействие полярного адсорбата с поверхностью динамически модифицированного полярного адсорбента (б).
В жидкостной хроматографии, как правило, рассматривается взаимодействие дипольного момента адсорбата с дипольными моментами полярных групп адсорбента; таким образом, диполь-дипольное взаимодействие является одной из причин удерживания молекул, обладающих дипольным моментом, на полярных неподвижных фазах в неполярных средах.
Наиболее характерный случай диполь-дипольного взаимодействия в жидкостной хроматографии соответствует ситуации, когда поверхность полярной неподвижной фазы модифицирована адсорбционным слоем полярного компонента подвижной фазы. Для этого случая моделью однородно модифицированной поверхности неподвижной фазы является эквипотенциальная поверхность, характеризующаяся некоторым усредненным значением напряженности электрического поля (рисунок 2.1.б). Энергия взаимодействия диполя адсорбата с электрическим полем неподвижной фазы равна произведению дипольного момента на напряженность электрического поля:
Напряженность электрического поля полярной адсорбционно модифицированной неподвижной фазы составляет величину порядка 10 9 В/м, а энергия «диполь-полевого» взаимодействия – порядка кДж/моль.
Большая Энциклопедия Нефти и Газа
Индуцированный дипольный момент
Из механизма образования индуцированного дипольного момента молекулы [ см. § 17 ] следует, что его направление совпадает с направлением напряженности электрического поля. [17]
Из результатов исследований можно вычислить индуцированный дипольный момент и соответственно электрическую поляризуемость, которая является количественной мерой деформации двойного слоя. Если па заряженные частицы накладывается переменное неоднородное поле подходящей частоты, электрофоретическая подвижность выпадает и остаются только диэлектрофоретическая и диполофоретическая составляющие. Следует ожидать, что в случае сильно удлиненных коллоидных частиц ( длиной порядка десятых микрона и больше) будет преобладать диполофоретическая слагаемая. [22]
Влияние неоднородности поля волны на индуцированный дипольный момент молекулы с макроскопической точки зрения означает, что поляризованность среды Р ( г) в каждой точке зависит от значения напряженности Е ( г) не только в той же точке г, но и в соседних точках области порядка молекулярных размеров. Другими словами, связь между Р и Е имеет нелокальный характер. То же самое относится, очевидно, и к связи между вектором индукции D и напряженностью Е поля. [23]
Поляризуемость ротатора а определяется как отношение индуцированного дипольного момента к напряженности внешнего поля. [26]
Этот эффект очень мал, но такие индуцированные дипольные моменты могут вызвать вращательные переходы в неполярных молекулах. Если штарковское поле само изменяется, то возникают новые явления [290, 453], когда частота изменения становится сравнимой с шириной линии поглощения. Когда частота модуляции делается равной частоте спектральной линии, имеет место резонанс [ 181, эффект Штарка становится очень большим и за точкой резонанса меняет знак. [28]
Дипольный момент и изомерия молекул.
Изомерные молекулы независимо от характера изомерии имеют разную равновесную конфигурацию. Следовательно, и разную симметрию. В частности, один изомер может иметь такую симметрию, что его ЭДМ=0, а другой изомер – такую симметрию, что его ЭДМ≠0. Примеры такого рода встречаются как для структурных изомеров, так и для поворотных изомеров (конформеров):
Атомы водорода не указаны
Циклопропан 
Поворотные изомеры (конформеры) 1,2-дихлорэтана:


Транс-1,2-дихлорэтан 

Транс-1,2-дихлорэтилен 



где 

Вектора 
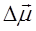




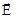


Если всевозможные ориентации молекулы относительно направления поля считать равновероятными, то средний момент 


Поскольку деформация молекулы в поле происходит не мгновенно при включении поля, то средняя поляризуемость зависит от частоты, с которой меняется напряженность поля. Если 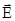

Размерность поляризуемости определяется из формулы (3.8)
Связь электрических свойств молекул с электрическими свойствами вещества.
3.3.1 Поляризация диэлектриков (связь e и а,m).
3.3.2 Поляризация диэлектрика в переменном поле.
3.3.3 Мольная рефракция (связь n и m).
Поляризация диэлектриков.
Мы рассмотрим этот вопрос на основе классической физики. Именно, мы не будем принимать во внимание ни квантование проекции дипольного момента молекулы, ни квантование вращательной энергии молекулы. Также не будем учитывать различий в дипольных моментах отдельных молекул, находящихся в разных электронных, колебательных и вращательных состояниях. Учет всех этих факторов в случае относительно слабых полей и высоких температур (порядка комнатной и выше) приводит в первом приближении к результатам, аналогичным получающимся на основе классической физики.
Рассмотрим изменение состояний отдельных молекул и вещества в целом при помещении его в однородное электрическое поле, например в поле плоского конденсатора. Если в отсутствие диэлектрика напряженность в плоском конденсаторе была Е, то при введении между его обкладками диэлектрика напряженность поля Е / станет меньше в e раз.


Это уменьшение напряженности происходит потому, что диэлектрик поляризуется, то есть на его поверхностях, обращенных к обкладкам конденсатора, появляются избыточные заряды.
Поляризация диэлектрика в поле объясняется двумя причинами.
Во-вторых, при помещении в поле молекул, имеющих собственные дипольные моменты 
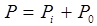
где Рi — поверхностная плотность заряда за счет индуцированного 
Р0 — за счет ориентации собственных моментов m..
Если выразить Рi и Р0 через микроскопические характеристики а и m и учесть зависимость между Р и e, то можно получить уравнение Ланжевена-Дебая.
Уравнение Ланжевена-Дебая для единицы объема вещества.


Если (3.9) умножить на объем одного моля

Уравнение Ланжевена-Дебая для неполярных молекул (m = 0):
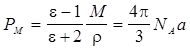
Большая Энциклопедия Нефти и Газа
Индуцированный дипольный момент
Индуцированный дипольный момент относительно легко возникает в молекулах ароматических углеводородов. Поэтому ароматические соединения сравнительно хорошо экстрагируются избирательным растворителем. [1]
Индуцированный дипольный момент р пары соседних ионов противоположного знака равен ег. [2]
Индуцированный дипольный момент пропорционален напряженности поля. Коэффициент пропорциональности между Р и Е обычно обозначают ае и называют электронной поляризуемостью. [3]
Индуцированный дипольный момент / ш пропорционален напряженности поля Е, то есть / ш аЕ, где а характеризует степень поляризуемости индуцированной молекулы. [4]
Индуцированный дипольный момент в свою очередь создает электрическое поле, действующее на свободный заряд. [5]
Индуцированные дипольные моменты iei ( и tiei () в молекуле изменяются во времени с такой же частотой, как и падающая волна. Однако имеются следующие особенности такого излучения, Векторы § и В изменяются в одной фазе. Таким образом, для волны электрического поля падающего линейно поляризованного света при прохождении в оптически активном веществе должно наблюдаться вращение плоскости поляризации, так как кроме компоненты электрического поля в плоскости падающей волны появляется перпендикулярная компонента. [6]
Индуцированный дипольный момент имеет то же направление, что и постоянный диполь, вызвавший его появление. Взаимодействие постоянного диполя одной молекулы и наведенного им диполя второй понижает потенциальную энергию системы из двух молекул и упрочняет систему. Рассмотрим простейший и в то же время важный случай взаимодействия полярной и неполярной молекул. [7]
Индуцированные дипольные моменты согласно уравнению ( 2) уменьшаются экспоненциально с ростом числа слоев. [8]
Величина индуцированного дипольного момента зависит от силы электрического поля, и поэтому за меру такого дипольного момента принимается момент, возникающий при силе поля, равной единице. [11]
Величина индуцированного дипольного момента зависит от силы электрического поля и поэтому за меру такого дипольного момента принимается момент, возникающий при силе поля, равной единице. [12]
Согласно (9.12) индуцированный дипольный момент молекулы Р изменяется во времени; вследствие этого наблюдается рассеянный свет. [13]
Остальные компоненты индуцированного дипольного момента для дисперсии несущественны, однако они вместе с Z-компонентом определяют способность атома рассеивать падающее на него излучение. [14]
Среди ароматических углеводородов индуцированный дипольный момент возникает в тех из них, в которых ароматическое ядро не очень экранировано алифатическими цепями или нафтеновыми кольцами. Чем длиннее эти цепи или чем сложнее их конфигурация, тем больше осложняется возникновение в ароматических углеводородах наведенного дипольного момента и ассоциация с молекулами полярного растворителя. [15]