Что такое иммуногенность вакцины
В качестве вакцин используются антигены разного происхождения, это могут быть живые и убитые бактерии, вирусы, анатоксины, а также антигены, полученные с помощью генной инженерии и синтетические.
От состава вакцин во многом зависят их иммунобиологические свойства, способность индуцировать специфический иммунный ответ. Однако некоторые составные части вакцин могут вызвать и нежелательные реакции, что следует учитывать при проведении иммунизации.
Существующее многообразие вакцин можно подразделить на две основные группы: на живые и убитые (инактивированные) вакцины. В свою очередь какждая из этих групп может быть разделена на подгруппы [11].
2. Убитые вакцины
— Молекулярные, полученные путем:
а) биологического синтеза;
б) химического синтеза.
— Корпускулярные:
а) из цельных микробов;
б) из субклеточных надмолекулярных структур.
В последние годы созданы синтетические молекулярные вакцины, а так же плазмидные (генные) вакцины.
Постановка вопроса о предпочтительном выборе либо живых, либо убитых вакцин нам кажется неоправданной, так как в каждом конкретном случае эти принципиально разные препараты имеют свои преимущества и свои недостатки.
Традиционные вакцины
Инактивированные вакцины получают путем воздействия на микроорганизмы химическим путем или нагреванием. Такие вакцины являются достаточно стабильными и безопасными, так как не могут вызвать реверсию вирулентности. Они часто не трубуют хранения на холоде, что удобно в практическом использовании. Однако у этих вакцин имеется и ряд недостатков, в частности, они стимулируют более слабый иммунный ответ и требуют применения нескольких доз (бустерные иммунизации).
б) живые аттенуированнные
Хотя живые вакцины требуют специальных условий хранения, они продуцируют достаточно эффективный клеточный и гуморальный иммунитет и обычно требуют лишь одно бустерное введение. Большинство живых вакцин вводится парентерально (за исключением полиомиелитной вакцины).
На фоне преимуществ живых вакцин имеется и одно предостережение, а именно: возможность реверсии вирулентных форм, что может стать причиной заболевания вакцинируемого. По этой причине живые вакцины должны быть тщательно протестированы. Пациенты с иммунодефицитами (получающие иммуносупрессивную терапию, при СПИДе и опухолях) не должны получать такие вакцины.
Многие микроорганизмы, вызывающие заболевания у человека, опасны тем, что выделяют экзотоксины, которые являются основными патогенетическими факторами заболевания (например, дифтерия, столбник). Анатоксины, используемые в качестве вакцин, индуцируют специфический иммунный ответ. Для получения вакцин токсины чаще всего обезвреживают с помощью формалина.
Ниже (табл. 15) приведена сравнительная характеристика вакцин [11], из которой следует, что инактивированные вакцины более стабильны, менее реактогенны, на их основе можно конструировать многокомпонентные вакцины, хотя в то же время по иммуногенности они уступают живым вакцинам.
Таблица 15. Факторы, влияющие на иммунный ответ на антиген
|
Новое поколение вакцин
Использование новых технологий позволило создать вакцины второй генерации.
Рассмотрим подробнее некоторые из них:
Некоторые бактерии, вызывающие такие опасные заболевания, как менингиты или пневмонию (гемофилюс инфлюэнце, пневмококки), имеют антигены, трудно распознаваемые незрелой иммунной системой новорожденных и грудных детей. В конъюгированных вакцинах используется принцип связывания таких антигенов с протеинами или анатоксинами другого типа микроорганизмов, хорошо распознаваемых иммунной системой ребенка. Протективный иммунитет вырабатывается против конъюгированных антигенов.
На примере вакцины против гемофилюс инфлюэнце (Hib-b) показана эффективность в снижении заболеваемости Hib-менингитами детей до 5-ти лет в США за период с 1989 по 1994 г.г. с 35 до 5 случаев.
б) субъединичные вакцины
Субъединичные вакцины состоят из фрагментов антигена, способных обеспечить адекватный иммунный ответ. Эти вакцины могут быть представлены как частицами микробов, так и получены в лабораторных условиях с использованием генно-инженерной технологии.
Примерами субъедиинчных вакцин, в которых используются фрагменты микроорганизмов, являются вакцины против Streptococcus pneumoniae и вакцина против менингококка типа А.
Рекомбинантные субъединичные вакцины (например, против гепатита B) получают путем введения части генетического материала вируса гепатита B в клетки пекарских дрожжей. В результате экспрессии вирусного гена происходит наработка антигенного материала, который затем очищается и связывается с адъювантом. В результате получается эффективная и безопасная вакцина.
в) рекомбинантные векторные вакцины
3.1. Компоненты вакцин
Как известно, основу каждой вакцины составляют протективные антигены, представляющие собой лишь небольшую часть бактериальной клетки или вируса и обеспечивающие развитие специфического иммунного ответа. Протективные антигены могут являться белками, гликопротеидами, липополисахаридобелковыми комплексами. Они могут быть связаны с микробными клетками (коклюшная палочка, стрептококки и др.), секретироваться ими (бактериальные токсины), а у вирусов располагаются преимущественно в поверхностных слоях суперкапсида вириона [11].
Поскольку для создания вакцин необходимо получение протективного антигена в достаточных количествах, то, прежде всего, нарабатываются большие объемы биомассы (культивируемые бактерии, вирусы). Далее производится выделение и очистка протективного антигена, причем в зависимости от условий это может быть как живая биомасса, так и инактивированная. Для инактивации используют формалин, фенол, перекись водорода, тепло, УФО-облучение и т.д.
Выделение и очистка протективного антигена также сопряжены с физическими или химическими методами воздействия, что определяется в основном свойствами антигена. Это могут быть методы изоэлектрического осаждения кислотами и щелочами, высаливание нейтральными солями, осаждение спиртом, сорбция и элюция, ультрафильтрация, колоночная хроматография и т.д.
Важно, что при всех указанных действиях должна максимально сохраняться первоначальная структура протективного антигена и в то же время должна быть получена максимальная степень чистоты препарата [11].
Несмотря на постоянное совершенствование вакцин, существует целый ряд обстоятельств, изменение которых в настоящий момент невозможно. К ним относятся следующие: добавление к вакцине стабилизаторов, наличие остатков питательных сред, добавление антибиотиков и т.д. Известно, что вакцины могут быть разными и тогда, когда они выпускаются разными фирмами. Кроме того, активные и инертные ингредиенты в разных вакцинах могут быть не всегда идентичными (для одинаковых вакцин).
Консерванты, стабилизаторы, антибиотики
Аллергические реакции могут иметь место, если реципиент чувствителен к одной из этих добавок (тимеросал или мертиолят, фенолы, альбумин, глицин, неомицин).
Растворители вакцин
Адъюванты
Многие антигены вызывают субоптимальный иммунологический ответ. Усиление иммуногенности включает связывание антигенов с различными субстанциями или адъювантами (например, фосфат алюминия или гидроокись алюминия).
В технологии создания вакцин предусматривается стерилизация растворов антигенов. С этой целью используются термическая обработка, облучение, фильтрация и т.п. Безусловно все эти воздействия не должны повлиять на сохранность протективного антигена и его количество [11].
3.2. Критерии эффективных вакцин
Актуальной задачей современной вакцинологии является постоянное совершенствование вакцинных препаратов. Эксперты международных организаций по контролю за вакцинацией разработали ряд критериев эффективных вакцин, которые соблюдаются всеми странами-производителями вакцин. Перечислим некоторые из них (Табл. 16)
Таблица 16. Некоторые критерии эффективных вакцин
(Janeway C.A., et al., 1996)
|
В настоящее время существуют определенные требования к вакцинам:
| 1. | Вакцина должна быть безопасной. |
| 2. | Вакцина должна индуцировать протективный иммунитет с минимальными побочными эффектами для большинства получивших ее. |
| 3. | Вакцина должна быть иммуногенной, т.е. должна вызывать достаточно сильный иммунный ответ. |
| 4. | Вакцина должна индуцировать «правильный» (необходимый) тип иммунного ответа. Когда микроорганизмы проникают в организм человека, они могут вызвать заболевание разными путями, и разные отдела имунной системы отвечают за эффективную борьбу с ними. Вакцины должны стимулировать специфический иммунный ответ, который эффективно защитит от инфекции. |
| 5. | Вакцины должны быть стабильны в течение срока хранения. Многие инактивированные вакцины проще для хранения, особенно если они в сухом виде и растворяются перед введением. Живые аттенуированные вакцины для сохранения их стабильности требуют охлаждения на всем протяжении пути от завода-изготовителя до клиники. |
3.3. Условия эффективной вакцинации
На сегодняшний день эффективной считается та вакцинация, в результате которой развивается длительная защита вакцинируемого от инфекции. Ряд требований эффективной вакцинации перечисляются ниже.
Что такое вакцина
Знаете ли вы, что такое прививка?
Вакцинация (прививка) – это введение в организм человека медицинских иммунобиологических препаратов для создания специфической невосприимчивости к инфекционным болезням.
Предлагаем разобрать каждую часть этого определения, чтобы понять, что же такое вакцина и как она работает.
Часть 1. Медицинский иммунобиологический препарат
Все вакцины — это медицинские иммунобиологические препараты, т.к. они вводятся под контролем врача и содержат обработанные по специальной технологии возбудители заболеваний (биологические), против которых планируется создать иммунитет (иммуно-).
Кроме возбудителей или их частей-антигенов, вакцины иногда содержат специальные разрешенные консерванты для сохранения стерильности вакцины при хранении, а также минимальное допустимое количество тех средств, которые использовались для выращивания и инактивации микроорганизмов. Например, следовые количества дрожжевых клеток, используемых в производстве вакцин против гепатита В, или следовые количества белка куриных яиц, которые в основном используются для производства вакцин против гриппа.
Стерильность препаратов обеспечивают консерванты, рекомендованные Всемирной организацией здравоохранения и международными организациями по контролю безопасности лекарственных средств. Эти вещества разрешены для введения в организм человека.
Полный состав вакцин указан в инструкциях по их применению. Если у человека имеется установленная тяжелая аллергическая реакция на какой-то из компонентов конкретной вакцины, то обычно это является противопоказанием к её введению.
Часть 2. Введение в организм
Для введения вакцины в организм используются разные методы, их выбор определяется механизмом формирования защитного иммунитета, а способ введения указан в инструкции по применению.
Кликните на каждый из способов введения, чтобы больше о нем узнать.
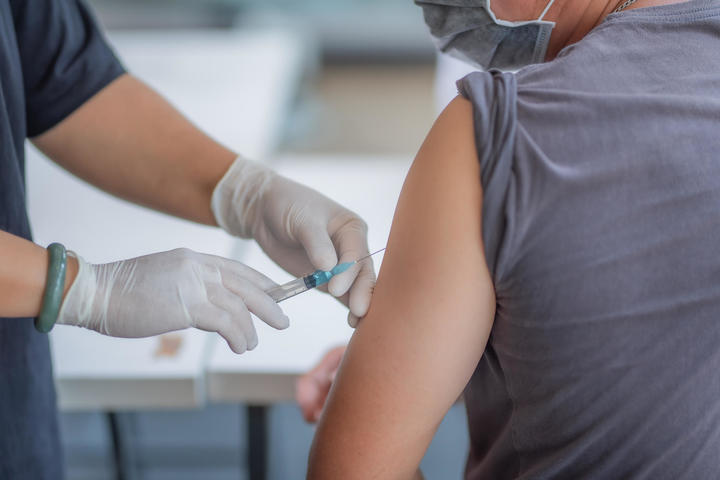
Внутримышечный путь введения вакцин
Наиболее часто встречающийся путь для введения вакцин. Хорошее кровоснабжение мышц гарантирует и максимальную скорость выработки иммунитета, и максимальную его интенсивность, поскольку большее число иммунных клеток имеет возможность «познакомиться» с вакцинными антигенами. Удаленность мышц от кожного покрова обеспечивает меньшее число побочных реакций, которые в случае внутримышечного введения обычно сводятся лишь к некоторому дискомфорту при активных движениях в мышцах в течение 1-2 дней после вакцинации.
Место введения: Вводить вакцины в ягодичную область не рекомендуется. Во-первых, иглы шприц-доз многих вакцин недостаточно длинны для того, чтобы достичь ягодичной мышцы, в то время, как известно, и у детей, и у взрослых кожно-жировой слой может иметь значительную толщину. Если вакцина вводится в ягодичную область, то она, возможно, будет введена подкожно. Следует также помнить о том, что любая инъекция в ягодичную область сопровождается определенным риском повреждения седалищного нерва у людей с нетипичным его прохождением в мышцах.
Предпочтительным местом введения вакцин у детей первых лет является передне-боковая поверхность бедра в средней его трети. Это объясняется тем, что мышечная масса в этом месте значительна, при том, что подкожно-жировой слой развит слабее, чем в ягодичной области (особенно у детей, которые еще не ходят).
У детей старше двух лет и взрослых предпочтительным местом введения вакцин является дельтовидная мышца (мышечное утолщение в верхней части плеча, над головкой плечевой кости), в связи с небольшой толщиной кожного покрова и достаточной мышечной массой для введения 0,5-1,0 мл вакцинного препарата. У детей первого года жизни это место обычно не используется в связи с недостаточным развитием мышечной массы.
Техника вакцинации: Обычно внутримышечная инъекция проводится перпендикулярно, то есть под углом 90 градусов к поверхности кожи.
Преимущества: хорошее всасывание вакцины и, как следствие, высокая иммуногенность и скорость выработки иммунитета. Меньшее число местных побочных реакций.
Недостатки: Субъективное восприятие детьми младшего возраста внутримышечных инъекций несколько хуже, чем при других способах вакцинации.
Пероральный (т.е. через рот)
Классическим примером пероральной вакцины является ОПВ – живая полиомиелитная вакцина. Обычно таким образом вводятся живые вакцины, защищающие от кишечных инфекций (полиомиелит, брюшной тиф).
Техника пероральной вакцинации: несколько капель вакцины закапываются в рот. Если вакцина имеет неприятный вкус, ее могут закапывать либо на кусочек сахара, либо печенья.
Преимущества такого пути введения вакцины очевидны: нет укола, простота метода, его быстрота.
Недостатками Недостатками перорального введения вакцин можно считать разлив вакцины, неточность дозировки вакцины (часть препарата может выводиться с калом, не сработав).
Внутрикожный и накожный
Классическим примером вакцины, предназначенной для внутрикожного введения, является БЦЖ. Примерами вакцин с внутрикожным введением также являются живая туляремийная вакцина и вакцина против натуральной оспы. Как правило, внутрикожно вводятся живые бактериальные вакцины, распространение микробов из которых по всему организму крайне нежелательно.
Техника: Традиционным местом для накожного введения вакцин является либо плечо (над дельтовидной мышцей), либо предплечье – середина между запястьем и локтевым сгибом. Для внутрикожного введения должны использоваться специальные шприцы со специальными, тонкими иглами. Иголочку вводят вверх срезом, практически параллельно поверхности кожи, оттягивая кожу вверх. При этом необходимо убедиться, что игла не проникла под кожу. О правильности введения будет свидетельствовать образование специфической «лимонной корочки» в месте введения – белесый оттенок кожи с характерными углублениями на месте выхода протоков кожных желез. Если «лимонная корочка» не образуется во время введения, значит вакцина вводится неверно.
Преимущества: Низкая антигенная нагрузка, относительная безболезненность.
Недостатки: Довольно сложная техника вакцинации, требующая специальной подготовки. Возможность неправильно ввести вакцину, что может привести к поствакцинальным осложнениям.
Подкожный путь введения вакцин
Довольно традиционный путь введения вакцин и других иммунобиологических препаратов на территории бывшего СССР, хорошо известный всем уколами «под лопатку». В целом этот путь подходит для живых и инактивированных вакцин, хотя предпочтительно использовать его именно для живых (корь-паротит-краснуха, желтая лихорадка и др.).
В связи с тем, что при подкожном введении может несколько снижаться иммуногенность и скорость выработки иммунного ответа, этот путь введения крайне нежелателен для введения вакцин против бешенства и вирусного гепатита В.
Подкожный путь введения вакцин желателен для пациентов с нарушениями свертывания крови – риск кровотечений у таких пациентов после подкожной инъекции значительно ниже, чем при внутримышечном введении.
Техника: Местом вакцинации могут быть как плечо (боковая поверхность середины между плечевым и локтевым суставами), так и передне-боковая поверхность средней трети бедра. Указательным и большим пальцами кожа берется в складку и, под небольшим углом, игла вводится под кожу. Если подкожный слой у пациента выражен значительно, формирование складки не критично.
Преимущества: Сравнительная простота техники, незначительно меньшая болезненность (что несущественно у детей) по сравнению с внутримышечной инъекцией. В отличие от внутрикожного введения, можно ввести больший объем вакцины или другого иммунобиологического препарата. Точность введенной дозы (по сравнению с внутрикожным и пероральным способом введения).
Недостатки: «Депонирование» вакцины и как следствие — меньшая скорость выработки иммунитета и его интенсивность при введении инактивированных вакцин. Большее число местных реакций — покраснений и уплотнений в месте введения.
Аэрозольный, интраназальный (т.е. через нос)
Считается, что подобный путь введения вакцин улучшает иммунитет во входных воротах воздушно-капельных инфекций (например, при гриппе) за счет создания иммунологического барьера на слизистых оболочках. В то же время, созданный таким образом иммунитет не является стойким, и в то же время общий (т.н. системный) иммунитет может оказаться недостаточным для борьбы с бактериями и вирусами, уже проникшими в организм через барьер на слизистых оболочках.
Техника аэрозольной вакцинации: несколько капель вакцины закапывают в нос либо распыляют в носовых ходах с помощью специального устройства.
Преимущества такого пути введения вакцины очевидны: как и для пероральной вакцинации, для аэрозольного введения не требуется укола; такая вакцинация создает отличный иммунитет на слизистых оболочках верхних дыхательных путей.
Недостатками интраназального введения вакцин можно считать существенный разлив вакцины, потери вакцины (часть препарата попадает в желудок).
Часть 3. Специфическая невосприимчивость
Вакцины защищают только от тех заболеваний, против которых они предназначены, в этом заключается специфика иммунитета. Возбудителей же инфекционных заболеваний множество: они делятся на различные типы и подтипы, для защиты от многих из них уже созданы или создаются специфичные вакцины с разными возможными спектрами защиты.
Так, например, современные вакцины против пневмококка (одного из возбудителей менингита и пневмонии) могут содержать по 10, 13 или 23 штамма. И хотя ученым известно около 100 подтипов пневмококка, вакцины включают самые часто встречающиеся у детей и взрослых, например, самый широкий на сегодня спектр защиты — из 23 серотипов.
Однако нужно иметь в виду, что привитой человек имеет вероятность встретиться с каким-то редким подтипом микроорганизма, который не входит в вакцину и может вызвать заболевание, так как вакцина не формирует защиту против этого редко встречающегося микроорганизма, не входящего в её состав.
Означает ли это, что прививка не нужна, раз не может защитить от всех болезней? НЕТ! Вакцина дает хорошую защиту от наиболее распространенных и опасных из них.
Календарь прививок, подскажет вам, против каких инфекций необходима вакцинация. А мобильное приложение «Беби-Гид» поможет не забыть о сроках детских прививок.
Вакцины, антитела, антигены. Гид по иммунологии для чайников
Андрей Смирнов
Антитела, антигены, титры, тесты, вакцины — сейчас все это буквально из каждого утюга. «СПИД.ЦЕНТР» объясняет, какими бывают антитела, откуда они берутся и как все это связано с вакцинами и иммунитетом.
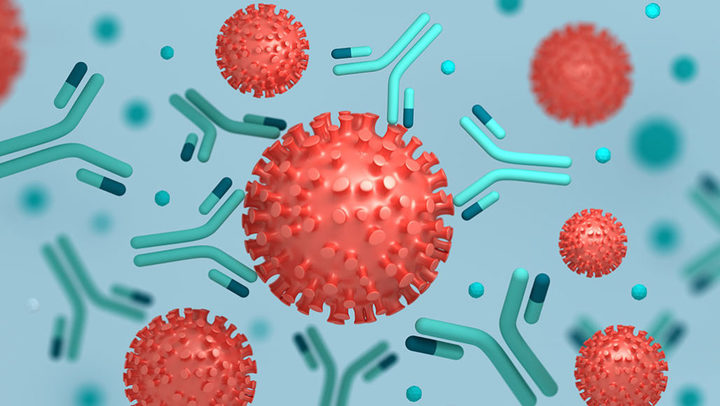
Что такое антитела?
Антитела (они же иммуноглобулины) — это специальные белки, которые вырабатывают клетки нашей иммунной системы для борьбы с «чужеродным вторжением» — проникновением в организм практически чего угодно, что наша иммунная система посчитает потенциально опасным. Это могут быть бактерии, вирусы, их токсины — так наш организм защищается от инфекции, или даже безобидная пыльца растений и лекарства — и в этом случае развивается аллергия.
Вещество, в ответ на которое начали вырабатываться антитела, называют антигеном. И да, антиген — это именно вещество, так как антитела вырабатываются не против вируса или бактерии «целиком», а против тех или иных конкретных вирусных или бактериальных белков. Например, если говорят об антителах против вируса гриппа, подразумевают антитела против двух белков из оболочки этого вируса — гемагглютинина и нейраминидазы. В случае SARS-CoV-2 речь чаще всего идет о шиповидном белке оболочки вируса (он же S-белок или спайк-белок).
Антитела обладают высокой специфичностью, то есть работают строго против определенного антигена или небольшой группы антигенов, очень сходных по своей структуре. Суть работы антител довольно простая — они химически связываются с антигеном и блокируют его взаимодействие с другими молекулами. Например, антитела против шиповидного белка оболочки коронавируса будут «прилипать» к этому белку, обволакивая вирусную частицу, — и такой вирус уже не сможет «прилипнуть» к клетке и проникнуть в нее. Кроме того, частицы с «налипшими» на них антителами гораздо «аппетитнее» выглядят для клеток нашей иммунной системы и будут быстрее поглощаться и перевариваться макрофагами — этот эффект называется «опсонизация».
Как организм понимает, какие антитела вырабатывать?
Выработка антител — довольно сложный и многостадийный процесс. Если очень коротко, то специальные клетки иммунной системы поглощают и переваривают потенциально опасную частицу (например, бактерию или вирус), буквально разбирают ее на кусочки. И затем показывают эти кусочки другим клеткам, которые подбирают подходящую структуру антитела так, чтобы это антитело могло химически связаться с одним из «кусочков» переваренной бактерии. Когда нужная структура найдена — запускается массовое производство антител. На этот процесс требуется немало времени, поэтому после первого контакта с антигеном накопление антител начинается примерно через 2 недели. Выработанные антитела циркулируют в крови около 4 недель, после чего разрушаются, при этом выработка новых антител может продолжаться.
Хорошая новость в том, что иммунная система умеет «запоминать» антигены, и при следующем контакте организму уже не нужно тратить 2 недели на поиск нужной структуры антитела — выработка начинается практически сразу. Именно так работает приобретенный иммунитет.
Иммунологическая память хранится разное время. Для некоторых инфекций, например для клещевого энцефалита, это 3–5 лет. Для других, например гепатита B или кори, — от десятков лет до пожизненной «гарантии». Именно от времени хранения иммунологической памяти, а не от текущей концентрации антител в крови зависит стойкость иммунитета и риск повторной инфекции.
Как антитела вырабатываются при вакцинации?
Для начала синтеза антител организму не обязательно сталкиваться с живой опасной бактерией или вирусом. Достаточно будет «убитого» или ослабленного микроба, кусочка его оболочки или даже отдельного белка — это тоже запустит иммунную реакцию и выработку антител. Эти антитела будут совершенно нормально работать и против живого опасного возбудителя инфекции. В этом и заключается смысл вакцинации — знакомим иммунную систему с ослабленным или убитым микробом, чтобы она научилась убивать живых и опасных.
Продолжительность вакцинного иммунитета тоже зависит от иммунологической памяти и может отличаться от естественного иммунитета, возникшего после болезни. Когда иммунитет угасает, нужно вакцинироваться снова. Для вакцин от разных инфекций есть свои графики повторной вакцинации, их частота зависит от времени хранения иммунологической памяти.
Вакцины, полученные по различной технологии, могут отличаться по времени действия вакцинного иммунитета. Обычно эти различия не слишком велики, так как продолжительность иммунитета в гораздо большей степени зависит от вида самого возбудителя, чем от конкретной вакцины.
На формирование защитного иммунитета также влияет состояние самого организма. Например, при тяжелых заболеваниях иммунной системы (наследственные иммунодефициты, злокачественные новообразования) иммунный ответ на вакцину может быть снижен или не формироваться вообще. Как показывает многолетний опыт использования разных вакцин, в случае ВИЧ-инфекции иммунный ответ на вакцины, как правило, ничем не отличается от иммунного ответа у ВИЧ-негативных людей. Поэтому графики вакцинации и дозы вакцины для ВИЧ-позитивных пациентов не будут иметь никаких особенностей.
по теме
Лечение
Безумно дорогое лекарство, которое спасет мир от пандемии
Некоторые лекарства, например глюкокортикоиды и иммунодепрессанты, могут подавлять формирование вакцинного иммунитета. В таких случаях тактику вакцинации нужно обсудить с врачом.
Для вакцин от новой коронавирусной инфекции время действия вакцинного иммунитета остается одним из главных вопросов. Предсказать продолжительность защиты той или иной вакцины очень трудно. Обычно это выясняют на практике, регистрируя частоту инфекций у привитых во время массовой вакцинации людей спустя разное количество времени, а также измеряя титр защитных антител.
Титр? Какой еще титр?
Как мы уже выяснили, антитела — это белки, которые циркулируют в крови. Для того чтобы обеспечивать эффективную защиту, эти белки должны быть в крови в определенной концентрации — ее и называют титром. Выражают титр в виде чисел, разделенных двоеточием, например 1:50 или 1:100 (читается как «один к пятидесяти» или «один к ста»).
Так как антитела — это сложные белки, определять их химическими методами крайне трудно. Поэтому для определения антител используют иммунологические реакции. Конкретных методов очень много, но в самом общем виде суть этих реакций очень простая. Мы берем раствор нужного антигена (например, того самого шиповидного белка коронавируса) и смешиваем его с сывороткой, в которой ищем антитела. Если антитела в сыворотке есть, то они связываются с антигеном и их соединение выпадает в виде осадка или раствор мутнеет. На практике проведение такой реакции выглядит сложнее, часто используют специальные гелевые среды и разные способы детектирования, но суть от этого не меняется.
Проблема в том, что такой подход отвечает нам только на вопрос, есть антитела в сыворотке или их нет, но ничего не говорит о количестве самих антител. Как в таком случае сравнить между собой две разные сыворотки? По количеству выпавшего осадка — не вариант, слишком большая погрешность. Но есть другой способ — можно разводить исследуемую сыворотку до тех пор, пока реакция (осадок) все еще будет обнаруживаться. И вот последнее, самое сильное разведение, при котором мы еще можем наблюдать реакцию сыворотки с раствором антигена, и называют титром этой сыворотки. То есть титр 1:50 говорит нам о том, что эту сыворотку можно развести в 50 раз и она еще будет давать реакцию с антигеном. Соответственно, чем больше вторая цифра в обозначении титра, тем выше концентрация антител в сыворотке.
Недостаток титра в том, что он указывает на относительное содержание антител. Если у нас есть две сыворотки с титрами 1:50 и 1:100, мы можем с уверенностью сказать, что во второй сыворотке антител в 2 раза больше, чем в первой. Но какая именно концентрация антител в каждой из этих сывороток, мы не знаем. На практике это часто бывает и не нужно: нам достаточно знать, с каким титром антител человек еще защищен от инфекции, а с каким — уже нет. Это легко выяснить, измеряя титр антител у вакцинированных людей, которые все же заразились.
В результатах лабораторных анализов обычно указывают концентрацию антител в международных единицах (МЕ) или относительных единицах (ОЕ). Результаты, полученные в МЕ, можно сравнивать между собой — значение не будет зависеть от лаборатории, тест-системы и условий анализа (для коронавируса таких пока нет). Результаты, выраженные в ОЕ, можно сравнивать между собой только для тестов одной марки, при этом сама лаборатория и время анализа роли не играют, то есть можно отслеживать динамику изменения уровня антител у одного человека.
Чтобы понять, нужна ли вакцина и подействовала ли она, достаточно измерить уровень антител? Какой нужен для ковида?
К сожалению, все немного сложнее. Антитела отвечают за гуморальный иммунитет — и это только лишь часть нашей иммунной системы. Помимо гуморального, есть еще клеточный иммунитет, работа которого не зависит от уровня антител. При защите от разных инфекций разные звенья иммунитета играют неодинаковые роли. В каких-то случаях ведущую роль имеет гуморальный иммунитет и антитела (например, в случае гепатита В, гриппа, столбняка и многих других инфекций). В других случаях — ведущая роль у клеточного иммунитета, например, при туберкулезе. По новой коронавирусной инфекции пока слишком мало данных, чтобы делать выводы о важности каждого из звеньев иммунитета и необходимом уровне антител. То есть даже если вы сделаете тест на антитела, эта информация практически ничего не даст по ряду причин.
Если вы еще не вакцинировались и тест на антитела будет положительным, что говорит о перенесенной инфекции в бессимптомной форме, это все равно не является противопоказанием к вакцинации. Мы не знаем, какова продолжительность естественного иммунитета, так что вакцина может продлить или усилить защиту.
Если вы делаете тест на антитела после вакцинации, сейчас нет надежных данных, с которыми можно было бы соотнести полученные результаты и сделать вывод о том, подействовала ли вакцина. Другими словами, пока никто не знает, сколько должно быть антител после вакцинации, чтобы гарантировать надежный уровень защиты. Плюс уровень антител ничего не говорит о состоянии клеточного иммунитета, а он тоже может быть очень важен для защиты.
Если вы наблюдаете за динамикой концентрации антител после вакцинации и видите ее снижение, это еще не говорит о снижении уровня защиты. Как мы выяснили выше, падение концентрации антител в крови с течением времени — это нормальное явление, а долговременную защиту обеспечивает иммунологическая память, которая с концентрацией антител не связана.
Не все антитела одинаково полезны
Для характеристики антител важно понимать их класс, тип и с каким антигеном они связываются.
Антитела бывают разных классов (A, M, G, E и др.). Основной класс защитных антител — G, в лабораторных исследованиях и тестах их обычно обозначают IgG. Наличие этих антител в крови говорит о наличие иммунитета после вакцинации или перенесенного заболевания. IgM — тоже защитные антитела, которые начинают вырабатываться первыми, раньше, чем IgG. Обычно IgM менее эффективны, чем IgG, и почти полностью исчезают к концу заболевания. Наличие этих антител обычно указывает на еще протекающее, или совсем недавно перенесенное заболевание, или на хроническую инфекцию. То есть, если нас интересует устойчивый иммунитет, в тестах ищем IgG.
Если антитело связывается с каким-то белком на поверхности вируса или бактерии, это далеко не всегда означает, что бактерия и вирус становятся после этого полностью безвредными. Например, вирус может использовать другой участок поверхностного белка для проникновения в клетку, не тот, с которым связалось антитело. Антитела, которые связываются с патогенами, но не подавляют их опасность, называют связывающими. Если же связывание антитела полностью «обезвреживает» микроб, «нейтрализует» его опасное влияние, такое антитело называют нейтрализующим. Связывающие антитела нельзя назвать полностью бесполезными — прикрепляясь к вирусу или бактерии, такие антитела делают их более заметными для клеток иммунной системы и ускоряют реакцию иммунитета. Но именно нейтрализующие антитела, которые могут самостоятельно обезвреживать опасные микробы, обеспечивают основную защиту, и именно их уровень важен при оценке вакцинного или естественного иммунитета. То есть в анализах нам нужно искать нейтрализующие IgG.
И, наконец, антиген. Как мы разбирали выше, антитела обладают очень высокой специфичностью и связываются только с определенными белками. Когда иммунная система, столкнувшись с инфекцией, подбирает нужное антитело, она чаще всего начинает синтезировать сразу несколько разных видов, нацеленных на разные белки возбудителя. Ведь клетки, синтезирующие антитела, получают для анализа разные кусочки полупереваренного микроба — и поверхностные, и внутренние белки — и для каждого из них ищут антитело. Для эффективной защиты важны именно те антитела, которые связываются с белками на поверхности вируса или бактерии. Ведь антитела — это крупные молекулы, которые не могут поникать внутрь вирусных частиц или бактерий, для них доступны только поверхностные белки. Именно поэтому защитный иммунитет в первую очередь обеспечивают антитела к поверхностным антигенам. Например, в случае коронавирусной инфекции вырабатывается как минимум 2 вида антител — к S-белку (который на поверхности вирусной частицы) и к N-белку (он же нуклеокапсидный белок, который находится внутри вирусной частицы). Так как до N-белка антитела добраться не могут, защиту будут обеспечивать именно антитела к S-белку. То есть, если вы все же хотите определить уровень защитных антител после прививки от ковида, нужно искать тест на нейтрализующие IgG к S-белку.